Похожие презентации:
Составление уравнений химических реакций. Закон сохранения массы веществ
1.
Составление уравненийхимических реакций.
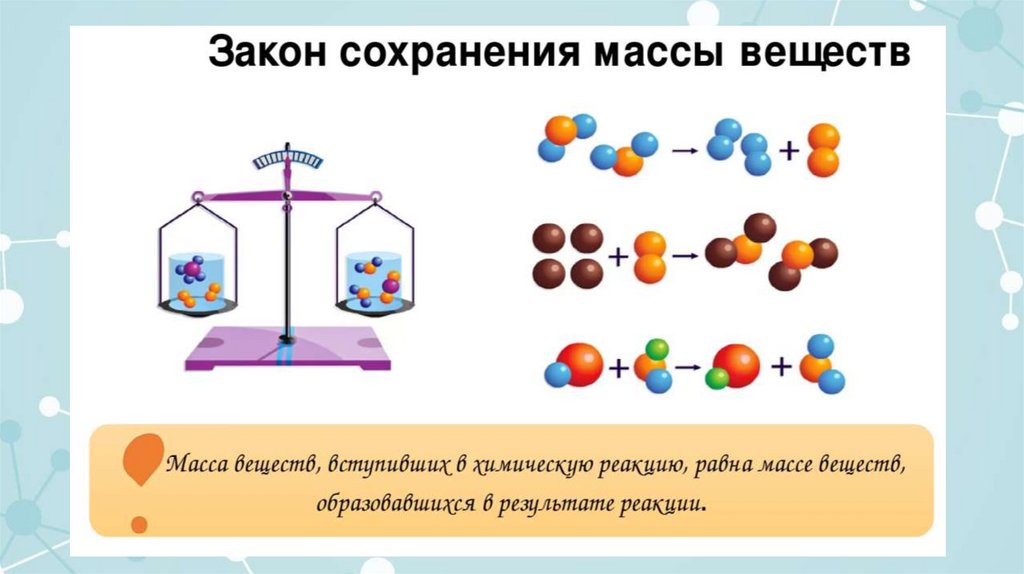
Закон сохранения массы веществ.
2.
8.2.3.3 -составлять уравнения химических реакций, записывая формулыреагентов и продуктов реакции
8.2.3.4 -знать закон сохранения массы веществ
3.
4.
5.
6.
7.
8.
Алгоритм составления уравнения химической реакции• Составим уравнение химической реакции взаимодействия
фосфора и кислорода
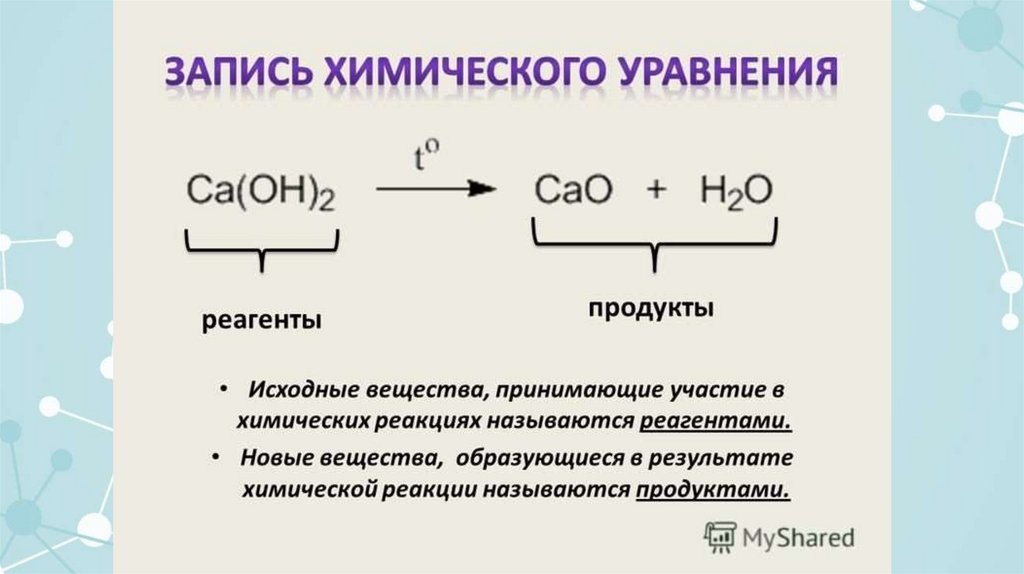
В левой части уравнения записываем химические формулы реагентов (веществ, вступающих в
реакцию).
Помните! Молекулы большинства простых газообразных веществ двухатомны –
H2; N2; O2; F2; Cl2; Br2; I2.
Между реагентами ставим знак «+», а затем стрелку:
P + O2 →
В правой части (после стрелки) пишем химическую формулу продукта (вещества,
образующегося при взаимодействии).
Помните! Химические формулы необходимо составлять, используя валентности атомов
химических элементов:
P + O2 → P2O5
9.
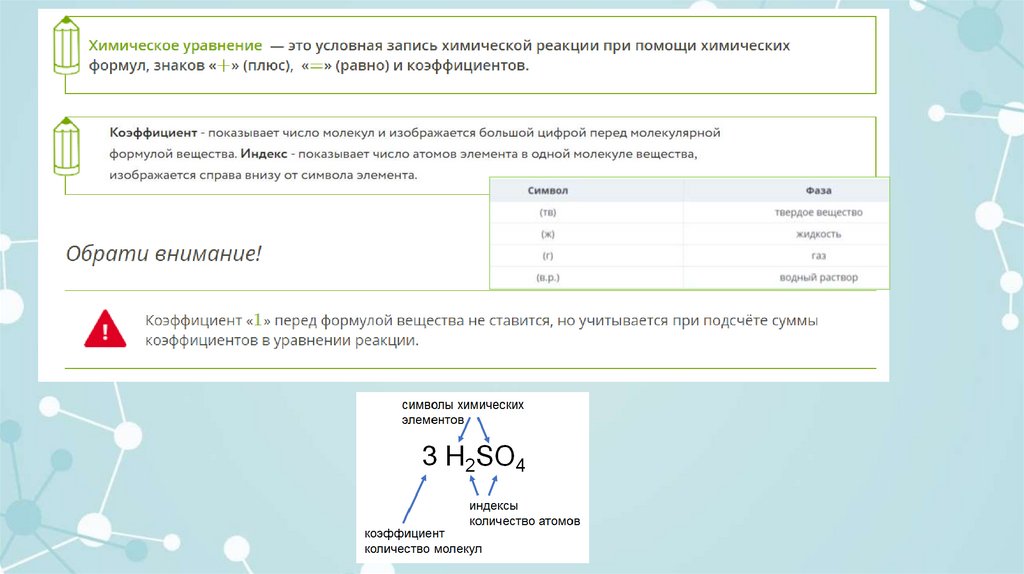
Согласно закону сохранения массы веществ число атомов до и после реакции должно бытьодинаковым. Это достигается путём расстановки коэффициентов перед химическими формулами
реагентов и продуктов химической реакции.
•Вначале уравнивают число атомов, которых в реагирующих веществах (продуктах) содержится
больше.
•В данном случае это атомы кислорода.
•Находим наименьшее общее кратное чисел атомов кислорода в левой и правой частях уравнения.
Наименьшее кратное для атомов натрия –10:
10.
Находим коэффициенты путём деления наименьшего кратного на число атомов данного вида, полученные цифрыставим в уравнение реакции:
Закон сохранения массы вещества не выполнен, так как число атомов фосфора в реагентах и продуктах реакции не
равно, поступаем аналогично ситуации с кислородом:
Получаем окончательный вид уравнения химической реакции. Стрелку заменяем на знак равенства. Закон
сохранения массы вещества выполнен:
4P + 5O2 = 2P2O5
11.
Fe + Cl2→ FeCl3Mg + HCl → MgCl2 + H2
Al(OH)3 → Al2O3 + H2O
HNO3→ H2O+NO2+O2
CaO+H2O→ Ca(OH)2
H2+Cl2→ HCl
KClO3→ KClO4+KCl
Fe(OH)2+H2O+O2→ Fe(OH)3
KBr+Cl2→ KCl+Br2
Используя алгоритм составления уравнений
химических реакций, составьте уравнения реакций
взаимодействия между следующими парами веществ:
1) Na и O2
2) Na и Cl2
3) Al и S
12.
Составление уравнений химических реакций. 1 часть. 8 класс.https://www.youtube.com/watch?v=g2IeqEOH0yE









 Химия
Химия








