Похожие презентации:
Химические свойства алкинов
1.
ХИМИЧЕСКИЕСВОЙСТВА
АЛКИНОВ
2.
АЛКИНЫ относятся к непредельным (ненасыщенным) соединениям, тоесть их химические свойства обусловлены наличием в
молекулах тройной связи, поэтому алкины преимущественно
вступают в реакции электрофильного присоединения AE.
3.
ЧЕМ ОТЛИЧАЮТСЯАЛКИНЫ ОТ АЛКЕНОВ?
ОТЛ И Ч И Е А Л К И Н О В ОТ А Л К Е Н О В
ЗАКЛЮЧАЕТСЯ В ТОМ, ЧТО РЕАКЦИИ
П Р И С О Е Д И Н Е Н И Я М О Г У Т П Р ОТ Е К АТ Ь В Д В Е
С ТАД И И . НА П Е Р В ОЙ С ТАД И И И Д Е Т
ПРИСОЕДИНЕНИЕ К ТРОЙНОЙ СВЯЗИ С
О Б РА З О В А Н И Е М Д В О Й Н О Й С В Я З И , А Н А
В ТОРОЙ СТАДИИ — П РИСОЕ Д И НЕ Н И Е К
ДВОЙНОЙ СВЯЗИ. РЕАКЦИИ ПРИСОЕДИНЕНИЯ
ДЛЯ АЛКИНОВ ПРОТЕКАЮТ МЕДЛЕННЕЕ, ЧЕМ
ДЛЯ АЛКЕНОВ. ЭТО ОБЪЯСНЯЕТСЯ ТЕМ,
ЧТО Π-ЭЛЕКТРОННАЯ ПЛОТНОСТЬ ТРОЙНОЙ
С В Я З И РА С П О Л ОЖ Е Н А Б О Л Е Е КО М П А К Т Н О ,
ЧЕМ В АЛКЕНАХ, И ПОЭТОМУ МЕНЕЕ
ДОСТУПНА ДЛЯ ВЗАИМОДЕЙСТВИЯ С
РА З Л И Ч Н Ы М И Р Е А Г Е Н ТА М И . РА С С М О Т Р И М
ПОДРОБНЕЕ ТИПЫ ЭТИХ РЕАКЦИЙ.
4.
РЕАКЦИИ ПРИСОЕДИНЕНИЯ• Галогенирование
(присоединение молекулы
галогена).
• Гидрогалогенирование
(присоединение галогеноводорода),
протекает в две стадии.
• Гидратация (присоединение воды)
алкинов.
5.
КИСЛОТНЫЕ СВОЙСТВААЛКИНОВ
ОСОБЕННОСТЬЮ АЛКИНОВ, ИМЕЮЩИХ
КОНЦЕ В У Ю Т РОЙ НУЮ СВ Я ЗЬ , Я В Л Я Е ТСЯ И Х
СПОСОБНОСТЬ ОТЩЕПЛЯТЬ ПРОТОН ПОД
Д Е Й С Т В И Е М С И Л Ь Н Ы Х О С Н О В А Н И Й , Т. Е .
ПРОЯВЛЯТЬ СЛАБЫЕ КИСЛОТНЫЕ СВОЙСТВА.
В О З М ОЖ Н О С Т Ь ОТ Щ Е П Л Е Н И Я П Р ОТО Н А
ОБУСЛОВЛЕНА СИЛЬНОЙ ПОЛЯРИЗАЦИЕЙ ΣСВЯЗИ: ≡C←H. ПРИЧИНОЙ ПОЛЯРИЗАЦИИ
ЯВЛЯЕТСЯ ВЫСОКАЯ
Э Л Е К Т Р О О Т Р И Ц А Т Е Л Ь Н О С Т Ь А Т О М А У ГЛ Е Р О Д А
В SP-ГИБРИДНОМ СОСТОЯНИИ. ПОЭТОМУ
А Л К И Н Ы , В ОТЛ И Ч И Е ОТ А Л К Е Н О В И А Л К А Н О В ,
С П О С О Б Н Ы О Б РА З О В Ы В АТ Ь С О Л И ,
НАЗЫВАЕМЫЕ АЦЕТИЛЕНИДАМИ R−C≡CME.
6.
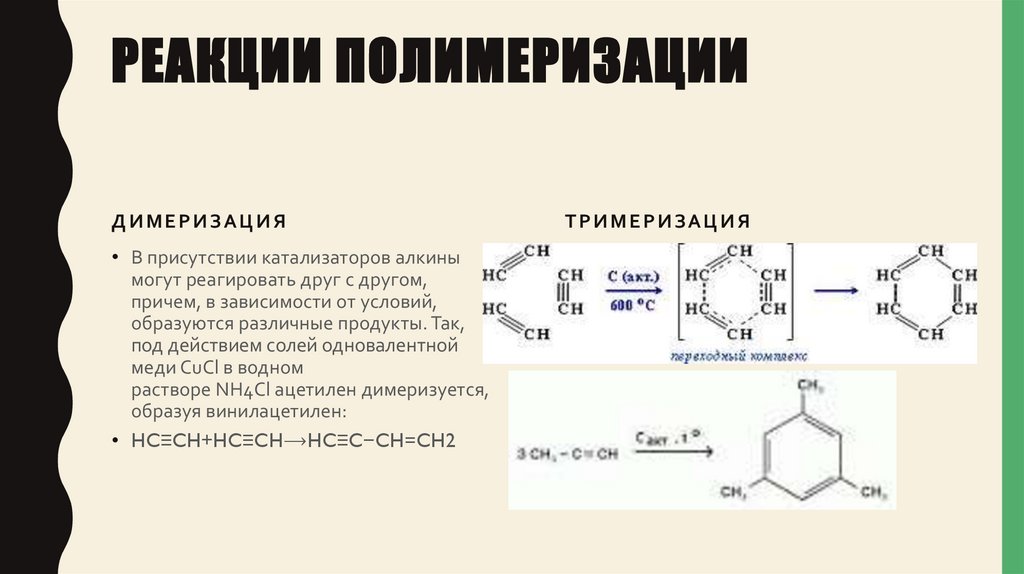
РЕАКЦИИ ПОЛИМЕРИЗАЦИИДИМЕРИЗАЦИЯ
• В присутствии катализаторов алкины
могут реагировать друг с другом,
причем, в зависимости от условий,
образуются различные продукты. Так,
под действием солей одновалентной
меди CuCl в водном
растворе NH4Cl ацетилен димеризуется,
образуя винилацетилен:
• HC≡CH+HC≡CH⟶HC≡C−CH=CH2
ТРИМЕРИЗАЦИЯ
7.
ОКИСЛЕНИЕ АЛКИНОВГО Р Е Н И Е ( Ж Е С Т КО Е О К И С Л Е Н И Е )
• Ацетилен и другие алкины горят
в кислороде с выделением очень
большого количества теплоты,
то есть реакция является
экзотермической.
О К И С Л Е Н И Е Н Е О Р ГА Н И Ч Е С К И М И
О К И С Л И Т Е Л Я М И ( М Я Г КО Е
ОКИСЛЕНИЕ)
Алкины, как и алкены, обесцвечивают
подкисленные растворы
перманганата калия, при этом
происходит разрушение кратной
связи и продуктами окисления
являются, в зависимости от условий,
карбоновые кислоты (KMnO4 в кислой
среде) или их соли (KMnO4 в
нейтральной или щелочной среде).
Подробнее см. тему "ОВР в
органической химии". В общем виде
уравнение реакции можно записать
следующим образом.
8.
ВОССТАНОВЛЕНИЕ АЛКИНОВ• В присутствии металлических катализаторов (никеля) алкины восстанавливаются путем
последовательного присоединения молекул водорода, превращаясь сначала в алкены,
а затем в алканы.
• При использовании платинового катализатора алкины восстанавливаются лишь до
алкенов.
9.
СПАСИБО ЗАВНИМАНИЕ!








 Химия
Химия








