Похожие презентации:
Кислород. Химический элемент кислород
1.
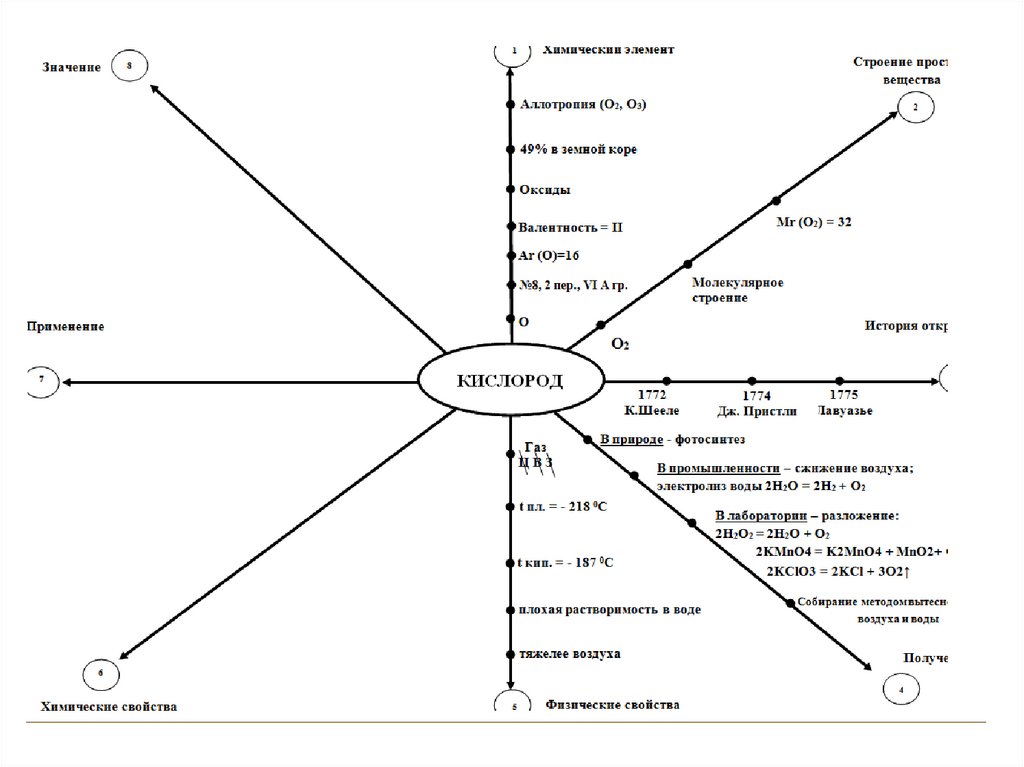
КИСЛОРОД2.
План:1.Химический элемент кислород
2.Кислород как простое вещество
3.Физические свойства кислорода
4.История открытия кислорода
5.Получение и собирание кислорода
6.Химические свойства кислорода
7.Применение кислорода
8.Роль кислорода в природе (значение)
3.
4.
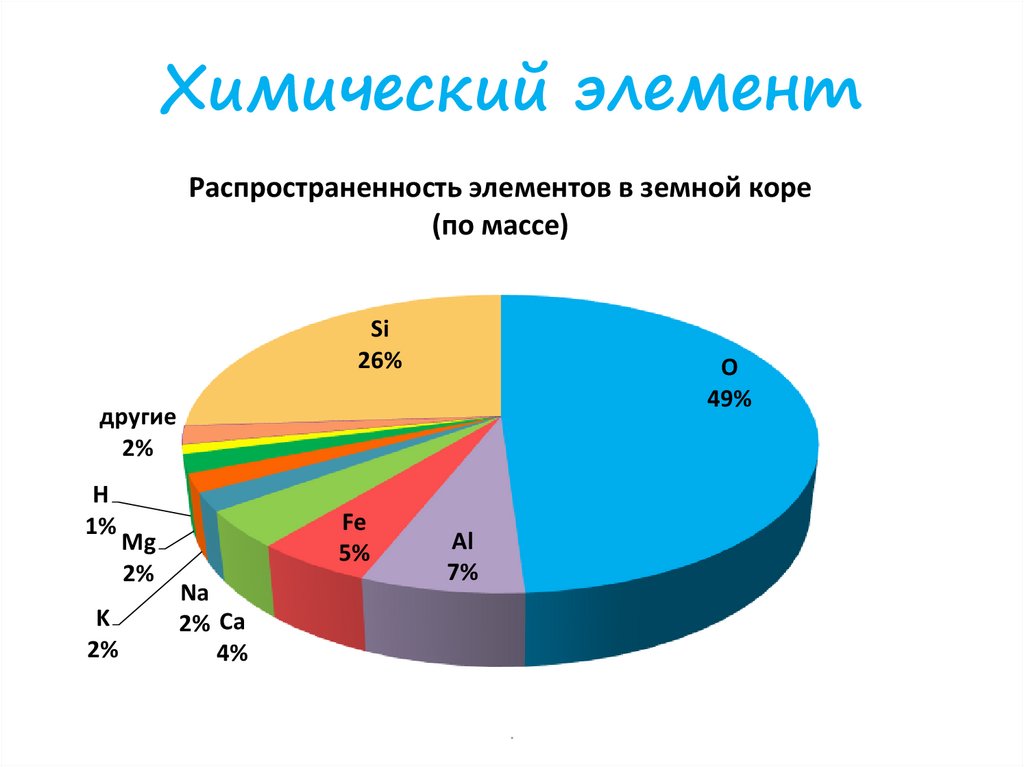
Химический элементРаспространенность элементов в земной коре
(по массе)
Si
26%
O
49%
другие
2%
H
1%
K
2%
Mg
2%
Fe
5%
Na
2% Ca
4%
Al
7%
.
5.
Химический элементХимический знак –
O
Положение в ПС – 2 период, VI А группа
Аr (O) =
16
Валентность =
порядковый номер №8
II
Соединения элементов с кислородом–
оксиды
6.
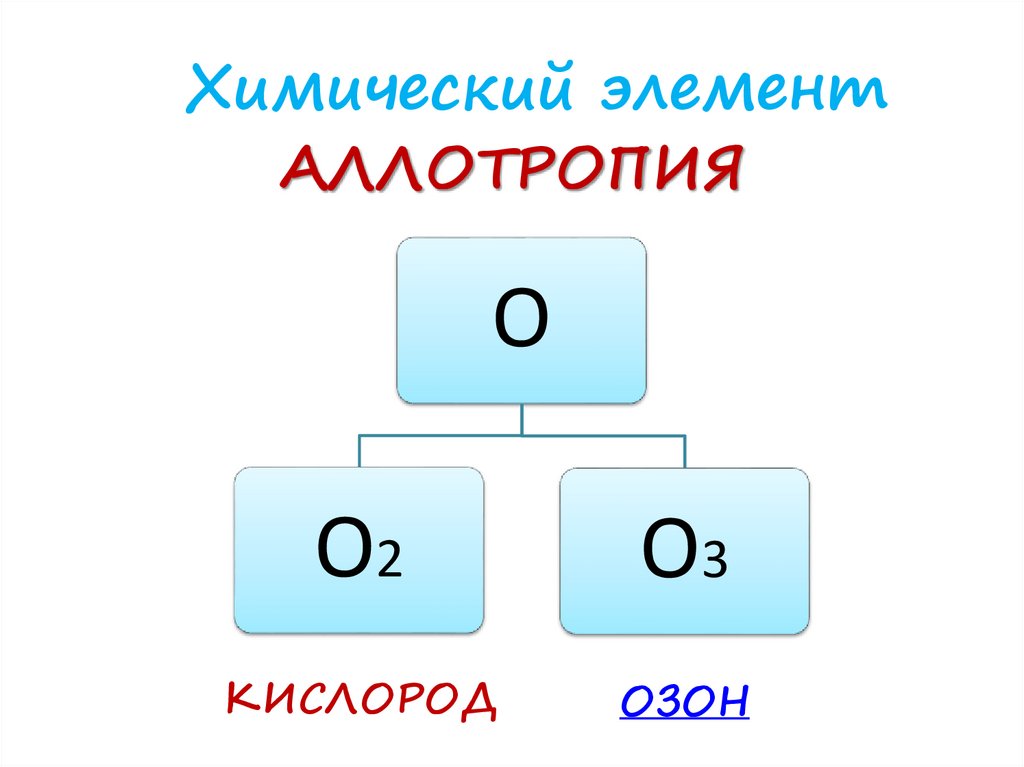
Химический элементАЛЛОТРОПИЯ
O
O2
O3
КИСЛОРОД
ОЗОН
7.
Простое веществоХимическая формула –
O2
Модель молекулы:
Mr (O2) =
Строение:
32
молекулярное
Алфероа М.В.
8.
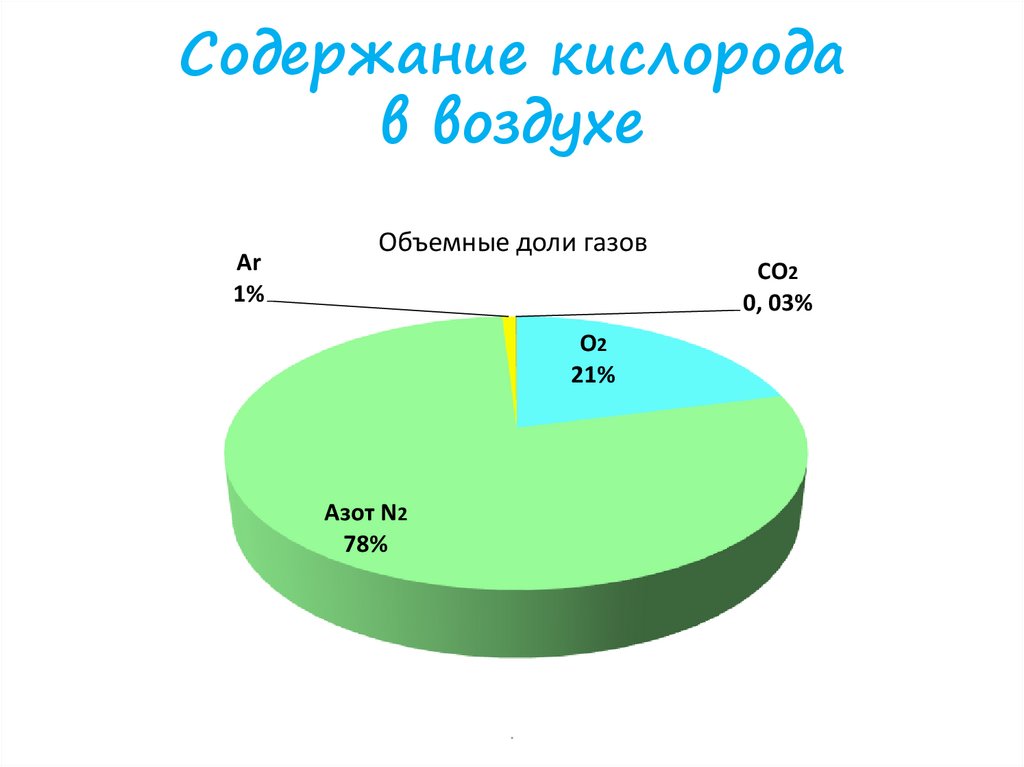
Содержание кислородав воздухе
Ar
1%
Объемные доли газов
CO2
0, 03%
О2
21%
Азот N2
78%
.
9.
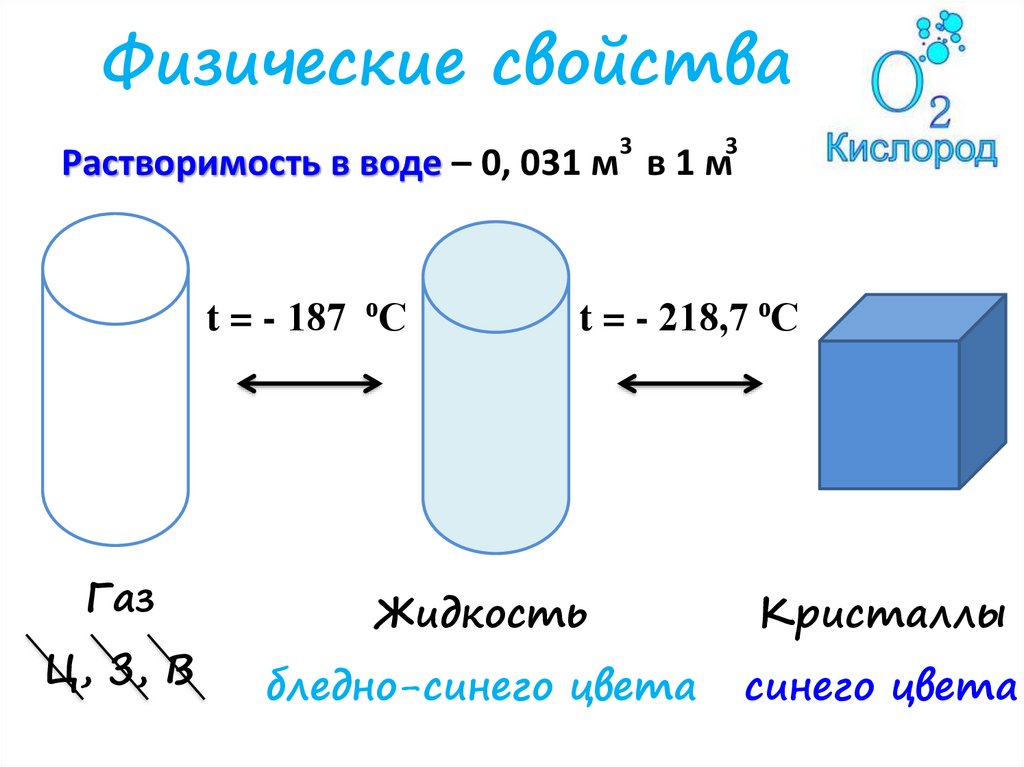
Физические свойства3
3
Растворимость в воде – 0, 031 м в 1 м
t = - 187 ⁰C
Газ
Ц, З, В
t = - 218,7 ⁰C
Жидкость
Кристаллы
бледно-синего цвета
синего цвета
10.
История открытия кислорода2HgO=2Hg+O2↑
1772 -1774 г.
– швед. ученый
Карл Шееле
1775 год –
франц. ученый
Лавуазье
.
1774 год –
англ. ученый
Джозеф Пристли
11.
Получение кислородаI.Промышленные способы:
1. Разделение воздуха на составные части
2. Электролиз воды: 2H2O = 2H2↑ + O2↑
II.Лабораторные способы:
1. Разложение пероксида водорода:
2H2O2 = 2H2O + O2↑
2. Разложение перманганата калия:
2KMnO4 = K2MnO4 + MnO2+ O2↑
3. Разложение хлората калия (бертолетовой
соли):
2KClO3 = 2KCl + 3O2↑
12.
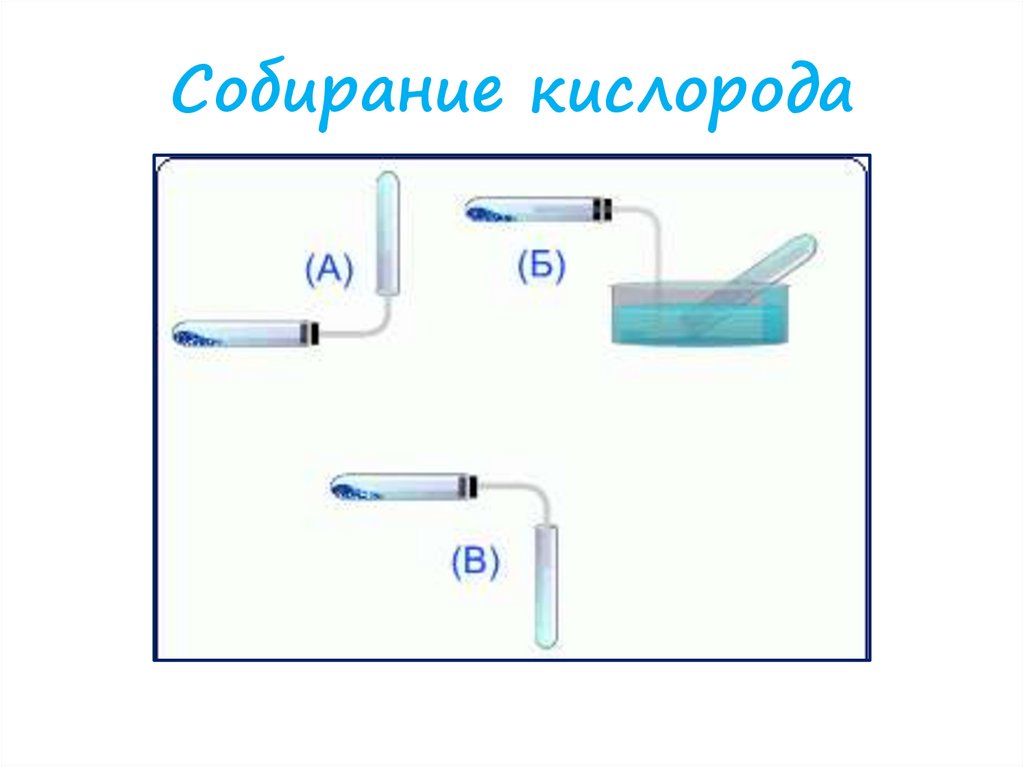
Собирание кислорода13.
Собирание кислородаМетод вытеснения воды
.
Метод вытеснения
воздуха









 Химия
Химия








