Похожие презентации:
Общая характеристика галогенов
1.
2.
Галогены1. История открытия галогенов
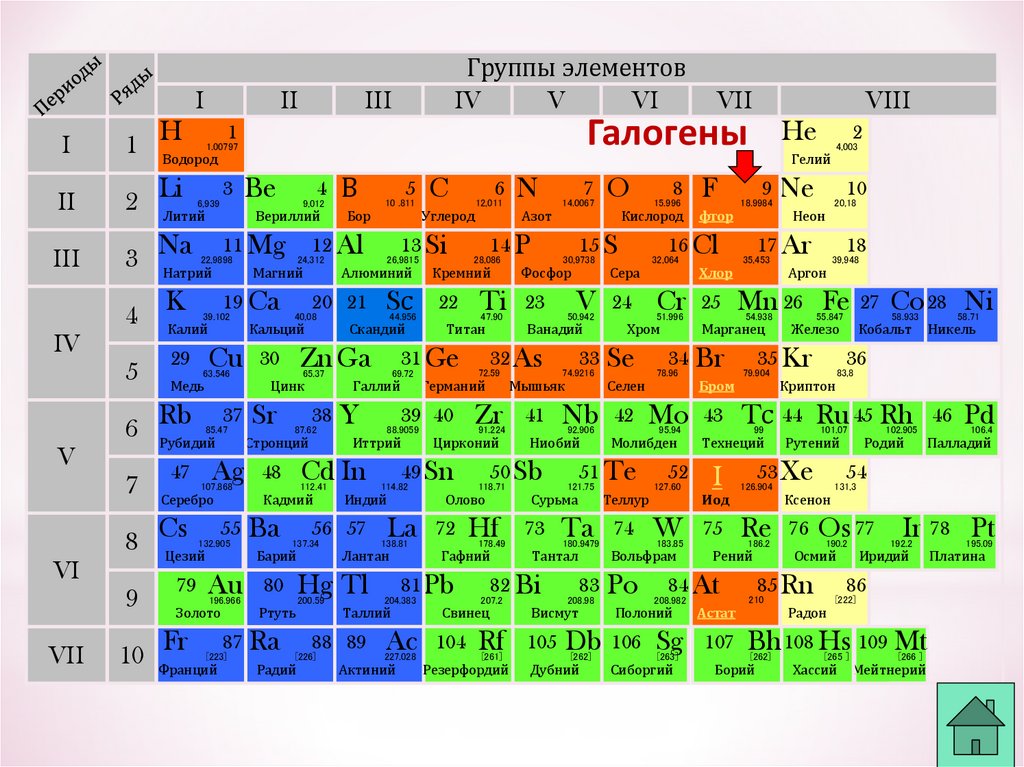
2. Положение в ПСХЭ
3. Химические свойства
4. Применение
5.Проверка знаний
6.Домашнее задание. Итоги урока.
Главная
3.
*К элементам VII группы, главной подгруппы относятсяфтор F, хлор Cl, бром Br, иод I, астат At
• Общее название - галогены (греч. «солеобразующие») большинство их соединений с металлами представляют собой
типичные соли (KCl, NaCl и т.д.).
4.
• В свободном виде не встречаютсяФлюорит
CaF2
5. Галит NaCl
*ГалитNaCl
6.
CильвинитKCl NaCl
7.
Иод — элемент редкий
Иодиды в морской воде
• 20 — 30 мг на тонну морской воды
В живых организмах, больше всего
в водорослях
• 5 кг на тонну высушенной морской капусты
(ламинарии)
8. История открытия галогенов
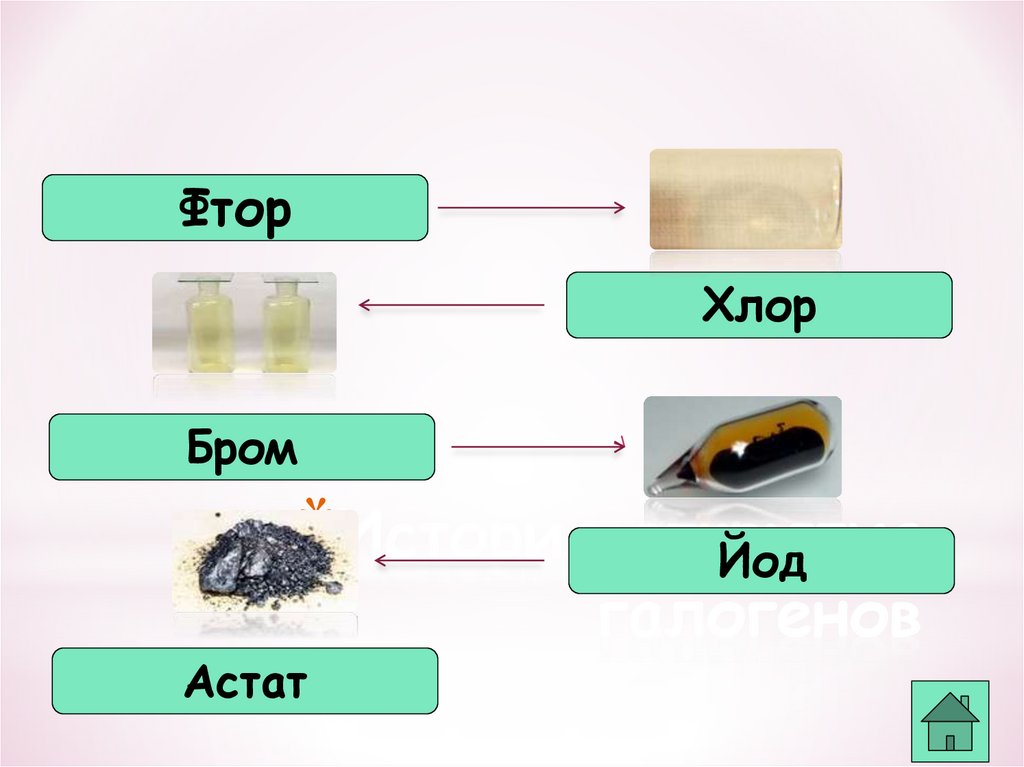
ФторХлор
Бром
*История
Астат
открытия
Йод
галогенов
9. История открытия фтора
В 1886 году французский химик А.Муассан,
используя
электролиз
жидкого фтороводорода, охлажденного
до температуры –23°C, смог на аноде
получить первую порцию нового, газа.
В первых опытах для получения фтора
Муассан использовал очень дорогой
электролизер,
изготовленный
из
История
открытия
платины и иридия.
При этом
каждый
грамм полученного фтора «съедал» до
6 г платины.
*
Анри Муассан
(1852 – 1907)
фтора
10. История открытия хлора
Карл ВильгельмШееле
(1742 – 1786)
В 1774 году шведский ученый
К.
Шееле открыл хлор, который принял за
сложное
вещество
и
назвал
"дефлогистированной соляной кислотой".
В 1807 году английский химик
Гемфри Дэви получил тот же газ. Он
пришел к выводу, что получил новый
элемент и назвал его "хлорин" (от
"хлорос" - желто-зеленый).
В 1812 году Гей-Люссак дал газу
название
хлор.
* История
открытия хлора
11. История открытия брома
В 1825 году французскийхимик А.Ж.Балар
при изучении
маточных рассолов выделил темнобурую жидкость, который он назвал
- "мурид" (от латинского слова
muria,
означающего
"рассол").
Комиссия Академии, проверив это
сообщение, подтвердила
открытие
История открытия
Балара
и
предложила
назвать
элемент бромом (от "бромос", с
греческого "зловонный").
*
брома
Антуан Жером
Балар
(1802 – 1876)
12. История открытия йода
В 1811 году французский химикБернар Куртуа открыл
иод
путём
перегонки маточных растворов от своего
азотнокислого кальция с серной кислотой
Чтобы другие химики могли изучать новое
вещество, Б. Куртуа подарил его (правда,
очень
небольшое
количество)
фармацевтической фирме в Дижоне.
Бернар Куртуа
(1777 – 1838 )
В 1813 году Гей-Люссак подробно
изучил
этот
элемент
и
дал
ему
современное название. Название "иод"
происходит от греческого слова "иодэс" "фиолетовый" (по цвету паров).
* История
открытия йода
13.
II
1
H
II
2
Li
III
3
Na
4
K
IV
5
6
V
7
8
VI
9
VII
10
II
Группы элементов
IV
V
VI
III
Водород
3
Литий
Cu
63.546
Медь
Rb
37
85.47
Рубидий
Ag
107.868
Серебро
Cs
55
132.905
Цезий
79
Au
196.966
Золото
Fr
Франций
65.37
Цинк
38
87.62
Стронций
Sс
44.956
Скандий
Иттрий
112.41
Кадмий
Индий
56 57
137.34
Барий
Ртуть
200.59
Радий
Ac
227.028
Актиний
Ti
47.90
Zr
91.224
Цирконий
Hf
178.49
Гафний
Свинец
Rf
[261]
Резерфордий
O
8
15.996
Кислород
15 S
Фосфор
V
23
50.942
Ванадий
33
74.9216
Мышьяк
41
Nb
92.906
Ниобий
73
Ta
180.9479
Тантал
83
208.98
Висмут
105
Db
[262]
Дубний
F
фтор
16 Cl
32,064
Сера
Cr
24
51.996
Хром
Se
34
78.96
Селен
42
Mo
95.94
Молибден
51 Te
121.75
Сурьма
82 Bi
207.2
7
14.0067
30,9738
50 Sb
118.71
Олово
104
Азот
32 As
72.59
Германий
72
N
14 P
28,086
Титан
81 Pb
204.383
Таллий
88 89
[226]
La
138.81
Лантан
Hg Tl
80
22
49 Sn
114.82
12,011
Кремний
39 40
88.9059
6
Углерод
31 Ge
69.72
Галлий
Y
C
13 Si
26,9815
Алюминий
Cd In
48
87 Ra
[223]
5
10 .811
Zn Ga
30
Ba
Бор
20 21
40,08
Кальций
Sr
В
12 Al
24,312
Магний
19 Ca
39.102
Калий
47
4
9,012
11 Mg
Натрий
29
Be
Вериллий
22,9898
VIII
Галогены
1
1.00797
6,939
VII
Теллур
74
52
127.60
W
183.85
Вольфрам
Po
25
Br
Бром
43
Sg
[263]
Сиборгий
9
18.9984
Иод
75
107
4,003
10
20,18
Неон
18
Аргон
39,948
Mn 26 Fe
54.938
27
55.847
Железо
35 Kr
79.904
Co 28 Ni
58.933
Кобальт
99
36
Криптон
101.07
Re
186.2
Ксенон
76
Родий
[262]
Pd
106.4
Палладий
131,3
Os 77 Ir 78 Pt
190.2
192.2
Осмий
Иридий
86
Радон
[222]
Bh 108 Hs 109 Mt
Борий
46
54
85 Rn
210
102.905
Рутений
53 Xe
126.904
58.71
Никель
83,8
Tс 44 Ru 45 Rh
Рений
Астат
Ne
17 Ar
35,453
Технеций
I
2
Гелий
Марганец
84 At
208.982
Полоний
106
Хлор
He
[265 ]
Хассий
[266 ]
Мейтнерий
195.09
Платина
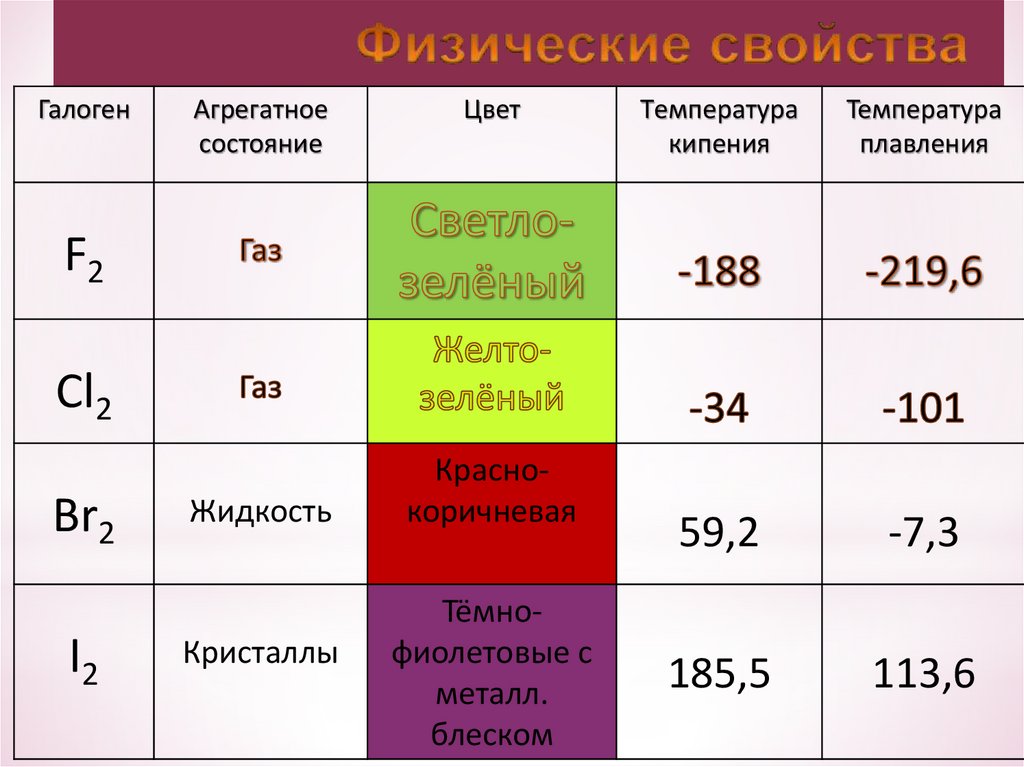
14.
ГалогенАгрегатное
состояние
Цвет
Tемпература
кипения
Температура
плавления
59,2
-7,3
185,5
113,6
F2
Cl2
Br2
I2
Жидкость
Кристаллы
Краснокоричневая
Тёмнофиолетовые с
металл.
блеском
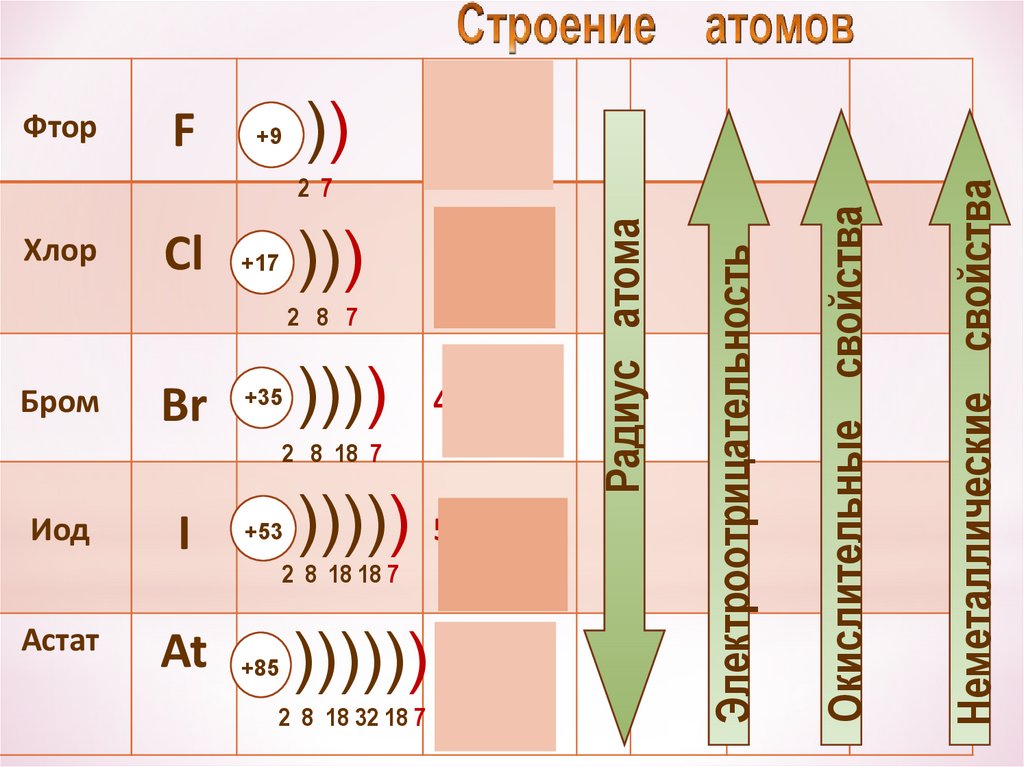
15.
F+9
))
2s22р5
)))
+17
3s23p5
2 8 7
Бром
Br
+35
))))
4s24p5
2 8 18 7
Иод
Астат
I
At
+53
)))))
5s25p5
2 8 18 18 7
+85
)))))) 6s 6p
2 8 18 32 18 7
2
5
Окислительные свойства
Cl
Электроотрицательность
Хлор
Радиус атома
2 7
Неметаллические свойства
Фтор
16.
918,998
7
2
*Название
"фтор" (от греческого phthoros разрушение, гибель)
• В свободном состоянии фтор был получен
26 июня 1886 г. французским химиком
Муассаном.
• Это зеленовато-желтый газ, немного
тяжелее воздуха, с характерным
запахом и необыкновенной химической
активностью.
• Ни один из химических элементов не
принес химикам столько трагических
событий, как фтор.
17.
1735,453
7
8
2
*Хлор был открыт шведским химиком
Карлом Шееле в 1774 г.
• в 1810 году сэр Гемфри Дэви назвал газ
"хлорином"(Chlorine), от греческого "зелёный".
• Этот термин используется в английском
языке,
а в других языках закрепилось
название "хлор".
• Газ желто-зеленого цвета с резким
запахом, ядовит
• в 2,5 раза тяжелее воздуха
• в 1 объеме воды при 20 °С
растворяется около 2 объемов
хлора
18.
3579,9
7
18
8
2
79Вr
(50,56%)
81Вr
(49,44%)
*от греч. bromos – зловоние
*единственный неметалл, жидкий при
комнатной температуре
• тяжелая
красно-бурая
жидкость
с
неприятным запахом
• пары брома имеют желто-бурый цвет
• при температуре –7,25° C бром затвердевает,
превращаясь в красно-коричневые игольчатые
кристаллы со слабым металлическим блеском
19.
53126,9
7
18
18
8
2
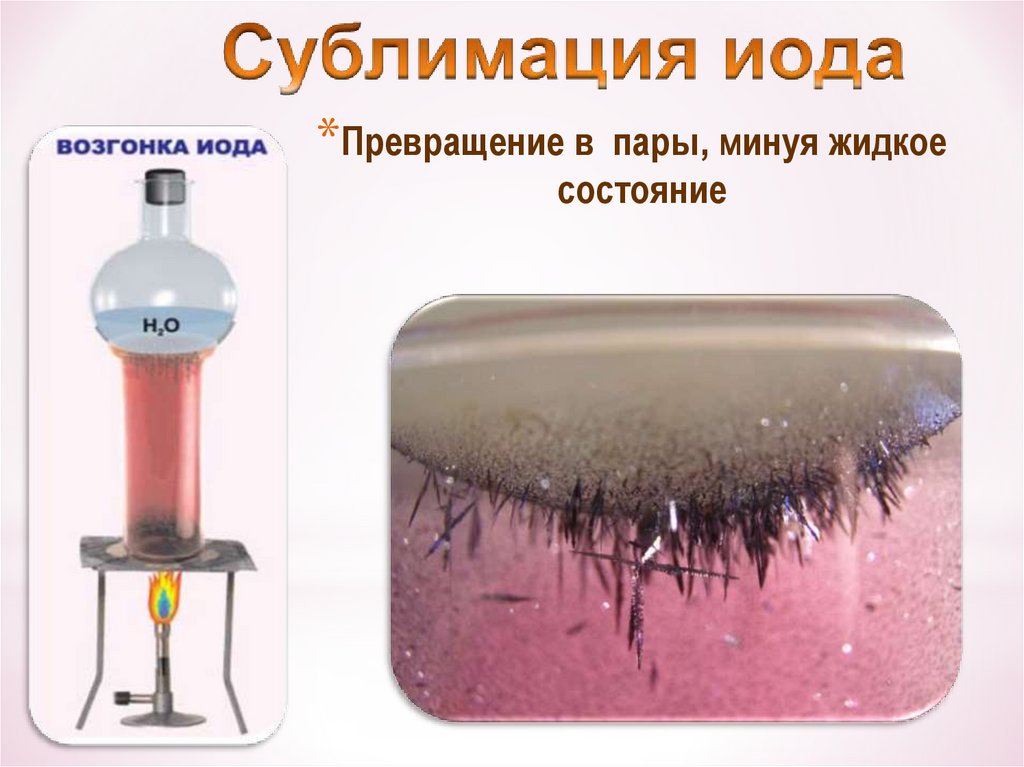
*от греч. iodes—имеющий фиалковый цвет
*в парообразное состояние переходит при
комнатной t°, не плавясь (сублимация);
* пары -фиолетового цвета
Иод был открыт в 1811 г. Куртуа в золе
морских водорослей, а с 1815 г. ГейЛюссак стал рассматривать его как
химический элемент
Известны 37 изотопов иода с
массовыми числами от 108 до 144.
20.
*Превращение впары, минуя жидкое
состояние
21.
II
1
II
2
III
3
4
IV
5
6
V
II
III
Группы элементов
IV
V
VI
VII
Аста́т / Astatium (At)
Внешний вид
Нестабильные
простого вещества чёрно-синие
кристаллы
Электронная
[Xe] 4f14 5d10 6s2 6p
5
конфигуранция
ЭО
2,2
(по Полингу)
Степень окисления 7, 5, 3, 1, −1
Плотность
n/a г/см
7
8
VI
9
VII
10
VIII
Температура
плавления
Температура
кипения
517 К
582 К
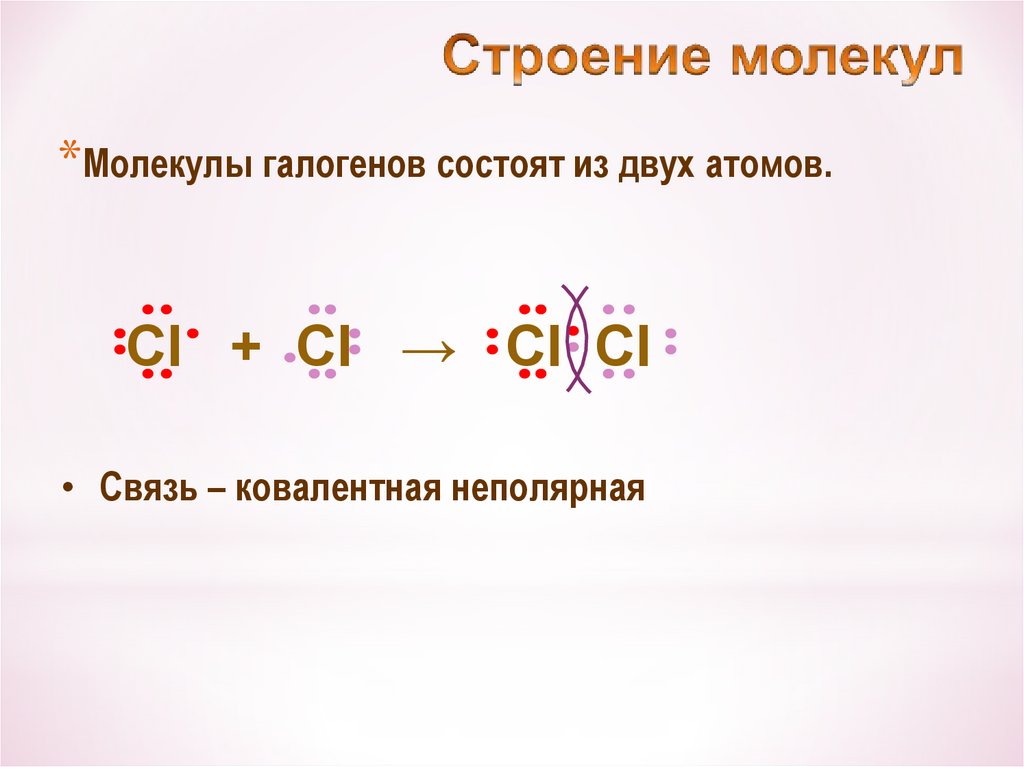
22.
*Молекулы галогенов состоят из двух атомов.Cl + Cl → Cl Cl
• Связь – ковалентная неполярная
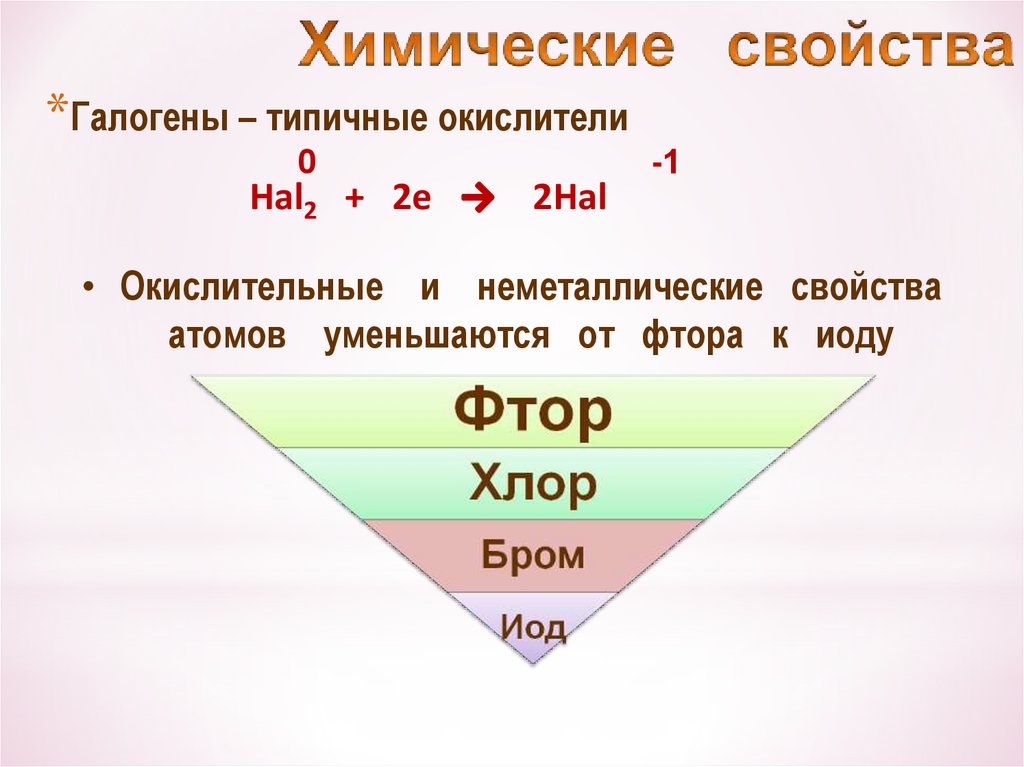
23.
*Галогены – типичные окислители0
Hal2 + 2e
2Hal
-1
• Окислительные и неметаллические свойства
атомов уменьшаются от фтора к иоду
24. Сравнение окислительных свойств
F))
+9
е-
2 7
)))
Cl
+17
Br
+35
Иод
I
+53
Астат
At
+85
Бром
2 8 7
))))
е-
2 8 18 7
)))))
е-
2 8 18 18 7
))))))
2 8 18 32 18 7
е-
Радиус атома
Хлор
е-
Неметаллические свойства
Фтор
Окислительные свойства
*
25. Восстановительные свойства ионов
**Ионы галогенов являются типичными восстановителями
-1
0
2Hal - 2e
Hal2
• С водородом галогены образуют летучие водородные
соединения
• Устойчивость галогеноводородов уменьшается в ряду:
HF
HCl
HBr
HI
• Cила галогеноводородных кислот увеличивается в ряду:
HF
HCl
HBr
HI
26.
1. Взаимодействие с металламиХлор непосредственно реагирует почти со
всеми металлами
(с некоторыми только в
присутствии влаги или при нагревании):
1. 2К + Cl2→ 2КCl
2. 2Fe + 3Cl2 → 2FeCl3
3. Cu + Cl2 → Cu Cl2
4. 2Al + 3Br2 → 2AlBr3
5. 2Al + 3I2 → 2AlI3
27.
2. Взаимодействие с неметалламиC неметаллами (кроме углерода, азота, кислорода и инертных
газов), образует соответствующие хлориды.
А) с водородом
1. H2 + F2 → 2HF +Q
2. H2 + Cl2 → 2HCl +Q
3. H2 + Br2 → 2HBr +Q
4. H2 + I2 → 2HCl - Q
В) с другими неметаллами
Скорость
реакции
уменьш.
1. 2P + 5Cl2 → 2PCl5 ( tº, в изб.Сl2)
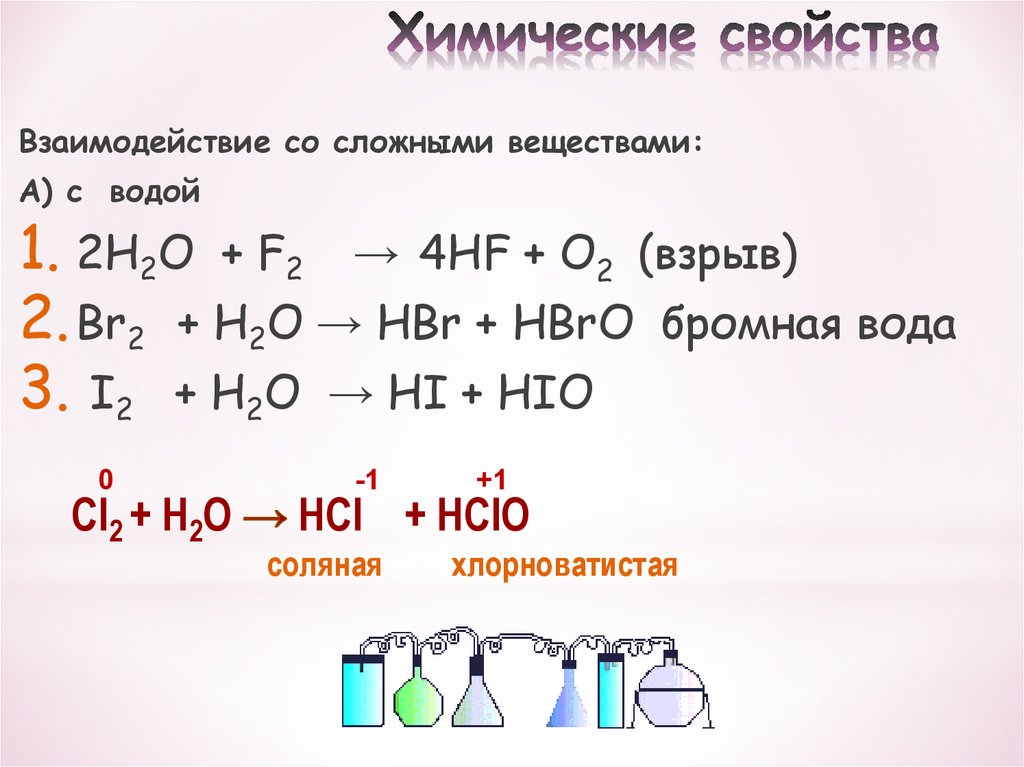
28. Химические свойства
Взаимодействие со сложными веществами:А) с водой
1. 2H2O + F2 → 4HF + O2 (взрыв)
2. Br2 + H2O → HBr + HBrO бромная вода
3. I2 + H2O → HI + HIO
0
Cl2 + H2О
-1
+1
HCl + HClO
соляная
хлорноватистая
29.
4. Взаимодействие с солями других галогеновболее активные галогены вытесняют менее активные из растворов их
солей
0
-1
Cl2 + 2NaBr
-1
0
2NaCl + Br2
5. Взаимодействие с растворами щелочей
с образованием солей
2NaOH + Cl2
6NaOH + 3Cl2
NaCl + NaClO + H2O
t
5NaCl + NaClO3 + 3H2O
30. Химические свойства
**
Взаимодействие со сложными веществами:
Б) «ряд активности» галогенов
F2 > Cl2 > Br2 > I2
1. 2KBr + Cl2 → Br2 + 2КCl
2. 2KI + Cl2 → I2 + 2КCl
3. 2KI + Br2 → I2 + 2КCl
В) с органическими веществами:
I2 + крахмал →
31.
FКости, зубы
Br
Регуляция
нервных
процессов
Сl
Кровь, желудочный
сок
I
Регуляция обмена
веществ
32.
ТефлонПрименение
фтора
Заменитель
крови
Фториды
в зубных
пастах
Фреон
Окислитель
ракетного
топлива
33.
Дезинфекцияводы
Органические
растворители
Отбеливатели
Лекарственные
препараты
Применение
хлора
Хлорирование
органических
веществ
Производство
HCl
Получение
неорганических
хлоридов
Получение
брома, йода
34.
Лекарственныепрепараты
Ветеренарные
препараты
Фотография
Применение
брома
Присадки
к бензину
Красители
Ингибиторы
35.
Лекарственныепрепараты
Дезинфекция
одежды
Применение
йода
Фотография
Электролампы
Красители
36. Подумайте…
*Что образуется в данной
реакции, оксид фтора
или фторид кислорода?
F2 + O2
37. Химические свойства галогенов Вставьте коэффициенты:
* Химические свойства галогеновВставьте коэффициенты:
Na + Cl2 = NaCl
S + F2 = SF6
Fe + Br2= FeBr3
P + Cl2 = PCl5
NaI + Cl2 = NaCl + I2
F2 + H2O = HF + O2
NaBr + Cl2 = NaCl + Br2
KOH + Cl2 = KCl + KClO3 + H2O




























 Химия
Химия