Похожие презентации:
Первое начало термодинамики. Теплоемкость
1.
ПЕРВОЕ НАЧАЛОТЕРМОДИНАМИКИ
ТЕПЛОЕМКОСТЬ
2.
ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИТеплота Q, подводимая к системе, идёт на изменение
ее внутренней энергии U и на совершение этой
системой работы A над внешними телами:
Q U A
3.
ЗНАЧЕНИЕ ПЕРВОГО ЗАКОНА ТЕРМОДИНАМИКИПервое начало термодинамики запрещает создание
вечных двигателей, принцип действия которых основан
на получении полезной работы без подвода внешней
энергии к системе
4.
ПРИМЕНЕНИЕПЕРВОГО ЗАКОНА
ТЕРМОДИНАМИКИ
Расчет работы газа в изопроцессах:
- работа газа при изменении его объёма от V1 до V2
5.
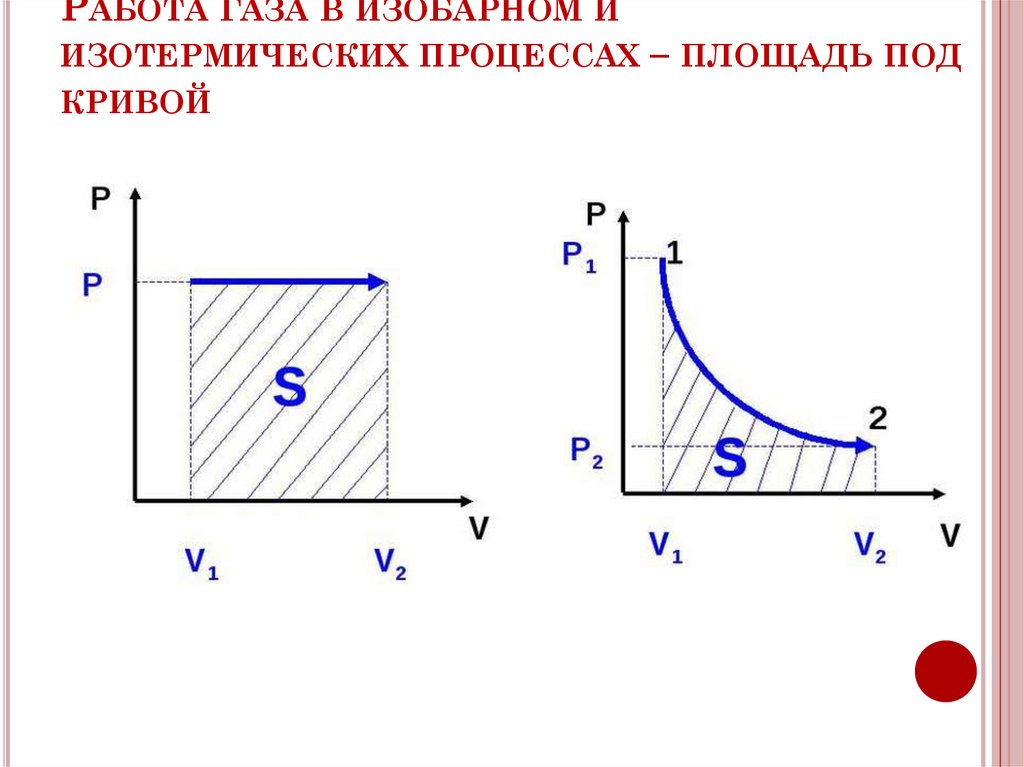
РАБОТА ГАЗА В ИЗОБАРНОМ ИИЗОТЕРМИЧЕСКИХ ПРОЦЕССАХ
КРИВОЙ
– ПЛОЩАДЬ ПОД
6.
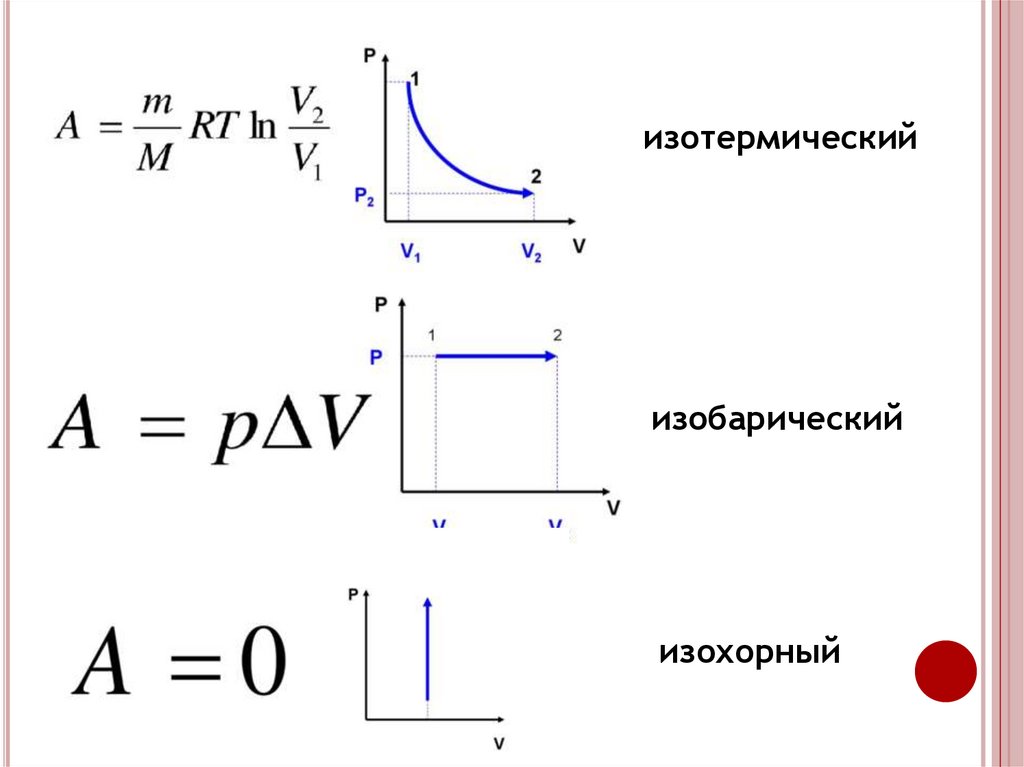
изотермическийизобарический
изохорный
7.
ТЕПЛОЁМКОСТЬТеплоёмкость тела –
количество теплоты, которое
требуется, чтобы изменить
температуру тела на 1 градус
Cтела
Удельная теплоёмкость –
теплоёмкость единицы
массы вещества
С уд
Молярная теплоёмкость –
теплоёмкость единицы
количества вещества
Q
C
dT
Q
mdT
Q Дж
К
dT
Дж
кг К
Дж
моль К
Суд C / - cвязь удельной и молярной теплоёмкости
8.
9.
ТЕПЛОЁМКОСТЬ ИДЕАЛЬНОГО ГАЗАТеплоемкость при постоянном объеме:
Теплоемкость при постоянном давлении:
Формула Майера:
CP CV R
i
CV R
2
i 2
CP
R
2
10.
АДИАБАТИЧЕСКИЙ ПРОЦЕССАдиабатический процесс протекает без теплообмена
термодинамической системы с окружающей средой
Уравнение Пуассона - уравнение адиабатического
процесса c идеальным газом:
PV const
где CP / CV
- показатель адиабаты (коэффициент Пуассона)
11.
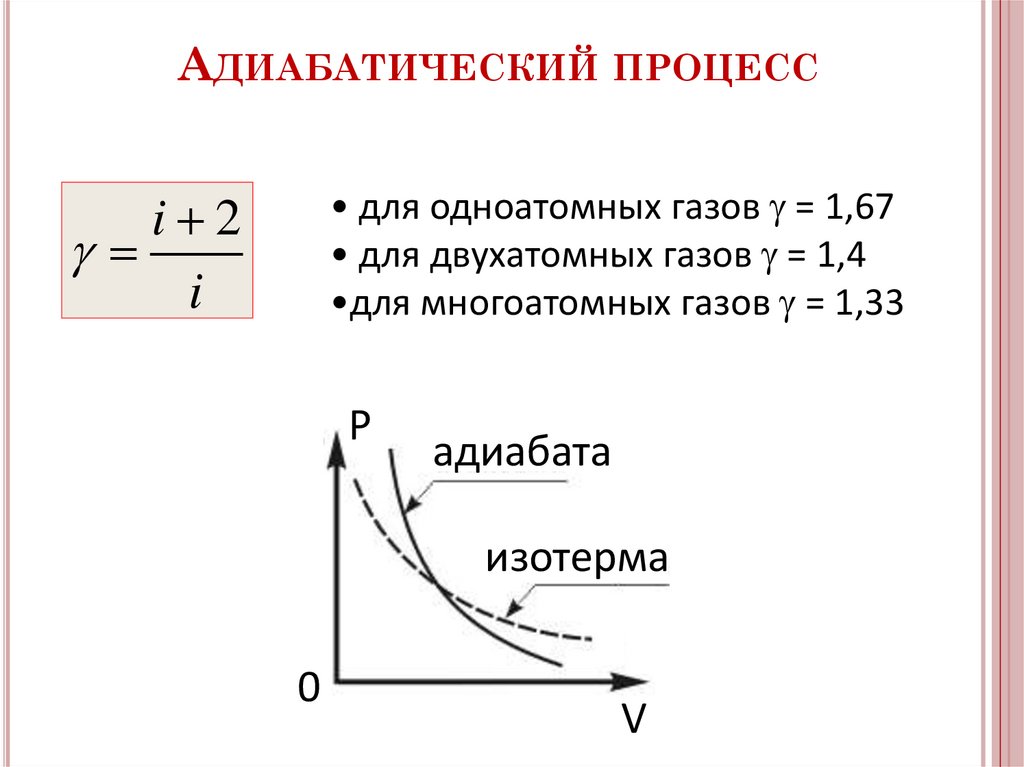
АДИАБАТИЧЕСКИЙ ПРОЦЕСС• для одноатомных газов = 1,67
• для двухатомных газов = 1,4
•для многоатомных газов = 1,33
i 2
i
Р
адиабата
изотерма
0
V
12.
ПРИМЕРЫ АДИАБАТНЫХ ПРОЦЕССОВ ВПРИРОДЕ
Образование облаков и осадков – дождя, снега, града
13.
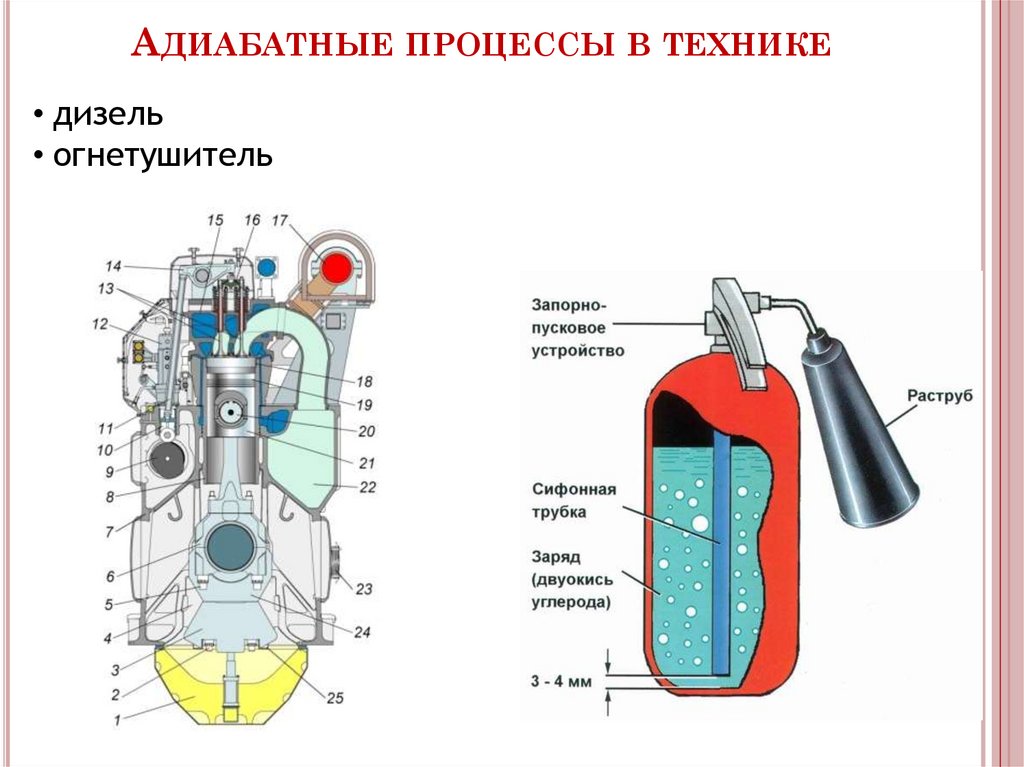
АДИАБАТНЫЕ ПРОЦЕССЫ В ТЕХНИКЕ• дизель
• огнетушитель










 Физика
Физика








