Похожие презентации:
Аммиак. Соли аммония
1.
Игра «Третий лишний»BaCL2
HCL.
CuCL2
H2SO4.
NaNO3
NaOH
NH4Cl
H2CO3,
(NH4)2S
2.
Аммиак и соли аммония.Лабораторный опыт №11
"Качественная реакция на ионы
аммония, сульфат"
3.
Цель обучения:• 11.2.1.9 составлять уравнения реакций,
характеризующих химические свойства
газообразного аммиака и его водного
раствора
4.
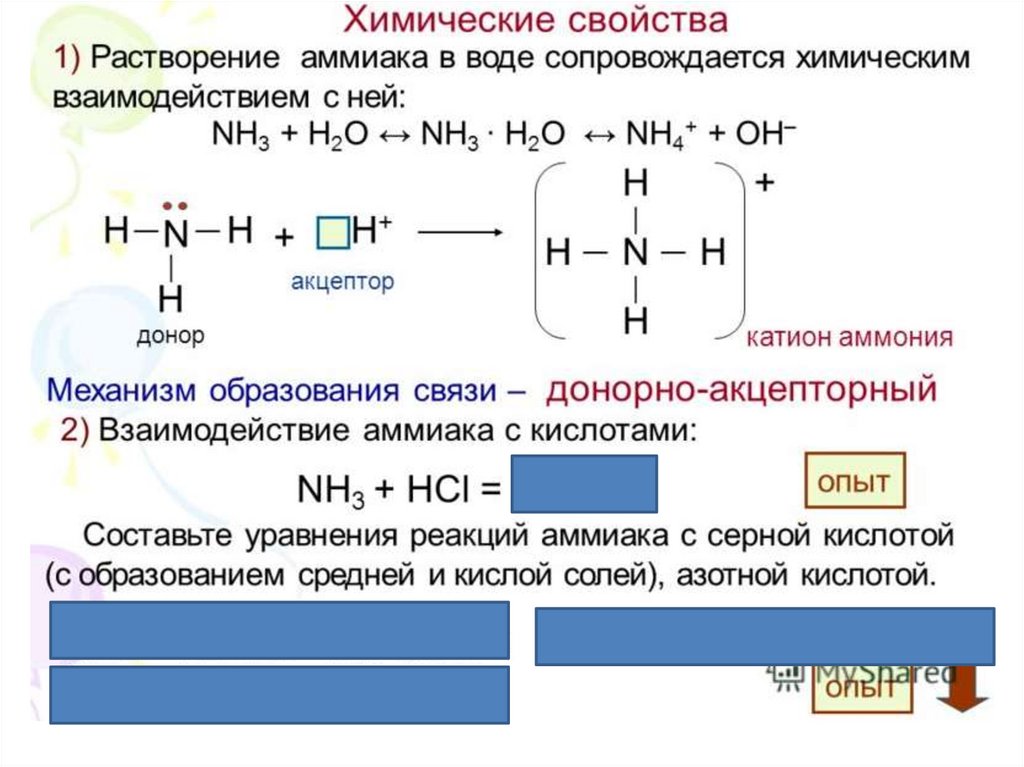
Цели урока:• Описывать химические свойства
аммиака
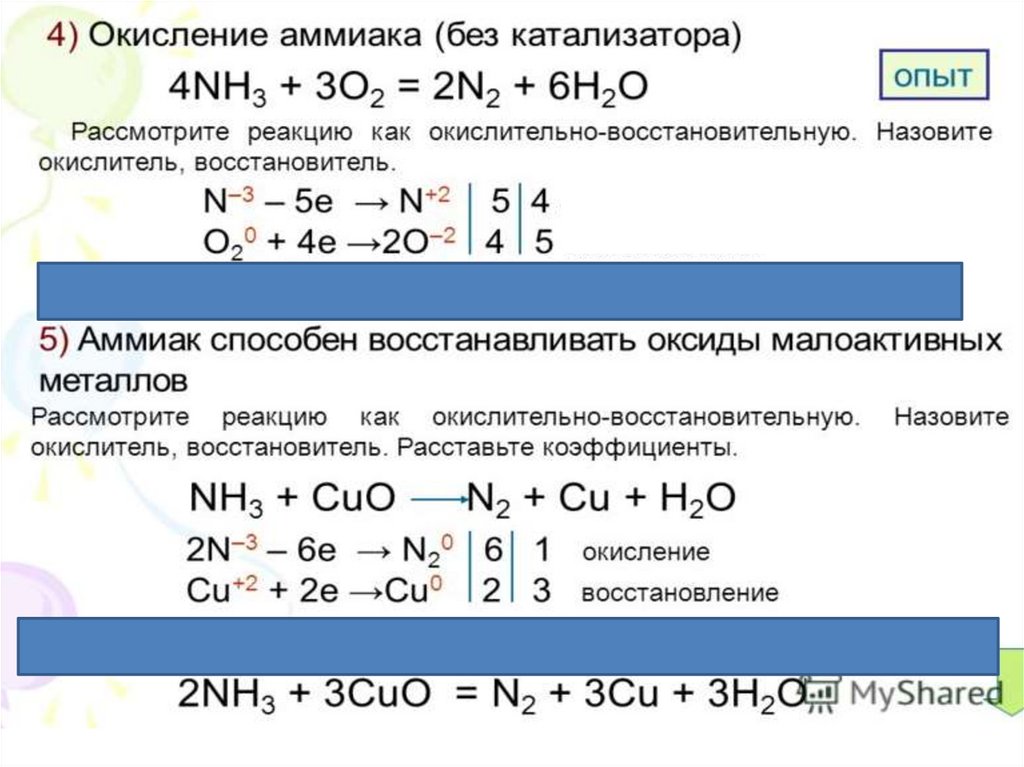
• Записывать уравнения химических
реакций аммиака.
• Собдюдая правила техники
безопасности, выполнить
лабораторный опыт
5.
Опыт фонтан:https://www.youtube.com/watch?v=xKVpspVsfJQ
https://www.youtube.com/watch?v=T5mIcDa6lEI
6.
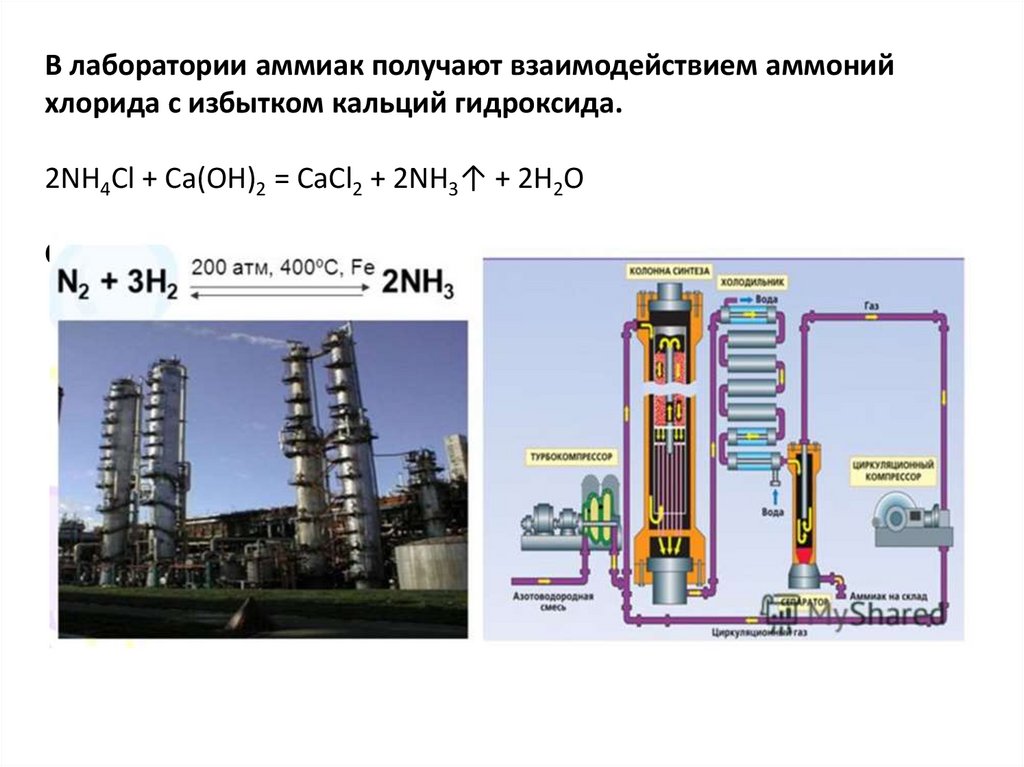
В лаборатории аммиак получают взаимодействием аммонийхлорида с избытком кальций гидроксида.
2NH4Cl + Ca(OH)2 = CaCl2 + 2NH3↑ + 2H2O
Өндірісте аммиакты азот пен сутектен тікелей синтездеп алады.
7.
8.
9.
10.
Лабораторный опыт №11"Качественная реакция на ионы
аммония, сульфат"
11.
Домашняя работа• Работа по рабочему листу на тему
«Аммиак. Соли аммония»







 Химия
Химия








