Похожие презентации:
Карбоновые кислоты. Свойства карбоновых кислот
1.
Карбоновые кислоты.Свойства карбоновых
кислот.
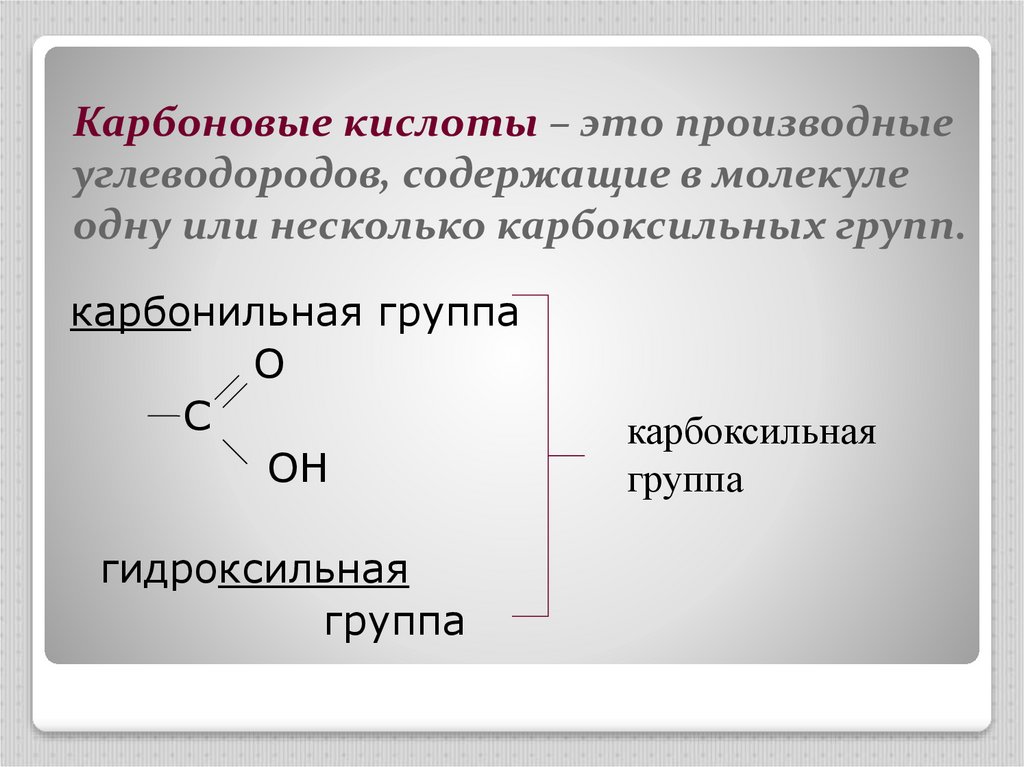
2. Карбоновые кислоты – это производные углеводородов, содержащие в молекуле одну или несколько карбоксильных групп.
карбонильная группаO
C
OH
гидроксильная
группа
карбоксильная
группа
3. Классификация карбоновых кислот
1. По числу карбоксильных групп:Одноосновные : CH3COOH уксусная
Двухосновные : HOOC – CH2 – COOH малоновая
Многоосновные: HOOC – CH2C(OH)(COOH)CH2 –
COOH лимонная
2. По характеру углеводородного радикала:
Предельные : CH3 – (CH2)10 – COOH лауриновая
Непредельные: CH2 = CH – COOH акриловая
Ароматические: C6H5 – COOH бензойная
4. Общая формула одноосновных карбоновых кислот
R – COOH или CnH2n+1COOHНоменклатура:
К названию соответствующего предельного УВ
прибавляется окончание - овая и слово кислота:
Метан – метановая кислота HCOOH
Этан – этановая кислота CH3 - COOH
Пропан – пропановая CH3 – CH2 - COOH
Бутан – бутановая кислота СН3 – СН2 – СН2 - СООН
5. Физические свойства одноосновных карбоновых кислот
Низшие карбоновые кислоты – жидкости с острымзапахом, хорошо растворимые в воде.
С повышением относительной молекулярной массы
растворимость кислот в воде уменьшается, а
температура кипения повышается.
Высшие кислоты, начиная с пеларгоновой (нонановой)
CH3 – (CH2)7 – COOH, - твердые вещества, без запаха,
нерастворимые в воде.
6. Химические свойства кислот
Общие свойства карбоновых кислот аналогичнысоответствующим свойствам неорганических
кислот:
1.
2.
3.
4.
5.
Диссоциируют в водном растворе.
Реагируют с металлами.
Реагируют с основными и амфотерными
оксидами и гидроксидами.
Реагируют с солями более слабых летучих кислот.
Реагируют со спиртами
7. 1. Кислоты диссоциируют на ионы водорода и ионы кислотного остатка:
CH3COOHH+ + CH3COO-
2. Реагируют с металлами:
2CH3COOH + Zn
(CH3COO)2Zn + H2
ацетат цинка
Соли уксусной кислоты – ацетаты
8.
3. Реагируют с основными и амфотерными оксидами игидроксидами.
2HCOOH + MgO
(HCOO)2Mg + H2O
2CH3COOH + Zn(OH)2
(CH3COO)2Zn + H2O
4. Реагируют с солями более слабых летучих кислот.
2HCOOH + Na2SiO3
2HCOONa + H2SiO3
2CH3COOH + Na2CO3
2CH3COONa + H2O + CO2
5. Реагируют со спиртами.
O
O
R C
+ H OR*
R C
+ H2O
OH
O R*
кислота
спирт
сложный эфир
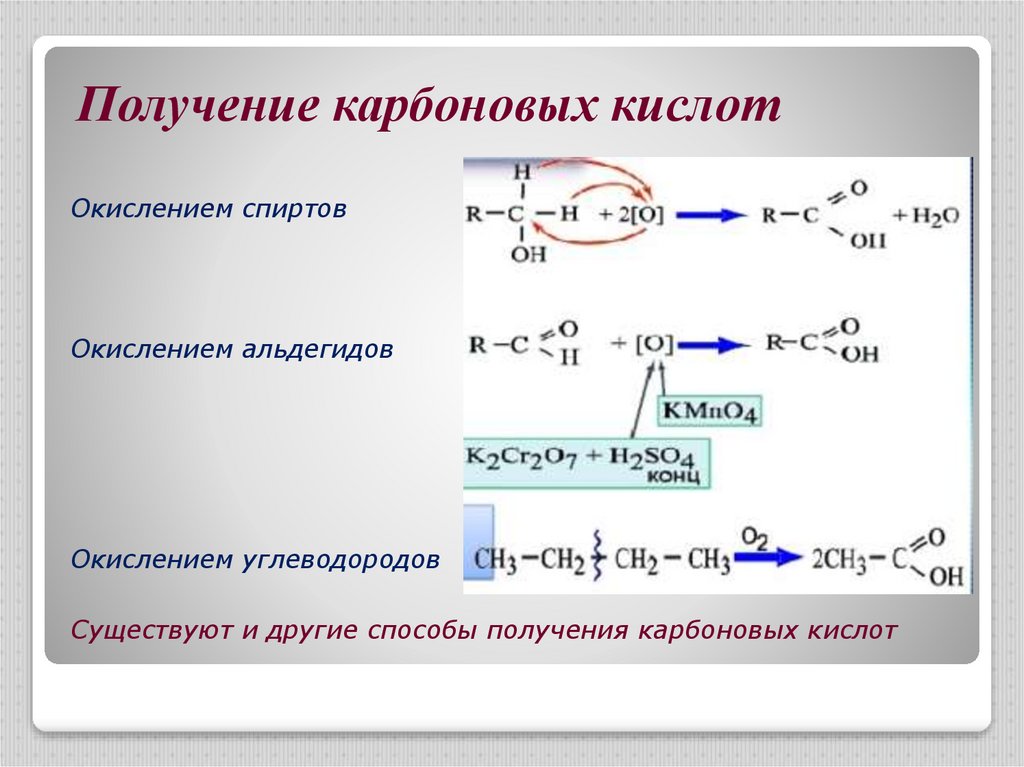
9. Получение карбоновых кислот
Окислением спиртовОкислением альдегидов
Окислением углеводородов
Существуют и другие способы получения карбоновых кислот
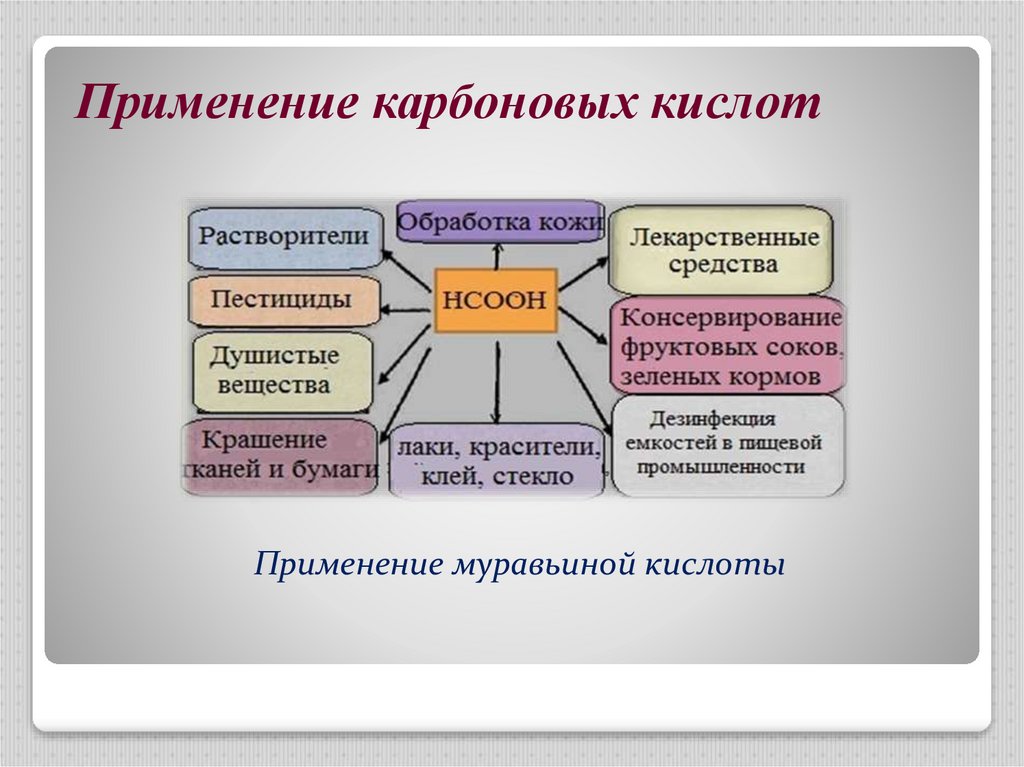
10.
Применение карбоновых кислотПрименение муравьиной кислоты









 Химия
Химия








