Похожие презентации:
Альдегиды, свойства, получение, применение
1. ПРЕЗЕНТАЦИЯ урока химии «Альдегиды, свойства, получение, применение»
2.
Цели урокаПродолжить
знакомить
учащихся
с
кислородсодержащими
органическими соединениями на примере альдегидов.
• Познакомить
учащихся
с
применением
ацетальдегида на основе их свойств.
формальдегида
и
• Продолжить развивать умения характеризовать строение и
химические свойства изученных органических соединений, объяснять
зависимость свойств веществ от их состава и строения, выполнять
химический эксперимент, соблюдая правила безопасного обращения с
веществами и лабораторным оборудованием, проводить наблюдения,
делать выводы.
• Продолжить формирование ключевых компетентностей учащихся
• Воспитывать бережное отношение к своему здоровью, здоровью
окружающих.
3.
Повторим?!CnH2n
ЕН
АЛКАНЫ
CnH2n-6
ИН
АЛКЕНЫ
CnH2n+2
АН
АЛКИНЫ
CnH2n+1OH
ОЛ
АРЕНЫ
БЕНЗОЛ
CnH2n-2
СПИРТЫ
O
???
CnH2n+1C
H
4.
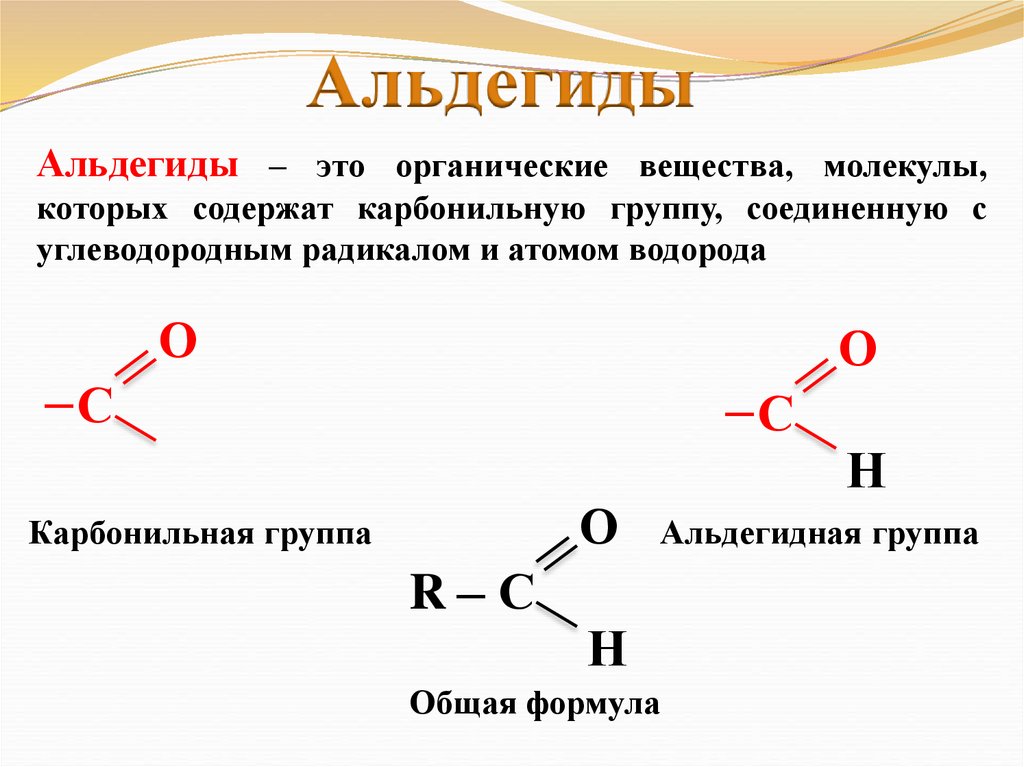
АльдегидыАльдегиды – это органические вещества, молекулы,
которых содержат карбонильную группу, соединенную с
углеводородным радикалом и атомом водорода
О
О
─С
─С
О
Карбонильная группа
R─ С
Н
Альдегидная группа
Н
Общая формула
5.
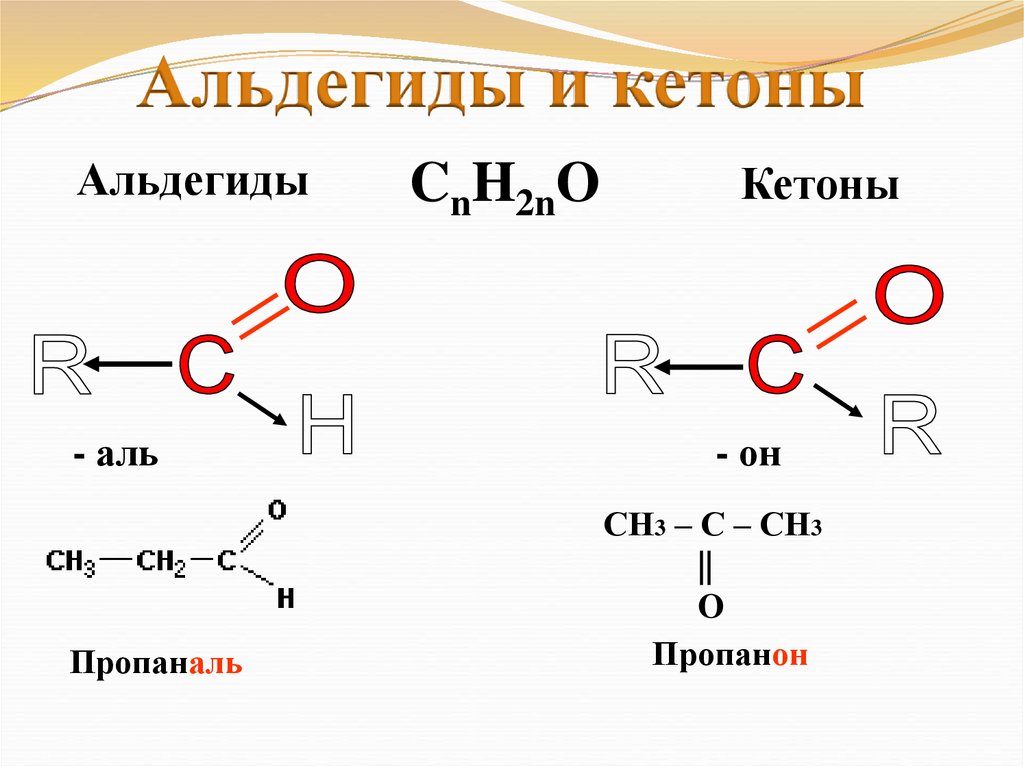
Альдегиды и кетоныАльдегиды
- аль
Пропаналь
CnH2nO
Кетоны
- он
СН3 – С – СН3
||
O
Пропанон
6.
Альдегиды.ГомологиМетаналь (формальдегид)
Этаналь (ацетальдегид)
Пропаналь
Бутаналь
Пентаналь
7.
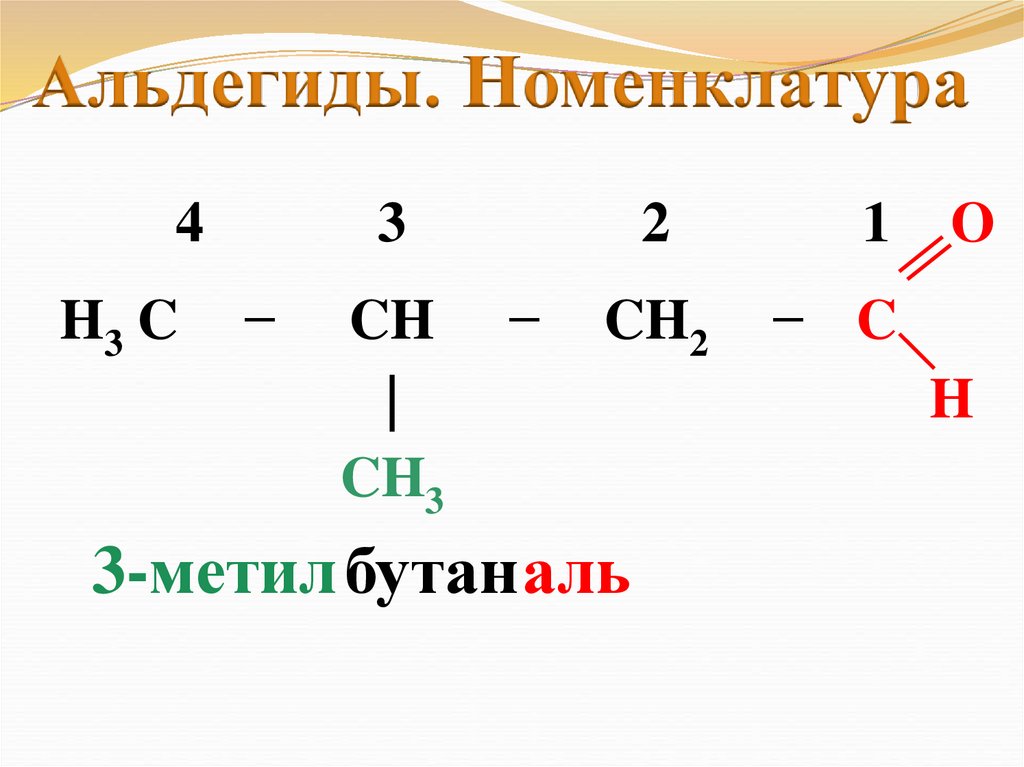
Альдегиды. Номенклатура4
H3 C
3
−
CH
|
CH3
2
−
CH2
3-метил бутаналь
1
O
− C
H
8.
Альдегиды.Номенклатура1. ВЫБОР ГЛАВНОЙ ЦЕПИ
2. НУМЕРАЦИЯ ГЛАВНОЙ ЦЕПИ (НАЧИНАЕТСЯ
С АТОМА УГЛЕРОДА ФУНКЦИОНАЛЬНОЙ ГРУПП
3. НАЗЫВАЮТСЯ ЗАМЕСТИТЕЛИ И ИХ ПОЛОЖЕНИЕ
В АЛФАВИТНОМ ПОРЯДКЕ
4. НАЗЫВАЕТСЯ УГЛЕВОДОРОД ПО ЧИСЛУ
АТОМОВ УГЛЕРОДА В ЦЕПИ С СУФФИКСОМ -АЛЬ
9.
Альдегиды. Изомерия.Вид изомерии
По углеродному
скелету,
начиная с С4
Межклассовая с
кетонами,
начиная с С3
Формулы изомеров
10.
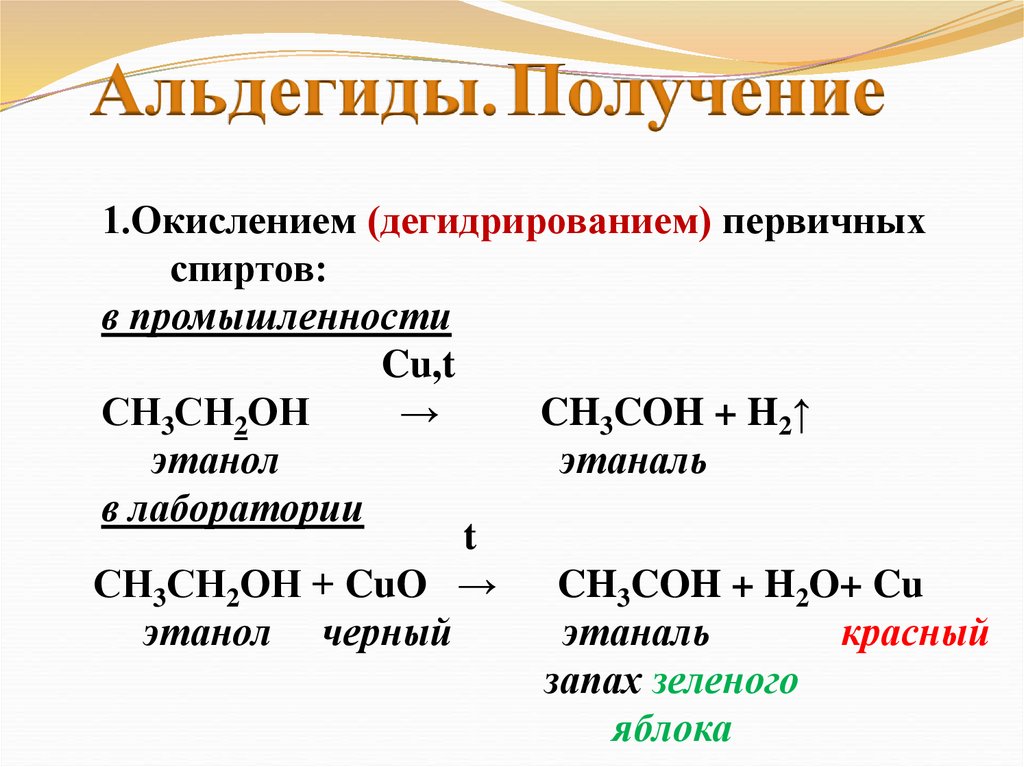
Альдегиды.Получение1.Окислением (дегидрированием) первичных
спиртов:
в промышленности
Cu,t
СН3СН2ОН
→
CH3COH + H2↑
этанол
этаналь
в лаборатории
t
СН3СН2ОН + CuO →
CH3COH + H2O+ Cu
этанол черный
этаналь
красный
запах зеленого
яблока
11.
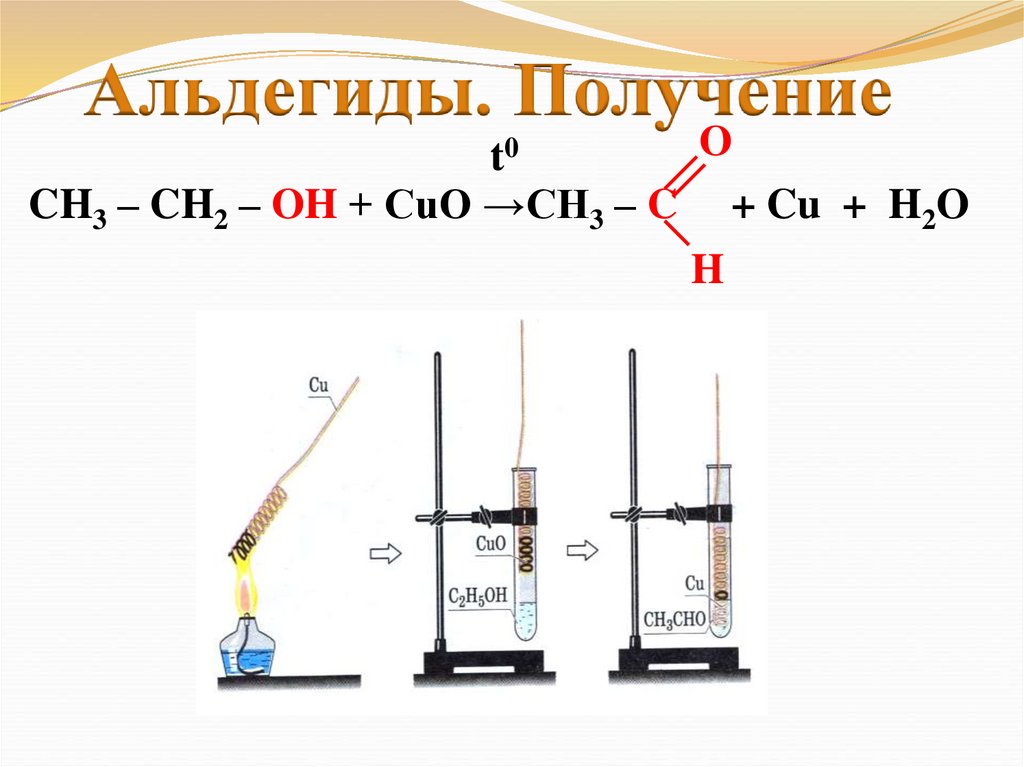
Альдегиды. ПолучениеO
t0
CH3 – CH2 – OH + CuO →CH3 – C + Cu + H2O
H
12.
Альдегиды. Получение2. Реакция Кучерова:
Hg2+
СН≡СН + Н2О →
СН3СОН
ацетилен
уксусный альдегид
13.
Альдегиды.СвойстваФизические свойства
С1
– газ с резким запахом;
С2 – С3 – жидкости с резким запахом;
С4 – С6 – жидкости с неприятным запахом;
>С6
– твердые, нерастворимые в воде с цветочным
запахом (применяются в парфюмерии).
НСОН, СН3СОН – растворимы в воде неограниченно,
температуры кипения ниже, чем у
соответствующих спиртов.
14.
Альдегиды. СвойстваХимические свойства альдегидов
Реакции
присоединения
Гидрирование
Реакции
окисления
Реакция
«серебряного
зеркала»
Присоединение
NaHSO3
Реакции
поликонденсации
Реакции
полимеризации
Окисление
Cu(OH)2
15.
Альдегиды. СвойстваРеакции окисления
R – C = O + [O]
Ι
H
альдегид
НСООН
СН3СООН -
→
R–C=O
Ι
OH
карбоновая
кислота
метановая (муравьиная) кислота
этановая (уксусная) кислота
16.
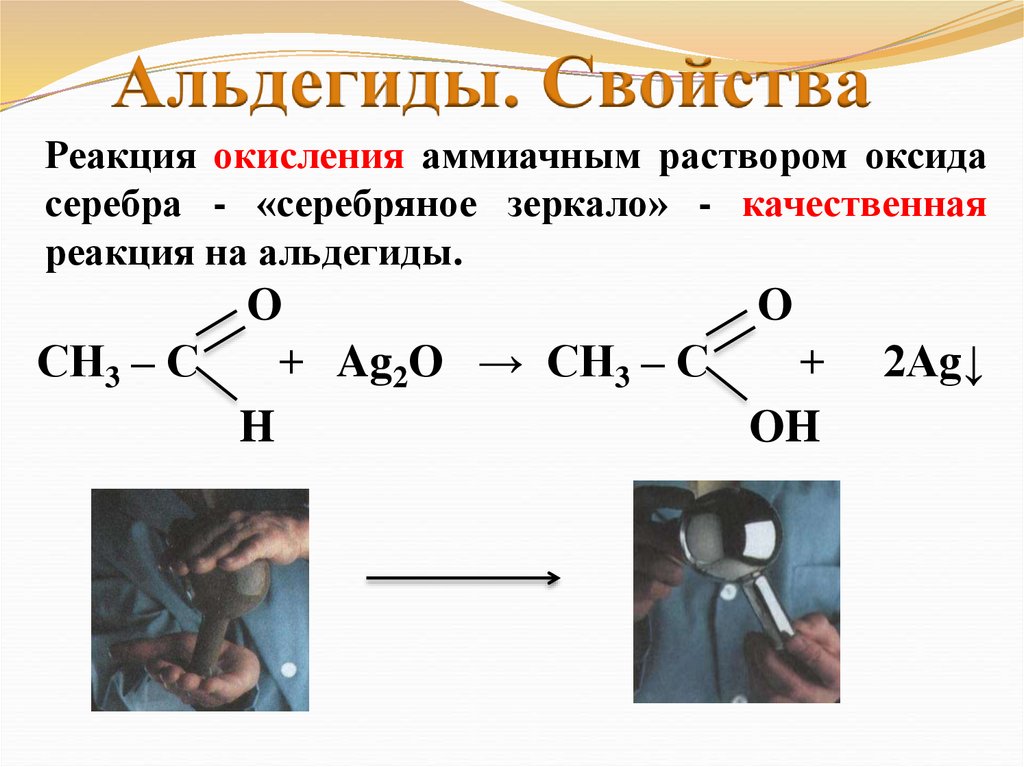
Альдегиды. СвойстваРеакция окисления аммиачным раствором оксида
серебра - «серебряное зеркало» - качественная
реакция на альдегиды.
O
O
СН3 – С
+ Ag2O → СН3 – С
+
H
OH
2Ag↓
17.
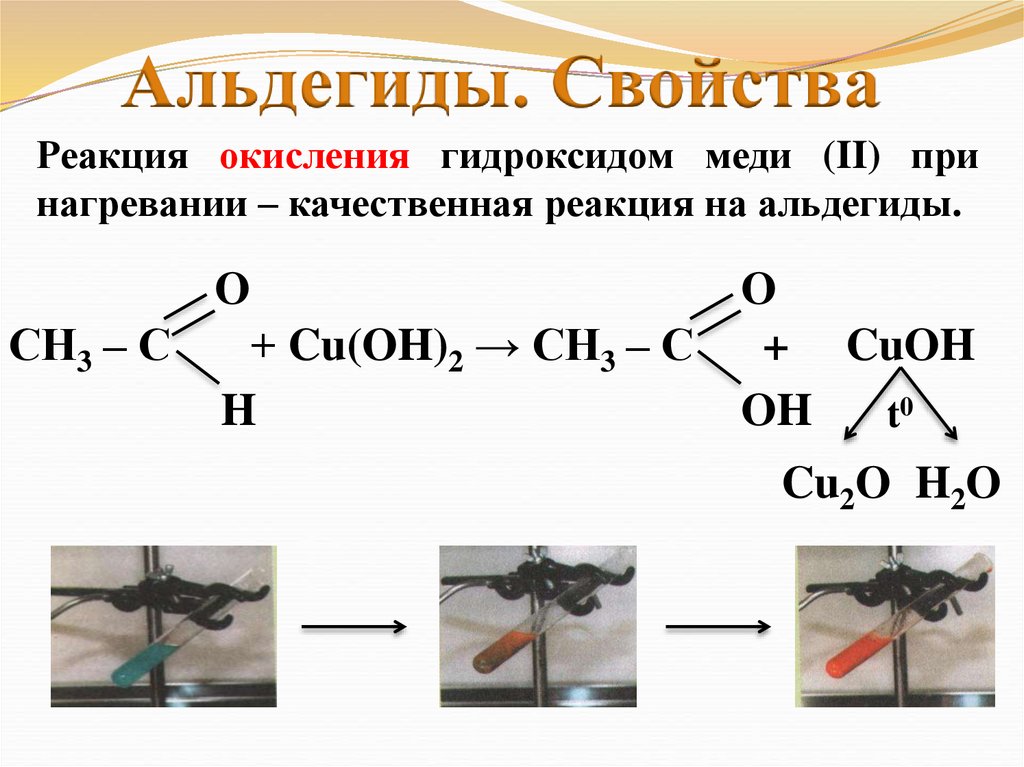
Альдегиды. СвойстваРеакция окисления гидроксидом меди (II) при
нагревании – качественная реакция на альдегиды.
O
СН3 – С
+ Cu(OH)2 → СН3 – С
H
O
+ CuOH
OH
t0
Cu2O H2O
18.
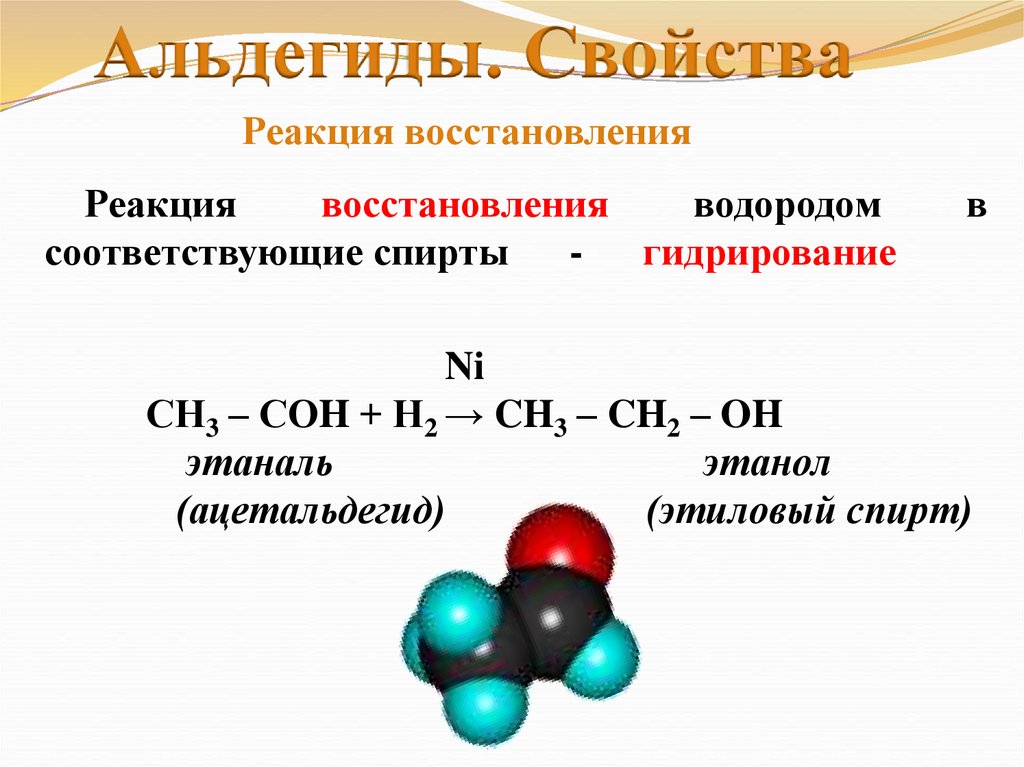
Альдегиды. СвойстваРеакция восстановления
Реакция
восстановления
водородом
соответствующие спирты
гидрирование
в
Ni
СН3 – СОH + Н2 → CH3 – CH2 – OH
этаналь
этанол
(ацетальдегид)
(этиловый спирт)
19.
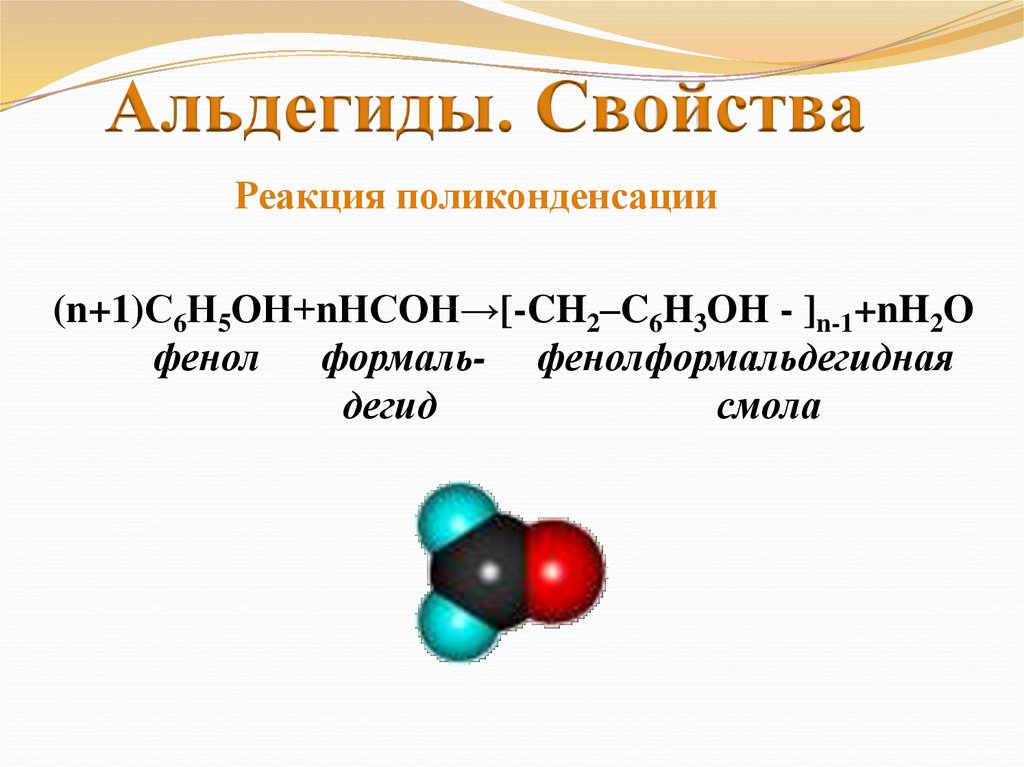
Альдегиды. СвойстваРеакция поликонденсации
(n+1)С6Н5ОН+nНСОН→[-CH2–C6H3OH - ]n-1+nH2O
фенол
формаль- фенолформальдегидная
дегид
смола
20.
Альдегиды. ПрименениеФенолформальдегидные
смолы
Сельское
хозяйство
Формальдегид
Кожевенная
промышленность
Медицина
21.
Альдегиды. ПрименениеФормальдегид
22.
Уксуснаякислота
Этиловый
спирт
Уксусный
альдегид
Пластмассы
Ацетатное
волокно
23.
Альдегиды. ПрименениеАцетальдегид
24.
Альдегиды в природеОтличительной чертой многих альдегидов является их
запах. Высшие альдегиды, особенно непредельные и
ароматические, входят в состав эфирных масел и содержатся
в цветах, фруктах, плодах, душистых и пряных растениях.
Их используют в пищевой промышленности и парфюмерии.
25.
Альдегиды в природеБулочки ванильные, корицы аромат,
Амаретто, шоколад
Альдегидов вкус таят.
В землянике и кокосе,
И в жасмине, и в малине,
И в духах, и в еде
Альдегидов след везде.
Что за запах, что за прелесть,
И откуда эта свежесть?!
Это высший альдегид
Аромат вам свой дарит!
26.
Альдегиды в природеВанилин
В плодах ванили содержится
ароматический
альдегид,
который
придает
им
характерный запах.
Ванилин
применяется
в
парфюмерии,
кондитерской
промышленности,
для
маскирования
запахов
некоторых продуктов.
27.
Альдегиды в природеЦитраль
Запах цитрусовых обусловлен данным диеновым
альдегидом. Его применяют в качестве отдушки средств
бытовой химии, косметических и парфюмерных веществ.
28.
Альдегиды в природеКоричный альдегид
Коричный альдегид содержится в масле корицы, его
получают перегонкой коры дерева корицы .
Применяется в кулинарии в виде палочек или порошка.
29.
Альдегиды в природеБензальдегид
Бензальдегид – жидкость с запахом
горького миндаля.
Встречается в косточках и семечках(абрикос,
персик)
30.
Альдегиды в природеФенилэтаналь
Фенилэтаналь по сравнению с
бензальдегидом лучше соответствует
рецептору цветочного запаха.
Фенилэтаналь пахнет гиацинтом.
31.
Кетоны в природеГептанон-2
Это соединение представляет собой жидкость с
гвоздичным запахом.
Гептаноном-2 обусловлен запах многих плодов
и
молочных продуктов, например, сыра «Рокфор»
32.
Кетоны в природеn-Гидроксифенилбутанон-2
Этот кетон обуславливает в основном запах
спелых ягод малины.
Его включают в состав синтетических
душистых композиций
33.
Выполни задания теста1. ( Общая формула альдегидов :
А. RCOH
В. R1COR2
Б. RCOOH
Г. ROH
2. Функциональная группа альдегидов :
А. - ОН
В. – СОН
Б. - СО
Г. – СООН
3. Формула формальдегида :
А.НСООН
В.СН3СОН
Б.НСОН
Г.СН3СООН
4. Вещество состава СН3СОН называется:
А. Метаналь
В. Уксусная кислота
Б. Этаналь
Г. Ацетальдегид
34.
5. Продуктами восстановления альдегидов водородом(катализатор Ni) являются :
А. Сложные эфиры
В. Одноатомные спирты
Б. Карбоновые кислоты Г. Кетоны
6. В реакцию «серебряного зеркала» могут вступать :
А. Фенол
В. Этанол
Б. Метаналь
Г. Этаналь
7. Продуктом окисления этанола является :
А. Ацетон
В. Уксусный альдегид
Б. Уксусная кислота
Г. Диэтиловый эфир
8. Правой частью уравнения СН3СОН + 2Cu(ОН)2↓→ :
А. НСООН + Cu2O↓ + 2H2O
Б. CH3COOH + Cu2O↓ + 2H2O

























 Химия
Химия








