Похожие презентации:
Основания, их классификация и свойства
1.
Из нас не сваришь супа,Содержим мы гидроксогруппу,
И активного металла
В нашей формуле немало.
Красим лакмус в синий цвет,
Мы опасны, спору нет.
2. Тема урока:
Основания,их классификация
и свойства
3. Определение оснований
KOHCa(OH)2
Fe(OH)3
Содержат ионы
металла
группа – ОН
(гидроксогруппа)
4.
Основания-
сложные вещества
состоящие из
положительного иона
металла и одной или
нескольких
гидроксогрупп
(гидроксид-ионов).
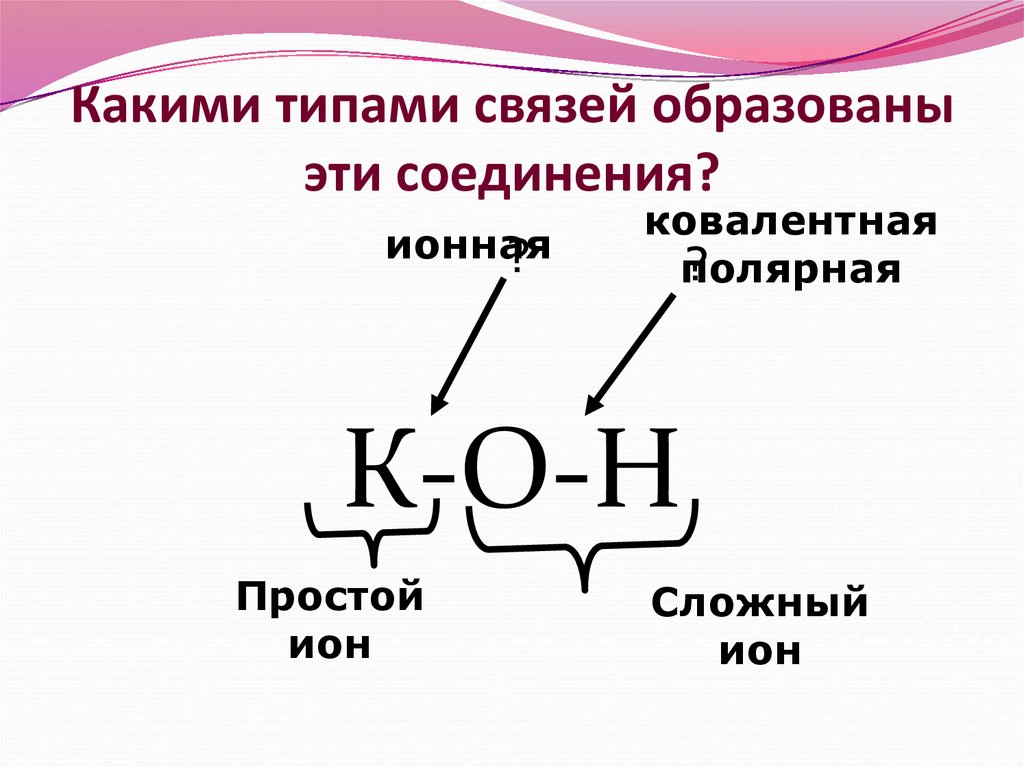
5. Какими типами связей образованы эти соединения?
ионная?
ковалентная
?
полярная
К-О-Н
Простой
ион
Сложный
ион
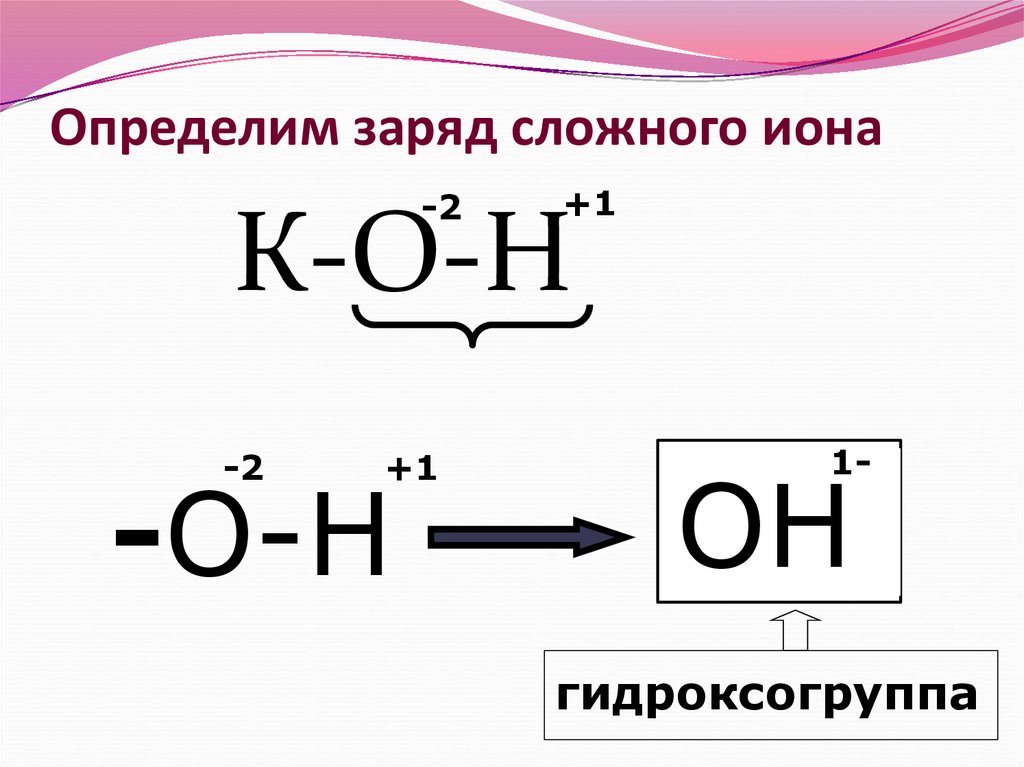
6. Определим заряд сложного иона
-2+1
К-О-Н
-2
+1
-О-Н
1-
ОН
гидроксогруппа
7. Классификация гидроксидов:
ГидроксидыАмфотерные
гидроксиды
Основания
Не растворимые
в воде
Щелочи
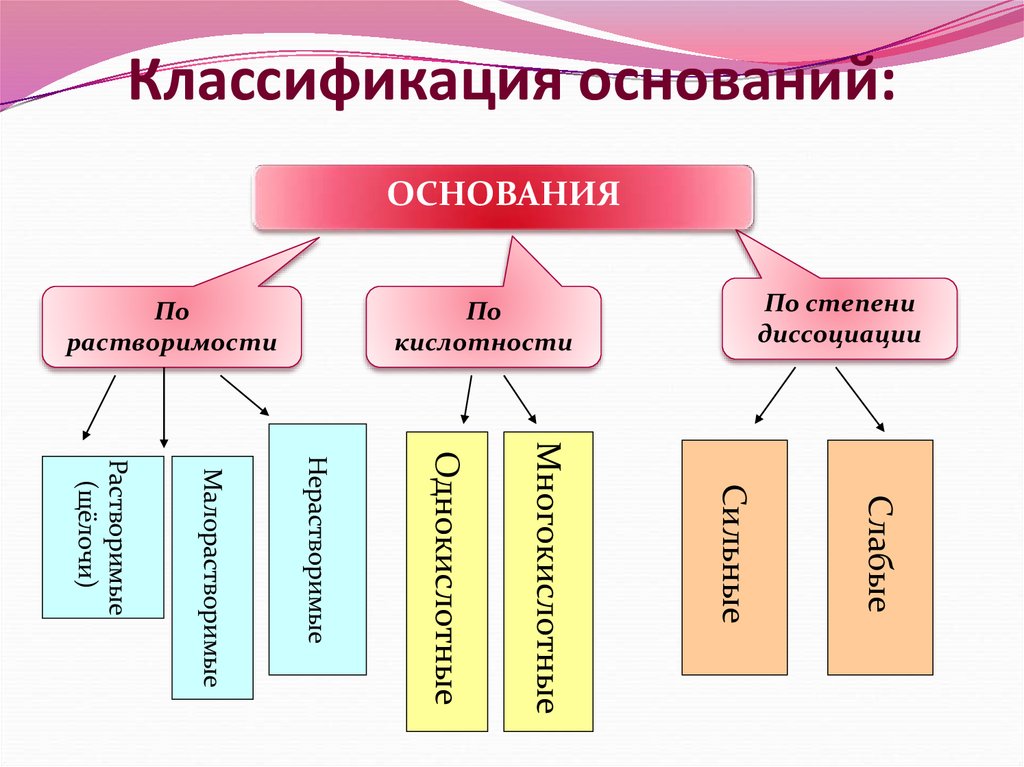
8. Классификация оснований:
ОСНОВАНИЯПо степени
диссоциации
По
кислотности
По
растворимости
Слабые
Сильные
Многокислотные
Однокислотные
Нерастворимые
Малорастворимые
Растворимые
(щёлочи)
9. Правила Т.Б. при работе со щелочами
При попадании раствора щелочи накожу, может образоваться язва.
Чтобы этого не случилось,
немедленно смойте ее большим
количеством проточной воды и
протрите поврежденный участок
слабым раствором борной кислоты.
10. Как отличить бесцветный прозрачный раствор гидроксида калия от воды?
Индикаторы – вещества изменяющие цвет взависимости от среды.
индикатор
Нейтральная
среда
фенолфталеин бесцветный
Щелочная
среда
малиновый
Метилоранжевый
оранжевый
желтый
Лакмус
фиолетовый
фиолетовый
синий
11.
Качественные реакции – это реакции, спомощью которых распознают определенные
вещества.
Все щёлочи можно определить с
помощью особых реактивов –
индикаторов-веществ, которые
изменяют свой цвет в зависимости
от среды раствора
12. Химические свойства оснований
1. NaOH + HCl =NaCl +H2O
1. Основание + кислота = соль + вода (р-ция обмена)
2. 2NaOH + CuSO4 = Na SO +Cu(OH)
2
4
2
2. Щёлочь + соль = новая соль +новое основание (р-ция обмена)
t
3. Cu(OH)2 = СuO + H2O
3. Нерастворимые основания при нагревании разлагаются
на оксид и воду
13. Домашнее задание
Параграф 41, 42 с. 145 тестовые задания, с.135 упр.2выучить свойства и определения
14. Рефлексия
Сегодня на уроке я узнал, ...По этой теме я хочу еще узнать……..











 Химия
Химия








