Похожие презентации:
Химическая связь (лекция 4)
1. Донской государственный технический университет Кафедра «Химия» ________________________________________________________
ХИМИЧЕСКАЯСВЯЗЬ
2.
Донской государственный технический университетКафедра «Химия»
________________________________________________________
Виды химической связи:
1. Ионная связь
2. Ковалентная связь
3. Водородная связь
4. Металлическая связь
5. Силы Ван-дер-Ваальса
3.
Донской государственный технический университетКафедра «Химия»
________________________________________________________
Ионная связь
Вальтер Коссель (нем. Walther Kossel)
(4 января 1888 — 22 мая 1956)
В 1916 выдвинул гипотезу, которая
легла в основу теории ионной
химической связи и гетеровалентности
4.
Донской государственный технический университетКафедра «Химия»
________________________________________________________
Ионная связь
Na+Cl=NaCl
1.Образование ионов
Na – ē = Na+
Cl + ē = Cl2. Образование молекулы
Na+ + Cl- = NaCl
(1s22s22p63s1) - ē = 11Na+ (1s22s22p6)
17Cl (1s22s22p63s23p5) + ē = 17Cl- (1s22s22p63s23p6)
11Na
5.
Донской государственный технический университетКафедра «Химия»
________________________________________________________
Ковалентная связь
Метод валентных связей (метод ВС)
Гилберт Ньютон Льюис (англ. Gilbert Newton Lewis)
(23 октября 1875 — 23 марта 1946)
В 1916 Льюис высказал идею, что ковалентная
химическая связь образуется за счёт обобществления
пары электронов, то есть электронная плотность
распределяется между двумя атомами
6.
Донской государственный технический университетКафедра «Химия»
________________________________________________________
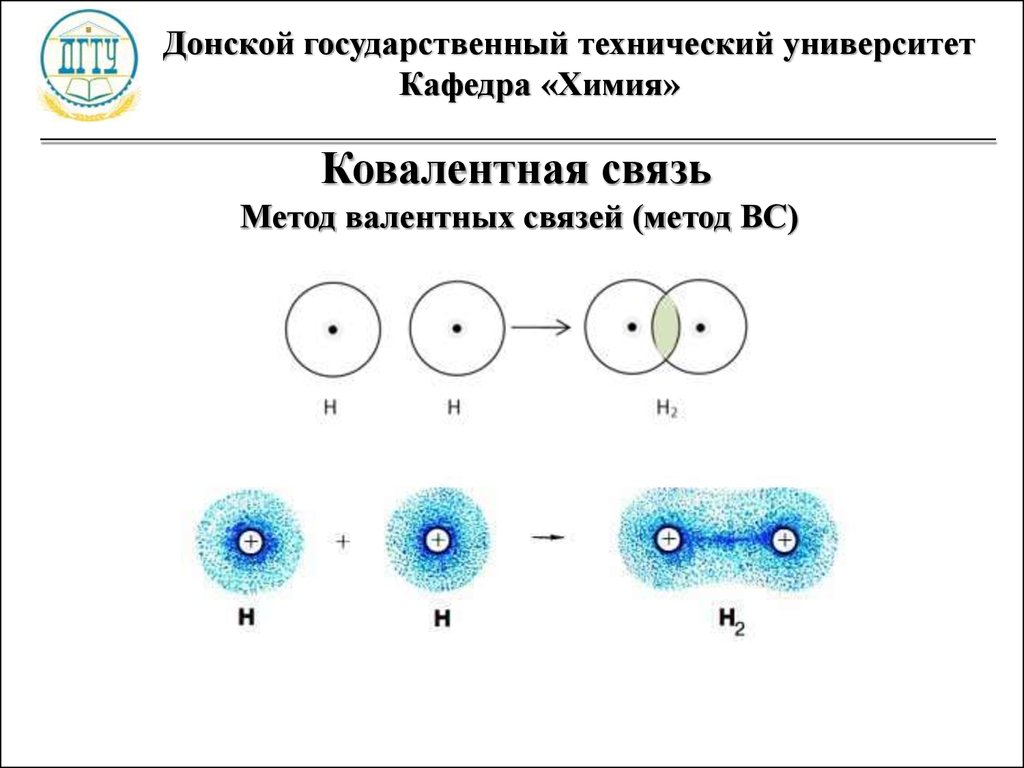
Ковалентная связь
Метод валентных связей (метод ВС)
7.
Донской государственный технический университетКафедра «Химия»
________________________________________________________
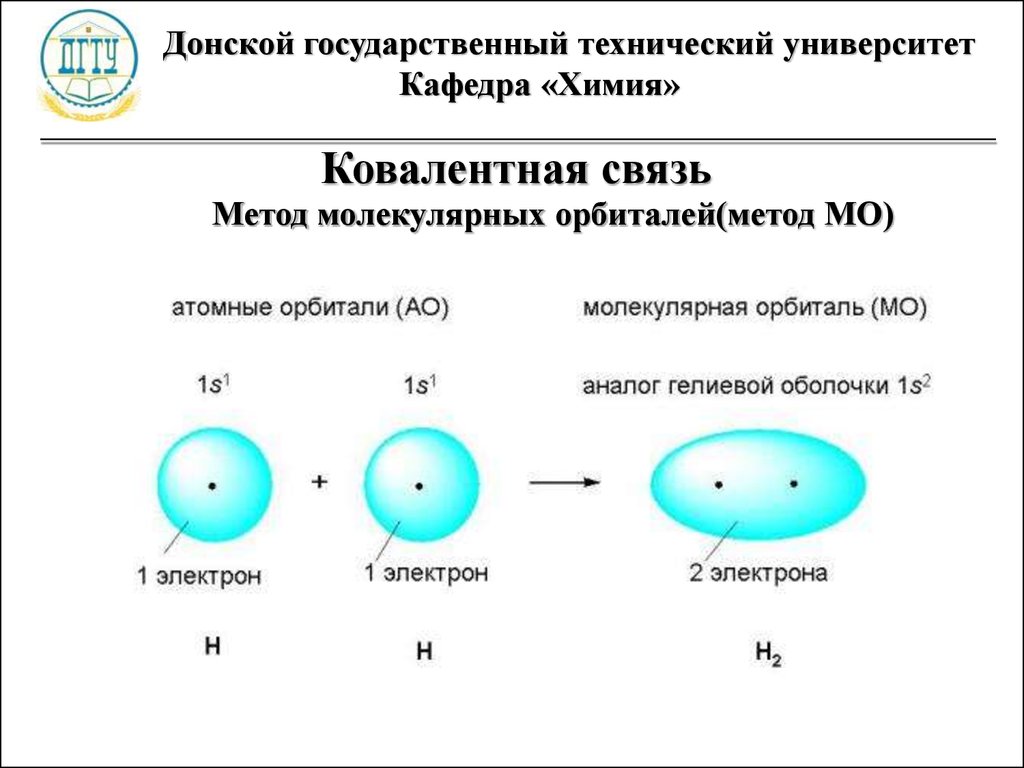
Ковалентная связь
Метод молекулярных орбиталей(метод МО)
8.
Донской государственный технический университетКафедра «Химия»
________________________________________________________
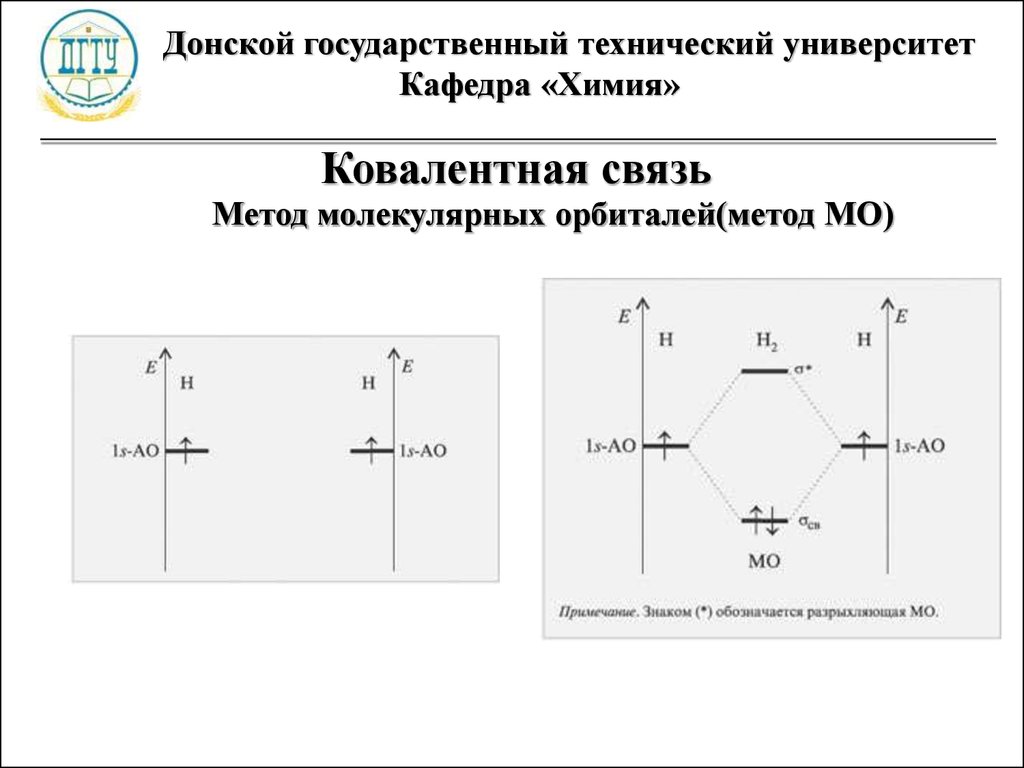
Ковалентная связь
Метод молекулярных орбиталей(метод МО)
σ - связь
π - связь
9.
Донской государственный технический университетКафедра «Химия»
________________________________________________________
Ковалентная связь
Метод молекулярных орбиталей(метод МО)
10.
Донской государственный технический университетКафедра «Химия»
________________________________________________________
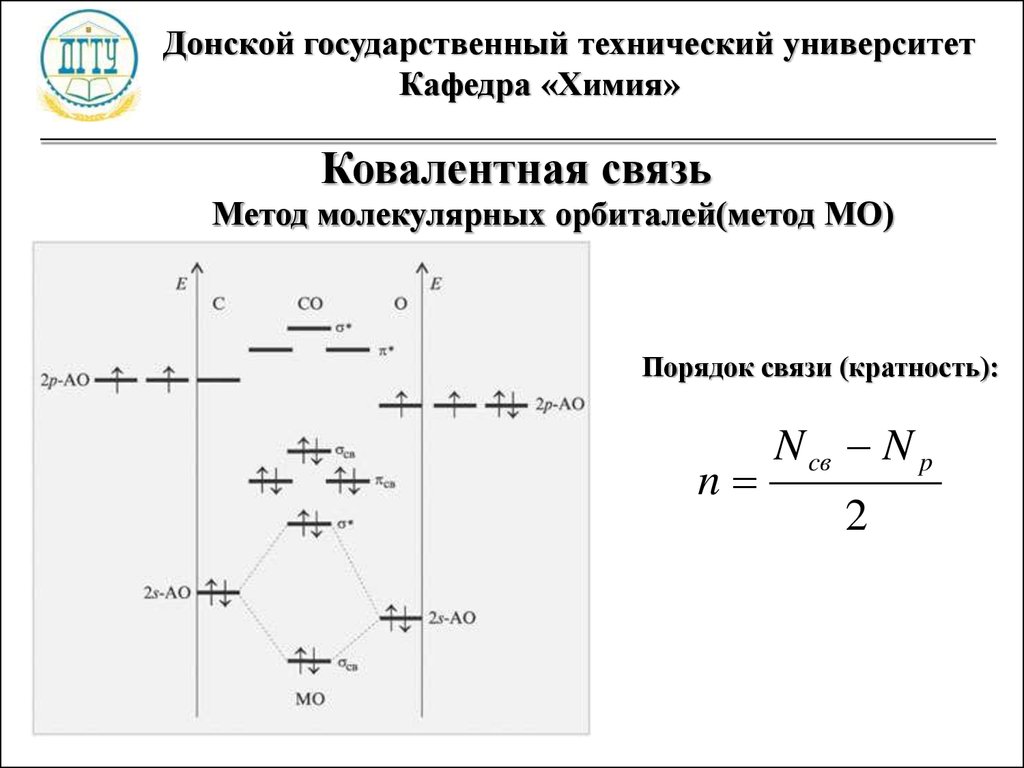
Ковалентная связь
Метод молекулярных орбиталей(метод МО)
11.
Донской государственный технический университетКафедра «Химия»
________________________________________________________
Ковалентная связь
Метод молекулярных орбиталей(метод МО)
Порядок связи (кратность):
n
N cв N p
2
12.
Донской государственный технический университетКафедра «Химия»
________________________________________________________
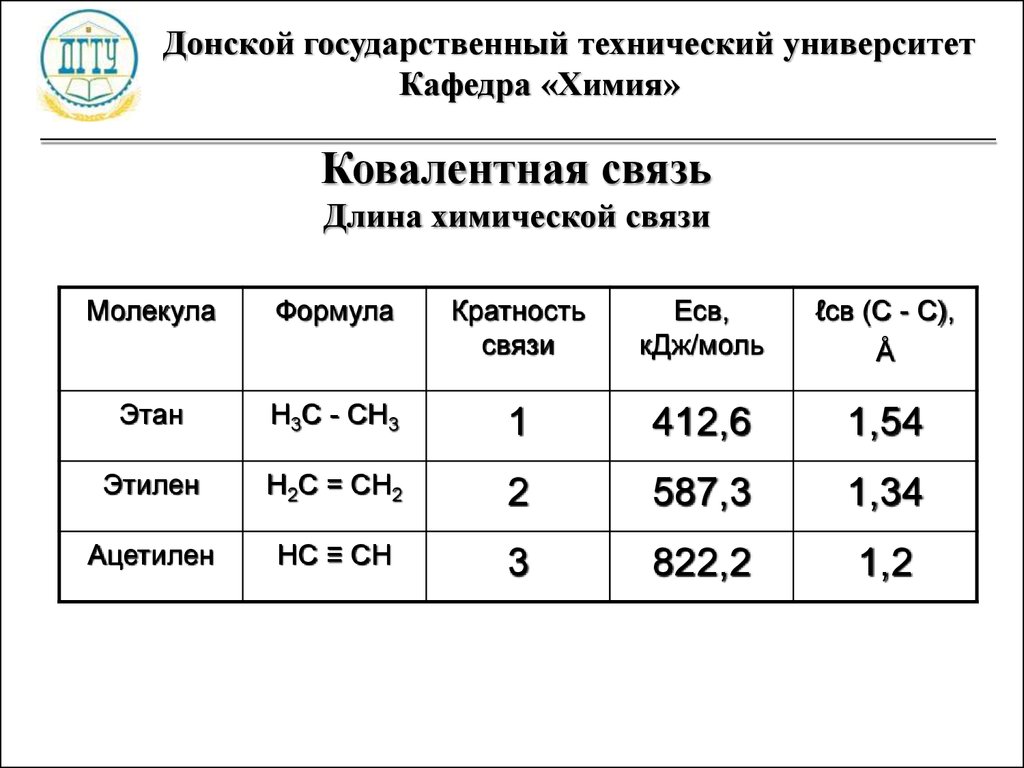
Ковалентная связь
Длина химической связи
Молекула
Формула
Кратность
связи
Есв,
кДж/моль
ℓсв (С - С),
Å
Этан
Н3С - СН3
1
412,6
1,54
Этилен
Н2С = СН2
2
587,3
1,34
Ацетилен
НС ≡ СН
3
822,2
1,2
13.
Донской государственный технический университетКафедра «Химия»
________________________________________________________
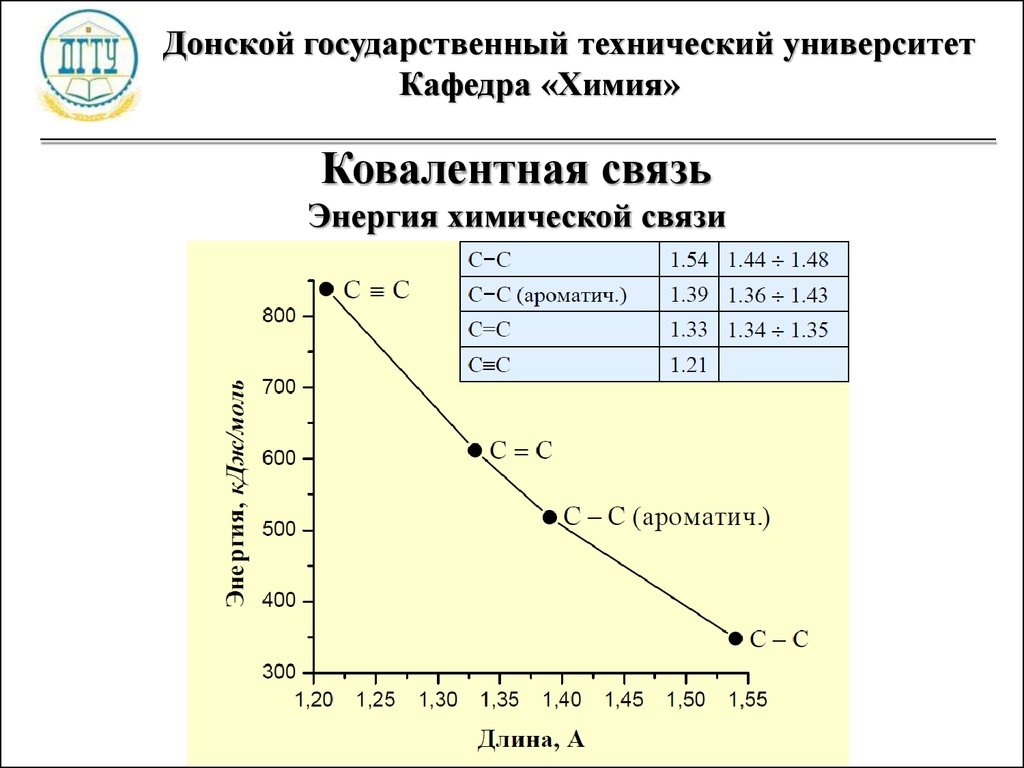
Ковалентная связь
Энергия химической связи
14.
Донской государственный технический университетКафедра «Химия»
________________________________________________________
15.
Донской государственный технический университетКафедра «Химия»
________________________________________________________
16.
Донской государственный технический университетКафедра «Химия»
________________________________________________________
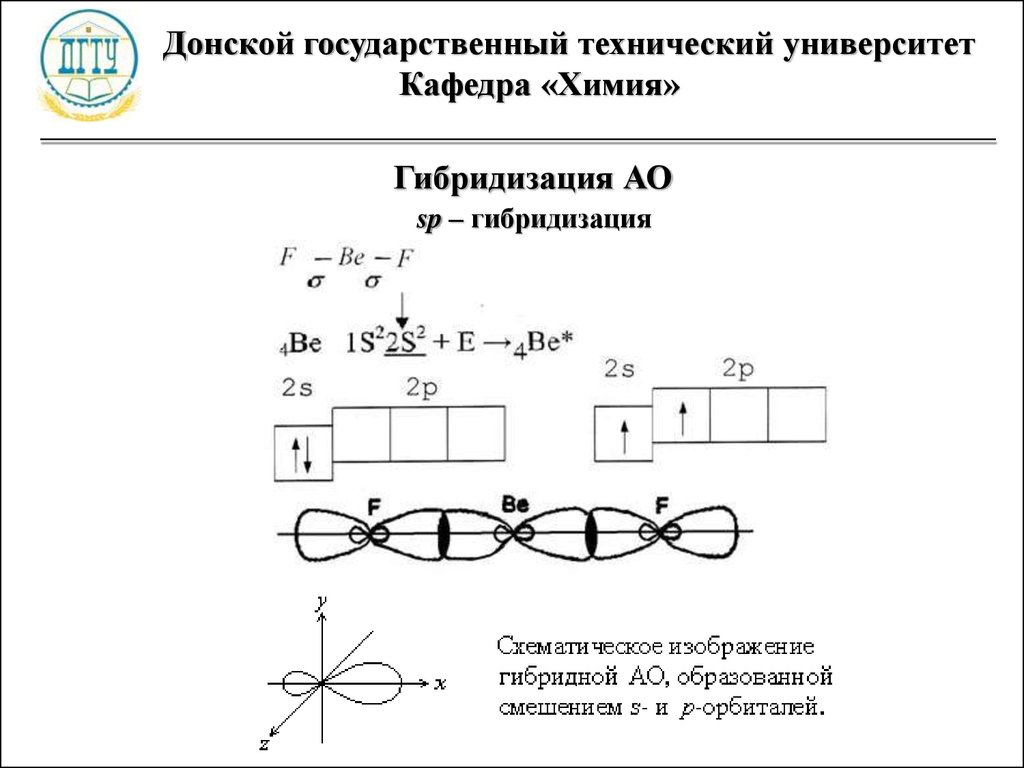
Гибридизация АО
sp – гибридизация
17.
Донской государственный технический университетКафедра «Химия»
________________________________________________________
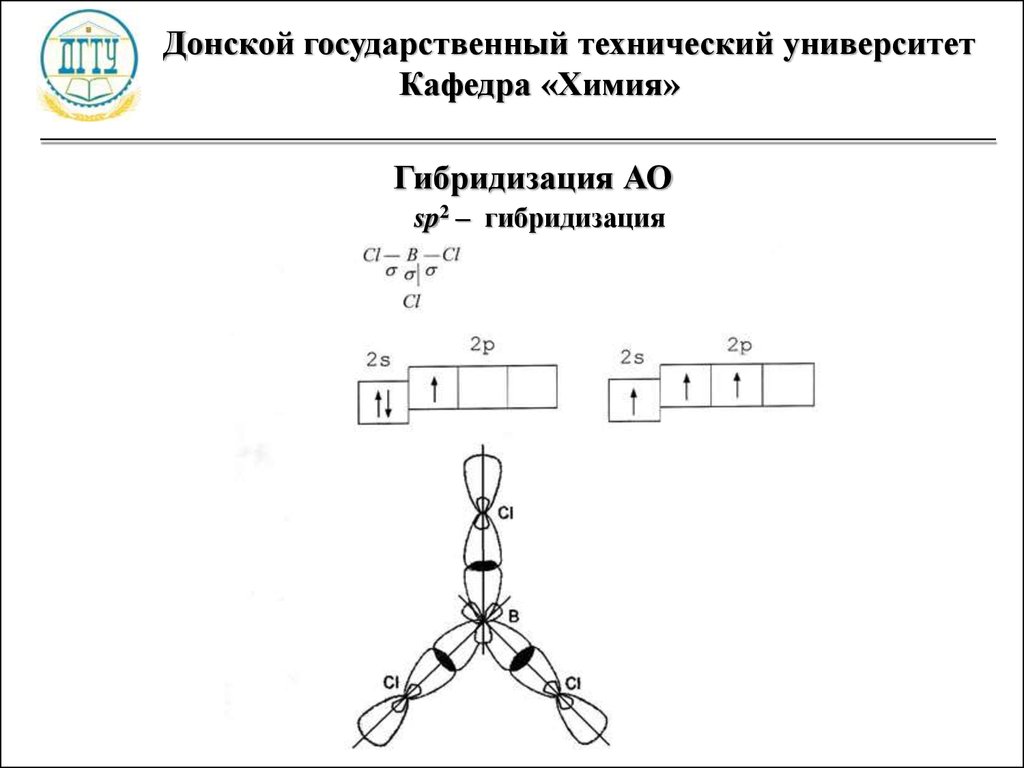
Гибридизация АО
sp2 – гибридизация
18.
Донской государственный технический университетКафедра «Химия»
________________________________________________________
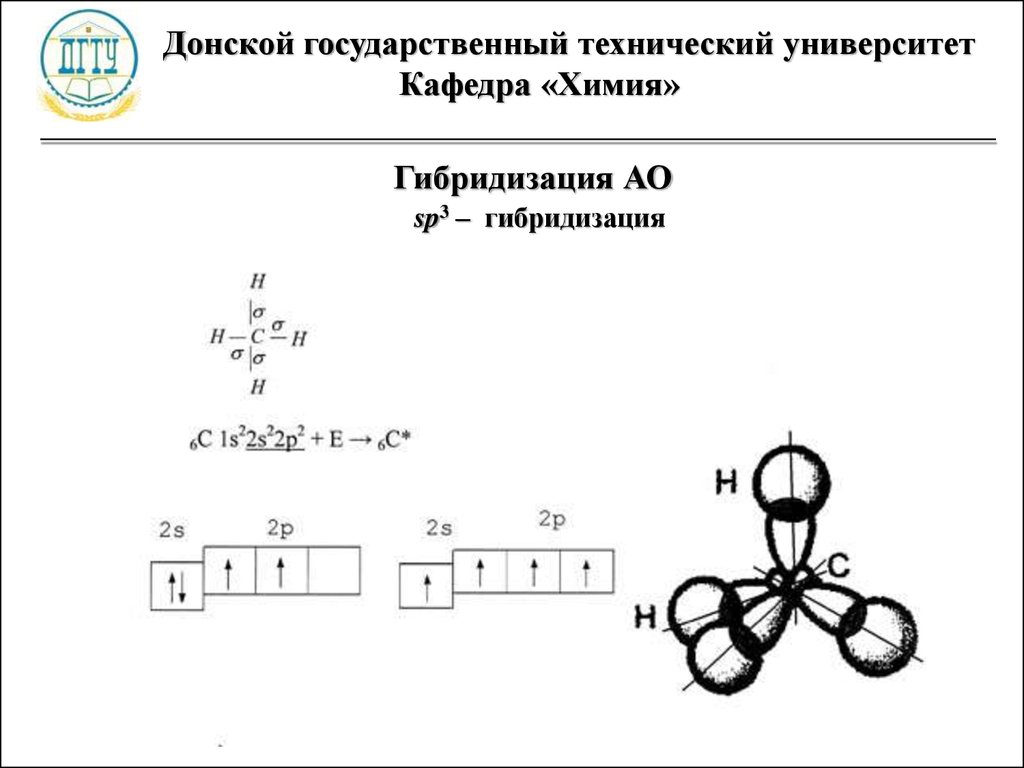
Гибридизация АО
sp3 – гибридизация
19.
Донской государственный технический университетКафедра «Химия»
________________________________________________________
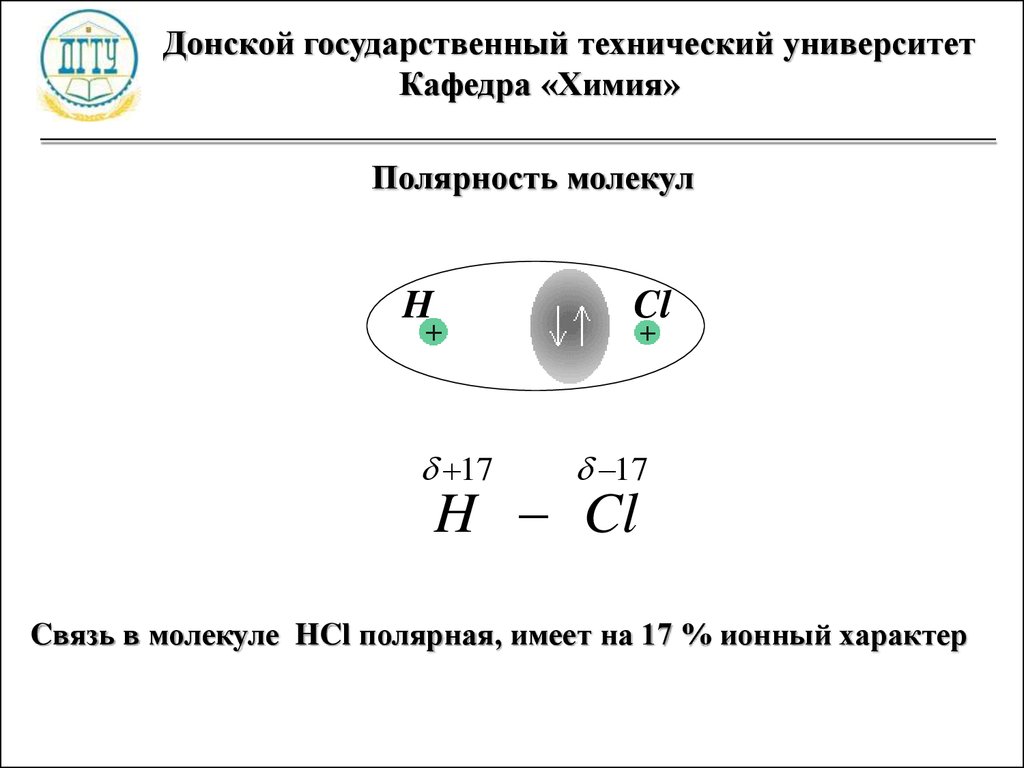
Полярность молекул
H
Cl
17
17
H Cl
Cвязь в молекуле HCl полярная, имеет на 17 % ионный характер
20.
Донской государственный технический университетКафедра «Химия»
________________________________________________________
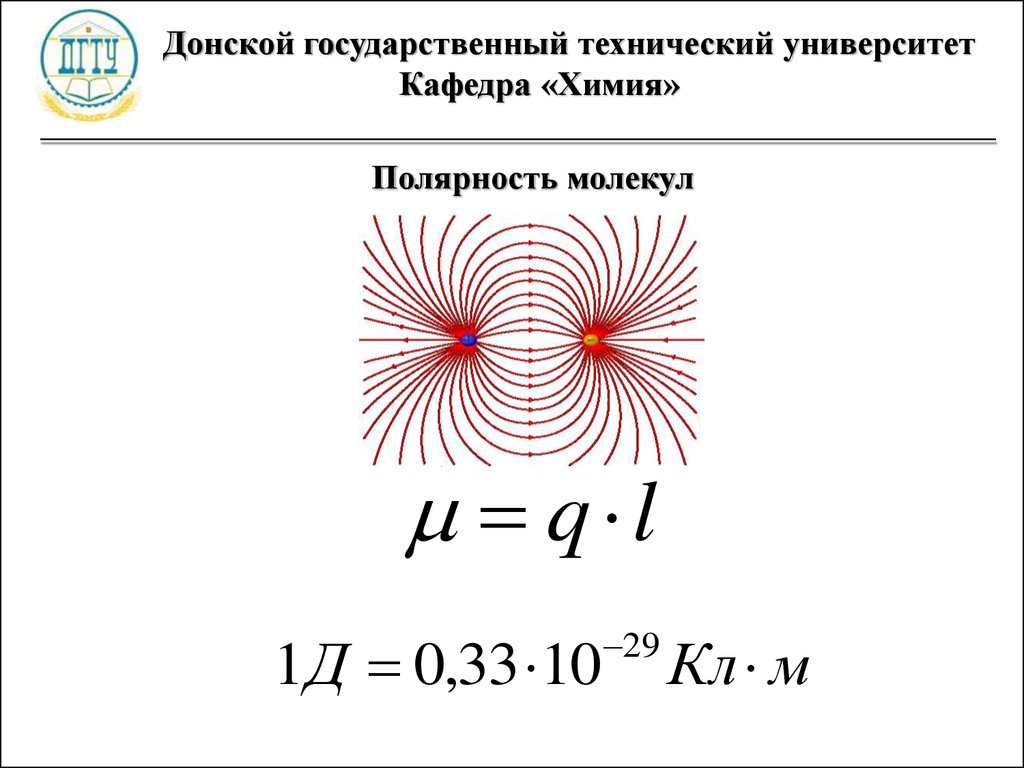
Полярность молекул
q l
1 Д 0,33 10
29
Кл м
21.
Донской государственный технический университетКафедра «Химия»
________________________________________________________
Полярность молекул
1
F
-
Ве
2
2 +
1 2 0
F
-
22.
Донской государственный технический университетКафедра «Химия»
________________________________________________________
Полярность молекул
1
+ H
2 -
+ H
S
2
1 2 0
23.
Донской государственный технический университетКафедра «Химия»
________________________________________________________
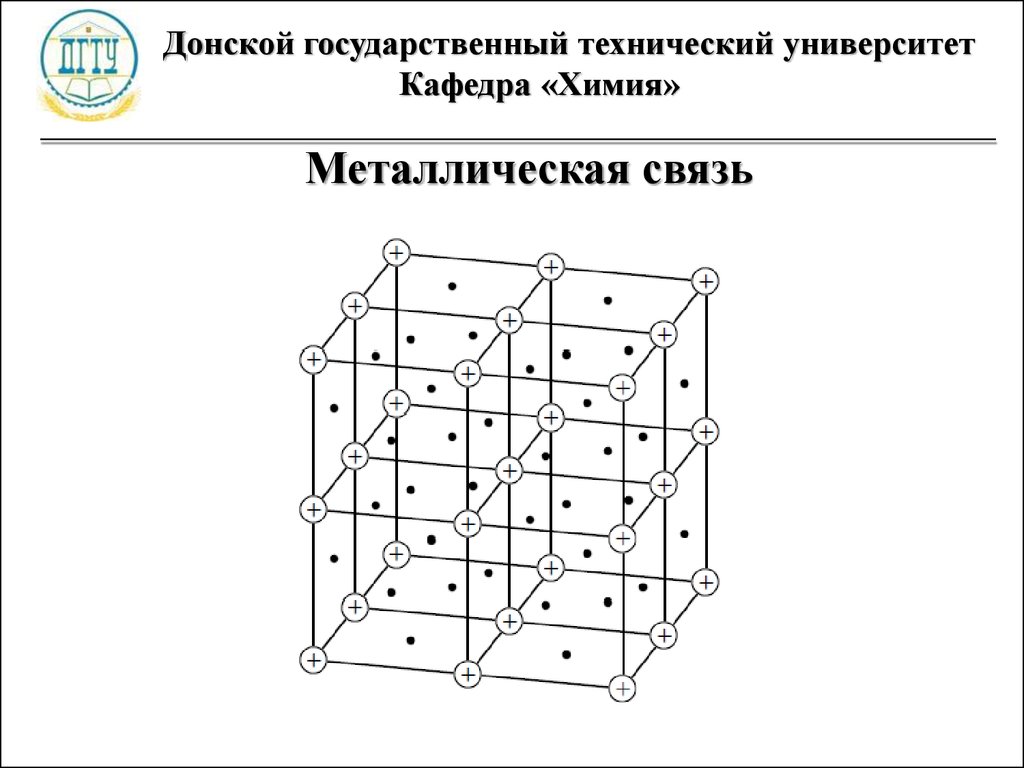
Металлическая связь
24.
Донской государственный технический университетКафедра «Химия»
________________________________________________________
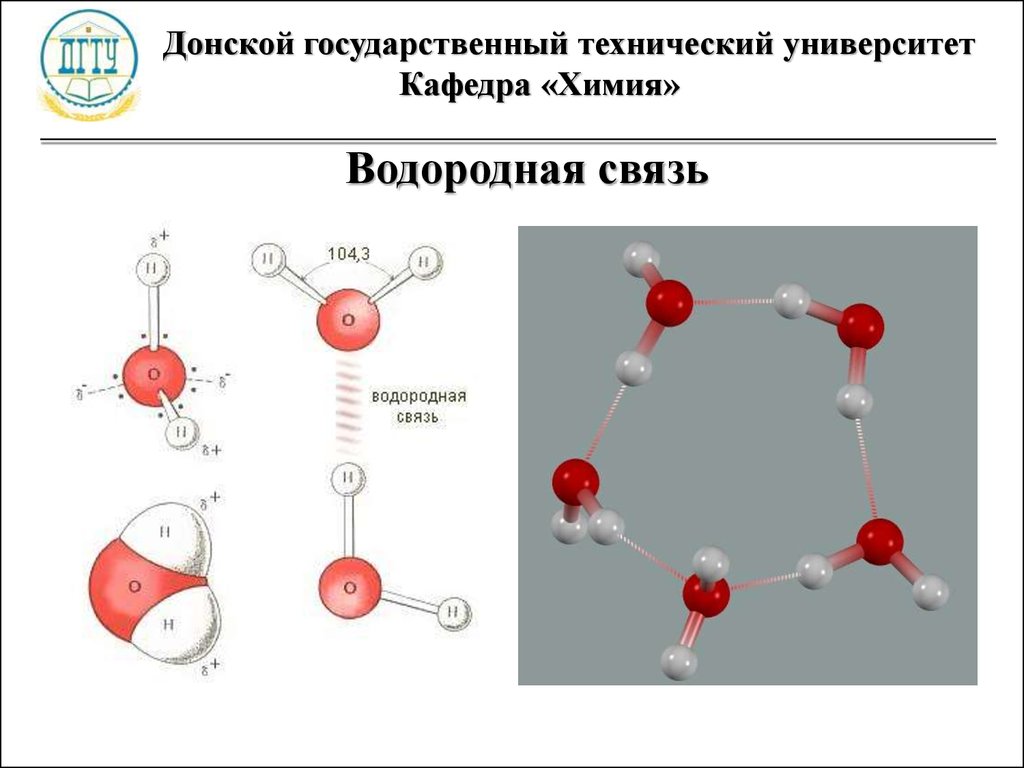
Водородная связь
25.
Донской государственный технический университетКафедра «Химия»
________________________________________________________
Водородная связь
о-салициловый альдегид
п – гидроксибензальдегид
26.
Донской государственный технический университетКафедра «Химия»
________________________________________________
Силы Ван-дер-Ваальса
Диполь-дипольное взаимодействие:
2 4
Е 6
3r КТ
Индукционное взаимодействие:
2 L 2
Е 6
r
Дисперсионное взаимодействие:
Ян Дидерик Ван-дер-Ваа́льс
(23 ноября 1837 — 8 марта 1923)
3L2 h o
Е
4r 6











 Химия
Химия








