Похожие презентации:
Щелочные металлы
1.
Щелочные металлыХИМИЯ
ОГЭ -9
2.
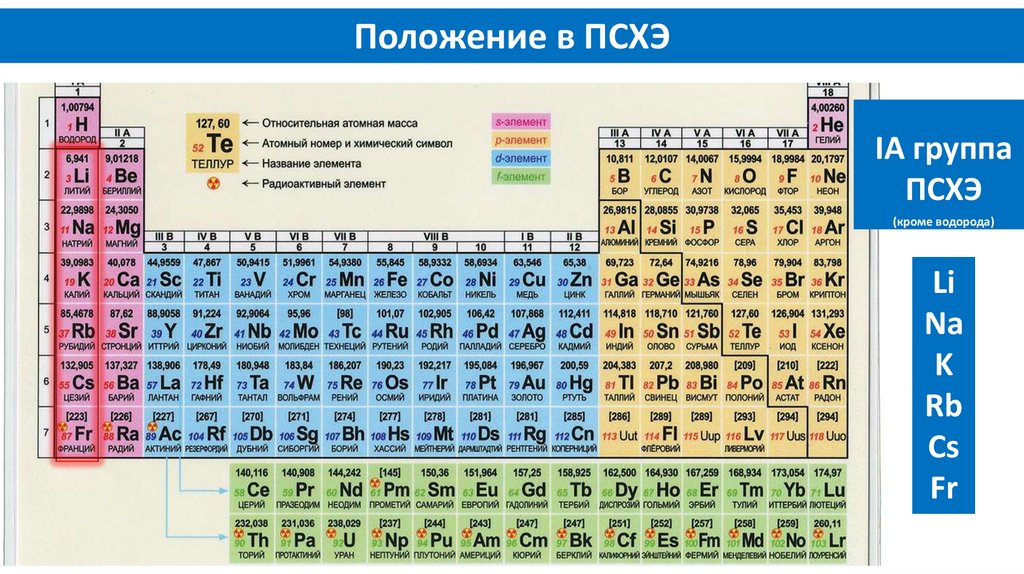
Положение в ПСХЭIА группа
ПСХЭ
(кроме водорода)
Li
Na
K
Rb
Cs
Fr
3.
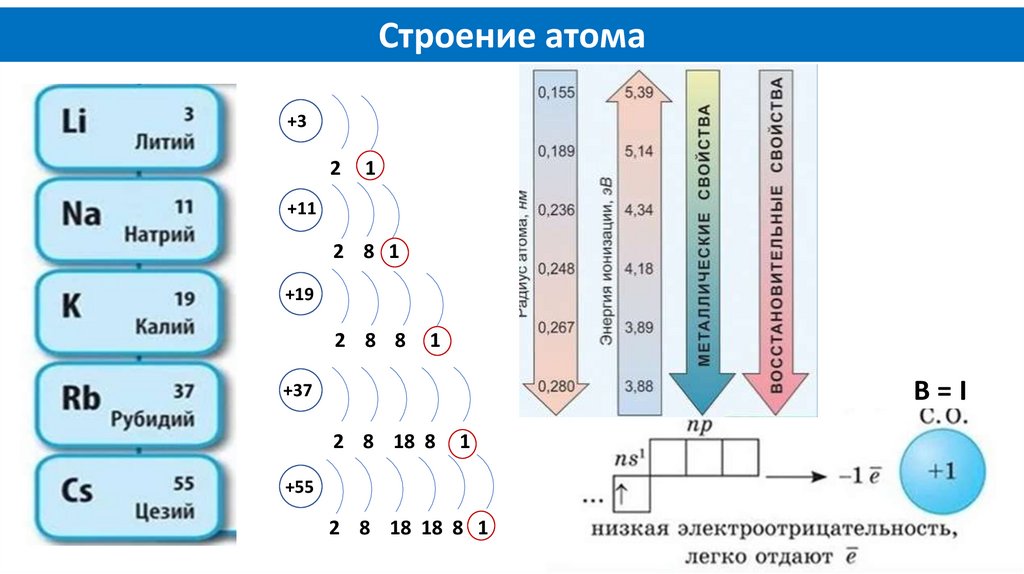
Строение атома+3
2
1
+11
2 8 1
+19
2 8 8
1
В=I
+37
2 8 18 8
1
+55
2 8 18 18 8 1
4.
Щелочные металлы в природе(только в виде соединений)
5.
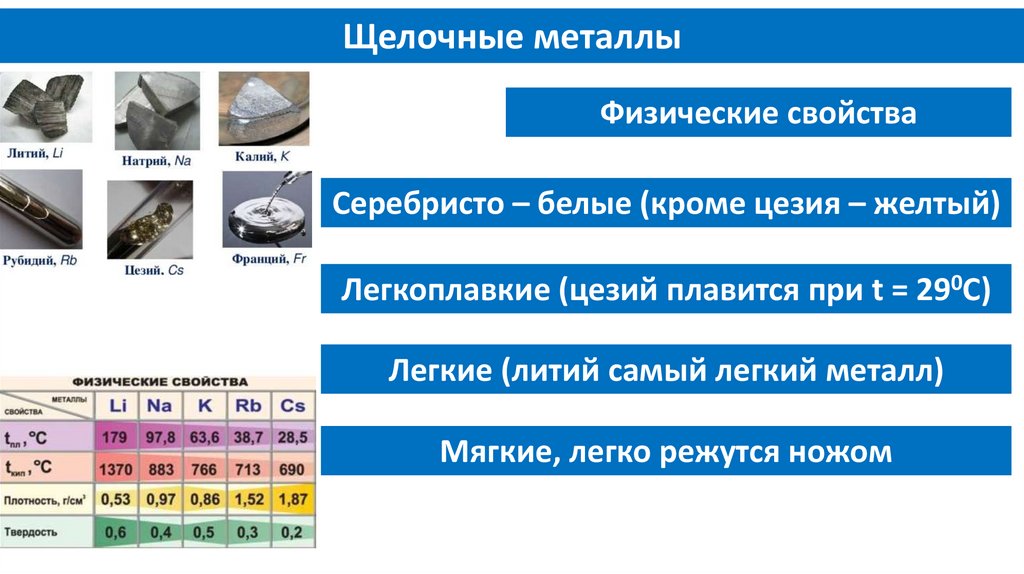
Щелочные металлыФизические свойства
Серебристо – белые (кроме цезия – желтый)
Легкоплавкие (цезий плавится при t = 290С)
Легкие (литий самый легкий металл)
Мягкие, легко режутся ножом
6.
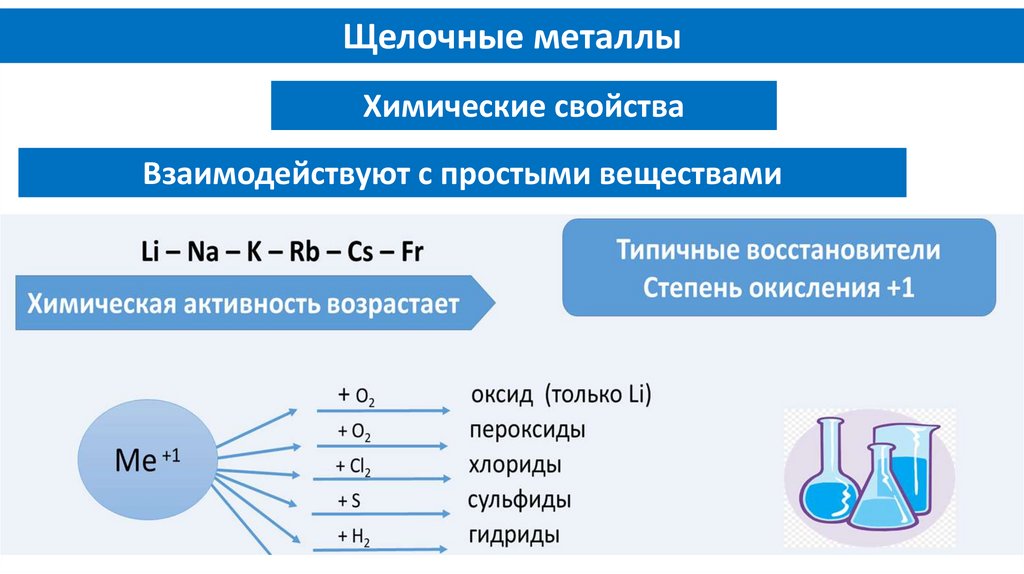
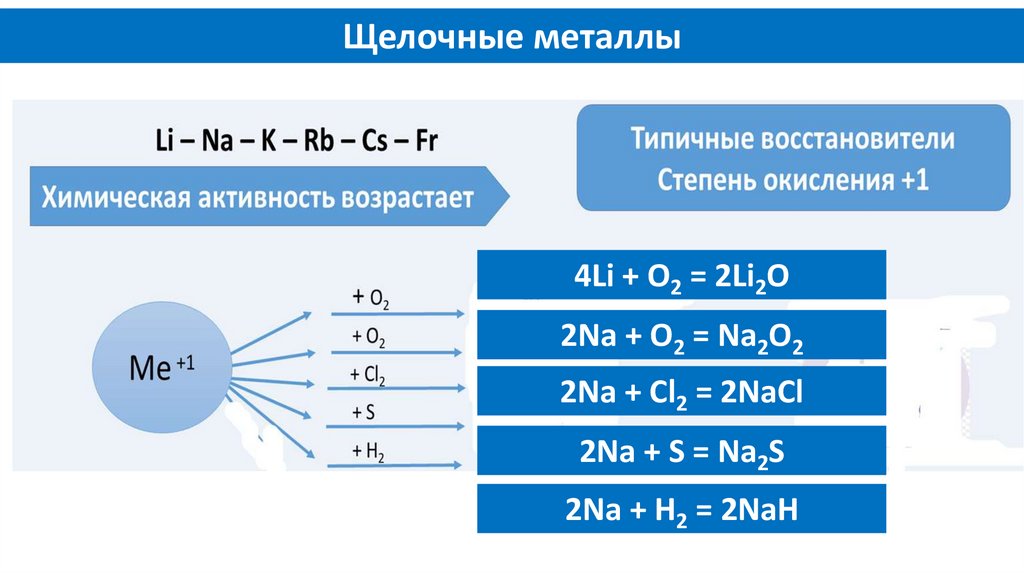
Щелочные металлыХимические свойства
Взаимодействуют с простыми веществами
7.
Щелочные металлы4Li + O2 = 2Li2O
2Na + O2 = Na2O2
2Na + Cl2 = 2NaCl
2Na + S = Na2S
2Na + H2 = 2NaH
8.
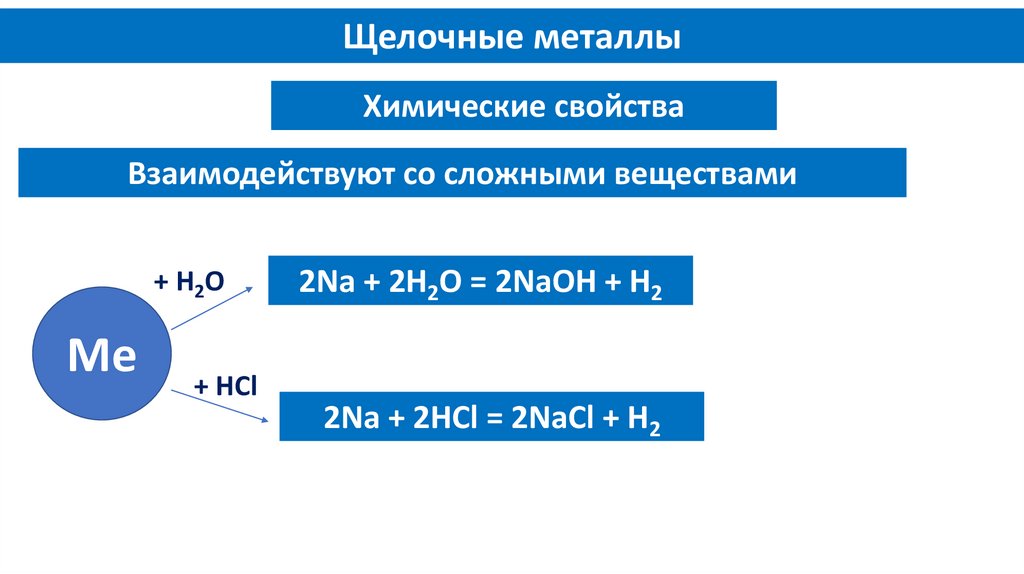
Щелочные металлыХимические свойства
Взаимодействуют со сложными веществами
+ H2O
Me
+ HCl
2Na + 2H2O = 2NaOH + H2
2Na + 2HCl = 2NaCl + H2
9.
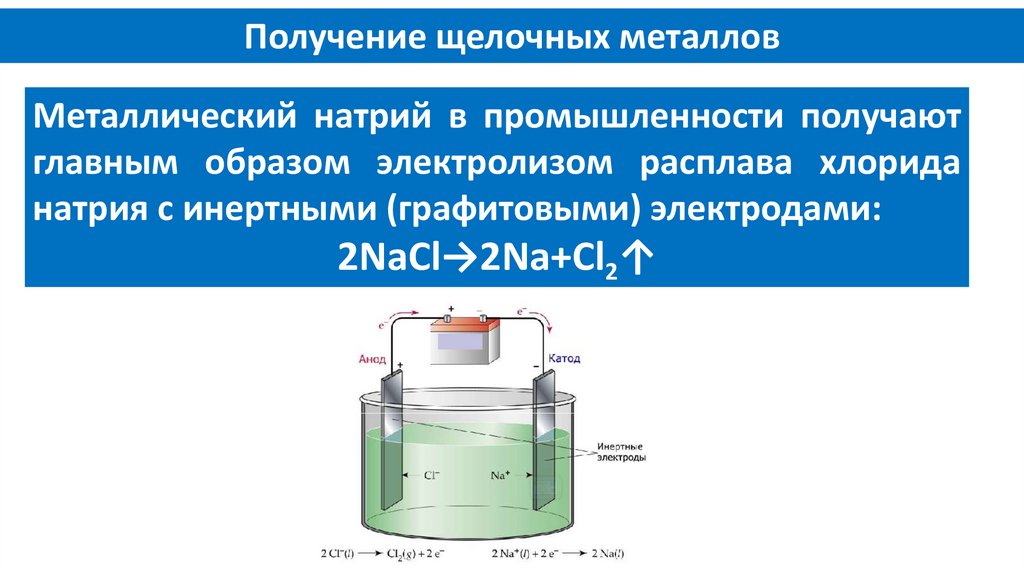
Получение щелочных металловМеталлический натрий в промышленности получают
главным образом электролизом расплава хлорида
натрия с инертными (графитовыми) электродами:
2NaCl→2Na+Cl2↑
10.
Качественный анализкатионы щелочных металлов окрашивают пламя в характерные цвета
Соли лития придают пламени карминово-красный цвет, соли натрия —
жёлтый, калия — фиолетовый, рубидия и цезия — светло-фиолетовый.
11.
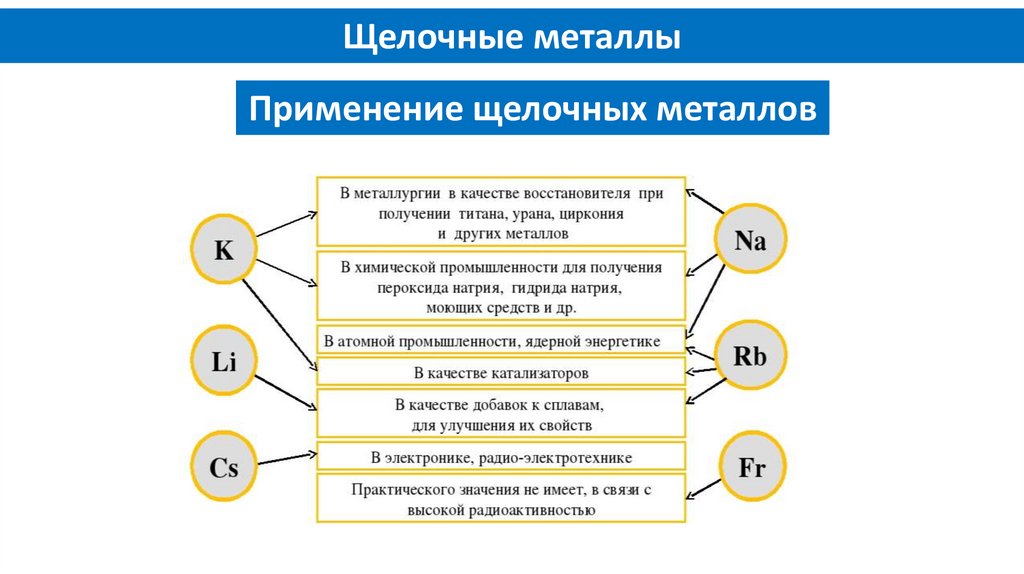
Щелочные металлыПрименение щелочных металлов



 Химия
Химия








