Похожие презентации:
Периодический закон. Периодическая таблица химических элементов. 8 класс
1.
“Будущее не грозит периодическомузакону разрушением, а только
надстройки и развитие обещает
(Д.И. Менделеев )”.
ПЕРИОДИЧЕСКИЙ ЗАКОН.
ПЕРИОДИЧЕСКАЯ ТАБЛИЦА ХИМИЧЕСКИХ
ЭЛЕМЕНТОВ.
Автор учитель биологии и
химии Щеглова О.Ф.
2.
В марте 1869 г. русский химик ДмитрийИванович Менделеев (1834-1907) представил
Русскому
химическому
обществу
(РХО) периодический закон химических элементов,
сформулированный в нескольких основных
положениях.
3.
LiBe
B
C
N
Li2O
BeO
B2O3
CO2
N 2 O5
LiOH
Be(OH)2
H2BeO2
B(OH)3
H3BO3
H2CO3
HNO3
Si
P
Na
Mg
Al
Na 2O
MgO
Al 2O3
NaOH
Mg(OH)2 Al(OH) 3
H3AlO3
HAlO2
O
F
S
Cl
SiO2
P 2 O5
SO3
Cl 2O7
H2SiO3
H3PO4
H2SO4
HClO4
4.
ArAr
Ar
Ar
Ca
Fe
Os
190
K
Sr
Co
Ir
192
Rb
Ba
Ni
Pt
195
Cs
5.
VIIF
Cl
Br
I
Ar
19
35,5
80
127
At
(210)
p
1,51г/см3
1,57 г/см3
3,14 г/см3
4,94 г/см3
tкип
-188С0
-34 С0
59 С0
185 С0
tплав
-220 С0
-101 С0
-7 С0
114 С0
агрегатное состояние
зеленовато-желтый газ
желто-зеленый газ
красно-бурая жидкость
сине-черный
кристаллический,
кристаллический,
металлический блеск
УВЕЛИЧИВАЕТСЯ
с О2
с Ме
HF
HCl
HBr
HI
сила
кислот
хим.
активность
6.
7.
«Свойства простых тел, а также формы исвойства соединений элементов находятся в
периодической зависимости от величины атомных
весов элементов»
Принцип построения периодической системы.
“Периодическая система построена в порядке
возрастания атомной массы”.
Принцип периодичности.
“Периодичность - это повторение химических
свойств через каждые семь элементов на восьмой.
8.
9.
10.
11.
12.
ГОРИЗОНТАЛЬНЫЙ РЯДПериод- горизонтальный ряд элементов, начинающийся
щелочным металлом и заканчивающийся инертным
газом
1-3 периоды – малые
4-7- периоды – большие
→увеличиваются: атомная масса
радиус атома
неметаллические свойства
окислительные свойства
электроотрицательность
(в малых периодах) валентность с кислородом(I-VIII)
(сV II до группы IV ) валентность с водородом в летучих
соединениях
13.
14.
ВЕРТИКАЛЬНЫЙ СТОЛБЕЦГруппа – вертикальный столбец;
Главная подгруппа- элементы малых и больших
периодов
Побочная подгруппа – элементы только больших
периодов
(для главных подгрупп)↓
увеличиваются: атомная масса
радиус атома
металлические свойства
восстановительные свойства
15.
16.
6.1 а6.2 а
6.1. б
6.2 б
17.
6.3. А) F˂ C ˂ B ˂ Li6.4.
Б) S˂ P ˂ Al ˂ Na
а) Si ˂ P ˂ S ˂ Cl б) B ˂ C ˂ O ˂ N
6.5 а) Mg ˂ Ca˂ Sr ˂ Ba б) Li ˂ Na ˂ Rb ˂ Cs
6.6 а) I ˂ Br ˂ Cl ˂ F
б) Po ˂Te ˂Se ˂ O







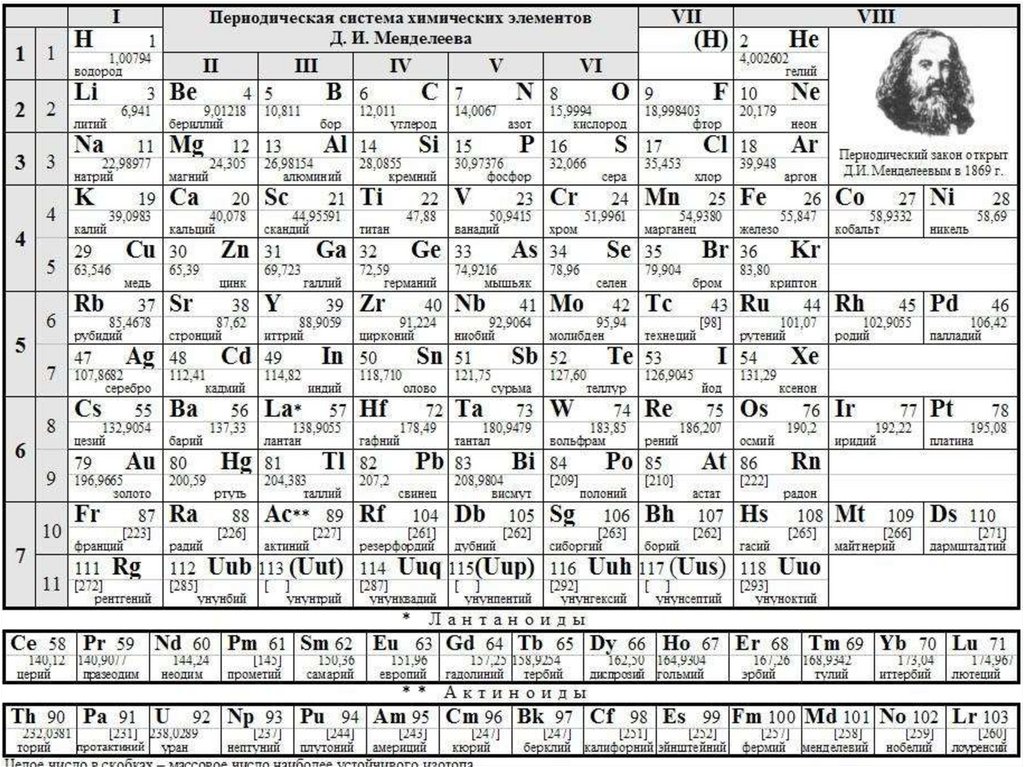
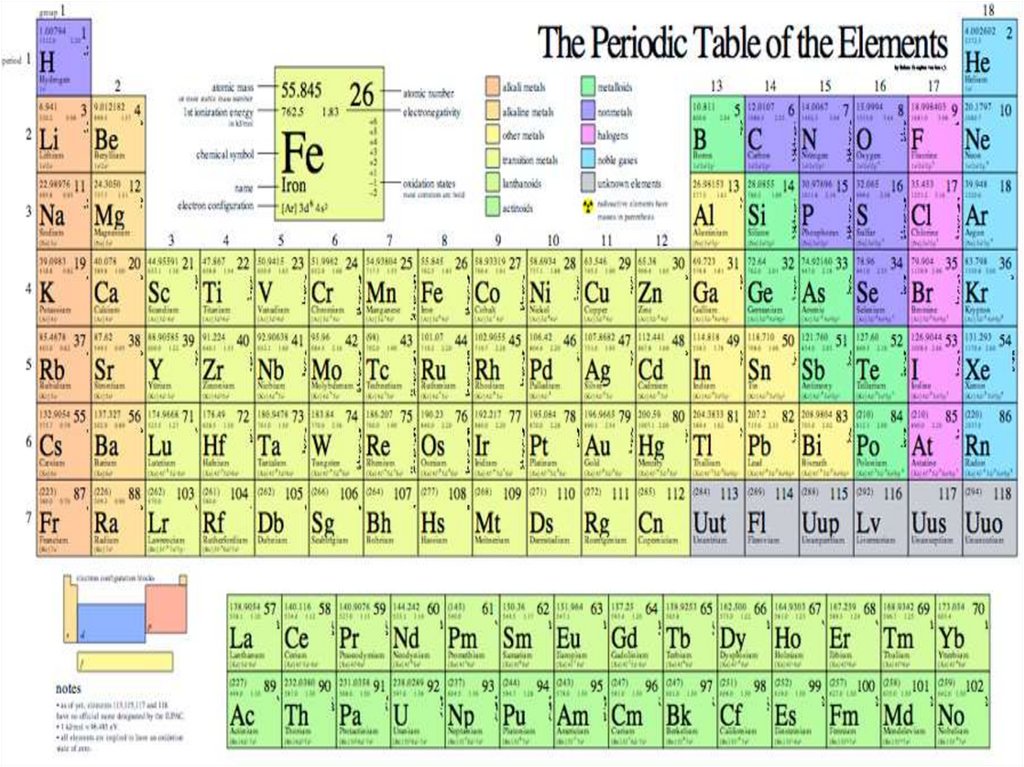

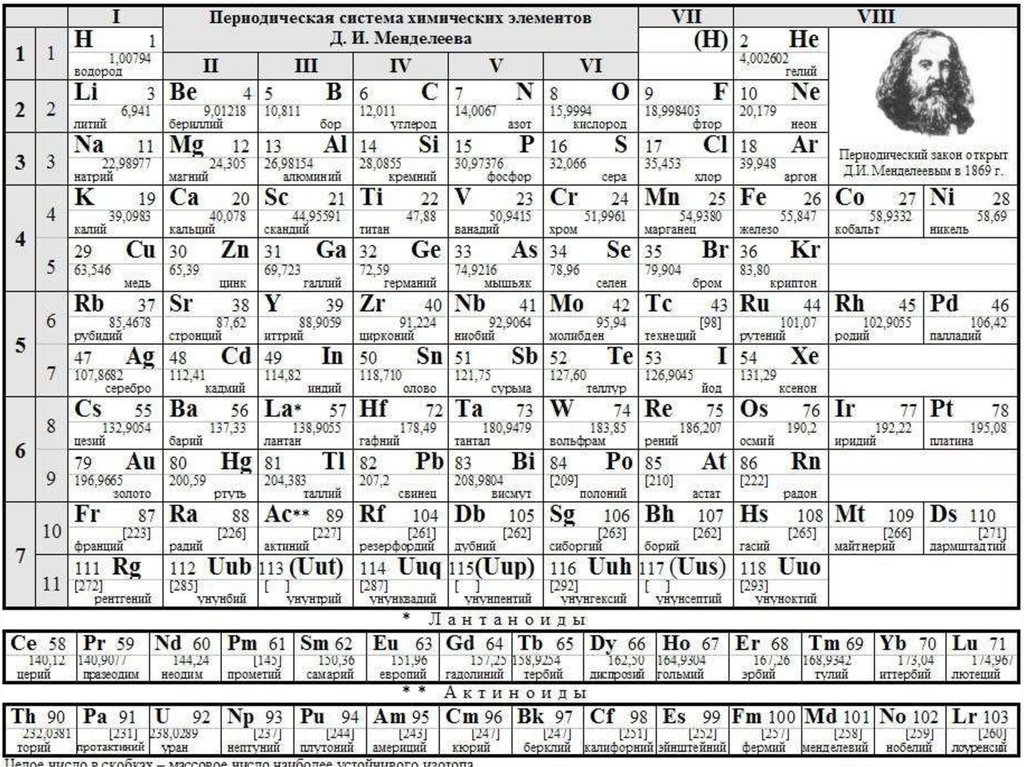






 Химия
Химия








