Похожие презентации:
Химическая связь. Строение вещества
1. педагогический стаж -11 лет, год окончания вуза - 2000, вуз - Бирский государственный педагогический институт, факультет
Итоговый урокпо теме: « Химическая связь.
Строение вещества».
педагогический стаж -11 лет,
год окончания вуза 2000,
вуз - Бирский государственный
педагогический институт,
факультет -биолого-химический,
отделение химия,
специальность – преподаватель химии
и биологии,
преподавание в классах- 8-11
1
2. Цель урока:
повторитьВиды химических связей
Типы кристаллических решеток
Степень окисления
Окислительно-восстановительные реакции
Расстановка коэффициентов методом
электронного баланса
3.
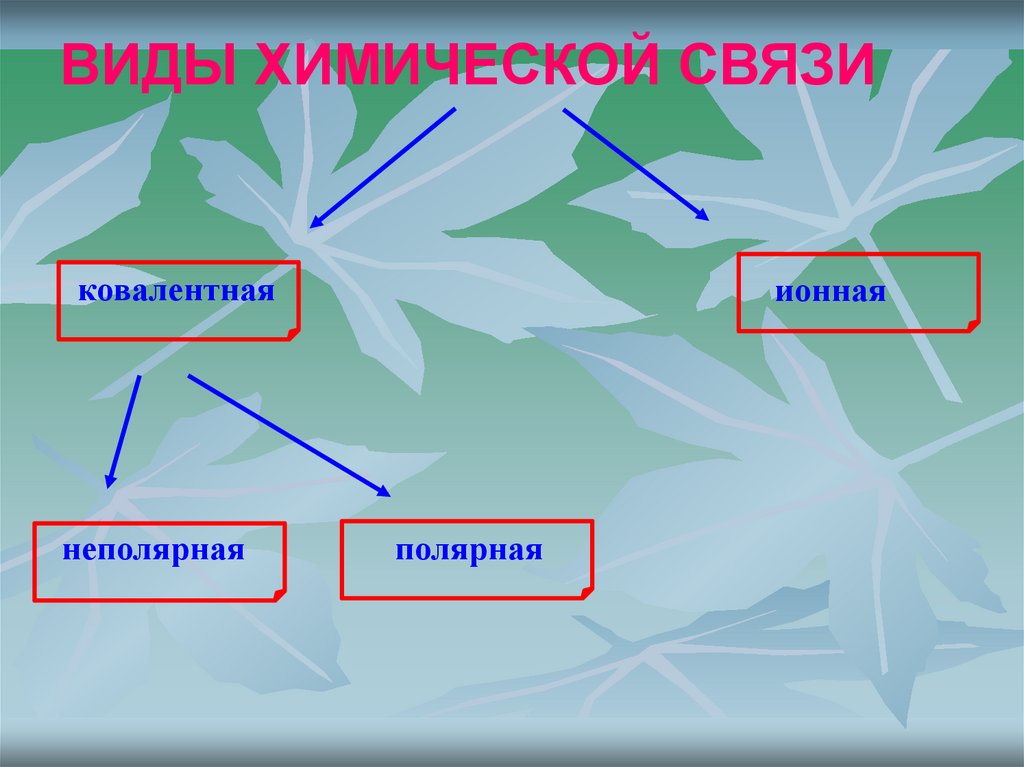
ВИДЫ ХИМИЧЕСКОЙ СВЯЗИковалентная
неполярная
ионная
полярная
4. Охарактеризуйте виды химических связей
К.Н.С. - это …К.П.С. - это …
И.С.
- это …
5.
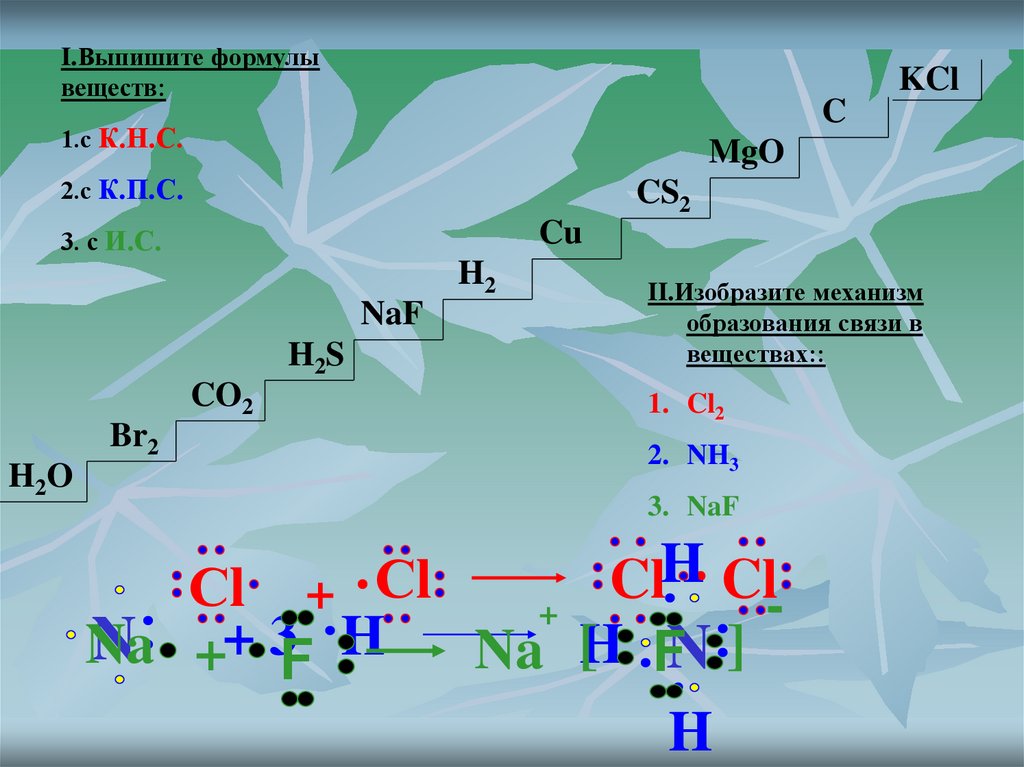
I.Выпишите формулывеществ:
KCl
C
1.с К.Н.С.
MgO
2.с К.П.С.
CS2
Cu
3. с И.С.
H2
NaF
H2S
CO2
Br2
H2O
II.Изобразите механизм
образования связи в
веществах::
1. Cl2
2. NH3
3. NaF
H
Сl
Cl
Cl
Сl +
+
N ++ 3F H Na H
Na
[ FN ]
H
6.
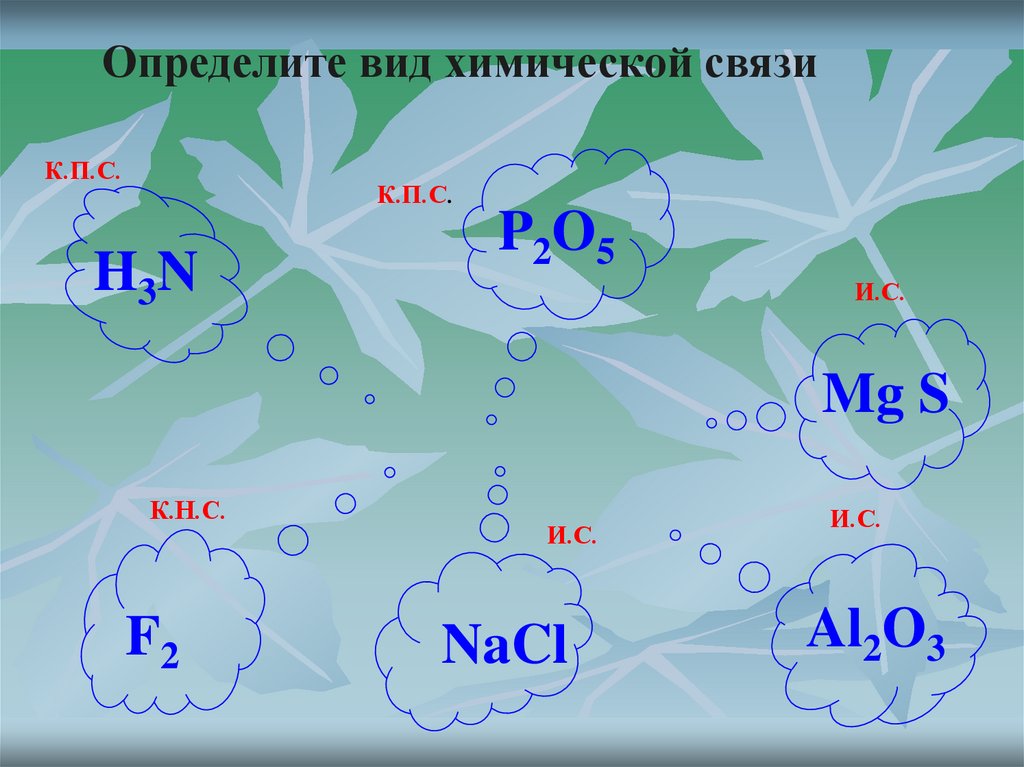
Определите вид химической связиК.П.С.
К.П.С.
H3N
P2O5
И.С.
Mg S
К.Н.С.
F2
И.С.
NaCl
И.С.
Al2O3
7.
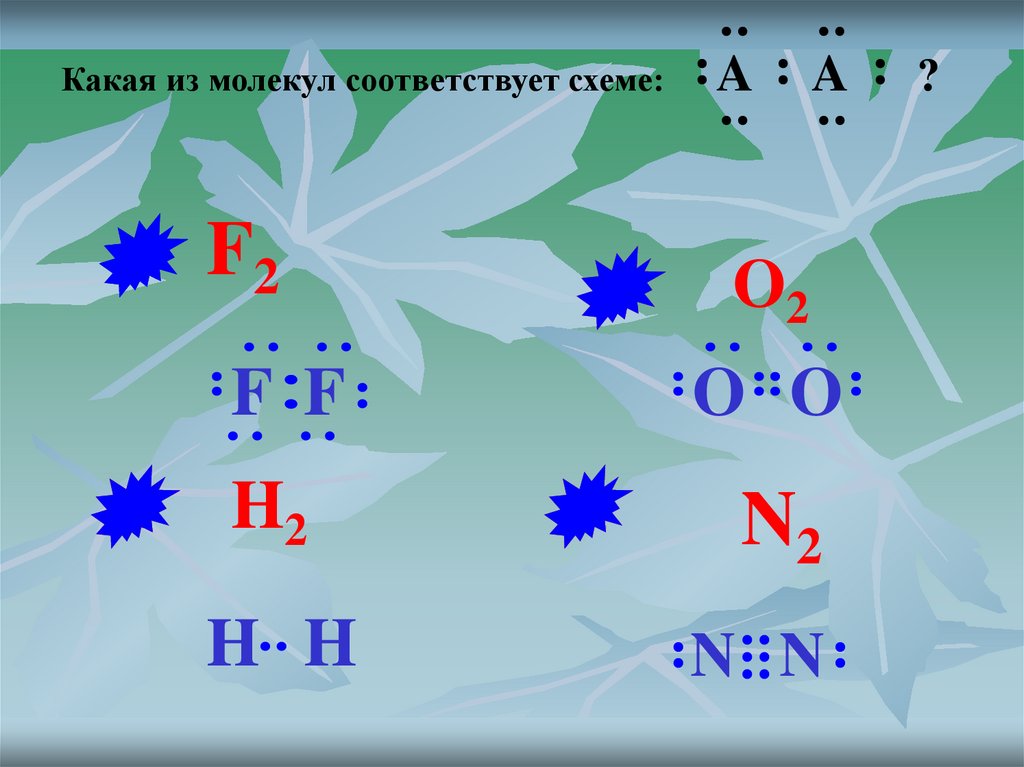
Какая из молекул соответствует схеме:F2
A
A
O2
F F
O O
H2
N2
H H
N N
?
8. Кристаллические решетки
атомныеионные
молекулярные
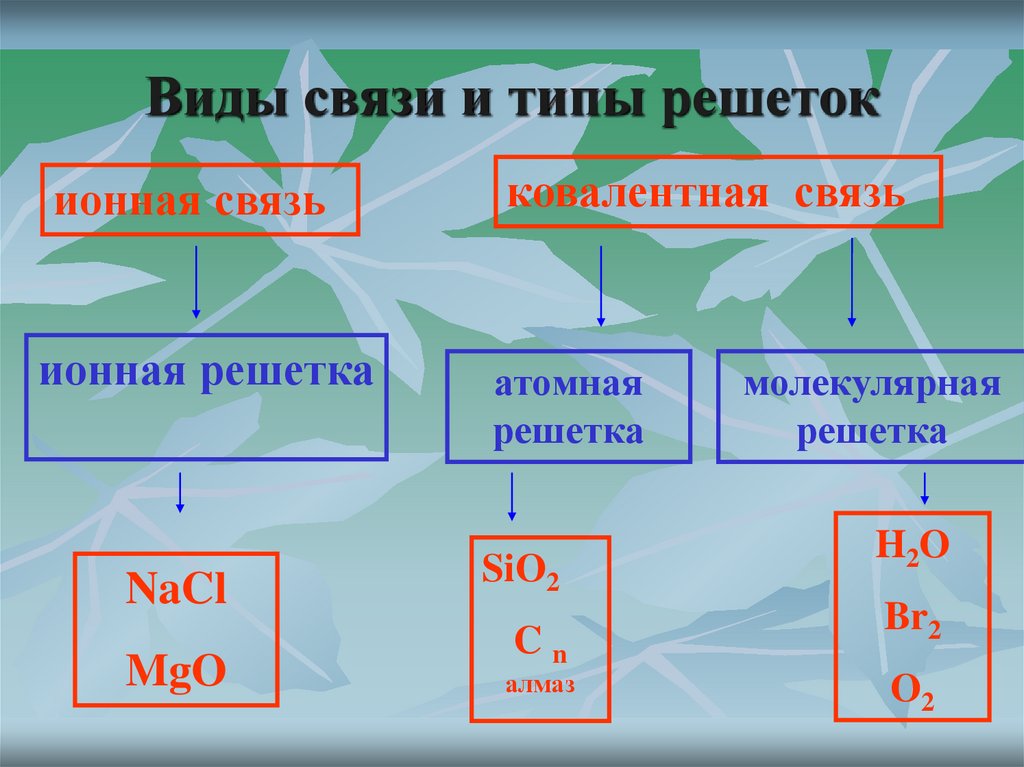
9. Виды связи и типы решеток
ионная связьионная решетка
NaCl
MgO
ковалентная связь
атомная
решетка
SiO2
Cn
алмаз
молекулярная
решетка
H2O
Br2
O2
10.
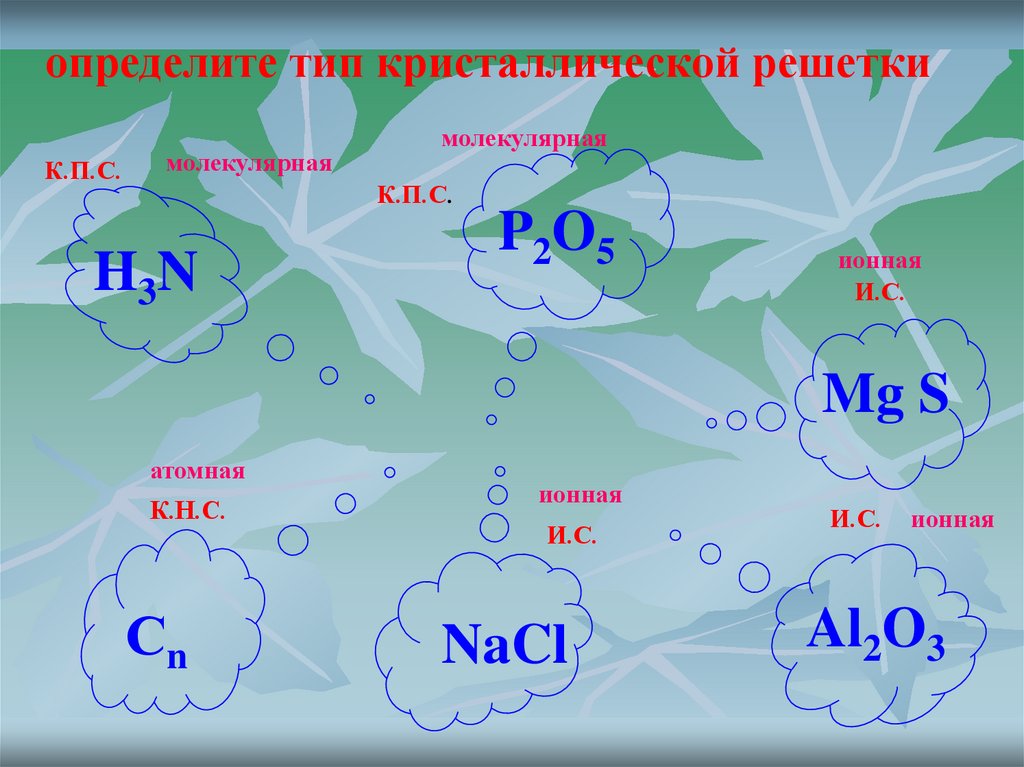
определите тип кристаллической решеткиК.П.С.
молекулярная
молекулярная
К.П.С.
H3N
P2O5
ионная
И.С.
Mg S
атомная
К.Н.С.
Сn
ионная
И.С.
NaCl
И.С.
ионная
Al2O3
11. Степень окисления
Дайте определение степени окисленияОкислительно-восстановительная реакция
Окислитель
Восстановитель
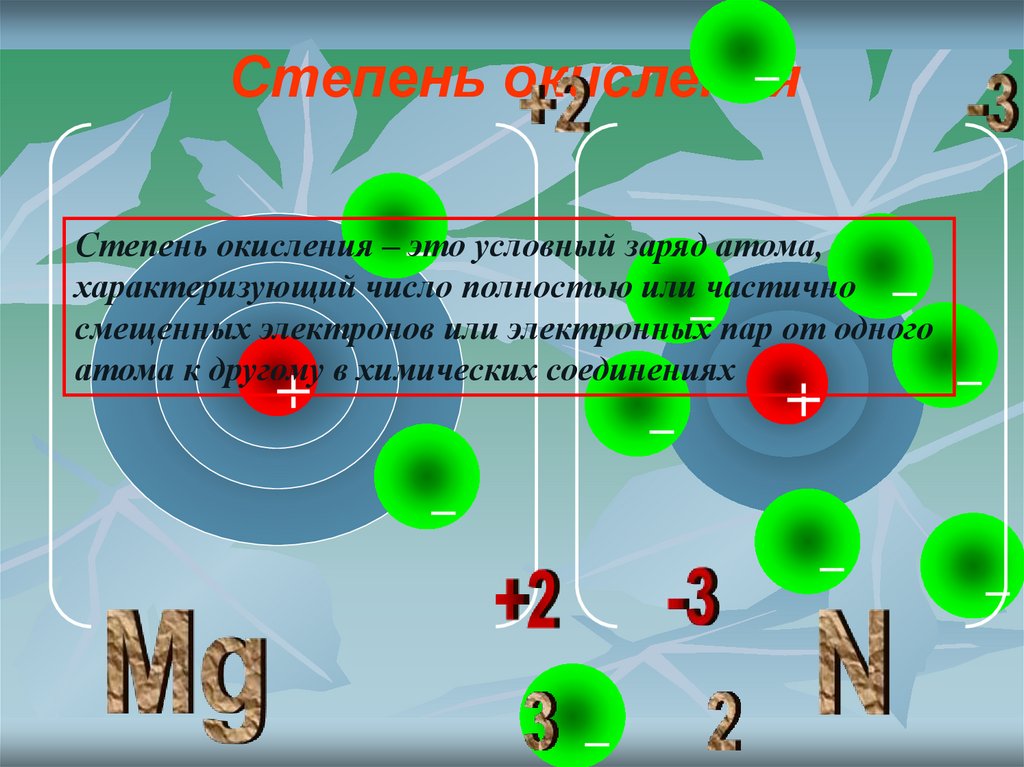
12.
Степень окисленияСтепень окисления – это условный заряд атома,
характеризующий число полностью или частично
смещенных электронов или электронных пар от одного
атома к другому в химических соединениях
13.
постояннаяпеременная
H,K,Zn
Cl,P,Se
Степень окисления
положительная
Na,Al,Ca
ст.о. элементов в
простых веществах
Fe0,Cl20,H20
отрицательная
S-2 ,N-3 ,O-2
14.
Какая реакция являетсяокислительновосстановительной?
+1 +6 -2
НЕТ
НЕТ
+1
-2
H2SO4 +Na2O
+6 -2
+1 +6 -2
Na2SO4 + H2O
+1 -2
+1 +6 -2
SO3 + H2O
+4 -2
H2SO4
0
+6 -2
2SO2 + O2
+1 -2
0
Н2S + O2
+1 -2
2SO3
+1 -2
0
H2O + S
15.
Определите в каком веществе степеньокисления серы равна +4
+1
НЕТ
-2
Н2S
+1 +6 -2
НЕТ
НЕТ
H2SO4
+6 -2
SO3
+4 -2
SO2
+1 +4 -2
H2SO3
16.
Какой коэффициент перед формулой окислителя?0
0
4 Al + 3O2
восстановитель
+3
-2
2Al2O3
окислитель
нет
нет
нет
ok
17.
Какой коэффициент перед формулойвосстановителя?
0
0
2 P + 3 Cl2
восстановитель
+3
-1
2 PCl3
окислитель
ok
нет
нет
нет
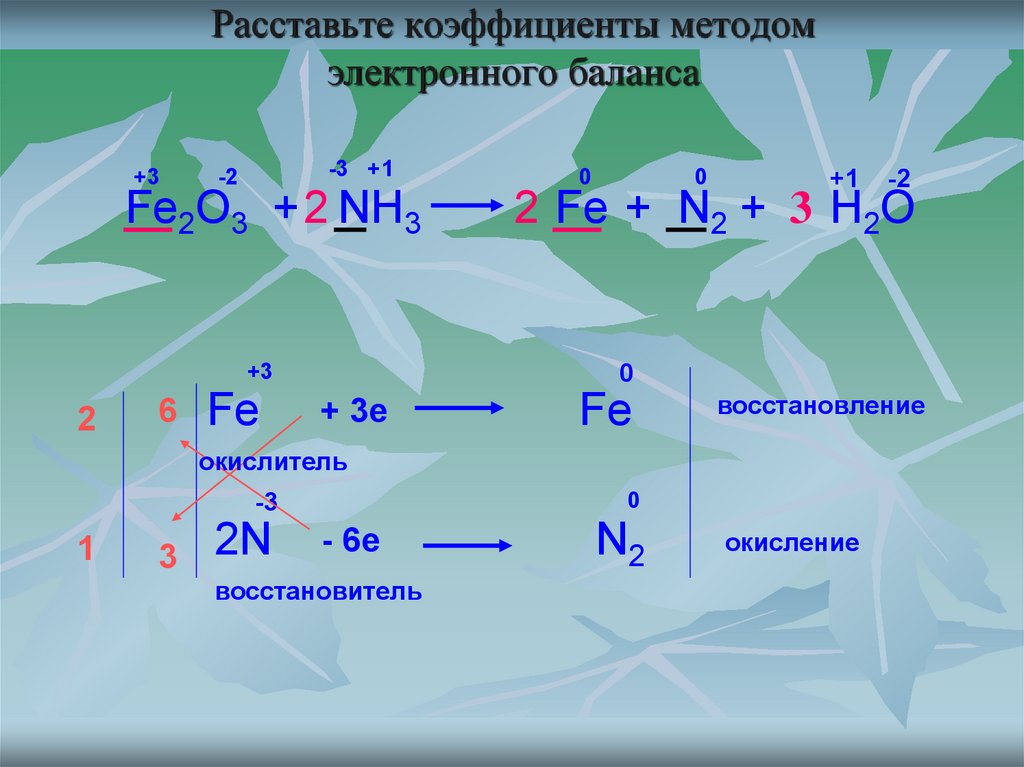
18. Расставьте коэффициенты методом электронного баланса
+3-3 +1
-2
Fe2O3 + 2 NH3
+3
2
6
Fe
0
0
+1
2 Fe + N2 + 3 H2O
0
+ 3е
Fe
восстановление
окислитель
0
-3
1
3
2N
-2
- 6е
восстановитель
N2
окисление
19. Кроссворд
х3
5
н
и
1
с
у
л
ь ф и д
2
б
р
о
м и
ф т
о
р
и д
4
и
о
т
р
и д
д
1. Формула вещества ЭxSy.
д
2. Формула вещества ЭxBry.
и д
3. Формула вещества ЭxFy.
4. Формула вещества ЭxJy.
Составьте формулы веществ и найдите свой вопрос :
нитрид кальция
бромид магния
иодид алюминия
фторид кислорода
5. Формула вещества ЭxNy.
20. итог
Что для вас оказалось самым сложным?Что понравилось ?
Что не понравилось?












 Химия
Химия








