Похожие презентации:
Скорость химических реакций
1. Урок-исследование Тема: Скорость химических реакций
2. Цель урока:
• Выяснить, что такое скоростьхимической реакции.
• Выяснить, какие факторы и как влияют
на скорость химической реакции.
3. Скорость химической реакции:
c c2 c12
1
моль
л с
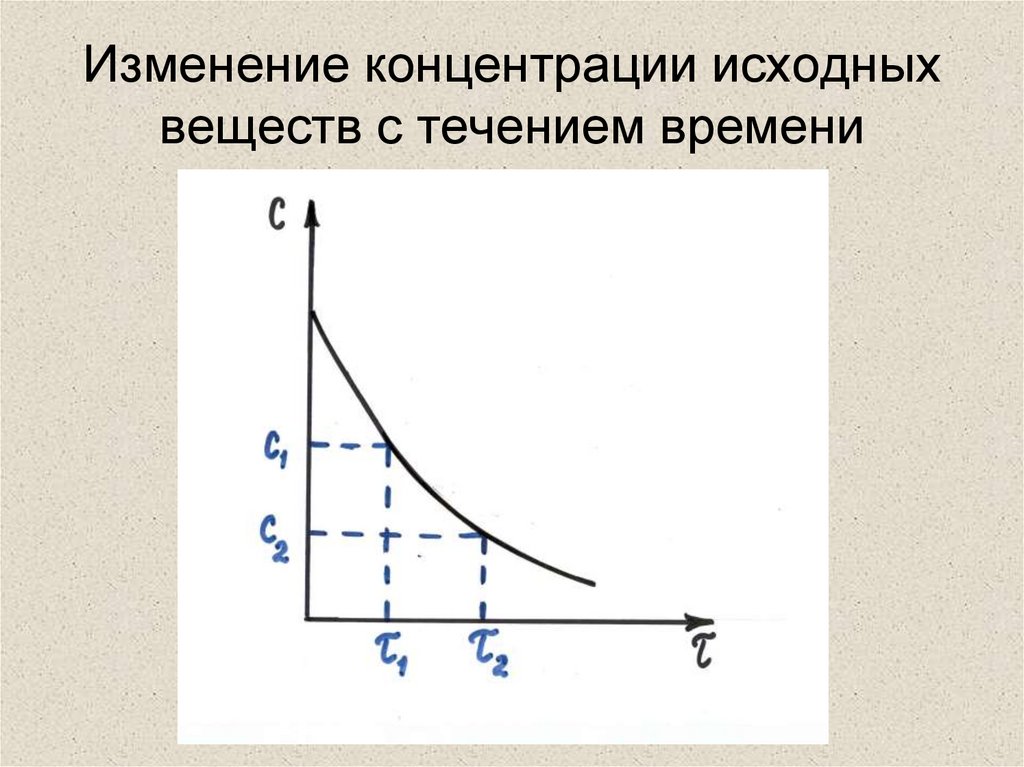
4. Изменение концентрации исходных веществ с течением времени
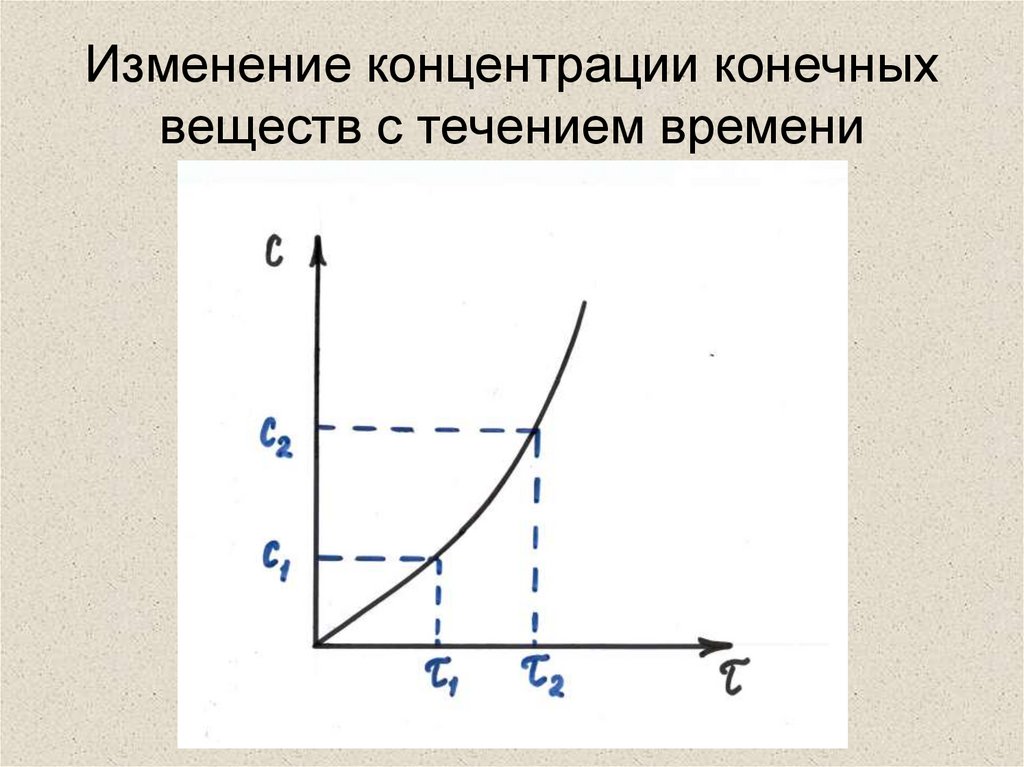
5. Изменение концентрации конечных веществ с течением времени
6. Скорость химической реакции в гомогенной системе:
c2 c1c
2 1
7. Скорость химической реакции в гетерогенной системе:
nS
моль
2
л м
8. Взаимодействие водорода с кислородом
2 моль H2 и 1 моль О2 при 25˚ Счерез 100 лет
3000 молекул H2О
9. Влияние на скорость реакции различных факторов
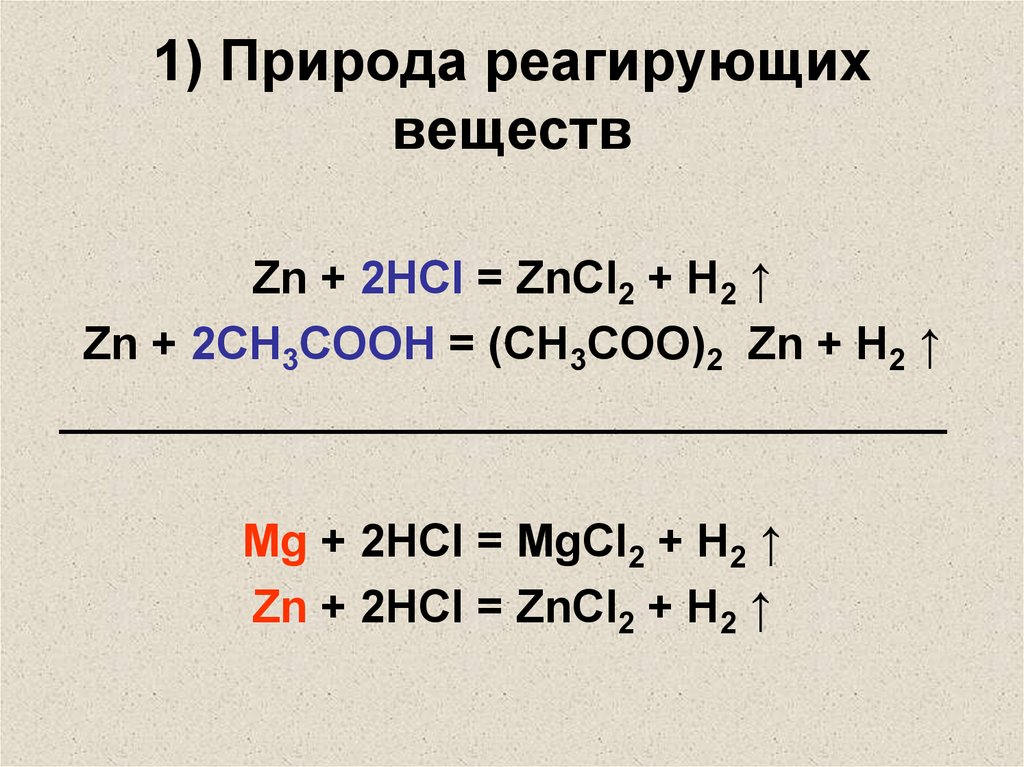
10. 1) Природа реагирующих веществ
Zn + 2HCl = ZnCl2 + H2 ↑Zn + 2CH3COOH = (CH3COO)2 Zn + H2 ↑
___________________________________
Mg + 2HCl = MgCl2 + H2 ↑
Zn + 2HCl = ZnCl2 + H2 ↑
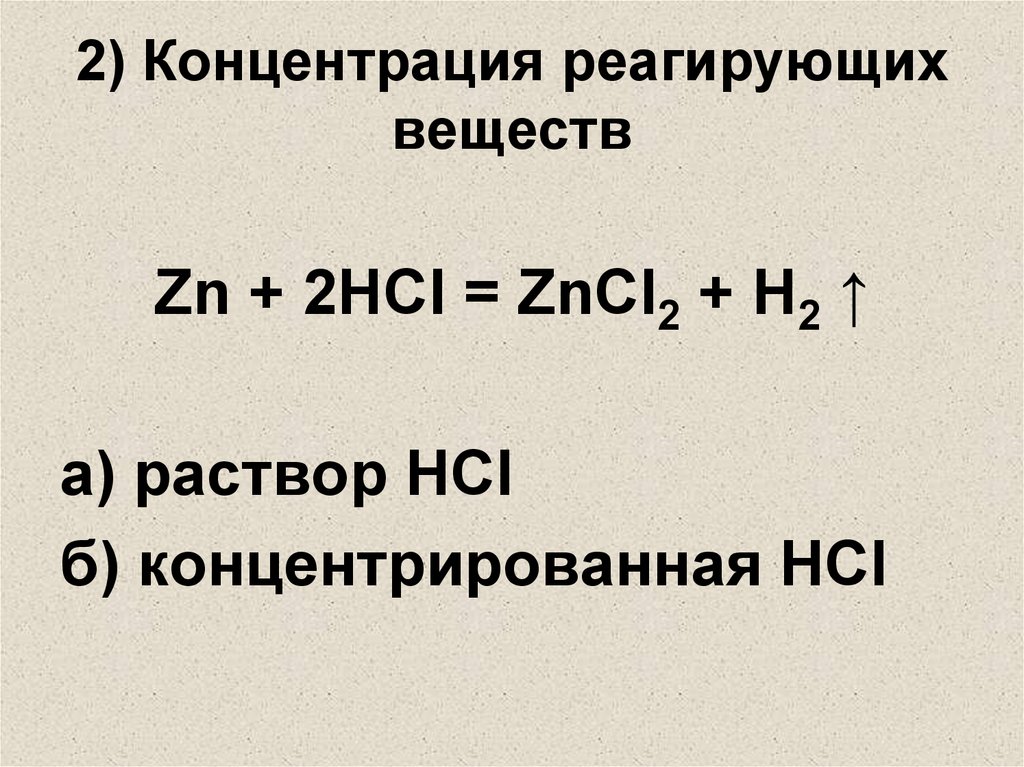
11. 2) Концентрация реагирующих веществ
Zn + 2HCl = ZnCl2 + H2 ↑а) раствор HCl
б) концентрированная HCl
12. Закон «действующих масс»:
• Скорость химической реакции прямопропорциональна произведению
концентраций реагирующих веществ.
mA nB pC lD
k C
m
A
C
n
B
13. Взаимодействие водорода с азотом
N 2 3H 2 2 NH 3k C
C
N2
3
H2
14. Горение угля
C O2 CO2k C
O2
15. 3) Величина поверхности соприкосновения реагирующих веществ
CaCO3 + 2HCl = CaCl2 + H2O + CO2 ↑а) кусочек CaCO3
б) измельченный CaCO3
16. 4) Температура
Правило Вант-Гоффа:При повышении температуры на
каждые 100 C скорость большинства
реакций увеличивается в 2-4 раза.
17. Правило Вант-Гоффа:
2Где
0
0
t 2 t1
0
10
1
- температурный коэффициент
18. Задача:
Во сколько раз увеличитсяскорость реакции?
t 50
0
2
0
2
?
1
19. Энергия активации
Н 2 I 2 2HIЕа 167,4 кДж / моль
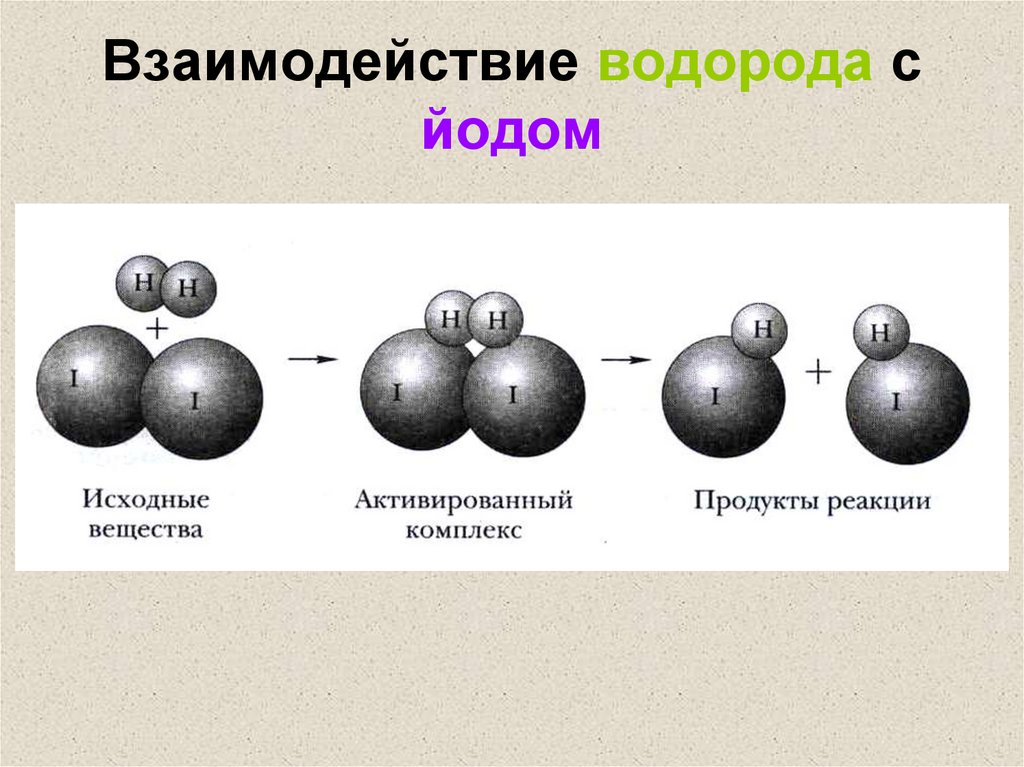
20. Взаимодействие водорода с йодом
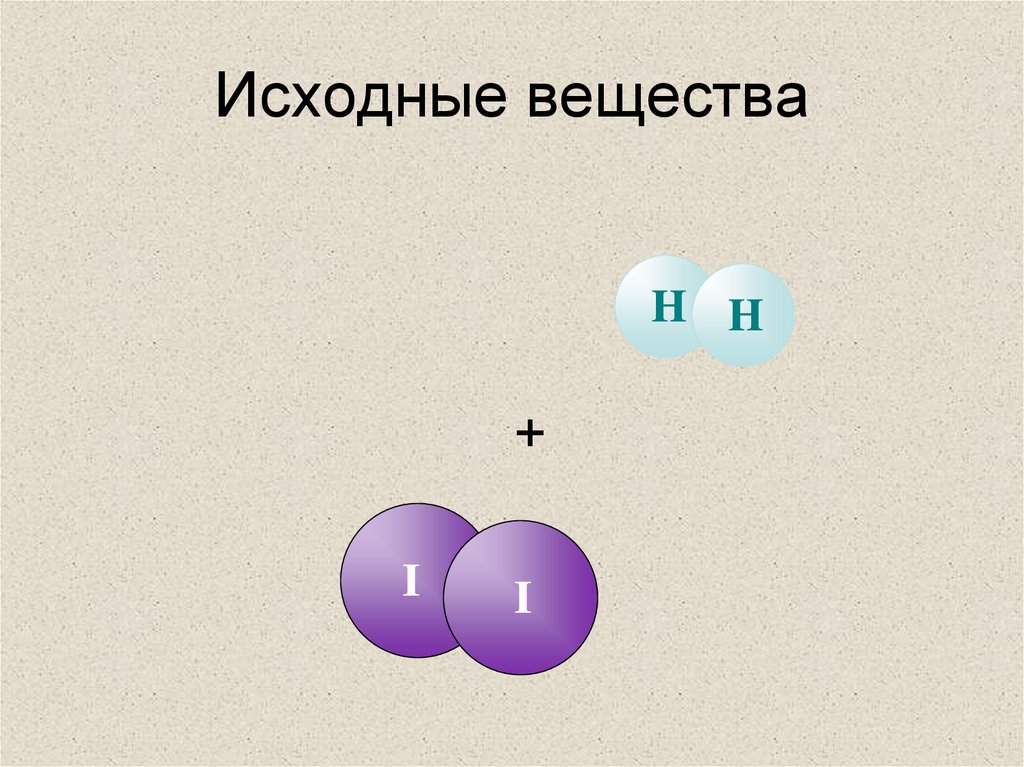
21. Исходные вещества
H H+
I
I
22. Упругое столкновение
H H+
I
I
23. Взаимодействие
H H+
I
I
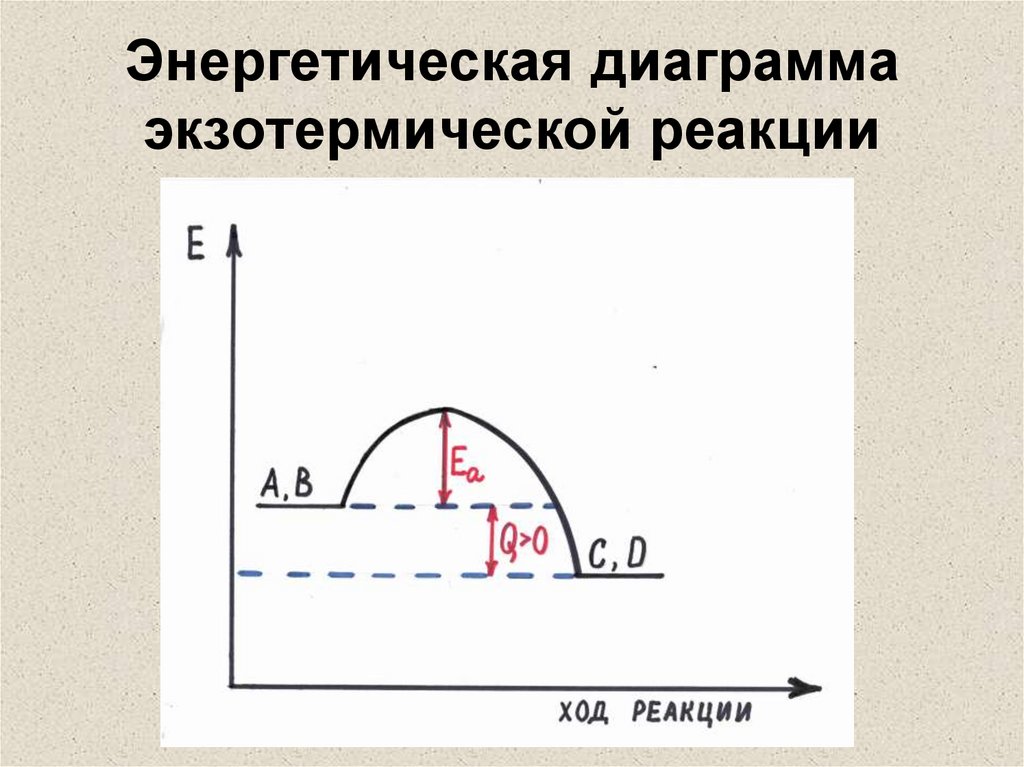
24. Энергетическая диаграмма экзотермической реакции
25. Энергетическая диаграмма эндотермической реакции
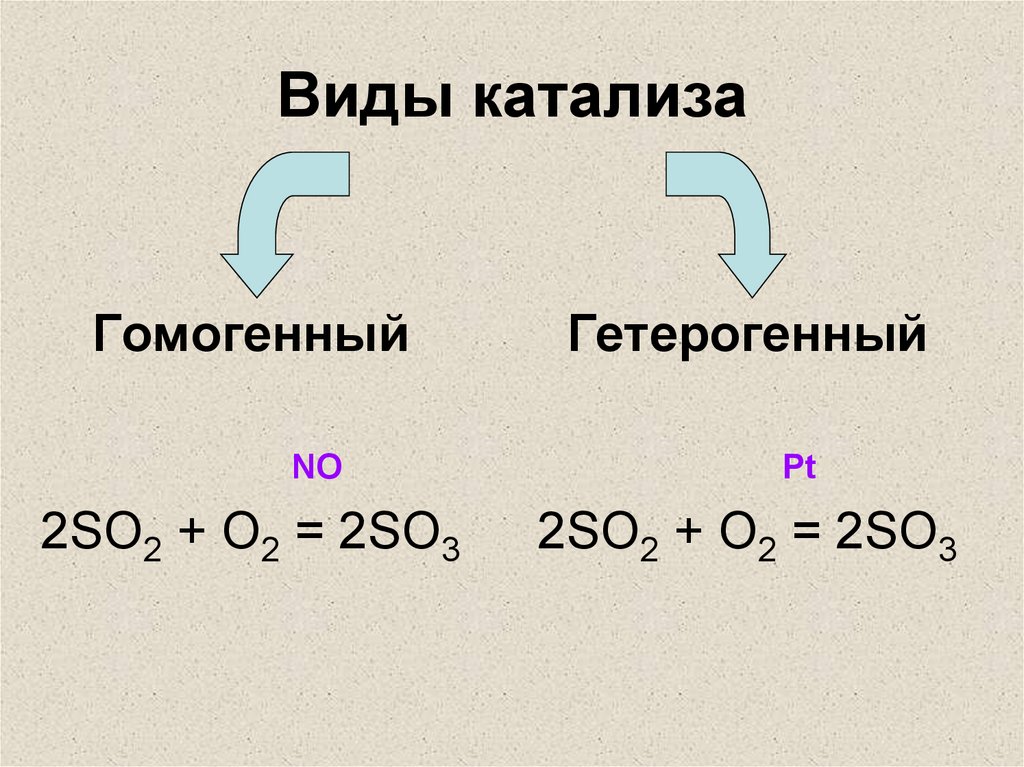
26. Виды катализа
ГомогенныйNO
2SO2 + O2 = 2SO3
Гетерогенный
Pt
2SO2 + O2 = 2SO3
27. Механизм действия катализаторов
Для гомогенного катализа:K
A + B = AB
A + K = [AK]
[AK] + B = AB + K
28. Окисление SO2 в SO3
NOSO2 + ½ O2 = SO3
NO + ½ O2 = NO2
SO2 + NO2 = SO3 + NO
29. Разложение H2O2
раствор K2Cr2O72H2O2 = 2H2O + O2 ↑
30. Разложение H2O2
MnO22H2O2 = 2H2O + O2 ↑


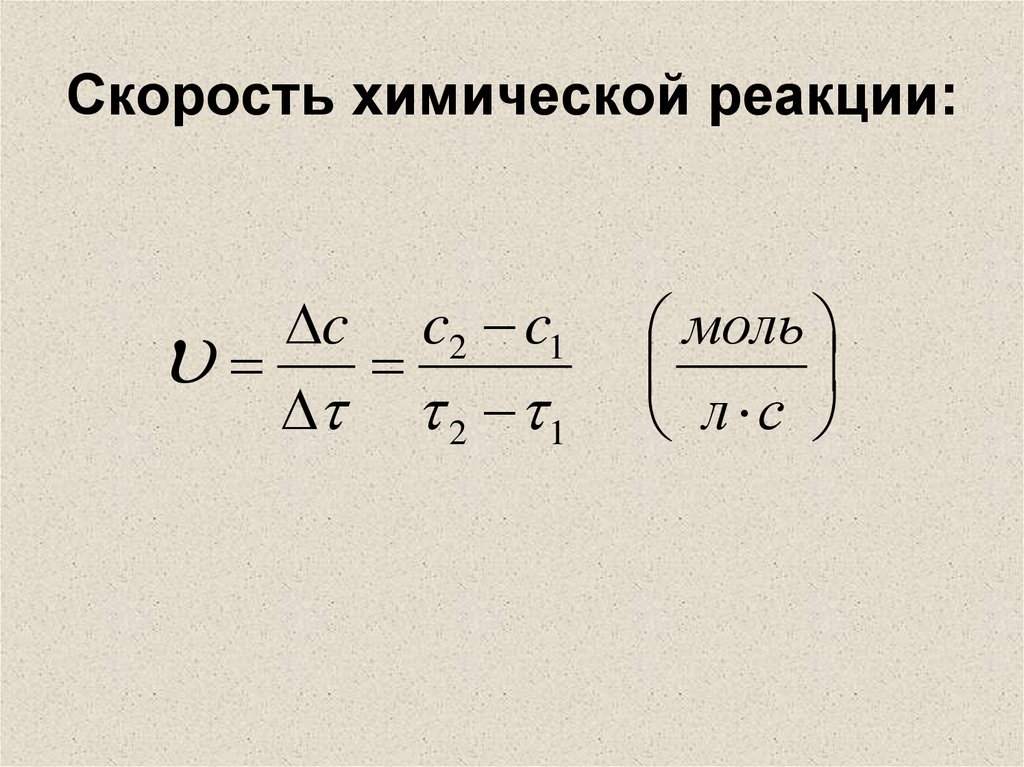















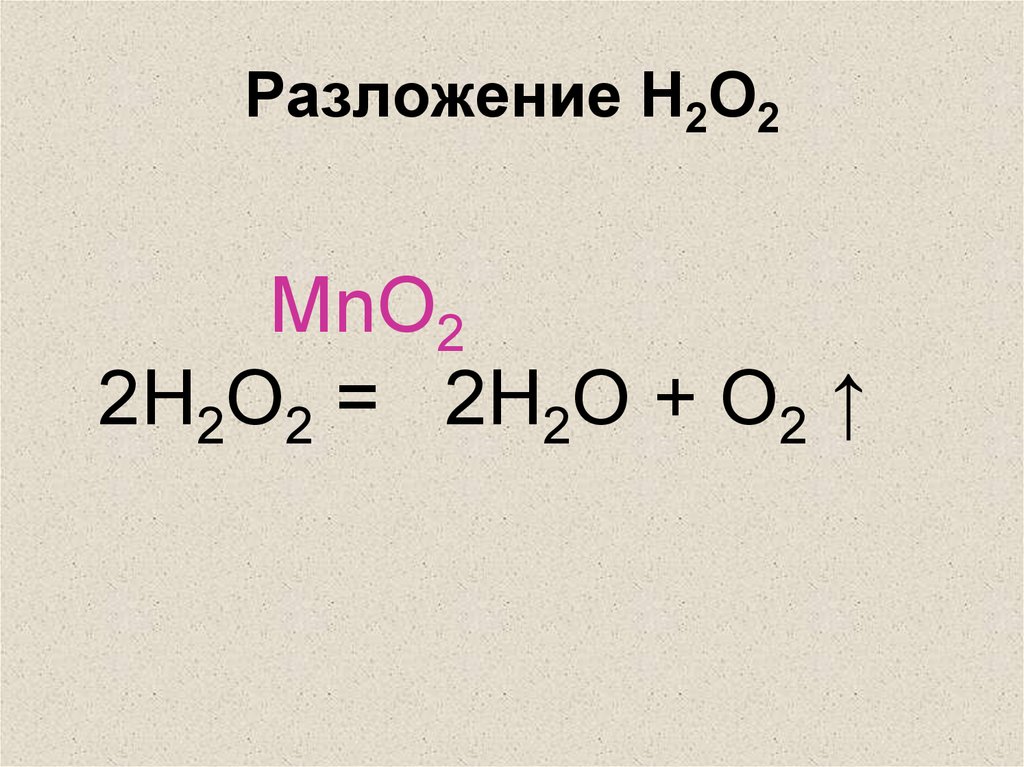
 Химия
Химия








