Похожие презентации:
Атомные спектры
1.
Атомные спектры2.
Открытие электрона• 1855 г.-Гейслер ( стеклянные сосуды особой
формы)
• 1875г.-У.Крукс ( сконструировал трубку в которой
можно было получить глубокий вакуум)
• 1876г.-Гольштейн(катодные лучи)
• 1897г.-Томсон ( катодные лучи отклоняются)
• 1911г.-Милликен ( измерил минимальный
электрический заряд)
3.
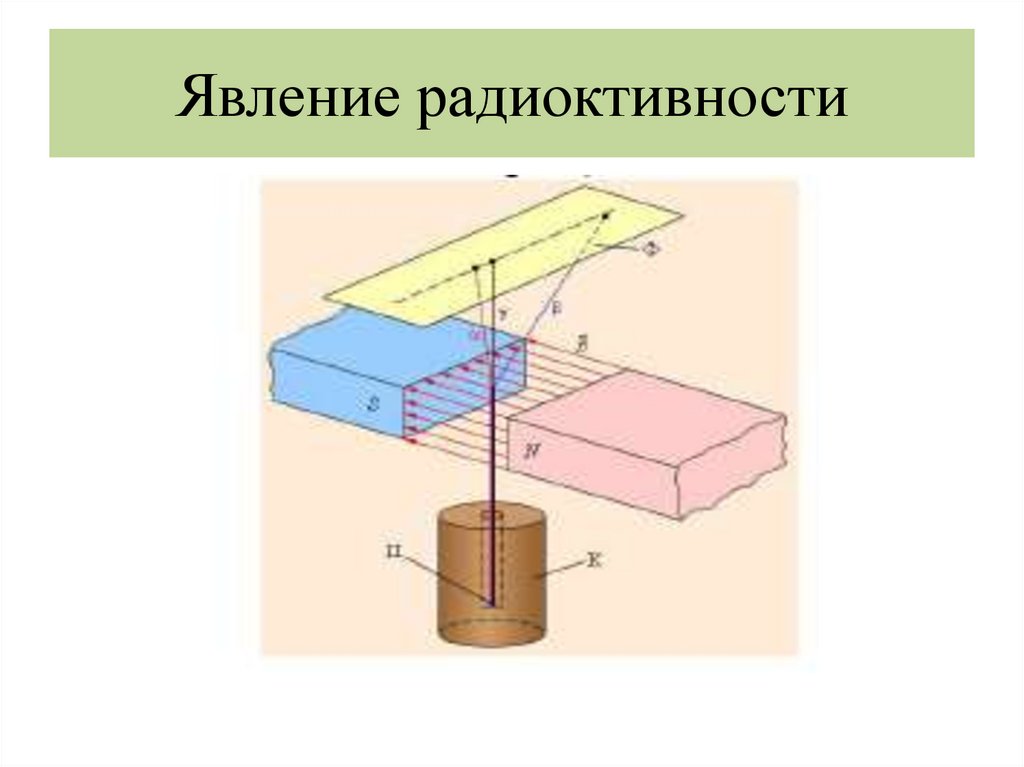
Явление радиоктивности4.
Планетарная модель атомамодель Резерфорда
недостатки
5.
Строение атома по Бору6.
Строение атома по БоруПервый постулат
• Электроны могут
обращаться вокруг ядра
атома только по строго
определенным,
разрешенным круговым
орбитам, причем, двигаясь
по таким орбитам,
электроны не излучают
электромагнитную
энергию
Второй постулат
• Излучение энергии атома
происходит только при
переходе электрона с
более отдаленных орбит
на орбиты,
расположенные ближе к
ядру
7.
Строение атома по Бору8.
Строение атома по Бору9.
Современные представления о строении атома10.
Уравнение М.Планка11.
Уравнение де Бройля12.
Принцип неопределенности В.Гейзенберга13.
Принцип неопределенности В.Гейзенберга14.
Квантовые числа15.
Квантовые числа• n-главное квантовое число, может
принимать только целочисленные
значения: 1,2,3,4 и т.д. Оно показывает
среднее расстояние электрона от ядра.
Его значение соответствует номеру
периода элемента в таблице
Менделеева
16.
Квантовые числа17.
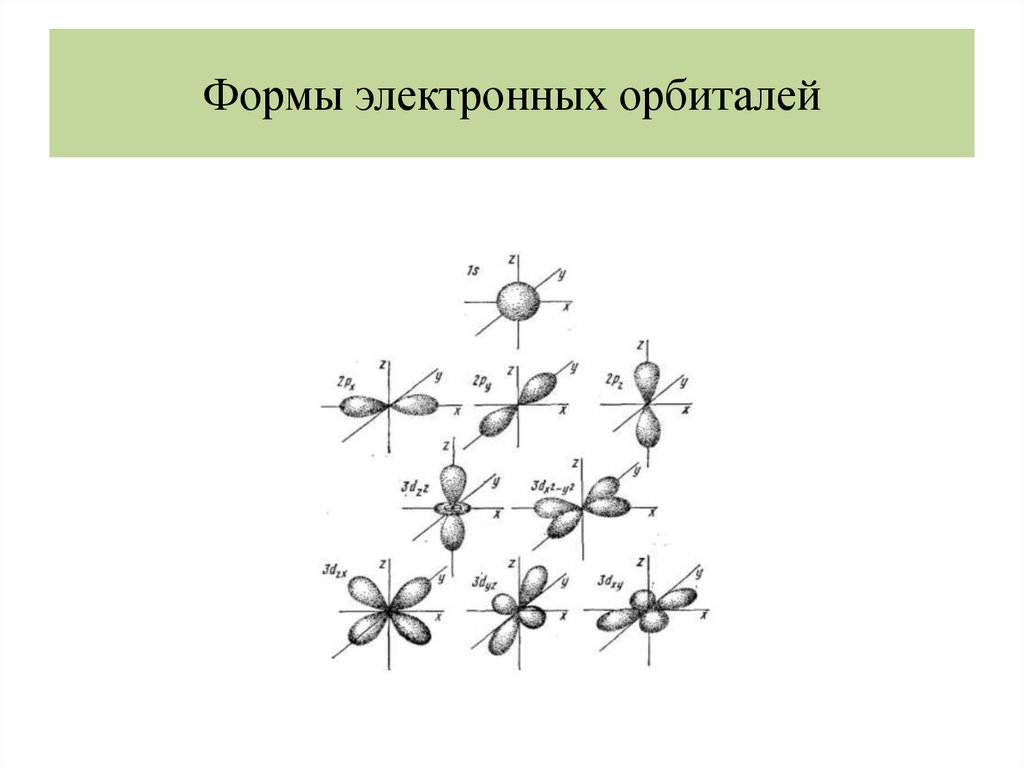
Формы электронных орбиталей18.
Квантовые числа19.
Возможные значения квантовых чисел20.
Заполнение электронами электронныхорбиталей многоэлектронных атомов
21.
Заполнение электронами электронныхорбиталей многоэлектронных атомов
22.
Изменение энергии электронных орбиталей23.
Принцип Паули ( запрет Паули)24.
Электронная емкость25.
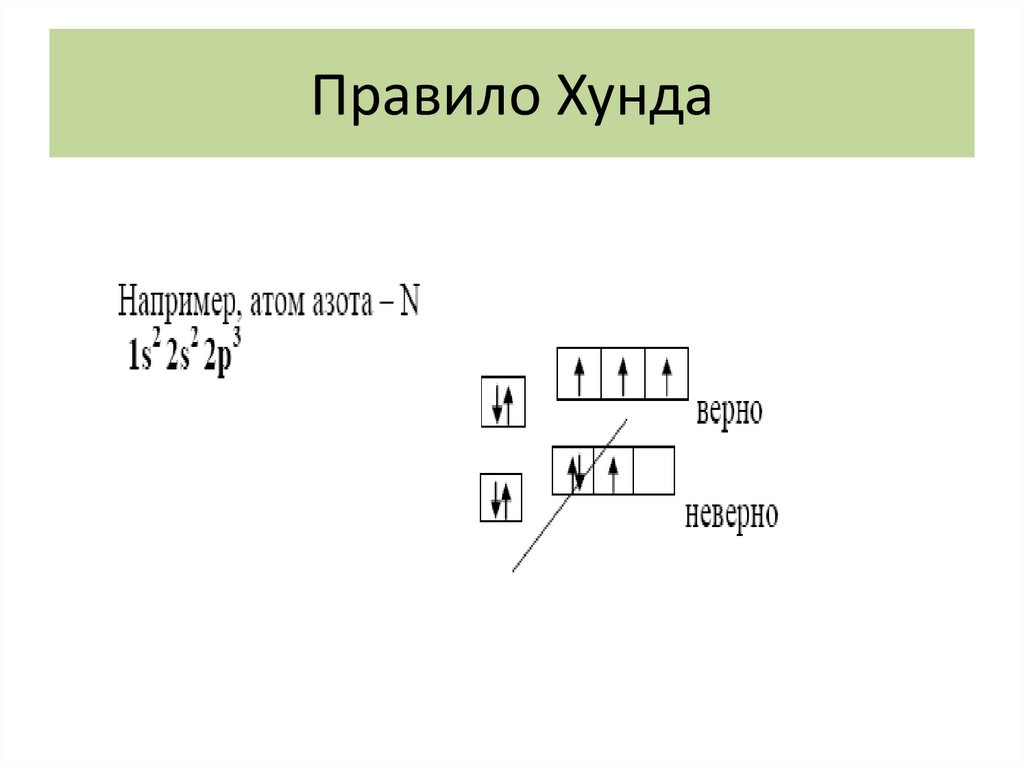
Правило Хунда26.
Правило Хунда27.
Основные характеристики атомов28.
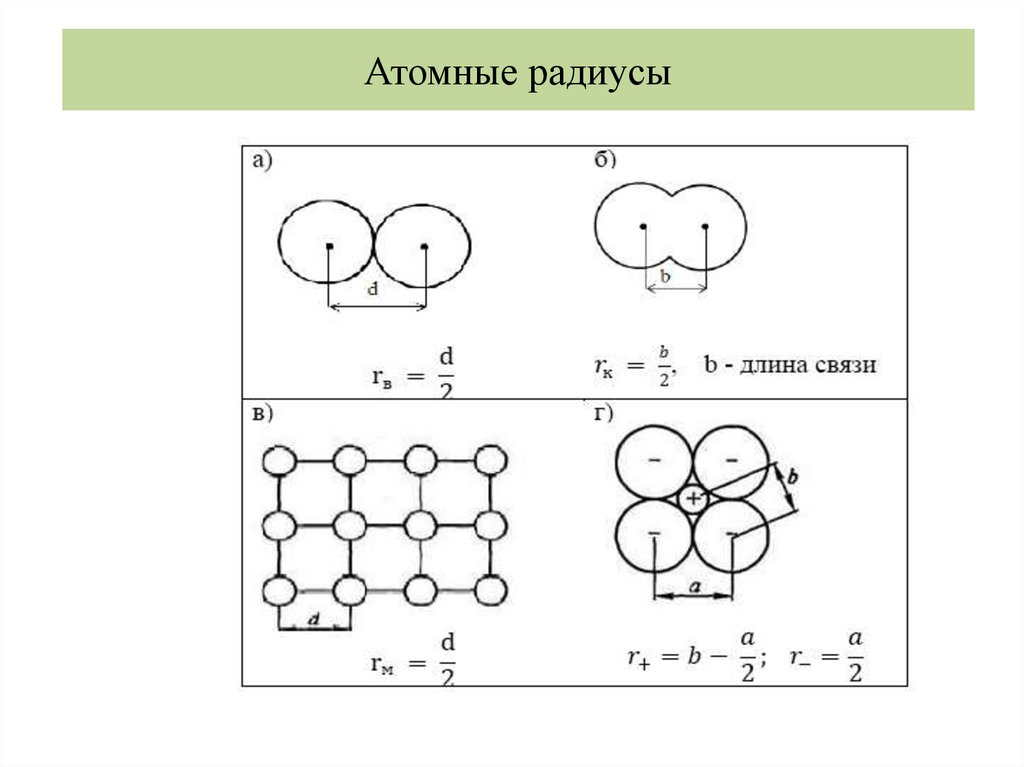
Атомные радиусы29.
Сопоставление разных типов радиусов30.
Потенциал ионизации31.
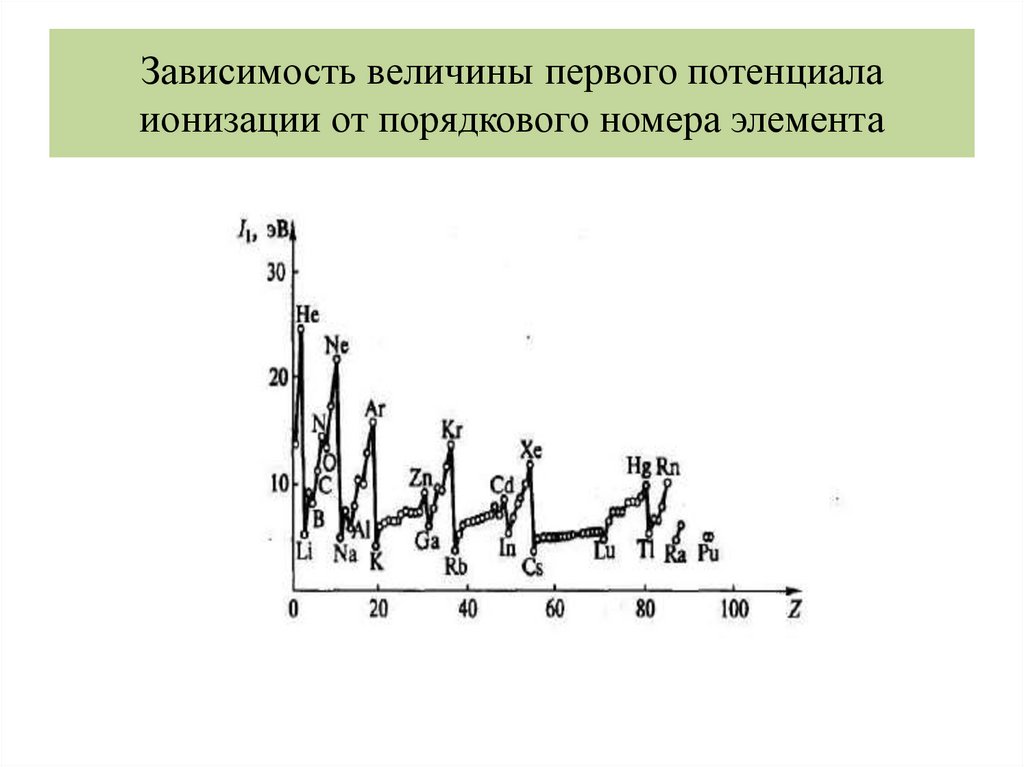
Зависимость величины первого потенциалаионизации от порядкового номера элемента





























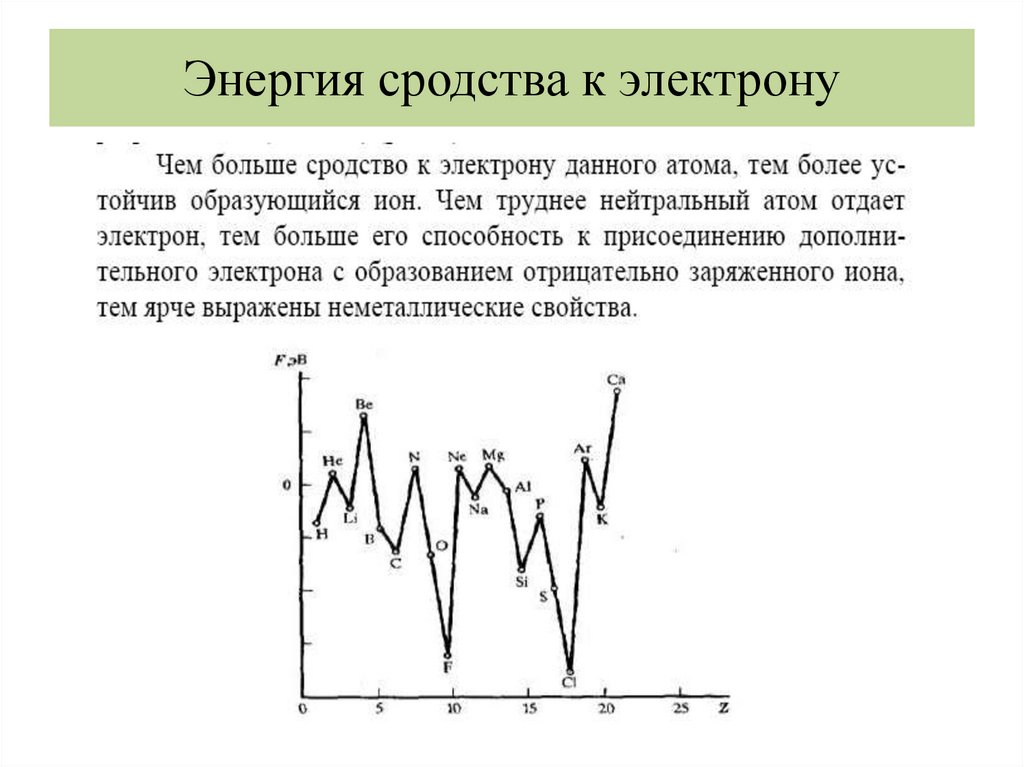


 Химия
Химия








