Похожие презентации:
Обобщение и систематизация знаний по теме « Химические реакции»
1. Обобщение и систематизация знаний по теме « Химические реакции»
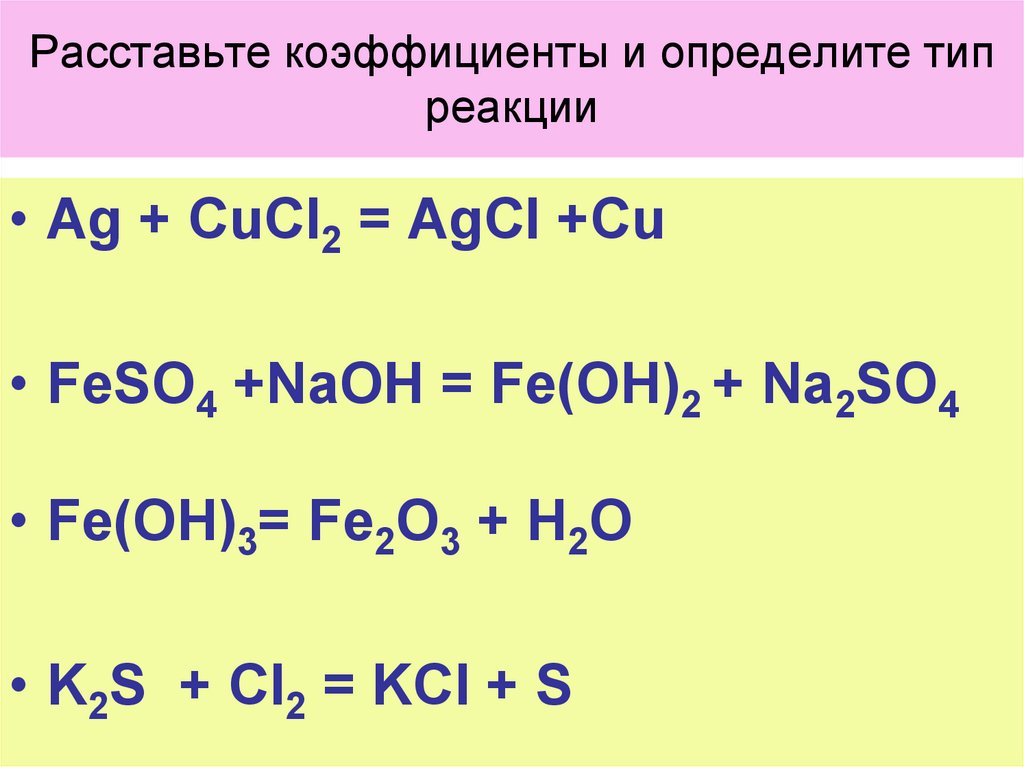
2. Расставьте коэффициенты и определите тип реакции
• Ag + CuCl2 = AgCl +Cu• FeSO4 +NaOH = Fe(OH)2 + Na2SO4
• Fe(OH)3= Fe2O3 + H2O
• K2S + Cl2 = KCl + S
3. Химическая реакция Признаки химических реакций Реагенты По каким признакам классифицируют химические реакции?
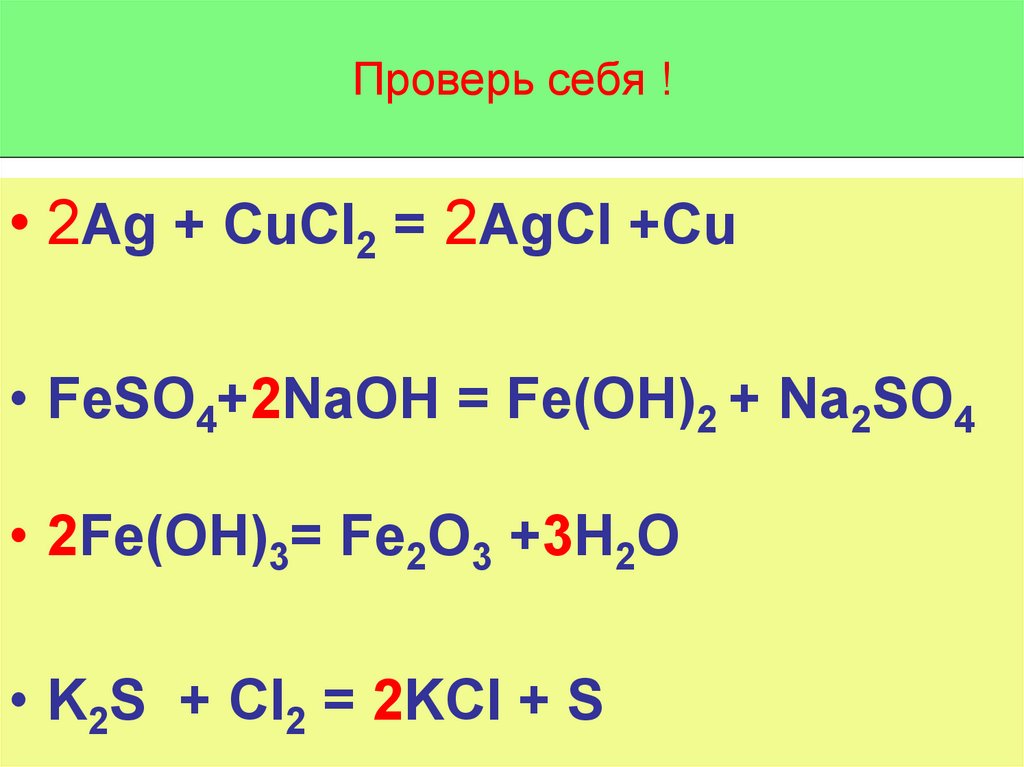
4. Проверь себя !
• 2Ag + CuCl2 = 2AgCl +Cu• FeSO4+2NaOH = Fe(OH)2 + Na2SO4
• 2Fe(OH)3= Fe2O3 +3H2O
• K2S + Cl2 = 2KCl + S
5. На примере реакции 2H2+ O2 = 2H2O докажите справедливость закона сохранения массы веществ
6. «Крестики-нолики» Выигрышный путь – металлы, вступающие в реакцию с кислотами
CuAl
Mn
Fe
Zn
Mg
Ag
Hg
Pt
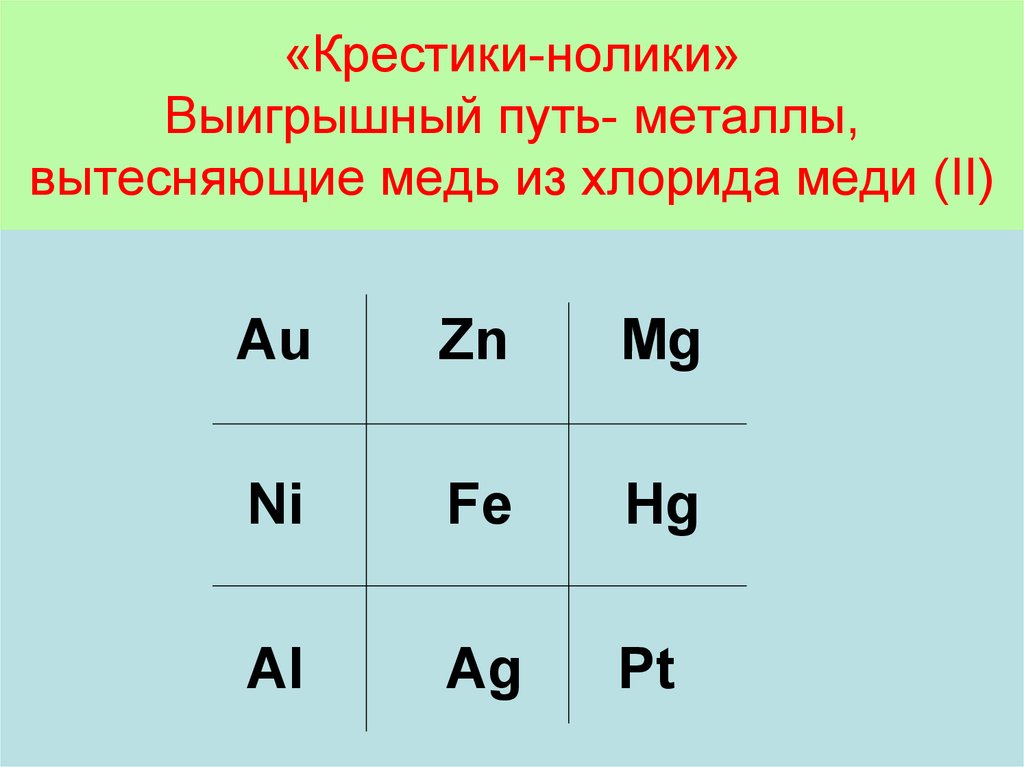
7. «Крестики-нолики» Выигрышный путь- металлы, вытесняющие медь из хлорида меди (II)
AuZn
Mg
Ni
Fe
Hg
Al
Ag
Pt
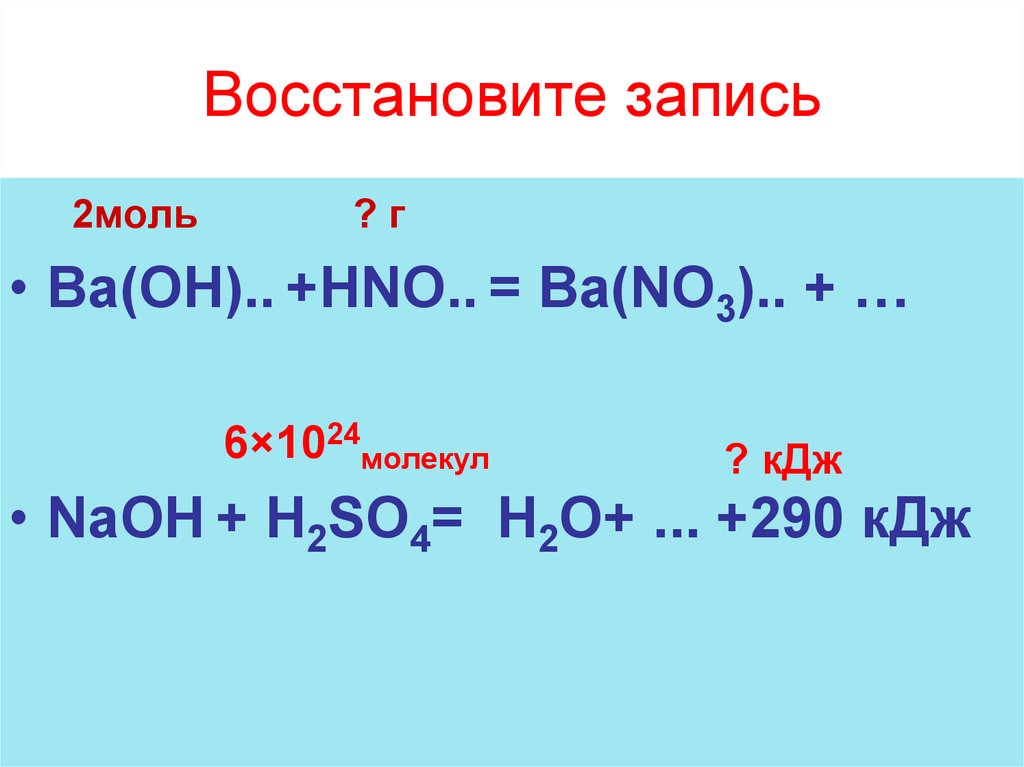
8. Восстановите запись
2моль?г
• Ва(OH).. +НNO.. = Ba(NO3).. + …
6×1024молекул
? кДж
• NaOH + H2SO4= H2O+ ... +290 кДж
9. Какая масса азотной кислоты потребуется для полной нейтрализации гидроксида бария количеством 2 моль?
2 моль?Г
• Ва(OH)2 +2НNO3 = Ba(NO3)2 + 2Н2О
10. Какое количество теплоты выделится при нейтрализации 6×1024 молекул серной кислоты?
Какое количество теплотывыделится при нейтрализации
24
6×10 молекул серной кислоты?
6×1024молекул
? кДж
2NaOH +H2SO4=2H2O+Na2SO4+290 кДж
11. Расставь коэффициенты. Найди реакции, в которых взаимодействуют между собой: а) желтo-зеленый и небесно-голубой; б) тяжелый и
светло-желтая;в) зловонный и светящийся.
• 1) O2+ C = CO2
1) Cl2 + Cs =CsCl
• 2) Ba + S = BaS
2) Al + O2= Al2O3
• 3) C + O2= CO
3) P + Br2 =PBr3
• 4) P + Br2= PBr5
1 вариант
4) H2 + F2 = HF
2 вариант
12. Самостоятельная работа
13. Расшифруйте схемы химических процессов, запиши их с помощью химических символов и индексов, расставьте коэффициенты, определите
тип реакцииа)
б)
в)
г)
1-1 + 8-8 = 1-8-1;
1-1 + 12-8 = 12 + 1-8-1;
1-1 + 16 = 1-16-1;
8-8-8 = 8-8









 Химия
Химия








