Похожие презентации:
Типы химических реакций
1. Типы химических реакций
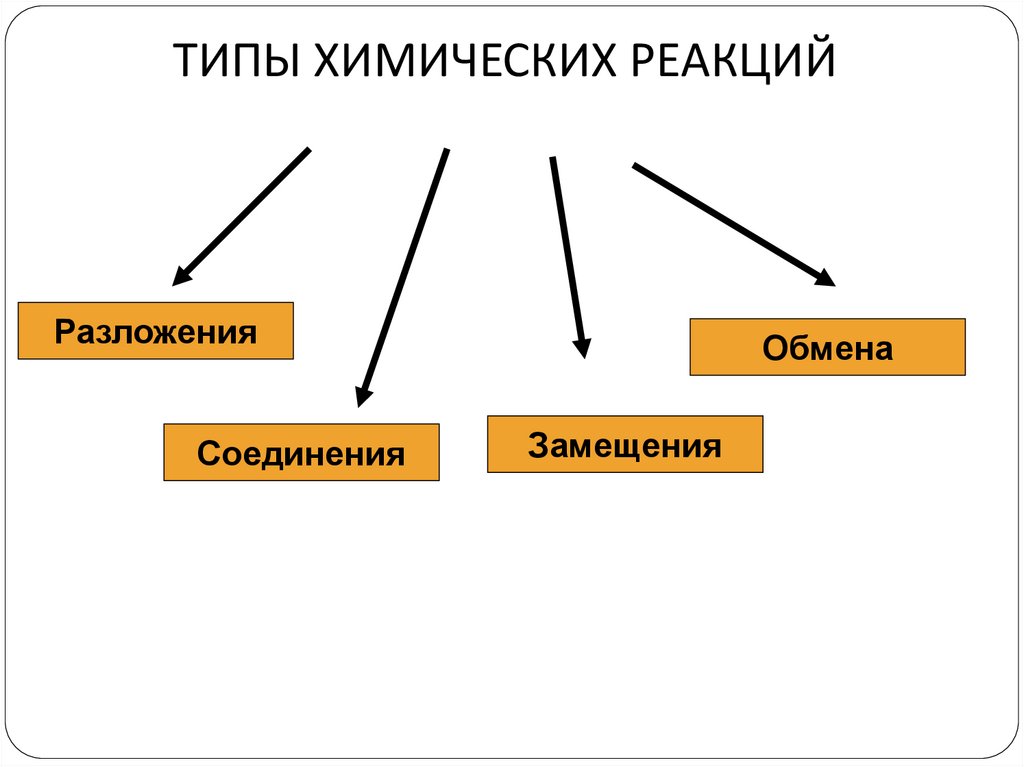
2. ТИПЫ ХИМИЧЕСКИХ РЕАКЦИЙ
РазложенияСоединения
Обмена
Замещения
3. Реакция разложения малахита:
(CuOH)2CO3 = 2CuO + H2O + CO2
Малахит
оксид
меди (II)
вода
оксид
углерода (IV)
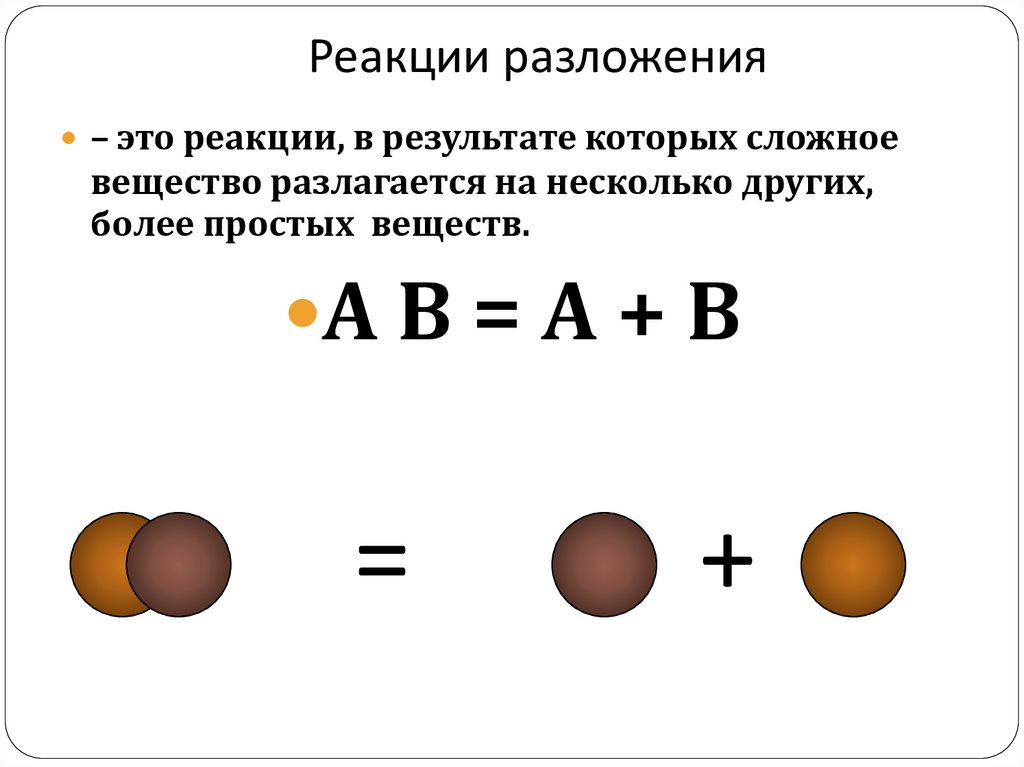
4. Реакции разложения
– это реакции, в результате которых сложноевещество разлагается на несколько других,
более простых веществ.
А В = А + В
=
+
5. Признаки реакции разложения
1.В реакции принимает участие только одно
исходное сложное вещество
2. Образуется два и более новых как простых,
так и сложных веществ
3. Как правило почти все реакции
разложения будут эндотермические (- Q)
(нужна непрерывная подача тепла)
6. Реакция соединения
Cu + Cl2 = CuCl22Fe + 3Cl2 = 2Fe Cl3
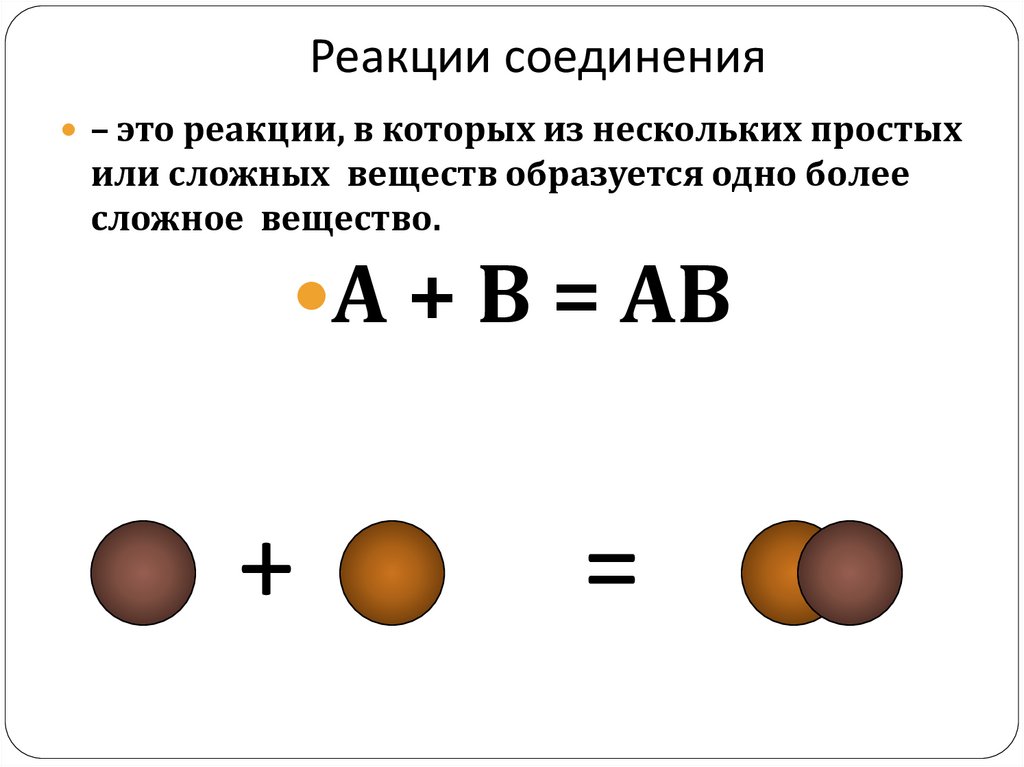
7. Реакции соединения
– это реакции, в которых из нескольких простыхили сложных веществ образуется одно более
сложное вещество.
А + В = АВ
+
=
8. Признаки реакции соединения
1. В реакции участвуют два или более какпростых, так и сложных веществ
2. Образуется одно сложное вещество
3. Как правило почти все реакции соединения
будут экзотермические (+ Q)
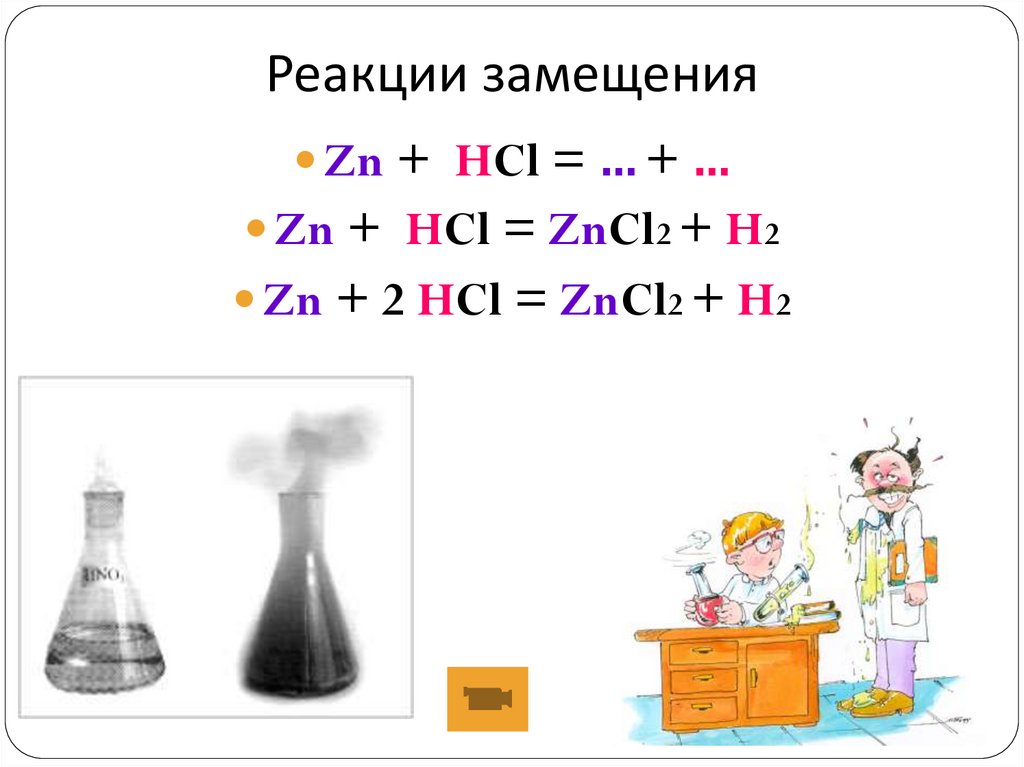
9. Реакции замещения
Zn + HCl = … + …Zn + HCl = ZnCl2 + H2
Zn + 2 HCl = ZnCl2 + H2
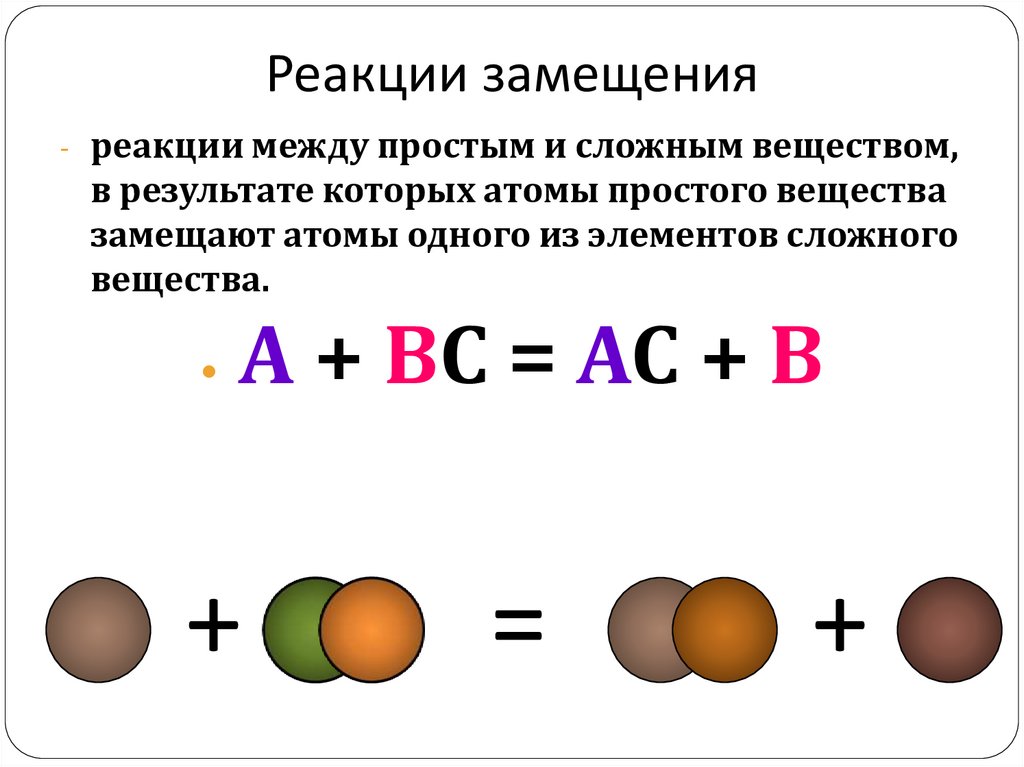
10. Реакции замещения
- реакции между простым и сложным веществом,в результате которых атомы простого вещества
замещают атомы одного из элементов сложного
вещества.
А + ВС = АС + В
+
=
+
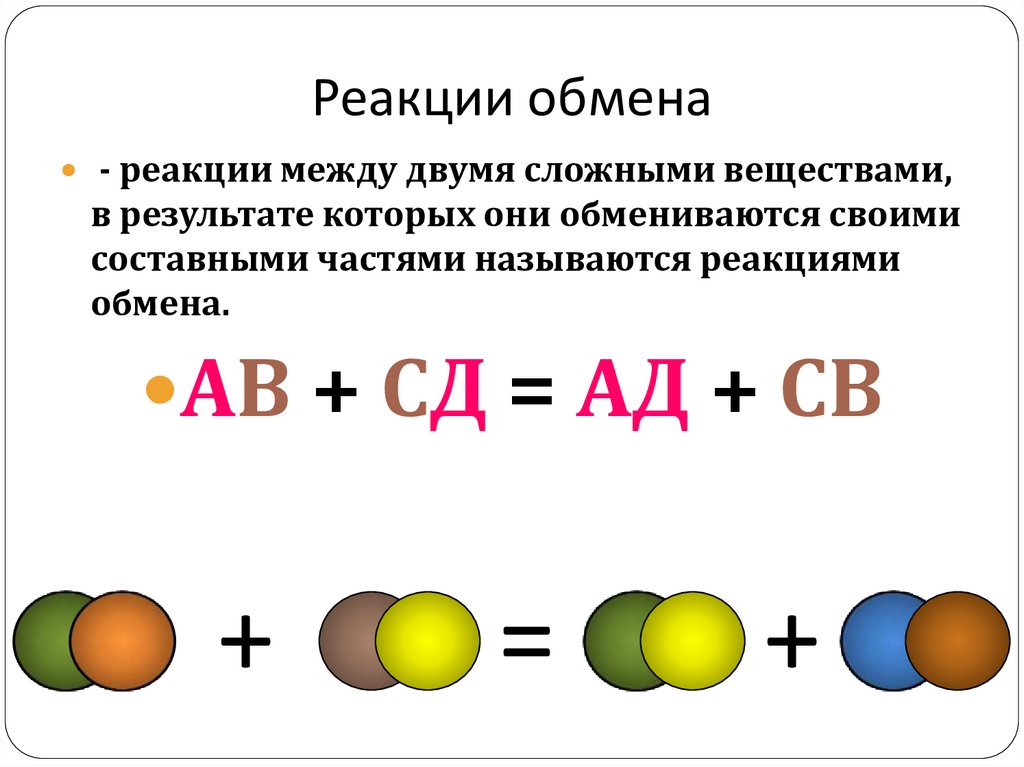
11. Реакции обмена
CuO + H2SO4 = CuSO4 + H2O12. Реакции обмена
- реакции между двумя сложными веществами,в результате которых они обмениваются своими
составными частями называются реакциями
обмена.
АВ + СД = АД + СВ
+
=
+
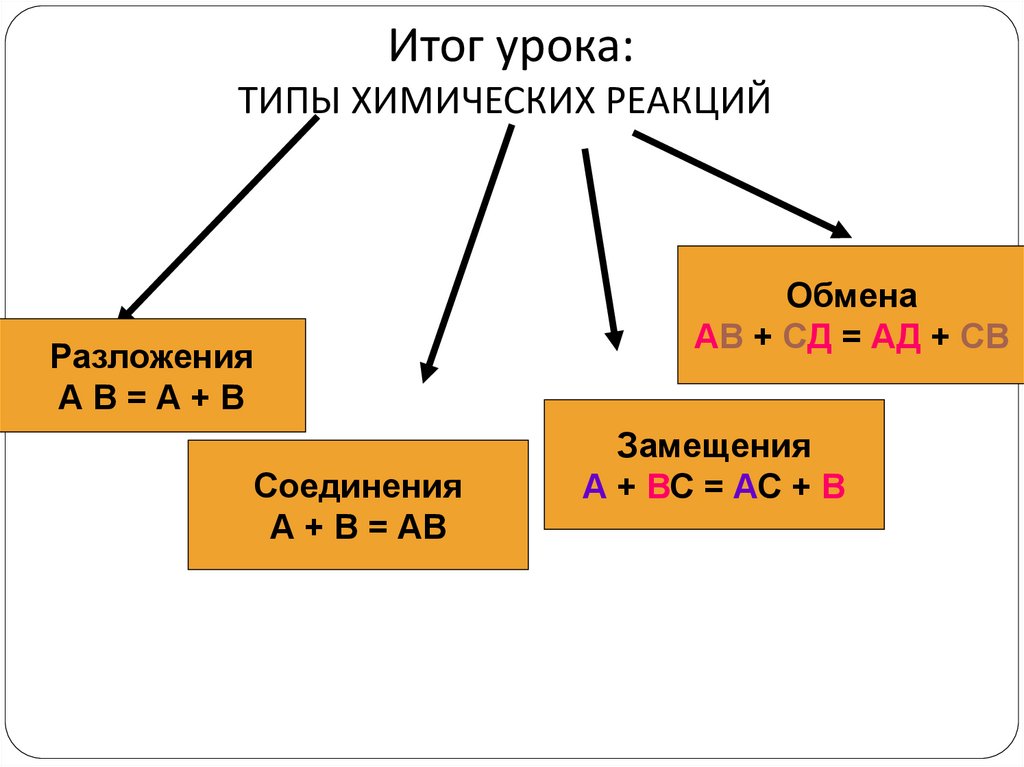
13. Итог урока: ТИПЫ ХИМИЧЕСКИХ РЕАКЦИЙ
РазложенияАВ=А+В
Соединения
А + В = АВ
Обмена
АВ + СД = АД + СВ
Замещения
А + ВС = АС + В
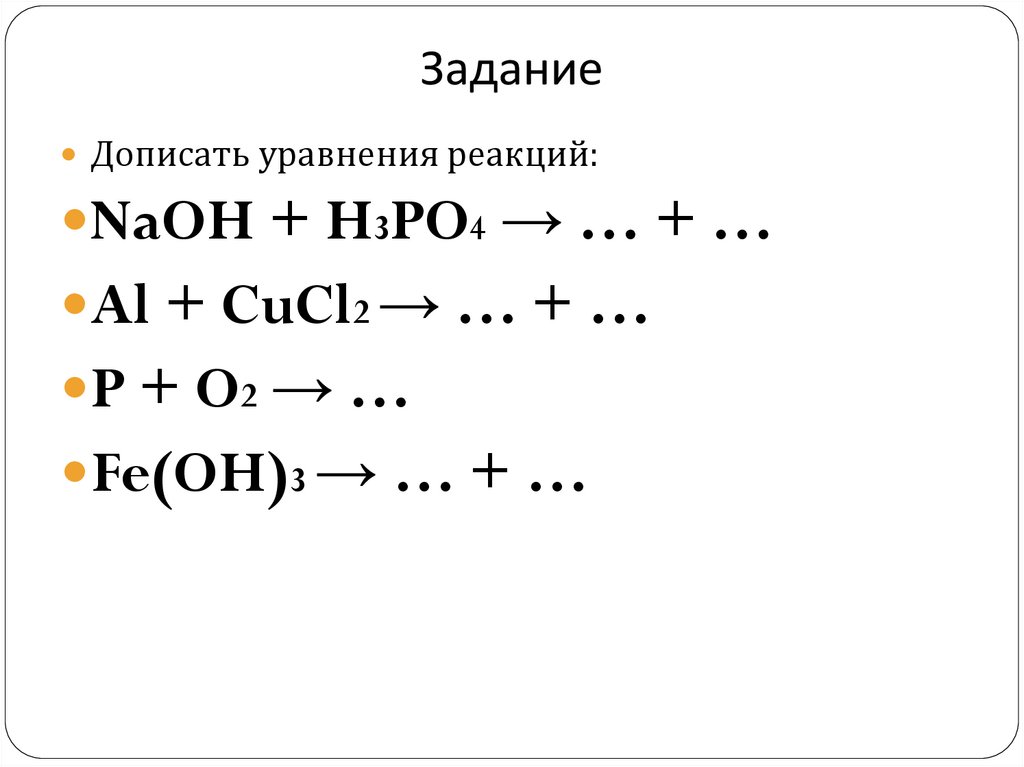
14. Задание
Дописать уравнения реакций:NaOH + H3PO4 → … + …
Al + CuCl2 → … + …
P + O2 → …
Fe(OH)3 → … + …
15. Задание
Дописать уравнения реакций:3NaOH + H3PO4 = Na3PO4 + 3H2O
2Al + 3CuCl2 = 3 Cu + 2AlCl3
4P + 5O2 = 2P2O5
2Fe(OH)3 → Fe2O3 + 3H2O
16. Определите тип реакции
1) CaO + CO2 = CaCO32) H2SO4 + 2NaOH = Na2SO4 + 2H2O
3) Fe + S = FeS
4) 2H2O = 2H2 + O2↑
5) CuO + H2 = Cu + H2O
6) Zn + 2HCl = ZnCl2 + H2↑
7) ZnO + H2SO4 = ZnSO4 + H2O
8) Cu(OH)2 = CuO + H2O
А) соединения
Б) обмена
В) разложения
Г) замещения
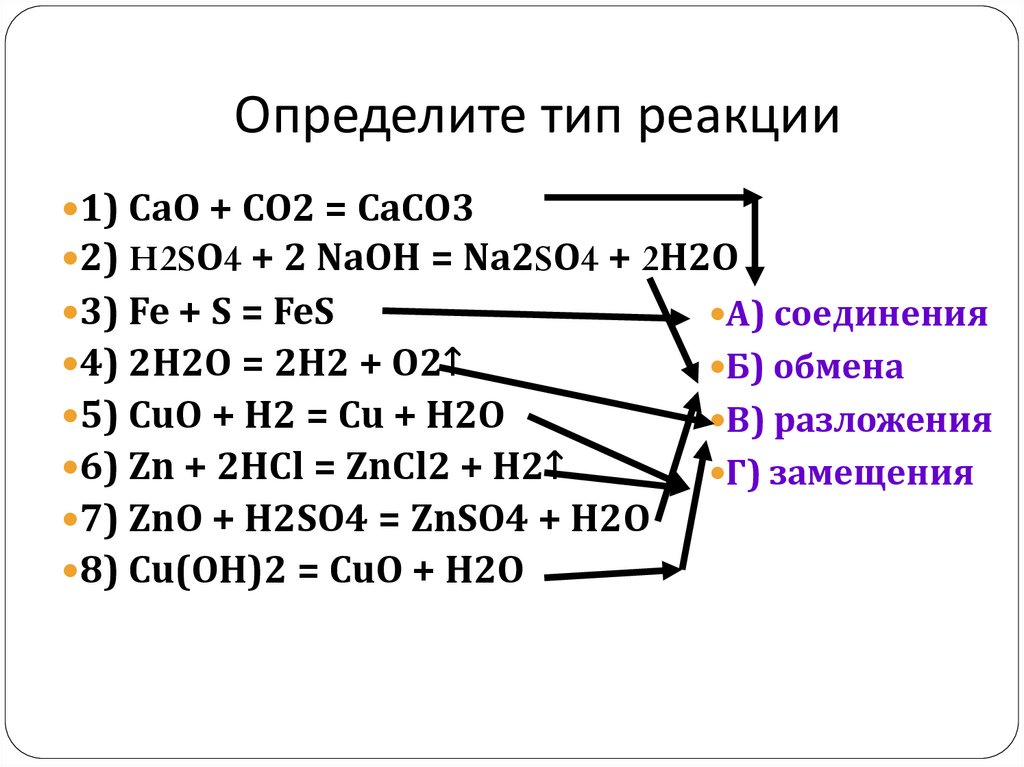
17. Определите тип реакции
1) CaO + CO2 = CaCO32) H2SO4 + 2 NaOH = Na2SO4 + 2H2O
3) Fe + S = FeS
А) соединения
4) 2H2O = 2H2 + O2↑
Б) обмена
5) CuO + H2 = Cu + H2O
В) разложения
6) Zn + 2HCl = ZnCl2 + H2↑
Г) замещения
7) ZnO + H2SO4 = ZnSO4 + H2O
8) Cu(OH)2 = CuO + H2O
18. Определите тип реакций и расставьте коэффициенты:
1) HgO → Hg + O22) CaCO3 → CaO + CO2
3) CuSO4 + Fe → Cu + FeSO4
4) CuO + H2 → Cu + H2O
5) H2 + O2 → H2O
6) H2SO4 + KOH → K2SO4 + H2O
7) BaO + SO2 → BaSO3










 Химия
Химия








