Похожие презентации:
Химические свойства спиртов и фенола
1. Химические свойства спиртов и фенола
2.
СпиртыСпирты– органические вещества,
молекулы которых содержат одну или
несколько гидроксильных групп,
соединенных с углеводородным
радикалом.
Общая формула одноатомных предельных
спиртов СnН2n+1ОН
3.
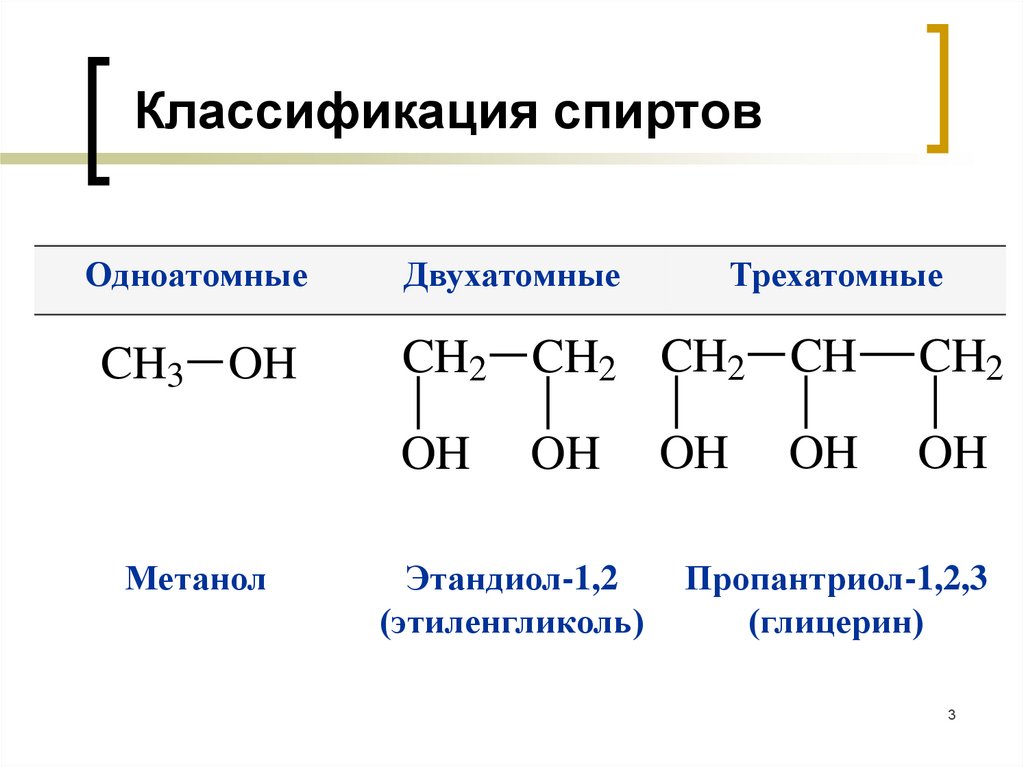
Классификация спиртовОдноатомные
CH3 OH
Двухатомные
CH2 CH2 CH2 CH
OH
Метанол
Трехатомные
OH
Этандиол-1,2
(этиленгликоль)
OH
OH
CH2
OH
Пропантриол-1,2,3
(глицерин)
3
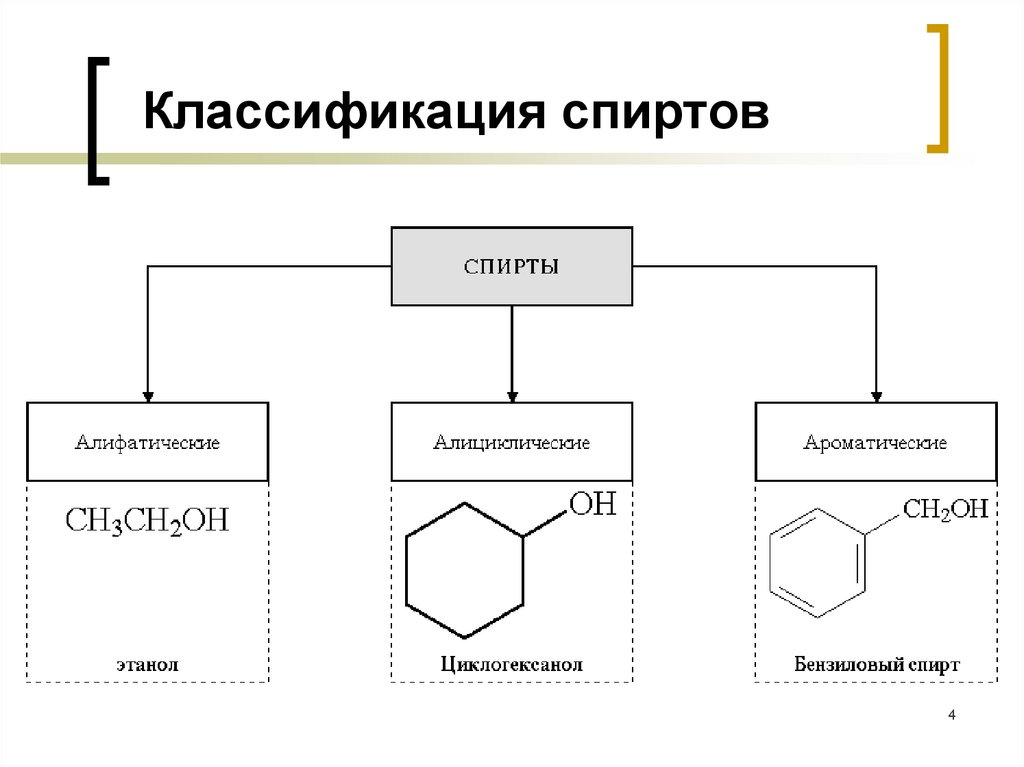
4.
Классификация спиртов4
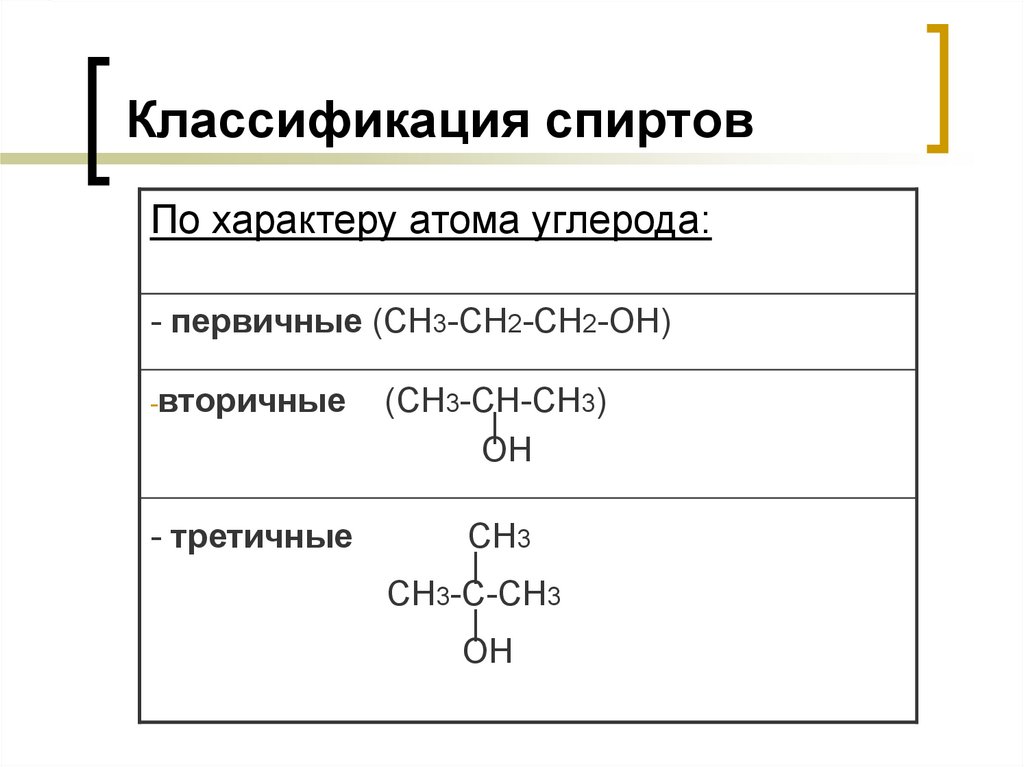
5. Классификация спиртов
По характеру атома углерода:- первичные (СН3-СН2-СН2-ОН)
-вторичные
(СН3-СН-СН3)
|
ОН
- третичные
СН3
|
СН3-C-СН3
|
ОН
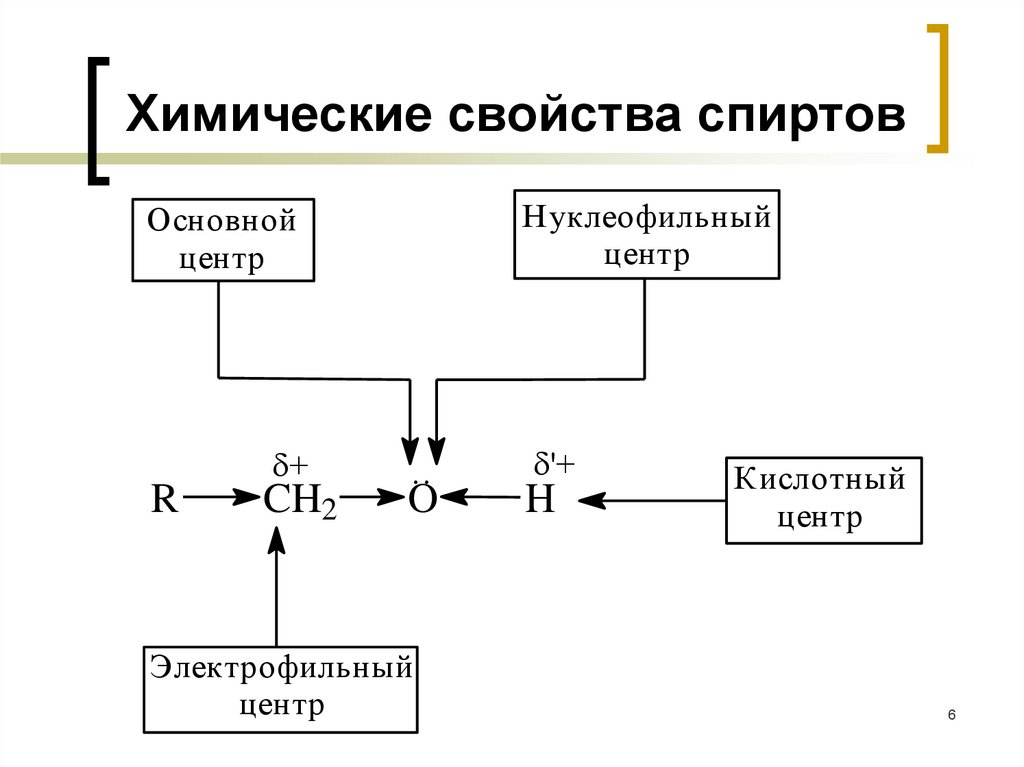
6.
Химические свойства спиртовНуклеофильный
центр
Основной
центр
R
+
CH2
..
O
Электрофильный
центр
'+
H
Кислотный
центр
6
7. Химические свойства спиртов
С щелочными металлами:2СH CH CH OH + 2Na
2СH CH CH ONa + H
3
2
3
2
2
2
2
Гидролиз алкоголятов:
С2Н5ОNa + Н2О = С2Н5ОН + NaОН
8.
Химические свойства спиртовС галогеноводородами:
R–OH + HBr R–Br + H2O
9.
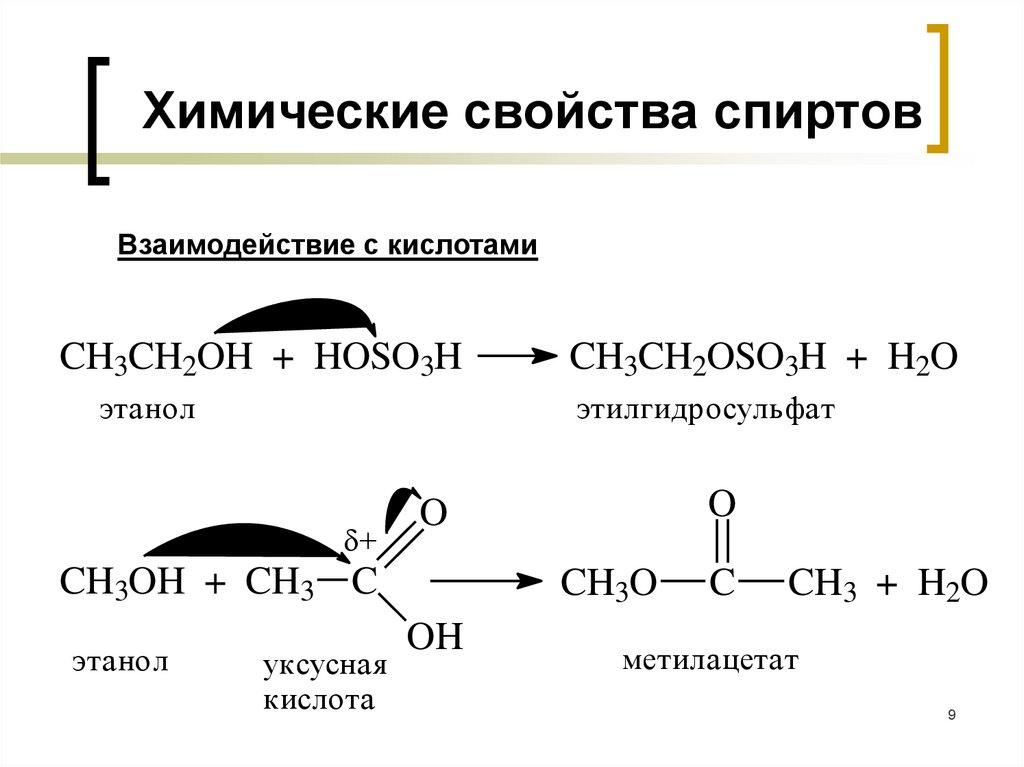
Химические свойства спиртовВзаимодействие с кислотами
CH3CH2OH + HOSO3H
этанол
этилгидросульфат
+
уксусная
кислота
O
O
CH3OH + CH3 C
этанол
CH3CH2OSO3H + H2O
CH3O
OH
C
CH3 + H2O
метилацетат
9
10.
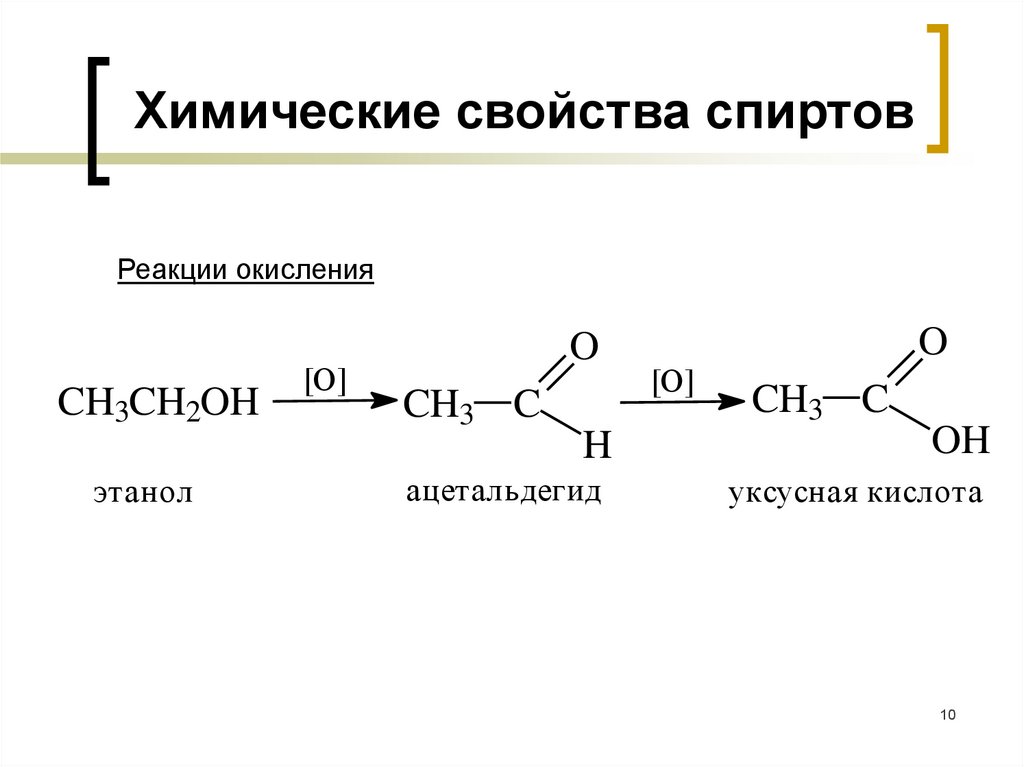
Химические свойства спиртовРеакции окисления
CH3CH2OH
этанол
[O]
O
CH3 C
H
ацетальдегид
[O]
O
CH3 C
OH
уксусная кислота
10
11.
Химические свойства спиртовМежмолекулярная дегидратация спиртов:
2CH3CH2OH
этанол
H+
CH3CH2OCH2CH3 + H2O
диэтиловый эфир
11
12.
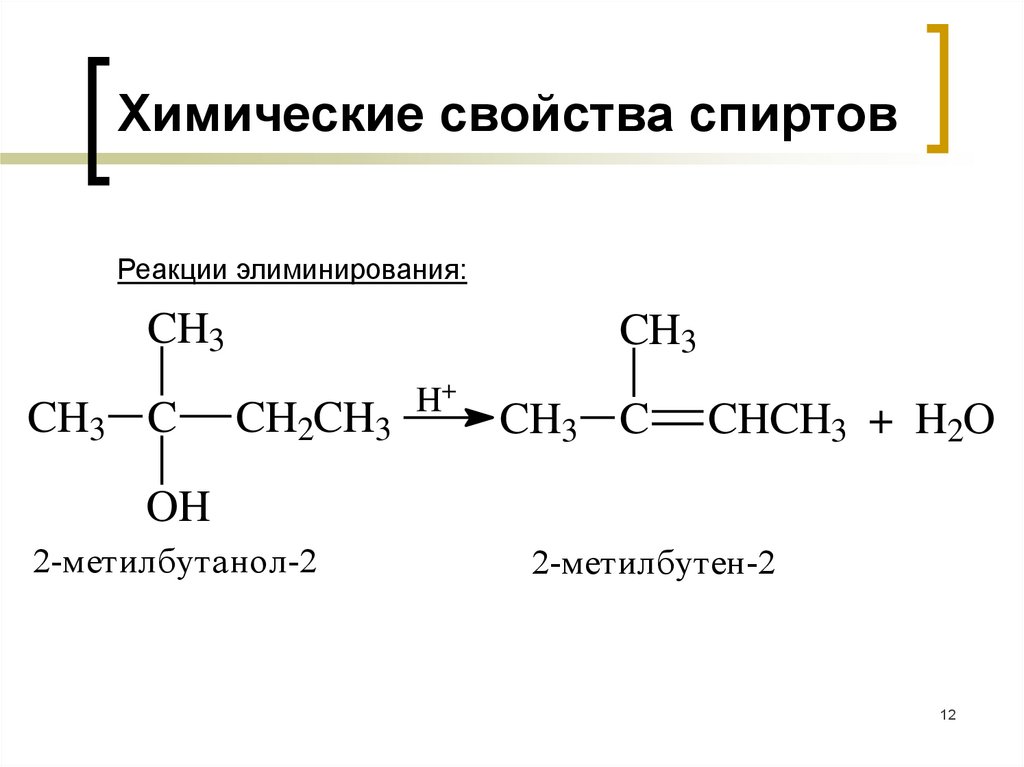
Химические свойства спиртовРеакции элиминирования:
CH3
CH3 C
CH3
CH2CH3
H+
CH3 C
CHCH3 + H2O
OH
2-метилбутанол-2
2-метилбутен-2
12
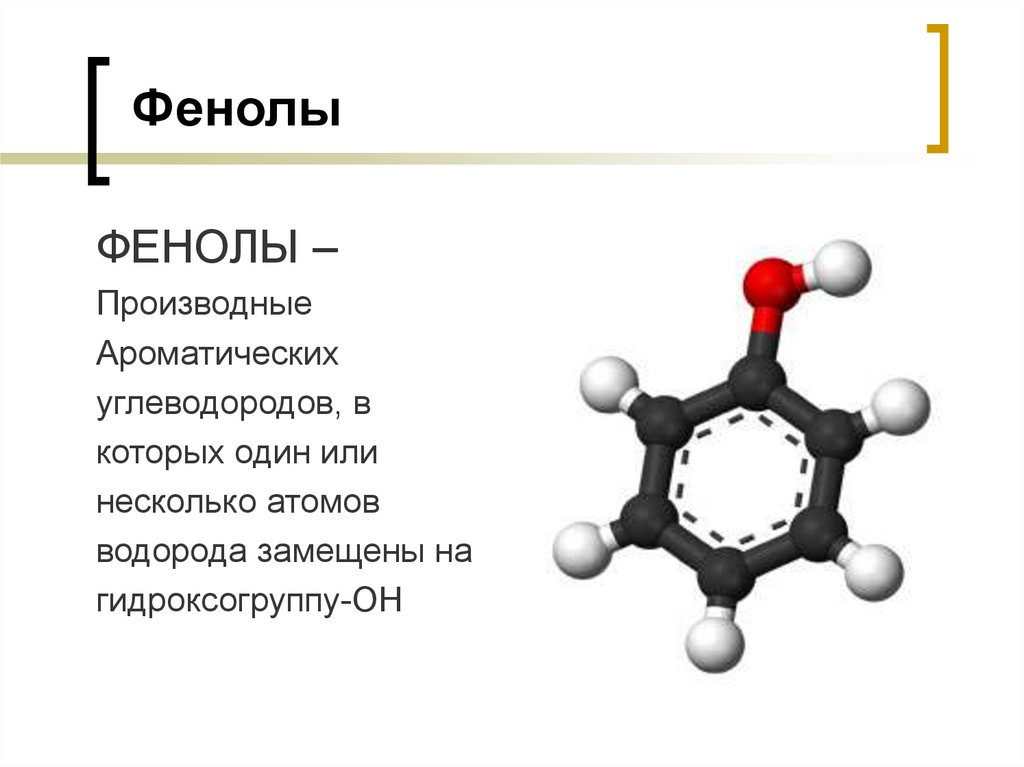
13. Фенолы
ФЕНОЛЫ –Производные
Ароматических
углеводородов, в
которых один или
несколько атомов
водорода замещены на
гидроксогруппу-ОН
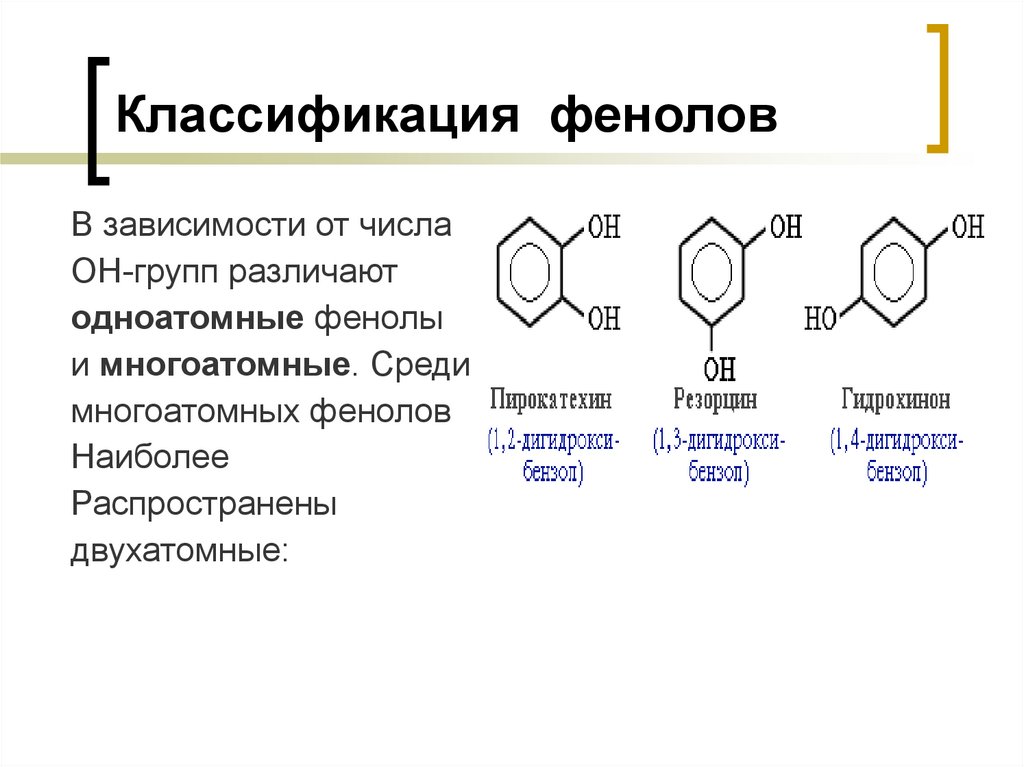
14. Классификация фенолов
В зависимости от числаОН-групп различают
одноатомные фенолы
и многоатомные. Среди
многоатомных фенолов
Наиболее
Распространены
двухатомные:
15.
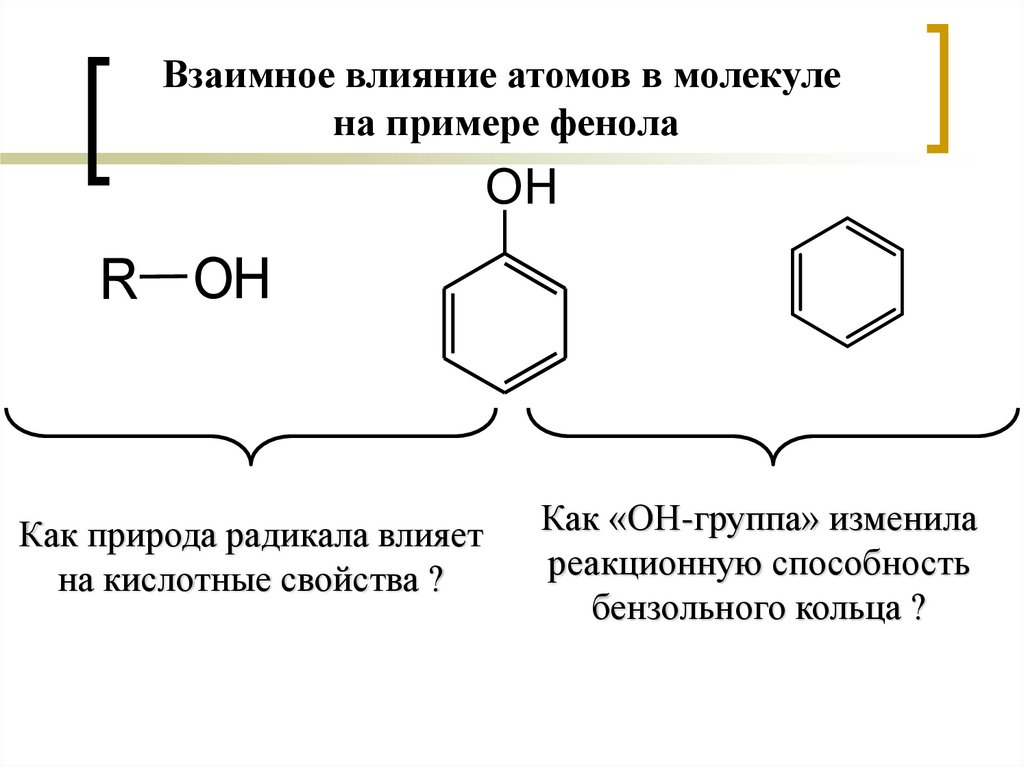
Взаимное влияние атомов в молекулена примере фенола
OH
R OH
Как природа радикала влияет
на кислотные свойства ?
Как «ОН-группа» изменила
реакционную способность
бензольного кольца ?
16. Химические свойства фенола:
2 С6Н5ОН + 2Na = 2С6Н5ОNa + H2С6Н5ОН + NaОН = С6Н5ОNa + H2О
17.
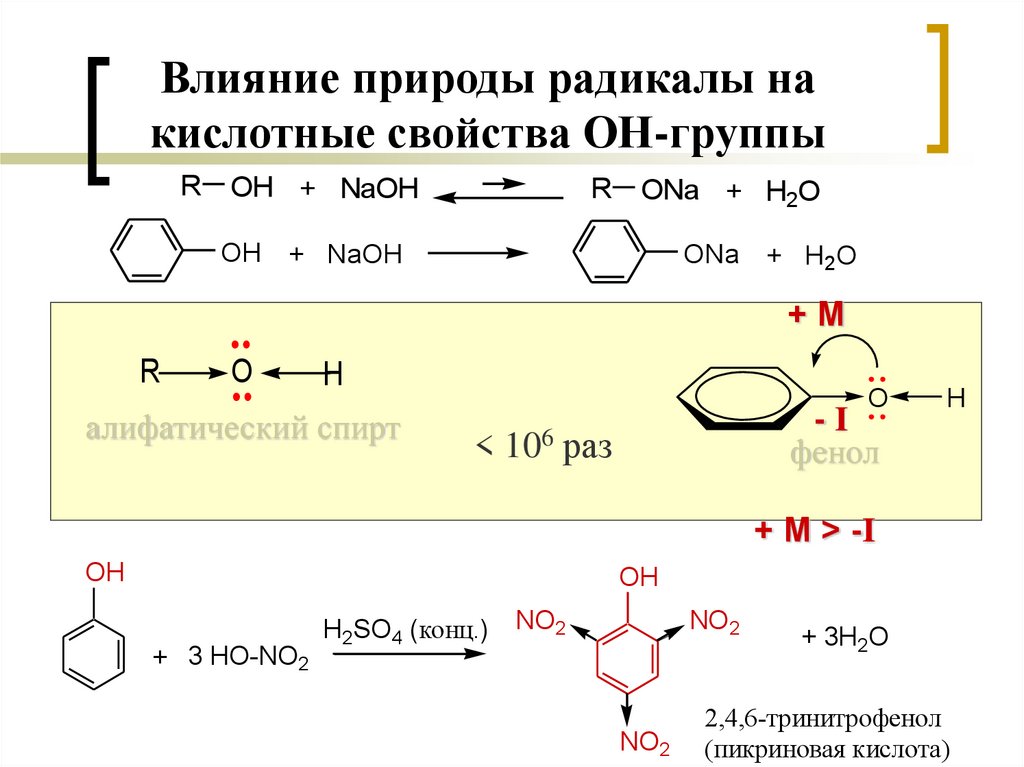
Влияние природы радикалы накислотные свойства ОН-группы
R
OH + NaOH
R
ONa + H2O
OH + NaOH
ONa + H2O
+М
R
O
H
алифатический спирт
O
<
106
-I
фенол
раз
H
+ М > -I
OH
OH
+ 3 HO-NO2
H2SO4 (конц.)
NO2
NO2
NO2
+ 3H2O
2,4,6-тринитрофенол
(пикриновая кислота)
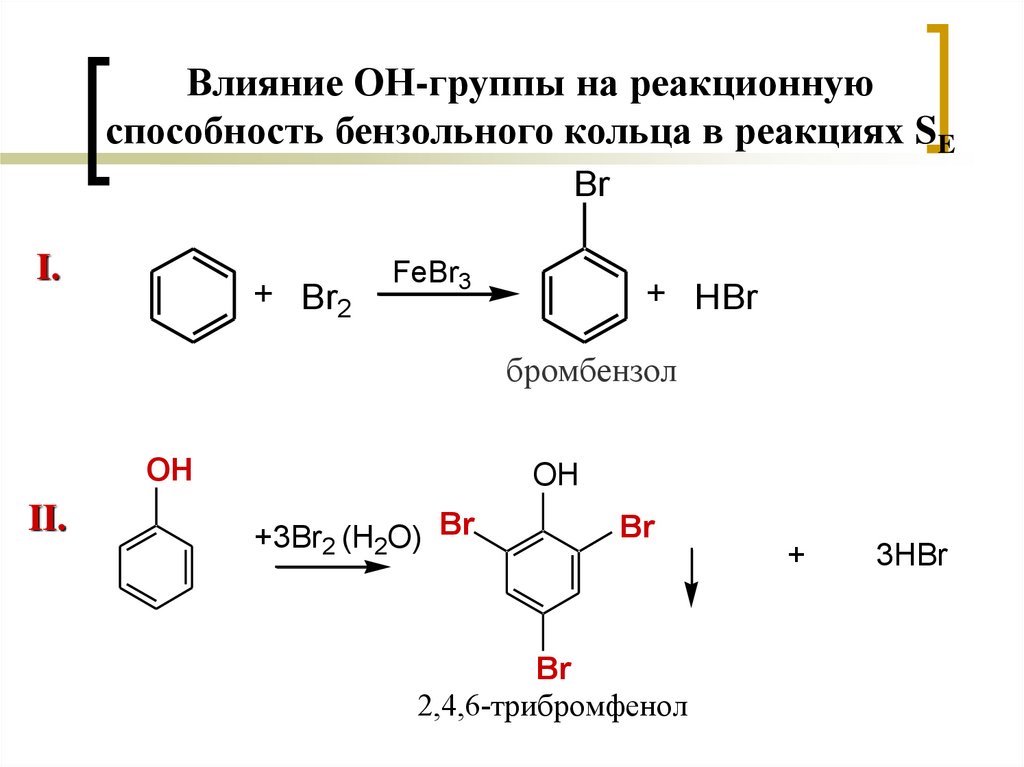
18.
Влияние ОН-группы на реакционнуюспособность бензольного кольца в реакциях SE
Br
I.
+ Br2
FeBr3
+ HBr
бромбензол
OH
II.
OH
+3Br2 (H2O) Br
Br
Br
2,4,6-трибромфенол
+
3HBr
19.
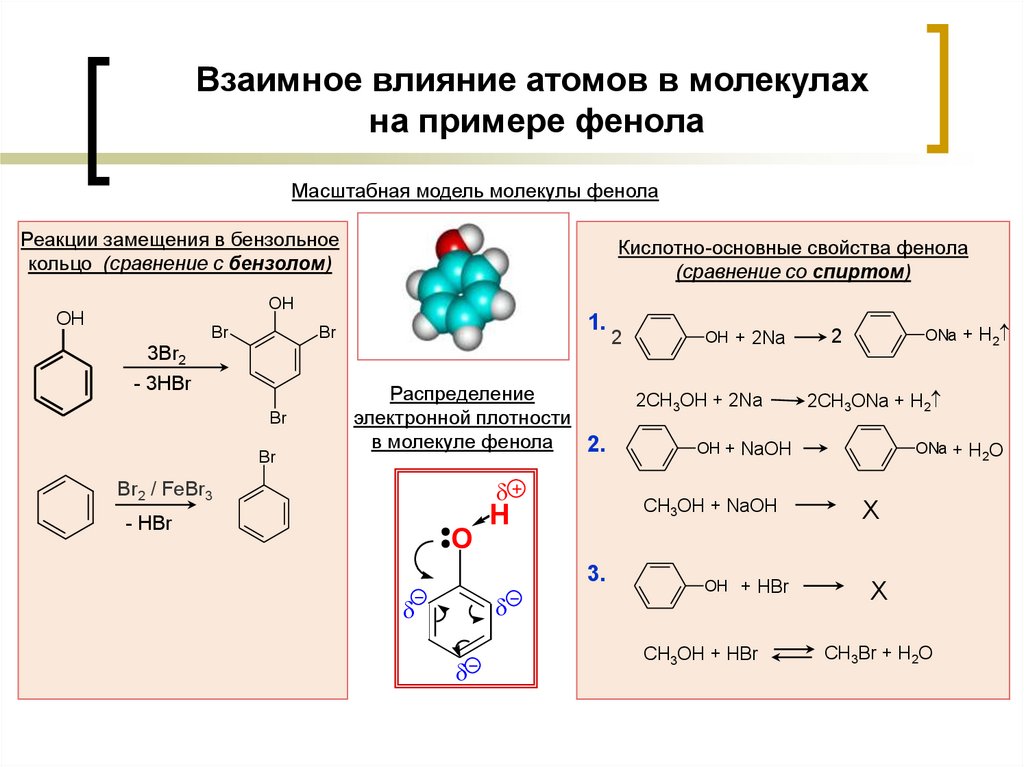
Взаимное влияние атомов в молекулахна примере фенола
Масштабная модель молекулы фенола
Реакции замещения в бензольное
кольцо (сравнение с бензолом)
Кислотно-основные свойства фенола
(сравнение со спиртом)
OH
OH
Br
1.
Br
3Br2
- 3HBr
Br
Br
Распределение
электронной плотности
в молекуле фенола
2.
Br2 / FeBr3
- HBr
O
OH + 2Na
2CH3OH + 2Na
ONa + H2
2
2CH3ONa + H2
OH + NaOH
CH3OH + NaOH
H
3.
2
OH + HBr
CH3OH + HBr
ONa + H2O
Х
Х
CH3Br + H2O






 Химия
Химия








