Похожие презентации:
Качественный анализ и его методы
1.
Качественный анализи его методы
Подготовила преподаватель
аналитической химии
Попова А.С.
2.
• Основная задача качественного анализа –определение химического состава
исследуемого соединения.
3.
• Качественный анализ проводятхимическими, физическими и физикохимическими методами.
• Физические и физико-химические методы
анализа основаны на измерении какоголибо параметра системы. Их еще называют
инструментальными.
• Например, это кулонометрия,
потенциометрия, радиохимический способ
и прочее.
4.
• Химические методы качественного анализаоснованы на превращении анализируемого
вещества в новые соединения,
обладающие определенными свойствами.
• По образованию характерных соединений
элементов и устанавливается
элементарный состав вещества.
5.
6.
• Качественные аналитические реакции поспособу их выполнения делятся на реакции
«мокрым» и «сухим» путем.
• Наибольшее значение имеют реакции
«мокрым» путем.
7.
• Для проведения их исследуемое веществодолжно быть предварительно растворено.
• В качественном анализе находят применение
только те реакции, которые сопровождаются
какими-либо хорошо заметными внешними
эффектами: изменением окраски раствора,
выпадением или растворением осадка,
выделением газов с характерным запахом или
цветом и т.п.
• Часто применяются реакции,
сопровождающиеся образованием осадков и
изменением окраски раствора. Такие реакции
называются реакциями «открытия», т.к. с их
помощью обнаруживаются присутствующие в
растворе ионы.
8.
• Анализ «сухим» путем проводится с твердымивеществами.
• Он делится на анализ методом растирания и
пиротехнический анализ.
• Последний основан на подогревании
исследуемого вещества в пламени горелки.
• Например, летучие соли многих металлов
окрашивают пламя в различные цвета,
характерные для этих металлов: Li и Sr –
карминово-красная окраска пламени, Na –
интенсивно-желтая, K – фиолетовая, Rb и Сs –
розово-фиолетовая, Ca – оранжево-красная, Ba
– зеленая, Cu и B – желто-зеленая, Pb и As –
бледно-голубая и т.д.
9.
10.
• В аналитической практике определяемыйион обычно приходится открывать в
присутствии других ионов. Реакции и
реагенты, дающие возможность открывать
данный ион в присутствии других,
называются специфичными.
• Групповыми называются реагенты, которые
обнаруживают ионы определенной
аналитической группы. Например, если к
раствору, содержащему ионы добавить
раствор HCl, то эти ионы выпадут в осадок.
11.
• В зависимости от реагентовсформировались различные методы
качественного анализа катионов:
сероводородный, аммиачно-фосфатный,
кислотно-основной, карбонатный,
сульфидно-основной, тиоцетамидный.
12.
• Наиболее распространенными являются трианалитические классификации катионов по
группам: сероводородная (сульфидная),
аммиачно-фосфатная (или фосфатноаммиачная) и кислотно-основная, причем
сероводородный метод анализа в последние
десятилетия применяются все реже, так как он
требует получения и применения токсичного
сероводорода. Каждая классификация
основана на химических свойствах катионов,
связана с положением соответствующих
элементов периодической системе и их
электронным строением.
13.
• Сероводородная (сульфидная)классификация
Группа
Катионы
Групповой реагент
I
Li , Na , K , NH4 , Mg
Нет
II
Ca, Sr, Ba
Раствор (NH4)2CO3 в
аммиачном
буфере (рН~9,2)
III
Al, Cr, Zn, Mn, Fe, Fe, Co,
Ni
Раствор (NH4)S (рН=7-9)
IV
Cu, Cd, Hg, Bi, Sn (2+;
4+)Sb (3+; 5+) As (3+; 5+)
Раствор H2S при рН=0,5
(HCl)
V
Ag ,Hg,Pb
Раствор HCl
14.
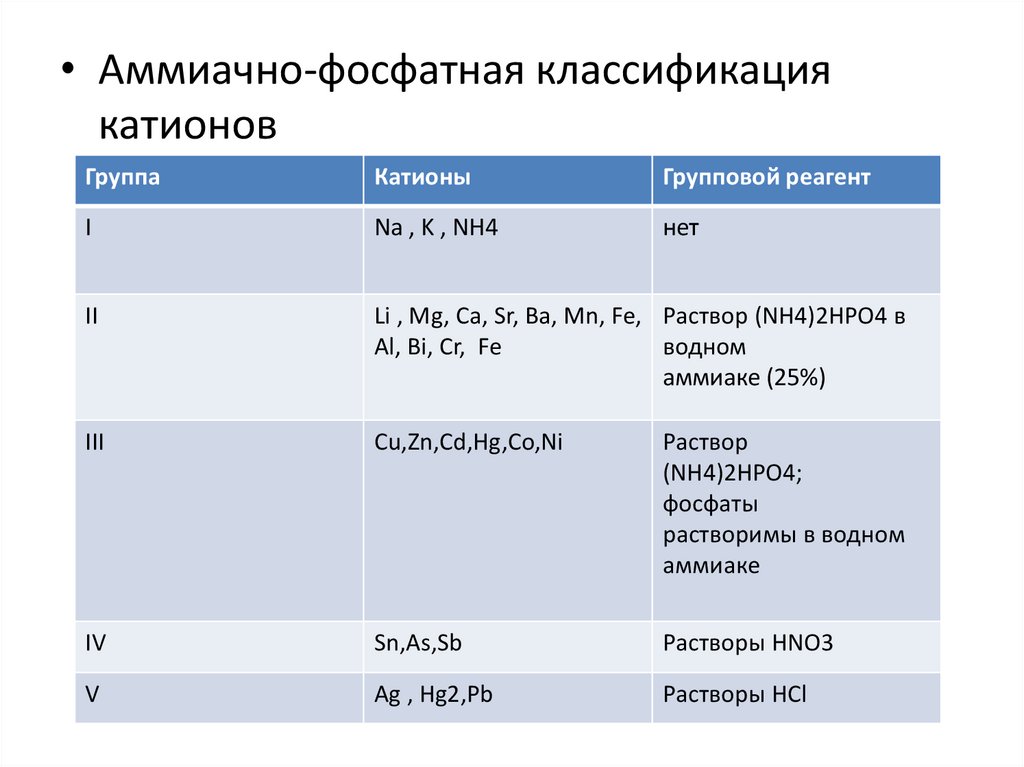
• Аммиачно-фосфатная классификациякатионов
Группа
Катионы
Групповой реагент
I
Na , K , NH4
нет
II
Li , Mg, Ca, Sr, Ba, Mn, Fe, Раствор (NH4)2HPO4 в
Al, Bi, Cr, Fe
водном
аммиаке (25%)
III
Cu,Zn,Cd,Hg,Co,Ni
Раствор
(NH4)2HPO4;
фосфаты
растворимы в водном
аммиаке
IV
Sn,As,Sb
Растворы HNO3
V
Ag , Hg2,Pb
Растворы HCl
15.
• Кислотно-основная классификациякатионов
Группа
Катионы
Групповой реагент
I
Li , Na , K , NH4
Нет
II
Ag , Hg2,Pb
Растворы HCl
III
Ca,Sr,Ba
Растворы H2SO4
IV
Zn,Al,Sn,As,Cr
Растворы NaOH
В присутствии Н2O2
V
Mg,Sb,Bi,Mn, Fe
Раствор NaOH или
Раствор аммиака (25%)
VI
Cu,Cd,Hg,Co, Ni
Раствор аммиака (25%)
16.
• Аналитическая классификация анионов погруппам разработана не столь подробно. Не
существует общепризнанной и повсеместно
принятой классификации. Чаще всего
принимают во внимание их окислительновосстановительные свойства в водных
растворах.
17.
• Классификация анионов, основания на О-Всвойствах
• индифферентные анионы не обладают
выраженными О-В свойствами в обычных
условиях.
Группа
Анионы
Групповой реагент
I
Окислители
BrO3 , AsO4, NO3 , NO2
Раствор KI в сернокислой
среде
II
Восстановители
S , SO3,S2O3,AsO3
Раствор I2 в KI
S , SO3, S2O3, AsO3, NO2,
C2O4, Cl , Br, I , CN , SCN
Раствор KМnO4 в
сернокислой
среде
III
Индифферентные
SO4, CO3, PO4, CH3COO ,
B4O7 (BO2 )
Отсутствует
18.
• Любая аналитическая классификациякатионов или анионов ограничена.
• Не существует такой аналитической
классификации, которая включала бы все
катионы или все анионы


















 Химия
Химия








