Похожие презентации:
Углеводы. Моносахариды. Лекция 5
1. Лекция 5.
Углеводы.Моносахариды.
2.
• Углеводы - большая группа природных биологическиактивных соединений – полигидроксикарбонильные
соединения, их некоторые производные и полимеры.
• Углеводы – твердые вещества разнообразного
строения и свойств, различной растворимости в
воде, практически нерастворимые в органических
растворителях.
• По
строению
и
составу
углеводы
можно
классифицировать на:
• Моносахариды (низкомолекулярные вещества, не
гидролизуются)
• Дисахариды (гидролизуются с образованием 2
молекул моносахаридов)
• Олиго- и полисахариды (высокомолекулярные
вещества, гидролизуются : олигосахариды дают 3 10 молекул моносахаридов, полисахариды – более
10 молекул).
3. Моносахариды.
• Моносахариды (Сn(H2O)n) содержат 1 карбонильнуюгруппу и несколько спиртовых ОН.
• Моносахариды – твердые вещества, хорошо
растворимые в воде, очень плохо растворимые в
органических растворителях, многие имеют сладкий
вкус.
• Моносахариды
можно
классифицировать
по
признакам:
• 1. По природе карбонильной группы:
• - альдозы (содержат альдегидную группу –СН=О)
• - кетозы (содержат кетонную группу >С=О)
• 2. По количеству атомов С в молекуле:
• триозы (С3) тетрозы (С4)
• пентозы (С5) гексозы (С6) гептозы (С7) прочие
4. Особенности строения моносахаридов.
• Почти все моносахариды – хиральные (оптически активные)соединения.
• Количество хиральных центров (N): N = nC - 2 (у альдоз), N = nC 3 (у кетоз).
• Количество оптических изомеров Ni = 2N
• Большинство моносахаридов организма человека относятся к Dстереохимическому ряду.
• Принадлежность к D-ряду определяется относительной
конфигурацией хирального центра с максимальным атомным
номером (С-5 у D-глюкозы).
CH=O
H
OH
CH2OH
Конфигурационный стандарт D-глицериновый альдегид.
• L-моносахариды – ксенобиотики.
• Для пентоз и гексоз характерна цикло-оксо-таутомерия
(кольчато-цепная).
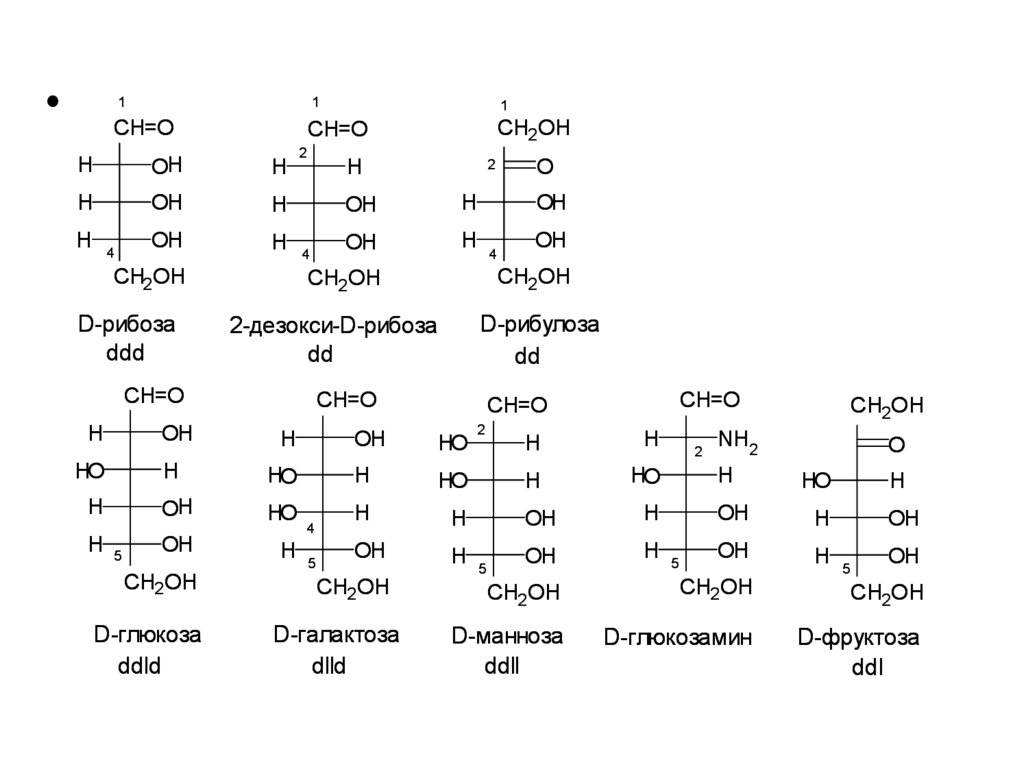
5. Важнейшие представители моносахаридов.
• Триозы: D-глицериновый альдегид (альдоза),диоксиацетон (кетоза)
• Альдопентозы: D-рибоза, 2-дезокси-Dрибоза, D-ксилоза
• Кетопентозы: D-рибулоза, D-ксилулоза
• Альдогексозы: D-глюкоза, D-галактоза, Dманноза, аминосахара: D-глюкозамин, Dгалактозамин, D-маннозамин,
• Кетогексозы: D-фруктоза
• Прочие: N-ацетилнейраминовая (сиаловая)
кислота, аскорбиновая кислота (витамин С)
6.
1
1
CH=O
OH
H
H
OH
H
OH
H
4
CH2OH
D-рибоза
ddd
2
H
4
OH
HO
H
H
5
H
OH
HO
D-глюкоза
ddld
H
OH
H
H
4
5
4
D-рибулоза
dd
CH=O
CH=O
HO
H
HO
H
H
OH
H
D-галактоза
dlld
OH
CH2OH
OH
CH2OH
O
OH
CH=O
HO
CH2OH
OH
2-дезокси-D-рибоза
dd
H
OH
2
CH2OH
CH=O
H
CH2OH
CH=O
H
H
1
2
5
H
H
H
HO
OH
H
OH
H
2
NH2
H
5
CH2OH
O
HO
H
OH
H
OH
OH
H
5
OH
CH2OH
CH2OH
CH2OH
D-манноза
ddll
D-глюкозамин
D-фруктоза
ddl
7. Стереохимические термины.
Стереохимические термины.
Пара энантиомеров – пара оптических изомеров,
относящихся друг к другу как предмет к своему
зеркальному отображению (D-глюкоза и L-глюкоза).
Диастереомеры
–
оптические
изомеры
(с
несколькими хиральными центрами), не являющиеся
энантиомерами (D-галактоза и D-манноза).
Эпимеры
–
диастереомеры,
различающиеся
конфигурацией только 1 хирального центра (из
нескольких) (D-глюкоза и D-галактоза).
Пара аномеров – пара диастереомеров (эпимеров)
циклических форм моносахаридов, различающиеся
конфигурацией только аномерного атома С (α-Dглюкопираноза и β-D-глюкопираноза).
Таутомеры – динамические структурные изомеры,
находящиеся в равновесии и взаимно переходящие
друг в друга путем переноса атома Н и
перераспределения
электронной
плотности
и
химических связей внутри молекулы. В большинстве
случаев неразделимы.
8. Химические свойства моносахаридов.
• Изомеризация – эпимеризация (в щелочнойсреде)
• Цикло-оксотаутомерия и мутаротация
• Образование гликозидов и полигликозидов
(полисахаридов)
• Образование простых и сложных эфиров
• Реакции окисления
• Реакции восстановления
• Образование фосфорных эфиров in vivo и их
превращения
• Прочие реакции
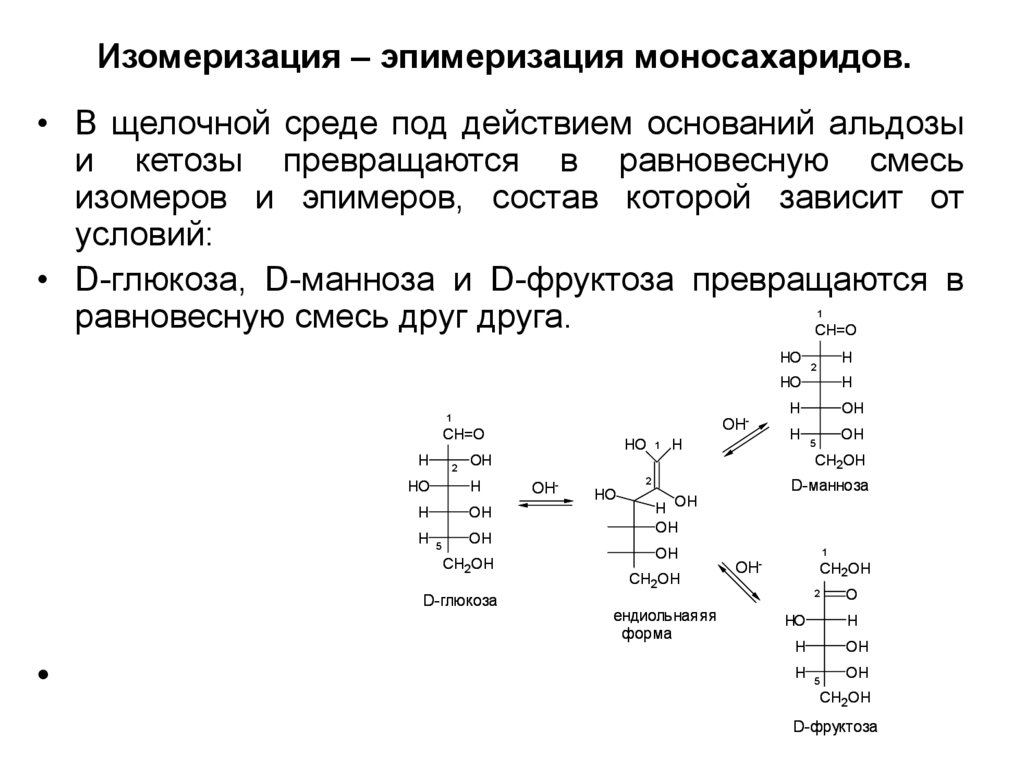
9. Изомеризация – эпимеризация моносахаридов.
• В щелочной среде под действием оснований альдозыи кетозы превращаются в равновесную смесь
изомеров и эпимеров, состав которой зависит от
условий:
• D-глюкоза, D-манноза и D-фруктоза превращаются в
равновесную смесь друг друга.
CH=O
1
HO
H
2
HO
H
1
OH-
CH=O
H
2
HO
H
OH
5
OH
CH2OH
D-глюкоза
HO
1
H
H
OH
H
H
H
OH
OH
5
CH2OH
OH-
2
HO
D-манноза
H OH
OH
OH
CH2OH
ендиольнаяяя
форма
1
OH-
CH2OH
2
HO
H
H
H
O
OH
5
OH
CH2OH
D-фруктоза
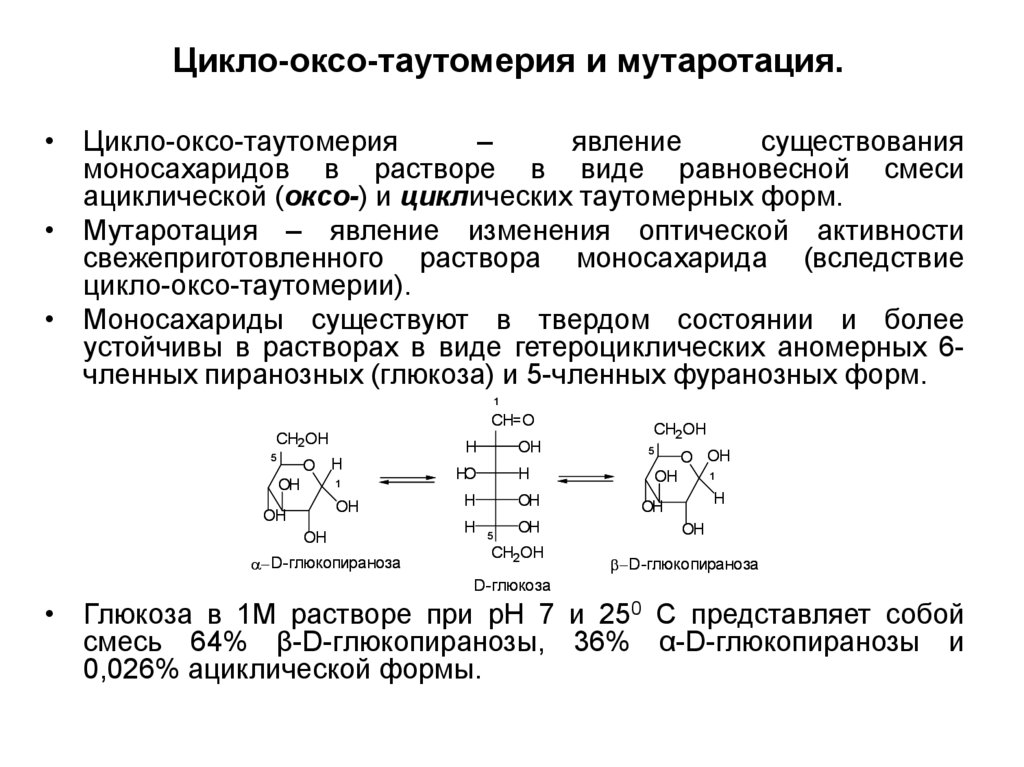
10. Цикло-оксо-таутомерия и мутаротация.
• Цикло-оксо-таутомерия–
явление
существования
моносахаридов в растворе в виде равновесной смеси
ациклической (оксо-) и циклических таутомерных форм.
• Мутаротация – явление изменения оптической активности
свежеприготовленного раствора моносахарида (вследствие
цикло-оксо-таутомерии).
• Моносахариды существуют в твердом состоянии и более
устойчивы в растворах в виде гетероциклических аномерных 6членных пиранозных (глюкоза) и 5-членных фуранозных форм.
1
CH=O
CH2OH
5
O
OH
H
H
1
OH
OH
OH
D-глюкопираноза
OH
HO
H
H
H
OH
5
OH
CH2OH
CH2OH
5
O OH
OH
1
H
OH
OH
D-глюкопираноза
D-глюкоза
• Глюкоза в 1М растворе при pH 7 и 250 С представляет собой
смесь 64% β-D-глюкопиранозы, 36% α-D-глюкопиранозы и
0,026% ациклической формы.
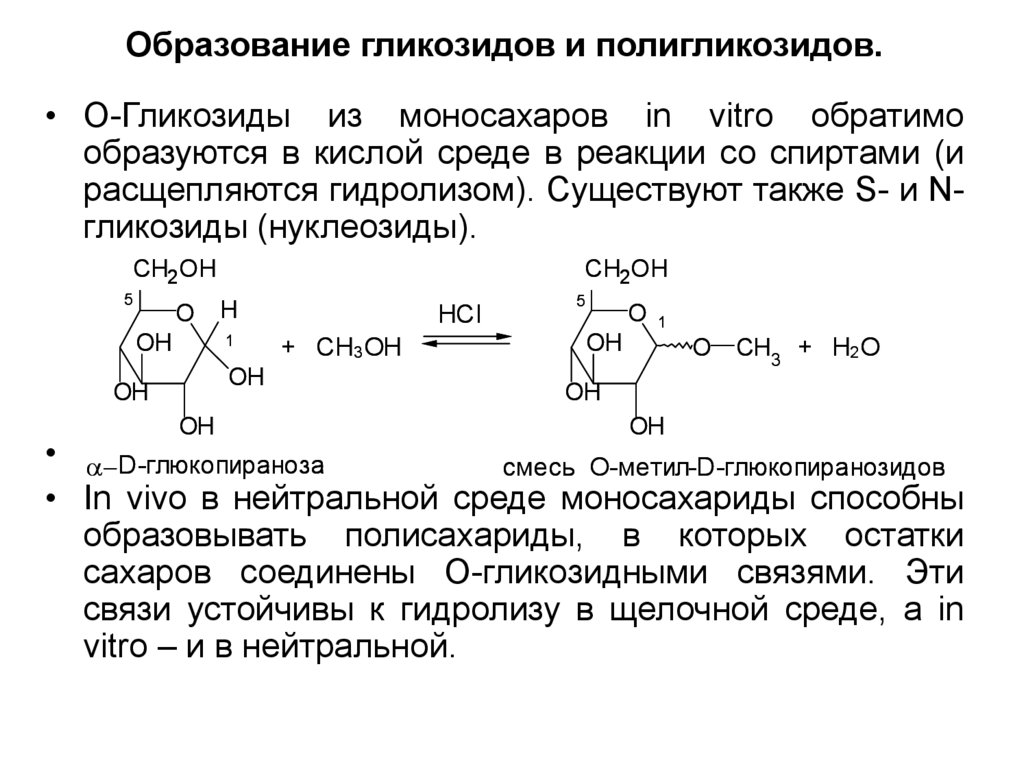
11. Образование гликозидов и полигликозидов.
• О-Гликозиды из моносахаров in vitro обратимообразуются в кислой среде в реакции со спиртами (и
расщепляются гидролизом). Существуют также S- и Nгликозиды (нуклеозиды).
CH2OH
5
O
OH
CH2OH
H
1
OH
OH
OH
HCl
+ CH3OH
5
O
1
OH
O
CH3 + H2O
OH
OH
• D-глюкопираноза
смесь О-метил-D-глюкопиранозидов
• In vivo в нейтральной среде моносахариды способны
образовывать полисахариды, в которых остатки
сахаров соединены О-гликозидными связями. Эти
связи устойчивы к гидролизу в щелочной среде, а in
vitro – и в нейтральной.
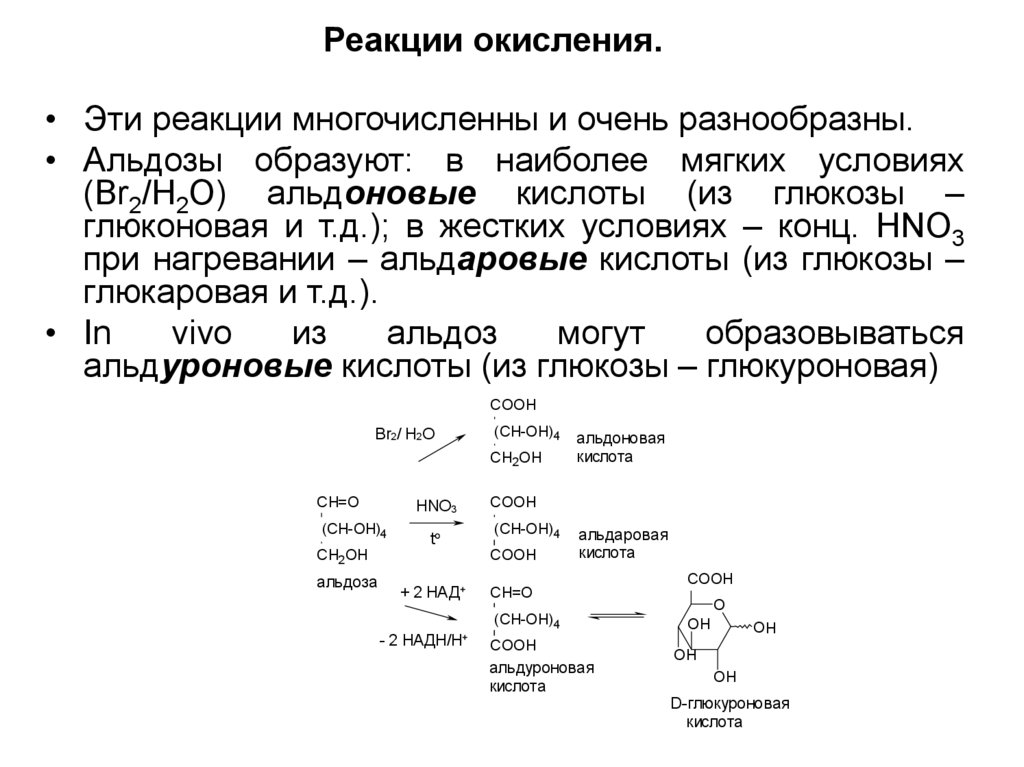
12. Реакции окисления.
• Эти реакции многочисленны и очень разнообразны.• Альдозы образуют: в наиболее мягких условиях
(Br2/H2O) альдоновые кислоты (из глюкозы –
глюконовая и т.д.); в жестких условиях – конц. HNO3
при нагревании – альдаровые кислоты (из глюкозы –
глюкаровая и т.д.).
• In
vivo
из
альдоз
могут
образовываться
альдуроновые кислоты (из глюкозы – глюкуроновая)
COOH
Br2/ H2O
(CH-OH)4
CH2OH
CH=O
HNO3
(CH-OH)4
to
CH2OH
альдоза
COOH
(CH-OH)4
COOH
+ 2 HAД+
альдоновая
кислота
альдаровая
кислота
COOH
CH=O
(CH-OH)4
- 2 HAДH/H+
COOH
альдуроновая
кислота
O
OH
OH
OH
OH
D-глюкуроновая
кислота
13. Реакции восстановления.
• Эти реакции многочисленны и разнообразны:карбонильная группа восстанавливается до спиртовой
с образованием многоатомных спиртов.
• Альдогексозы дают по 1 шестиатомномуспирту
(глюкоза – глюцит (сорбит(ол)), манноза – маннит(ол),
галактоза – дульцит (галактит(ол)), кетогексозы –
эквимолярную смесь 2 эпимерных по С-2 спиртов
(фруктоза – глюцит + маннит).
CH=O
H
OH
HO
H
H
H
5
CH2OH
H2
H
HO
OH
H
OH
H
CH2OH
D-глюкоза
2
OH
H
5
CH2OH
O
H2
HO
OH
H
OH
H
CH2OH
глюцит
H
5
H2
HO
HO
OH
H
OH
H
CH2OH
D-фруктоза
CH=O
CH2OH
2
H
H
5
H2
HO
H
HO
H
OH
H
OH
H
CH2OH
маннит
OH
5
OH
CH2OH
D-манноза
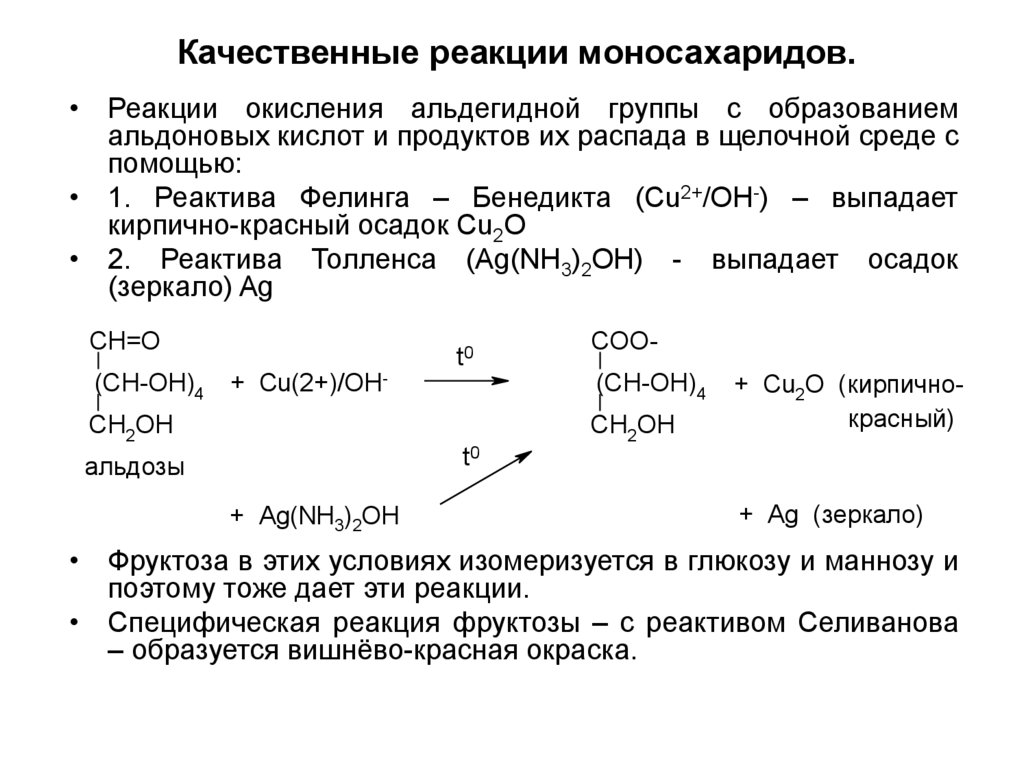
14. Качественные реакции моносахаридов.
• Реакции окисления альдегидной группы с образованиемальдоновых кислот и продуктов их распада в щелочной среде с
помощью:
• 1. Реактива Фелинга – Бенедикта (Cu2+/OH-) – выпадает
кирпично-красный осадок Cu2O
• 2. Реактива Толленса (Ag(NH3)2OH) - выпадает осадок
(зеркало) Ag
CH=O
(CH-OH)4
t0
+ Cu(2+)/OH-
COO(CH-OH)4
CH2OH
CH2OH
+ Cu2O (кирпичнокрасный)
t0
альдозы
+ Ag(NH3)2OH
+ Ag (зеркало)
• Фруктоза в этих условиях изомеризуется в глюкозу и маннозу и
поэтому тоже дает эти реакции.
• Специфическая реакция фруктозы – с реактивом Селиванова
– образуется вишнёво-красная окраска.
15. Фосфорные эфиры моносахаридов in vivo.
• In vivo моносахариды фосфорилируются с помощьюАТФ. Метаболитами являются: глюкоза-6-фосфат,
глюкоза-1-фосфат, фруктоза-6-фосфат, фруктоза1,6-дифосфат, рибоза-5-фосфат и др.
CH=O
H
CH=O
HO
OH + АТФ
H
HO
H
OH - АДФ
H
OH
H
H
H
CH2OH
D-глюкоза
H
O
HO
OH
H
OH
H
CH2OPO3H2
глюкоза-6-фосфат
H
H
фруктоза-6-фосфат
CH=O
O
HO
- АДФ
OH
- АДФ
H
+ АТФ
CH2OPO3H2
- АДФ
OPO3H2
CH2OH
H
OH
+ АТФ
O
OH
OH
+ АТФ
CH2OH
OH
CH2OH
H
OH
OH
CH2OH
D-фруктоза
CH2OPO3H2
H
OH
H
OH
HO
H
OH
H
O
H
фруктоза-1,6-дифосфат
OH
• Глюкоза-6-фосфат – главный внутриклеточный
метаболит глюкозы, используемый во множестве
метаболических путей.
OH
глюкоза-1-фосфат
CH2OPO3H2
рибоза-5-фосфат
H
OH
CH2OPO3H2
16. Биороль моносахаридов.
• Моносахариды (глюкоза, фруктоза, галактоза) –важнейший источник энергии для организма (около
500 г/сут). Широко распространены в природе в
форме разнообразных полисахаридов.
• Используются почти во всех биосинтетических
процессах
организма
(гликоген,
структурные
полисахариды, жиры, ХС и стероиды и др.).
• Рибоза
и
2-дезоксирибоза
необходимы
для
биосинтеза нуклеотидов и нуклеиновых кислот.
• Глюкуроновая
кислота
необходима
для
обезвреживания и выведения ксенобиотиков из
организма.
• Сиаловые кислоты входят в состав поверхностных
антигенов клетки, необходимых для правильной
работы иммунной системы.
• Применяются в лечебных целях (глюкоза, глюконат
кальция, витамин С) и входят в состав лекарств.
17. Особая роль D-глюкозы.
• Универсальное питательное вещество для любыхклеток.
• Используется клетками как в энергетических, так и в
пластических целях.
• Единственный источник энергии для клеток человека
в анаэробных условиях, абсолютно необходима для
эритроцитов, чрезвычайно важна для нейронов.
• Используется клетками для биосинтеза практически
всех метаболитов и запасающих веществ, содержится
в
крови
(3,3-5,5
ммоль/л),
при
недостатке
биосинтезируется из лактата, глицерина, аминокислот
(белков организма).
• Широко распространена в природе, в основном в виде
биополимеров – полисахаридов.
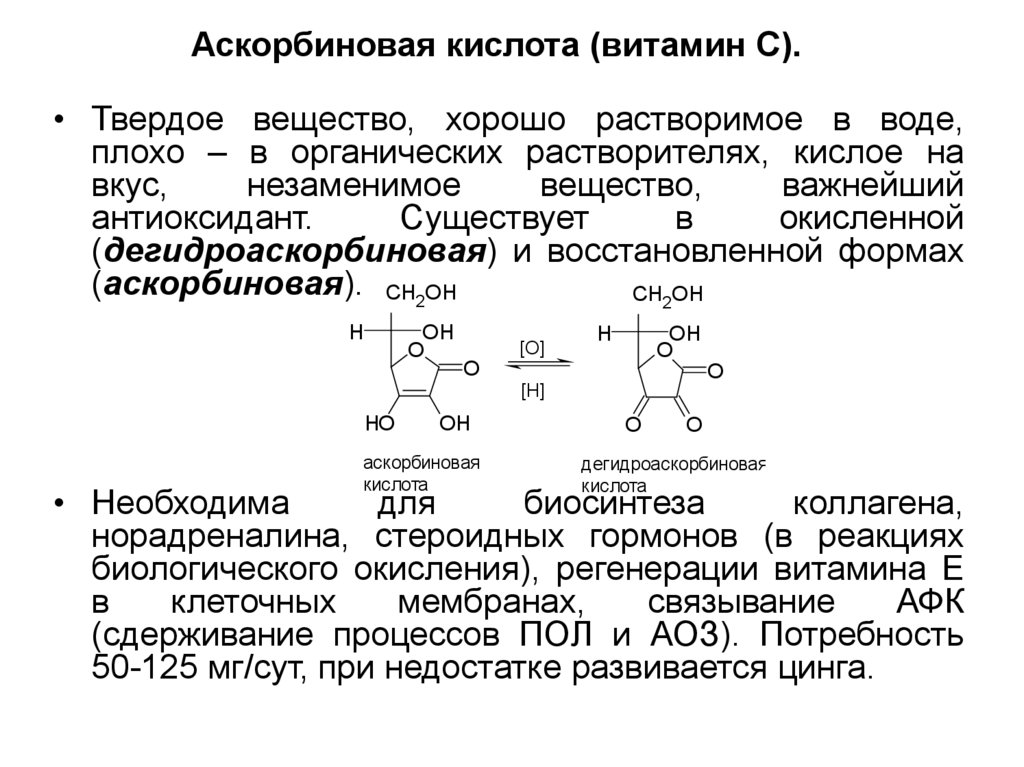
18. Аскорбиновая кислота (витамин С).
• Твердое вещество, хорошо растворимое в воде,плохо – в органических растворителях, кислое на
вкус,
незаменимое
вещество,
важнейший
антиоксидант.
Существует
в
окисленной
(дегидроаскорбиновая) и восстановленной формах
(аскорбиновая). CH2OH
CH2OH
H
OH
O
[O]
H
OH
O
O
O
[H]
HO
OH
аскорбиновая
кислота
O
O
дегидроаскорбиновая
кислота
• Необходима
для
биосинтеза
коллагена,
норадреналина, стероидных гормонов (в реакциях
биологического окисления), регенерации витамина Е
в
клеточных
мембранах,
связывание
АФК
(сдерживание процессов ПОЛ и АОЗ). Потребность
50-125 мг/сут, при недостатке развивается цинга.











 Химия
Химия