Похожие презентации:
Familia retroviridae. Virusul HIV. Oncogeneza virala
1.
FAMILIA RETROVIRIDAE.VIRUSUL HIV. ONCOGENEZA
VIRALA
2.
FAMILIA RETROVIRIDAE.VIRUSUL HIV ŞI INFECŢIA HIV/SIDA
Prima descriere clinică a SIDA – 1981
1983–HIV a fost identificat (Françoise Barré-Sinoussi +Luc Montagnier,
Institutul Pasteur, Paris)
1984 – HIV a fost confirmat de echipa condusă de Robert Gallo (CDC,
National Cancer Institute, SUA)
1986 - propusă denumirea HIV (Human Immunodeficiency Virus)
1986 – a fost izolat HIV-2, Africa de Vest
2008 – Premiul Nobel în Medicină (Françoise Barré-Sinoussi și Luc
Montagnier)
3.
Epidemia la nivel mondial-
-
-
Finele anului 2020
37.7 mln persoane trăiau cu HIV
79.3 mln au fost infectate cu HIV de la inceputul epidemiei
36.3 mln au decedat de cauze legate de SIDA de la
inceputul epidemiei
73% adulți, 53% copii și 85% gravide aveau acces la
terapia antiretrovirală (TARV)
Pe parcursul anului 2020
1.5 mln persoane au fost inregistrate cu infectia HIV
680 000 au decedat de cauze legate de SIDA
Zilnic se infectează 5-6 mii persoane
4.
5.
Decline in HIV incidence and mortality over timeSource: UNAIDS/WHO estimates
6.
People living with HIV by WHO region, 2020Africa
25.4million
America
3.7 million
37.7
million
people living
South-East Asia
3.7 million
with HIV globally
Europe
2.6 million
Eastern Mediterranean
420 000
Western Pacific
Source: UNAIDS/WHO estimates
1.9 million
7.
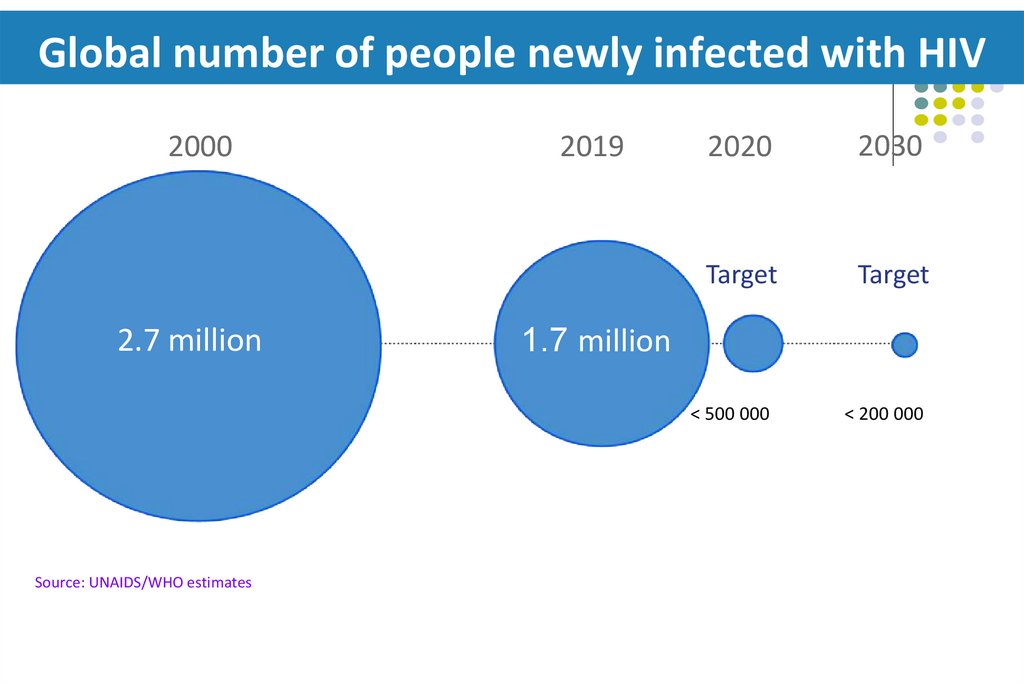
Global number of people newly infected with HIV2000
2.7 million
2019
2020
2030
Target
Target
1.7 million
< 500 000
Source: UNAIDS/WHO estimates
< 200 000
8.
Global number of HIV-related deaths2000
1.4 million
2019
2020
2030
Target
Target
690 000
< 500 000
Source: UNAIDS/WHO estimates
< 400 000
9.
Global number of people receivingantiretroviral treatment
2000
2005
0.6 million
2.0 million
2010
7.8 million
2019
25.4 million
40%
Source: UNAIDS/WHO estimates
2020
2030
27.5 million
33 million
10.
Global ART coverage over timeSource: UNAIDS/WHO estimates
11.
12.
Epidemia infecției cu HIV în RM(La 1 ianuarie 2020)
Numărul estimativ al persoanelor HIV infectate - 14589;
Numărul cumulativ al persoanelor diagnosticate cu HIV 13706;
Numărul persoanelor HIV infectate, în viață – 8500;
Numărul persoanelor ce sunt în evidența medicală –
7500;
Numărul persoanelor HIV infectate care primesc TARV –
5 200;
Numărul de cazuri noi de infectie cu HIV, diagnosticate în
perioada 1ianuarie-31 octombrie 2020 – 568.
Anual 300 persoane decedeaza de SIDA
13.
Numărul de cazuri HIV+ înregistrate în RepublicaMoldova, 2007 - 2016
900
800
779
833
817
832
450
462
471
355
361
2015
2016
769
740
700
720
702
714
700
600
500
429
400
430
400
354
389
379
382
349
311
383
332
300
380
348
300
341
200
100
0
2007
2008
2009
2010
2011
Males
2012
Females
2013
Total
2014
14.
Incidenta infectiei cu HIV in RM (2001 – 2015)15.
Rata transmiterii verticale ainfecției HIV în RM
16.
Prin Hotărârea Guvernului Nr. 1164 din22.10.2016 a fost aprobat Programul naţional
de prevenire şi control al infecţiei HIV/SIDA şi
infecţiilor cu transmitere sexuală pentru anii
2016-2020 care se aliniază la strategia
mondială 90-90-90 (identificarea şi
diagnosticarea a 90% din numărul estimat de
persoane infectate cu HIV (2019 - 54%),
înrolarea în tratament antiretroviral a 90%
(34%) din cei diagnosticaţi şi suprimarea
încărcăturii virale la 90% (26%) din cei care
urmează tratamentul).
17.
CLASIFICAREA FAM. RETROVIRIDAERetroviridae – familie numeroasă de virusuri ARN
dotate cu o enzimă numită transcriptază inversă
(reverstranscriptază, ADN polimerază ARNdependentă).
ARN
ADNd.c
Subfamilia Orthoretrovirinae
Genurile: Alpharetrovirus, Betaretrovirus,
Gammaretrovirus, Deltaretrovirus, Epsilonretrovirus
(induc tumori şi leucemii), Lentivirus (virusul HIV, SIV)
Subfamilia Spumaretrovirinae
Genul: Spumavirus (nepatogeni)
18.
CARACTERE MORFOSTRUCTURALE GENERALE ALEFAMILIEI RETROVIRIDAE
Dimensiuni – 80-130 nm
Formă – sferică
Genom – două molecule de ARN+,
capacitate de integrare în nucleu
sub formă de ADN proviral
Enzime – reverstranscriptaza,
integraza, proteaza
2 molecule ARNt de origine
celulară (câte una pentru fiecare
copie a genomului, utilizate în
calitate de primer pentru RT)
Capsidă – icosaedrică
Supercapsidă – derivată din MCP,
lipidică cu GP virale înserate
Ciclul replicativ este identic
19.
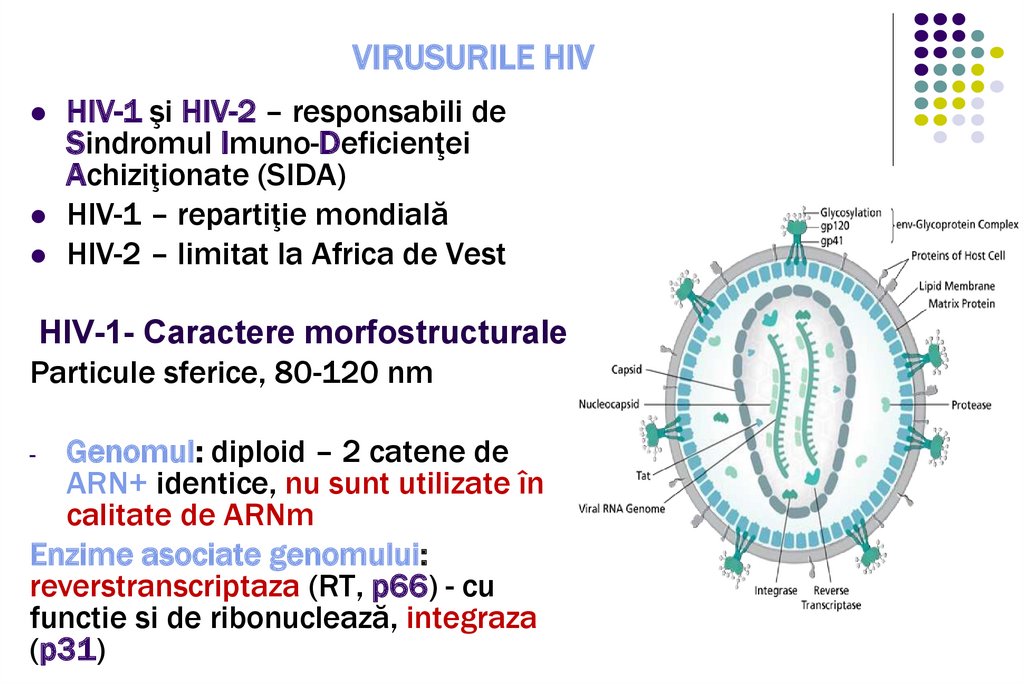
VIRUSURILE HIVHIV-1 şi HIV-2 – responsabili de
Sindromul Imuno-Deficienţei
Achiziţionate (SIDA)
HIV-1 – repartiţie mondială
HIV-2 – limitat la Africa de Vest
HIV-1- Caractere morfostructurale
Particule sferice, 80-120 nm
Genomul: diploid – 2 catene de
ARN+ identice, nu sunt utilizate în
calitate de ARNm
Enzime asociate genomului:
reverstranscriptaza (RT, p66) - cu
functie si de ribonuclează, integraza
(p31)
-
20.
HIV-1- Caractere morfostructuraleCapsida: în formă de trunchi
de con, constituită din 2
proteine:
p24 (CA, a capsidei,
majoră)
p7 (NP, a nucleocapsidei,
asociată ARN)
21.
Supercapsida: dublu strat fosfolipidic de originecelulară în care sunt înserate 2 GP virale
1.
Gp120, de suprafaţă, asigură fixarea virusului de
receptorul celular CD4 şi de coreceptori. Regiunea V3
(variabilă) induce sinteza anticorpilor neutralizanţi
specifici
2.
Gp41, transmembranară, legată de gp120,
responsabilă de fuziunea supercapsidei cu membrana
celulară
Proteina matrice p17 (MA), căptuşeşte stratul intern al
supercapsidei, este asociată cu proteaza (p9)
Genomul, proteinele interne (p24, p7, p17) şi enzimele
constituie nucleoidul (core) viral
-
22.
23.
24.
--
-
-
Structura genomului (apr. 10 mii nucleotide)
Gena gag (group antigens), codifică o
poliproteina-precursor, clivata ulterior de catre
proteaza virala in proteinele structurale interne
(p24, p7 şi p17)
Gena pol (polimerase), codifică 3 enzime: RT
(p66), integraza (p31), proteaza (p9)
Gena env (enveloppe), codifică o proteină
precursor gp160, clivată ulterior în gp41 şi
gp120 de catre o proteaza a celulei-gazda
Gene regulatoare tat, rev, nef, vif, vpr şi vpu
25.
26.
27.
Variabilitatea geneticăSe disting 3 grupe
genomice ale HIV-1:
M (main, major), O
(outlier) şi N (new). Grupul
M comportă 11 subtipuri
(A - K), repartizate
geografic neuniform
(majoritatea – în Africa, B
– Europa occidentală şi
America de Nord, F, B –
România, G – Rusia, etc)
28.
29.
Omologia dintre HIV-1 şi HIV-2 estede 42%, mai înaltă la nivelul
genelor gag şi pol (peste 50%) şi
redusă la nivelul genelor env
(39%)
30.
Rezistența HIV la agențifizici și chimici
HIV este un virus slab rezistent în mediul extern
HIV este sensibil la solvenţi lipidici şi detergenţi
La 56 grade C este inactivat în 30 min
Sub acțiunea a 0,2 % hipoclorit de Na, 70% etanol,
0,2% glutaraldehidă- este neutralizat în în 5 minute
Nu rezistă la pH-uri extreme, radiaţii UV şi RX
O picătură de sânge infectat își reduce contagiozitatea
cu 80% în 15 minute, după 30 minute practic își pierde
capacitatea de infectare.
31.
Cultivarea HIV-
Celule mononucleate de
la persoane sănătoase
Linii celulare din LT –
MT2
Animale sensibile –
maimuţele cimpanzei
(HIV-1), Rhesus (HIV-2)
32.
CELULELE-ŢINTĂ ŞI REZERVORUL CELULAR1.
Limfocite TCD4+ (Th) (99% de replicare, ECP sinciţii)
2. CPA: monocite/macrofage tisulare, celulele
microgliei (replicare redusă, ECP minim).
Celulele dendritice (prezente în timus,
tegument, mucoase, organe limfoide, SNC şi
sânge perif.) au rol de vector şi rezervor de
virus (adsorb HIV la suprafaţa lor şi-l
transportă în organele limfoide, unde el este
prezentat celulelor CD4+ în care se replică).
33.
34.
Se disting:- tulpini ale HIV cu tropism macrofagic (M, sau
R5), utilizează coreceptorul CCR5, se
multiplica in macrofage si in limf T CD4;
- tulpini cu tropism limfocitar (T, sau X4),
utilizează coreceptorul CXCR4
În primo-infecţie predomina tulpini R5, în stadiu
de SIDA – tulpini X4
În cursul multiplicării mutații la nivelul genei env
afectează structura gp120 și duc la modificarea
tropismului virusului – din M/R5 în T/X4
- tulpini cu tropism mixt R5X4.
35.
36.
37.
CICLUL DE REPLICAREhttps://www.youtube.com/watch?v=GyofqO1TRjU
Ataşarea HIV la celula-gazdă prin legarea
gp120 de receptorul celular CD4. Rezultă o
modificare conformaţională a gp120, ce
permite buclei V3 a acestei gp să se fixeze
de coreceptorii de pe suprafaţa celulei:
CCR5 şi CXCR4, CCR3, CCR2b ş.a.
Penetrarea prin fuziunea supercapsidei
(gp41) cu MCP (sau prin endocitoza
clathrin-dependenta)
Decapsidarea şi eliberarea ARN viral
asociat cu enzimele virale
38.
39.
Retrotranscrierea
ARN+ în ADNIn continuare RT
(funcţie de RNA-aza H)
degradează ARN+,
Urmează transcrierea
ADN- în ADNd.c., care
va fi transportat in
nucleul celulei,
circularizat, apoi
integrat (integraza) în
cromozomul celular,
constituind provirusul.
40.
41.
Biosinteza:Transcrierea ADNv în ARNm şi ARN viral
prin intermediul ARN-polimerazei II
celulare
Sinteza proteinelor virale sub controlul
factorilor celulari şi proteinelor
reglatoare
- Poliproteina gag/pol 160 kd (p17 MA,
p24 CA, p7 NC, p9 (proteaza), p66 (RT),
p31 (integraza)
- Poliproteina env 160 kd (gp41 şi gp120)
42.
43.
Asamblarea si eliberarea virionilor:Poliproteina
env (gp160) este transportata din
RE in complexul Golgi, unde este clivata in
gp120 si gp41 de catre o proteaza celulara.
Ulterior aceste gp sunt inserate in MCP a celulei
gazda.
Poliproteina gag/pol, precum și 2 molecule de
ARN+ se leagă de membrana citoplasmatică ce
conține gp env.
Eliberarea virionilor imaturi prin înmugurire la
nivelul MCP modificată prin inserarea gp virale
gp120 şi gp41.
44.
45.
Maturizarea virionului se produce prin clivarea poliproteineigag/pol în proteine individuale şi enzime de către proteaza virală
46.
47.
48.
1-10 mlrd de virioni/zi/o persoană infectatăVariabilitatea HIV este determinată de erorile comise de
RT (o eroare la fiecare 2 mii baze). Mutaţiile survin în
special la nivelul genei env (bucla V3 din gp120, care
intervine în fixarea HIV de coreceptori, reprezintă
epitopul major de neutralizare).
Nu există 2 tulpini virale identice. La bolnav este
prezentă o populaţie virală polimorfă, cu genomuri
diferite
Consecinţe:
- dificultatea de a obţine vaccin eficient
- selecţia mutantelor rezistente la antiretrovirale
49.
Mecanismele de distrugere a limfocitelorT CD4:
- Liza directă a celulelor infectate (ECP)
- Limfocitele T CD8 (LTc) elimină limfocitele T
CD4 infectate
- Apoptoză în urma stimulării antigenice a
celulelor care au fost în contact cu Ag HIV
- Limfocitele infectate, acoperite cu gp120 pot
provoca fixarea, fuziunea şi moartea
limfocitelor neinfectate (formarea sincitiilor)
- Hiperstimulare celulară cu dezvoltarea anergiei
celulare
50.
51.
52.
53.
PATOGENEZA ŞI CLINICA INFECŢIEI CU HIV1.
2.
3.
Transmiterea:
Cale sexuală (hetero-, homo).
Cale sangvină (utilizatori de droguri injectabile,
hemofili, transfuzii de sânge sau transplante de
organe, manopere medicale penetrante injecţii, acupunctură, tatuaj, piercing)
Cale verticală (in utero în ultimele săptămâni de
sarcină, în timpul naşterii sau în timpul
alăptării)
54.
În ultimii ani, evoluţia epidemiei infecţiei HIV/SIDA înţara noastră se caracterizează prin următoarele
particularităţi:
extinderea ariei geografice de răspândire în zona
rurală;
reducerea cazurilor de infecţie în rândul
utilizatorilor de droguri intravenos şi creşterea
numărului persoanelor infectate pe cale
heterosexuală;
majorarea cazurilor în rândurile femeilor infectate
cu HIV, inclusiv a gravidelor;
afectarea persoanelor de vârstă tânără, fertilă;
sporirea numărului persoanelor cu forme severe
ale maladiei.
55.
EVOLUŢIA MALADIEIIncubaţia – de la câteva zile până la câteva săptămâni
(2 - 4) de la expunere la infectie
Primo-infecţia, infecţia acută (incepe peste 2-4
saptamani de la infectare). Durata 4-12
săptămâni. Are loc multiplicarea intensă şi
diseminarea virusului, scăderea numărului de
limfocite T CD4 şi creşterea numărului
limfocitelor TCD8. Diminuarea ulterioară a şarjei
virale şi creşterea nr LT CD4 este determinată de
răspunsul imun specific celular (limf TCD8) şi
umoral (Ac anti-gp120, anti-gp41, anti-p24, apar
la finele primoinfectiei). Persoana infectată
devine seropozitivă.
56.
Factorii care influenţează evoluţia primoinfecţiei: tipul virusului, raspunsul imun algazdei şi factori genetici (homozigoţii cu
mutaţie la nivelul genei receptorului CCR5
prezintă rezistenţă la infecţia cu HIV 1)
Evoluţia primoinfecției poate fi
asimptomatică sau simptomatică (50%):
adenopatie cervicală, febră, faringită, ulcere
ale mucoasei bucale, oboseală, mialgie,
artralgie, erupţii cutanate.
Durata fazei simptomatice – 7 – 10 zile
57.
58.
Faza asimptomatică, de latenţă clinică (duratavariabilă: 2 săptămâni – zeci de ani).
Virusul se replică în organele limfoide, numărul
LT CD4 diminuează lent. Apar variante noi de
virus care se multiplică, Sistemul Imun le
recunoaşte şi reacţionează specific, ciclul se
repetă de multiple ori. Aceasta duce
la diminuarea progresivă a LT CD4 şi LT CD8 şi
epuizarea Sistemului Imun, urmată de
multiplicarea necontrolată a HIV şi dispariţia
completă a LT CD4.
59.
Faza clinică (SIDA)Numărul LT CD4 - 500-200 celule/µl.
Se manifestă clinic prin febră cronică, pierdere în greutate,
diaree, afecţiuni ale tuturor organelor şi sistemelor, tumori
(sarcomul Kaposi, limfoame), infecţii oportuniste cu:
Paraziţi: Toxoplasma, Histoplasma, Leishmania
Bacterii: Mycobacterium, Salmonella, enterobacterii
condiţionat patogene, etc
Fungi: Pneumocystis carinii, Cryptococcus neoformans,
Cryptosporidium, Candida, etc
Virusuri: HSV, HZV, CMV
60.
61.
62.
63.
64.
65.
66.
67.
68.
Răspunsul imun:Celular – LT CD8 recunosc şi elimină celulele infectate (în
special LT CD4) prin citotoxicitate directă (LTc, restricţie
CMH I) sau prin intermediul citokinelor, chemokinelor.
Imunitatea celulara este crucială pentru controlul replicării
HIV şi are un impact substanţial în evoluţia infecţiei
Umoral – Ac apar precoce în infecţia primară, dar depistarea
lor poate fi efectuată după 3-6 săptămâni de la infectare.
Rolul – neutralizarea virionilor, Ac anti-gp120 împiedică
fixarea HIV pe celulele-ţintă. Eficienţă maximă în fazele
precoce ale infecţiei.
-
5-10% din infectaţi sunt “asimptomatici de lungă durată”:
Şarjă virală redusă
Numărul LT CD4 stabil (peste 500 celule/ µl)
Răspuns imun celular şi umoral constant
Absenţa semnelor clinice
69.
DIAGNOSTICUL DE LABORATORAL INFECŢIEI HIV/SIDA
Teste directe
1. Detectarea Ag p24 (marker direct al
infecţiei HIV) prin tehnici ELISA. Poate fi
detectat în primo-infecţie până la
seroconversie.
Ag p24 reapare în momentul evoluţiei spre
SIDA.
70.
2. Detectarea ARN-lui plasmatic sau ADNv printeste de amplificare genică (7-10 zile dupa
infectare).
Prezenţa ARNv în ser denotă replicarea constantă
a virusului. Determinarea şarjei virale este
utilizată pentru monitorizarea unui pacient
infectat.
3. Izolarea HIV în cultură
Se realizează prin inocularea cu plasmă sau celule
mononucleate de la bolnav a unei culturi de
celule mononucleate de la donatori sănătoşi.
Replicarea este detectată prin evidenţierea Ag
p24, RT sau a ARNv.
71.
Teste indirecte de depistare /screening- Teste ELISA de depistare a Ac
- (după minimum 22 zile de la contagiu)
- Teste rapide (RA cu particule de gelatină
sensibilizate cu Ag, teste imunocromatografice)
Teste combinate Ag - Ac (detectarea
- Ag p24 şi Ac anti-HIV prin tehnici ELISA)
Teste de confirmare (în caz de reacţie pozitivă)
Teste molecular-genetice (GeneXpert)
Western-blot (separarea el-foretică a proteinelor virale,
transferarea lor pe o bandă de nitroceluloză, tratarea cu
serul cercetat, apoi efectuarea RIE). Pot fi detectaţi Ac
contra tuturor Ag HIV.
72.
73.
74.
Diagnosticul de laborator alinfectiei cu HIV in RM
Screening-ul infectiei cu HIV
La toate nivelurile din sistemul medical;
În cadrul ONG-urilor din domeniul de prevenire HIV;
În maternități (după caz);
În cadrul procesului de autotestare.
Confirmarea infectiei cu HIV
Este efectuată obligator în sistemul medical;
În cadrul laboratoarelor din Centrele TARV;
Pe minim 2 probe de sânge și cu minim 3 testări.
75.
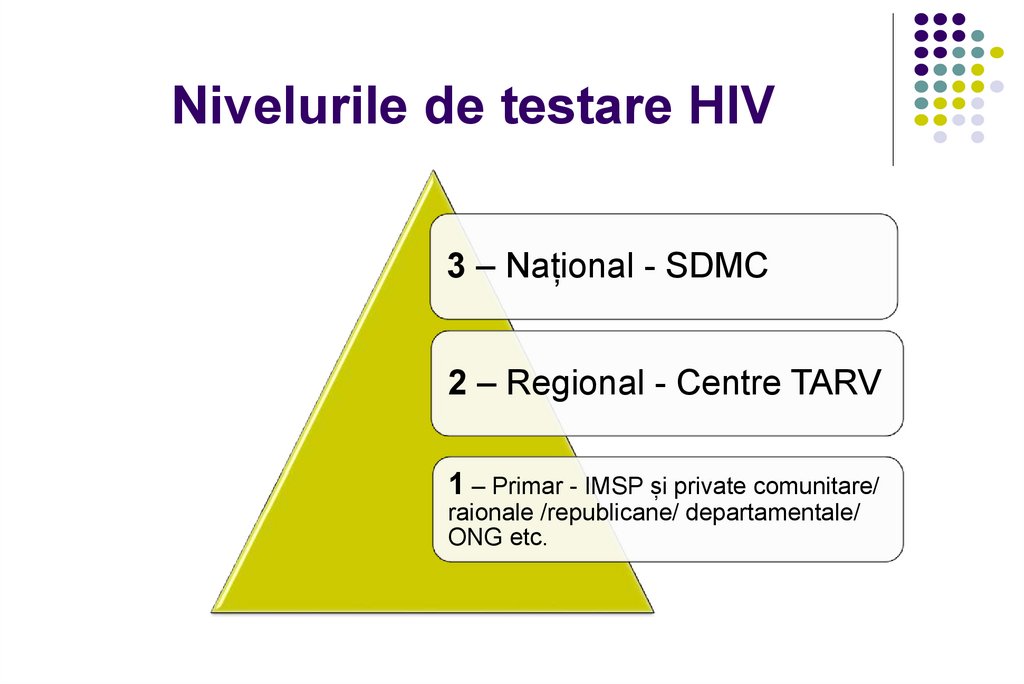
Nivelurile de testare HIV3 – Național - SDMC
2 – Regional - Centre TARV
1 – Primar - IMSP și private comunitare/
raionale /republicane/ departamentale/
ONG etc.
76.
Liniile de testare HIVA1
• TRD pe sânge (test rapid diagnostic)
• TRD pe fluid oral
A2
• TRD pe sânge
A3
• Confirmare cantitativa HIV 1 (VL)
• Confirmare calitativă HIV 1 (NAT)
• Confirmare HIV 2 (TRD)
77.
Nivelurile si liniile de testare HIVNivelul 1 - Primar
A1 – Teste rapide de diagnostic pe baza de sânge sau fluid oral
Nivelul 2 – Centre TARV
A1 - TRD
A2 - TRD
A3 – Confirmarea HIV1
Nivelul 3 – Național SDMC
A1 - TRD
A2 - TRD
A3 – Confirmarea HIV 1
și HIV 2
78.
Screening HIVPentru screening-ul
infecției HIV ½ se vor
utiliza teste rapide de
diagnostic de generația
III/IV
(imunocromatografice). Ele
pot fi efectuate atât în
laboratoare medicale cât și
încăperi special amenajate
cu asigurarea de minim
necesar testării.
79.
Confirmarea infectiei cu HIVConfirmarea va fi efectuată
utilizând platforma
GeneXpert care este
implementată în RM
La moment în țară sunt
utilizate 60 de
instrumente, care sunt
repartizate în fiecare
centru raional, 6 în
municipiu și 2 în
sistemul penitenciar.
80.
Metoda GeneXpertMetoda GeneXpert este o metodă molecular
genetică, complet automatizată, real-time,
ce detectează:
Xpert HIV-1 Viral Load - încărcătura virală
HIV 1
Xpert® HIV-1 Qual - acizii nucleici totali
(ADN și ARN) – se va utiliza și pentru
confirmarea infecției cu HIV 1 a nounăscuților de la mame HIV infectate.
81.
82.
--
Diagnosticul primo-infecţiei (markerii virali)
ARNv plasmatic (apare după 8-10 zile de la
contagiu)
Ag p24 în ser (până la apariţia Ac anti-p24)
Ac anti-HIV (după minimum 3 săptămâni de la
contagiu)
Monitorizarea seropozitivilor
Parametrii imuno-hematologici - formula
sangvină, determinarea subpopulaţiilor de LT
(valori absolute, raport T CD4/T CD8), dozarea Ig,
microglobulinei beta2
Markerii virali - şarja virală plasmatică (ARNv), Ag
p24, Ac anti-p24
83.
Algoritmul de testare HIV84.
CHIMIOTERAPIA ANTIRETROVIRALĂ1.
2.
3.
4.
5.
6.
7.
După mecanismul de acţiune:
Inhibitori nucleozidici ai RT (Abacavir, Didanosin,
Lamivudin, Stavudin, Zalcitabin, Zidovudin, Tenofovir)
Inhibitori nenucleozidici ai RT (Delavirdin, Efavirenz,
Nevirapin)
Inhibitori ai receptorului CCR5 (Maraviroc)
Inhibitori ai proteazei (Amprenavir, Indinavir, Lopinavir,
Nelfinavir, Ritonavir, Sanquinavir)
Inhibitorii adeziunii şi penetrării – (Enfuvirtid /T20, CD4)
Inhibitori ai integrazei - (Raltegravir, Elvitegravir,
Dolutegravir, Efavirenz)
Inhibitor al asamblării şi eliberării - Interferonul alpha
85.
86.
87.
Este indicată asocierea a 3 chimioterapice:2
INRT + 1 IP; 2 INRT + 1 INNRT, 3 INRT,
1
INRT+1 INNRT+IP
Dificultăţi:
- Durata şi costul tratamentului
- Toxicitatea preparatelor
- Dezvoltarea rezistenţei
Monitorizarea terapiei antiretrovirale:
- Măsurarea şarjei virale (copii ARNv în plasmă
fiecare 6 luni)
- Determinarea numerică a LT CD4+ fiecare 3 luni
88.
Persoanele infectate cu HIV şibolnave de SIDA sunt asigurate cu
tratament antiretroviral gratuit.
Tratamentul antiretroviral se
realizează conform Protocoalelor
naţionale care sunt ajustate la
Protocoalele OMS.
https://edition.cnn.com/2021/11/16/health/hivpatient-cured-intl-scli-scn/index.html
89.
PROFILAXIA INFECŢIEI HIV/SIDA1.
2.
3.
4.
Măsuri nespecifice: prevenirea transmiterii HIV
Profilaxia post-expunere (un curs de tratament antiretroviral
imediat dupa un contact infectant)
Profilaxia specifică – dificilă!!!
Existenţa a 2 virusuri HIV-1 şi HIV-2 cu numeroase subtipuri
genetice şi antigenice, variabilitatea genetica
Infecţia naturală nu este stopată de răspunsul imun, iar
memoria imunologică este mediocră
Nu este definitif clar rolul LT CD8+ (Tc)
Lipsa unui model animal satisfăcător
90.
STRATEGII DE VACCINARE1.
2.
3.
4.
5.
6.
Elaborarea vaccinurilor vii atenuate
Elaborarea vaccinurilor inactivate
Vaccinuri recombinante subunitare (numai
imunitate umorală)
Epitopi peptidici anti-gp 120 (numai imunitate
umorală)
Utilizarea vectorilor (inserţia genelor env)
Vaccinuri ADN
91.
92.
VIRUSURILE HTLV(Human T-cell Lymphotropic Virus)
Genul Deltaretrovirus
Specii HTLV-1 şi HTLV-2
Structura – comună retrovirusurilor
Transmiterea – contact sexual, vertical, prin sânge (cu
limfocite).
Puterea oncogenă determinată de gena
transactivatoare tax.
Manifestări clinice – 1-5% din persoanele infectate
dezvoltă peste 20-30 ani leucemie acută cu celule T.
Diagnostic – depistarea virusului prin ELISA şi
confirmarea W-B, PCR
Tratament – antiretrovirale, IFN
93.
ONCOGENEZA VIRALĂCancerul este consecinţa dereglării procesului
normal de proliferare celulară.
Căile de apariţie a cancerului:
Hiperactivitatea genelor de stimulare a creşterii
Blocarea genelor care inhibă creşterea
1.
2.
94.
Virusuri cu potenţial oncogen:1.
Virusuri cu genom ADN (Papovaviridae, Adenoviridae,
Herpesviridae, Hepadnaviridae)
2.
Virusuri cu genom ARN (Retroviridae)
Caracter comun – capacitatea genomului viral de a se
integra în cromosomul celulei-gazdă, inducând
transformarea ei.
Transformarea celulară – modificări ale funcţiilor
biologice ale celulei, ce duc la multiplicarea
necontrolată a celulelor şi capacitatea de invazie a
ţesuturilor.
95.
-Virusurile oncogene conţin gene care pot induce
tumori – v-onc
Toate celulele conţin gene omoloage: protooncogene / c-onc (induc o proteină care
controlează replicarea ADN şi multiplicarea
celulară)
V-onc şi c-onc nu sunt identice!!! C-onc pot induce
tumori numai în urma unor mutaţii.
Mecanismele oncogenezei:
Virusul aduce în celulă o oncogenă
Virusul activează proto-oncogenele celulare
96.
Vă doresc perseverență și mult succes!Să vă ”contaminați” doar cu bunătate,
generozitate, omenie, compasiune și zâmbete!!!



























































































 Медицина
Медицина








