Похожие презентации:
Ароматические соединения
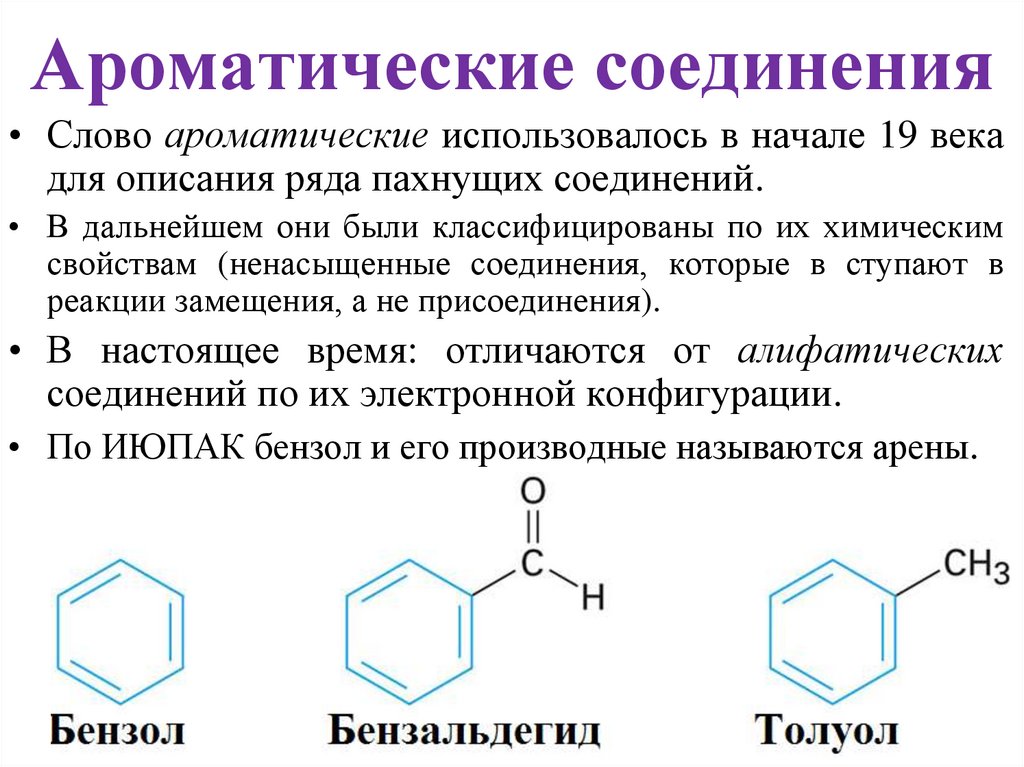
1. Ароматические соединения
• Слово ароматические использовалось в начале 19 векадля описания ряда пахнущих соединений.
• В дальнейшем они были классифицированы по их химическим
свойствам (ненасыщенные соединения, которые в ступают в
реакции замещения, а не присоединения).
• В настоящее время: отличаются от алифатических
соединений по их электронной конфигурации.
• По ИЮПАК бензол и его производные называются арены.
2. Природные ароматические соединения
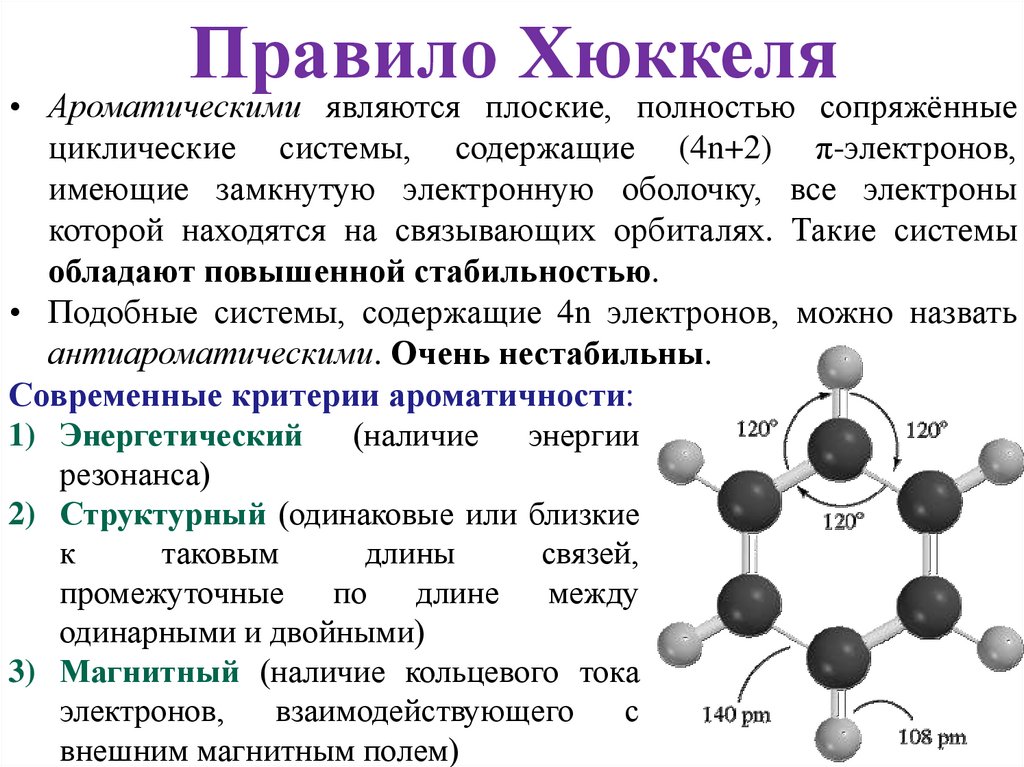
Правило Хюккеля• Ароматическими являются плоские, полностью сопряжённые
циклические системы, содержащие (4n+2) π-электронов,
имеющие замкнутую электронную оболочку, все электроны
которой находятся на связывающих орбиталях. Такие системы
обладают повышенной стабильностью.
• Подобные системы, содержащие 4n электронов, можно назвать
антиароматическими. Очень нестабильны.
Современные критерии ароматичности:
1) Энергетический
(наличие
энергии
резонанса)
2) Структурный (одинаковые или близкие
к
таковым
длины
связей,
промежуточные по длине между
одинарными и двойными)
3) Магнитный (наличие кольцевого тока
электронов,
взаимодействующего
с
внешним магнитным полем)
3. Синтетические ароматические соединения в медицине
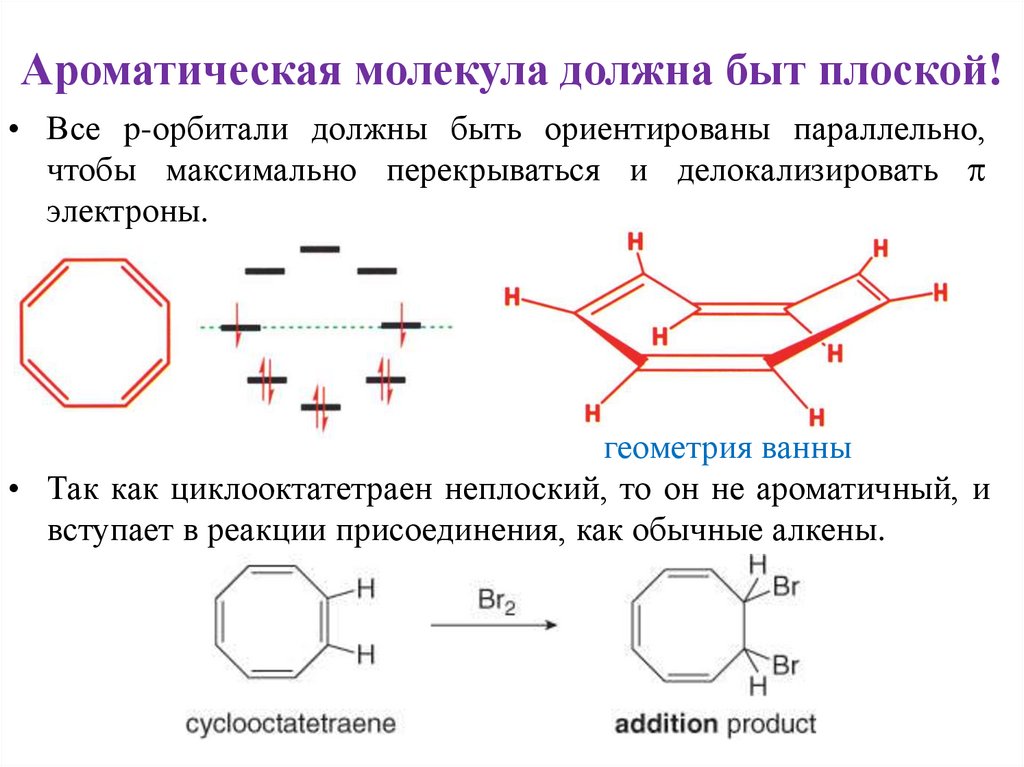
Ароматическая молекула должна быт плоской!• Все p-орбитали должны быть ориентированы параллельно,
чтобы максимально перекрываться и делокализировать
электроны.
геометрия ванны
• Так как циклооктатетраен неплоский, то он не ароматичный, и
вступает в реакции присоединения, как обычные алкены.
4.
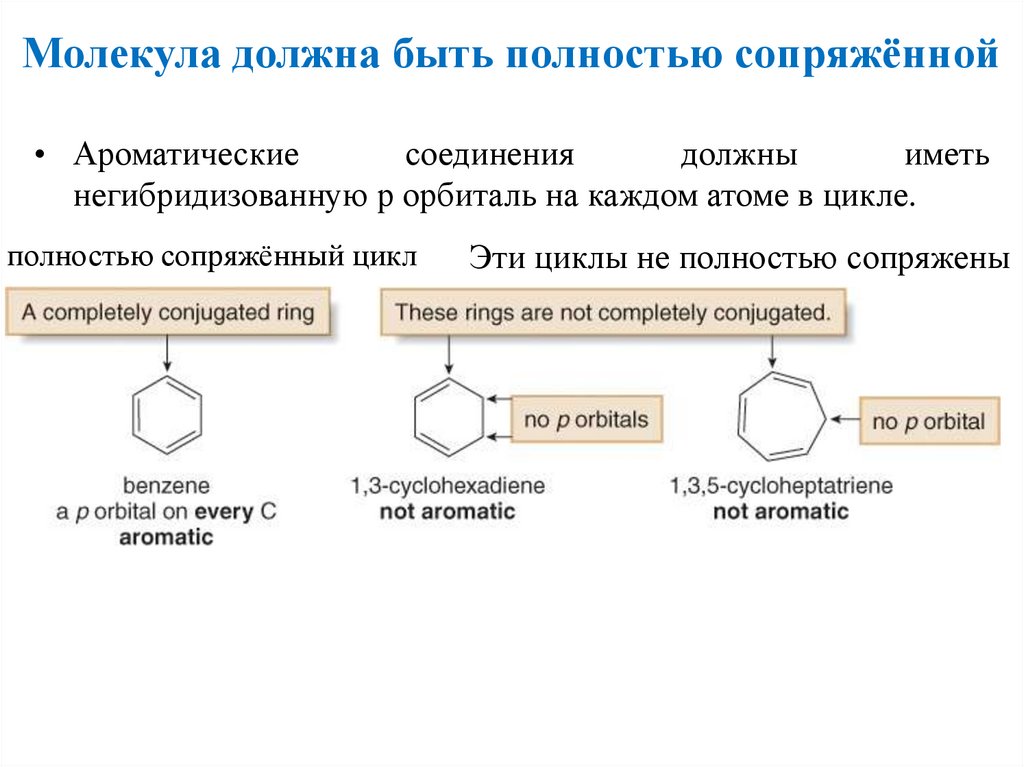
Молекула должна быть полностью сопряжённой• Ароматические
соединения
должны
иметь
негибридизованную р орбиталь на каждом атоме в цикле.
полностью сопряжённый цикл
Эти циклы не полностью сопряжены
5.
Химические критерииароматичности
1. Термическая устойчивость
2. Нет склонности к окислению
3. Склонность к реакциям замещения
6.
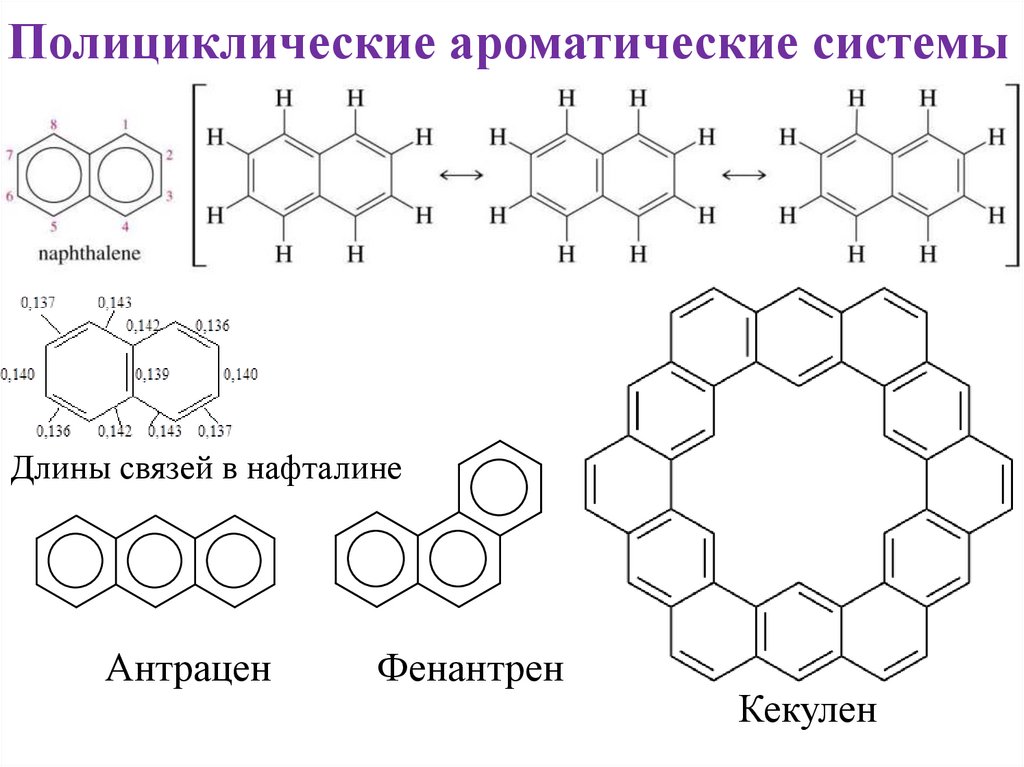
Полициклические ароматические системыДлины связей в нафталине
Антрацен
Фенантрен
Кекулен
7.
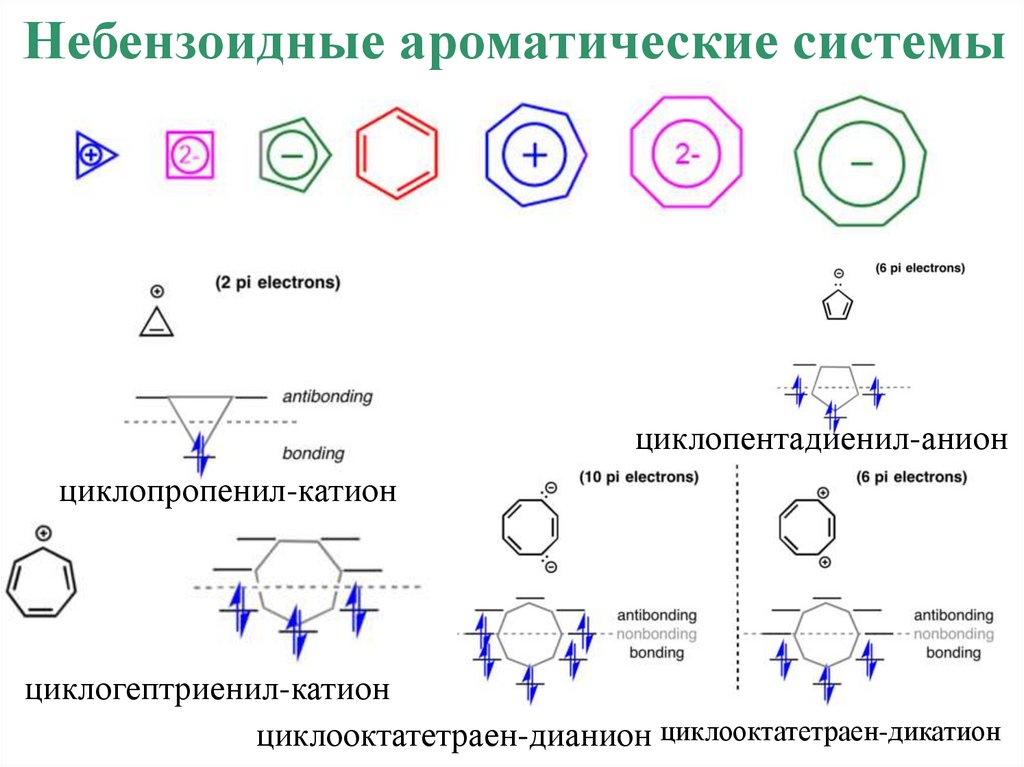
Небензоидные ароматические системыциклопентадиенил-анион
циклопропенил-катион
циклогептриенил-катион
циклооктатетраен-дианион циклооктатетраен-дикатион
8.
• Резонансный гибрид показывает, что все пятьатомов углерода в циклопентадиенильном
анионе эквивалентны.
• Каждый атом углерода несёт одну пятую
отрицательного заряда аниона.
9.
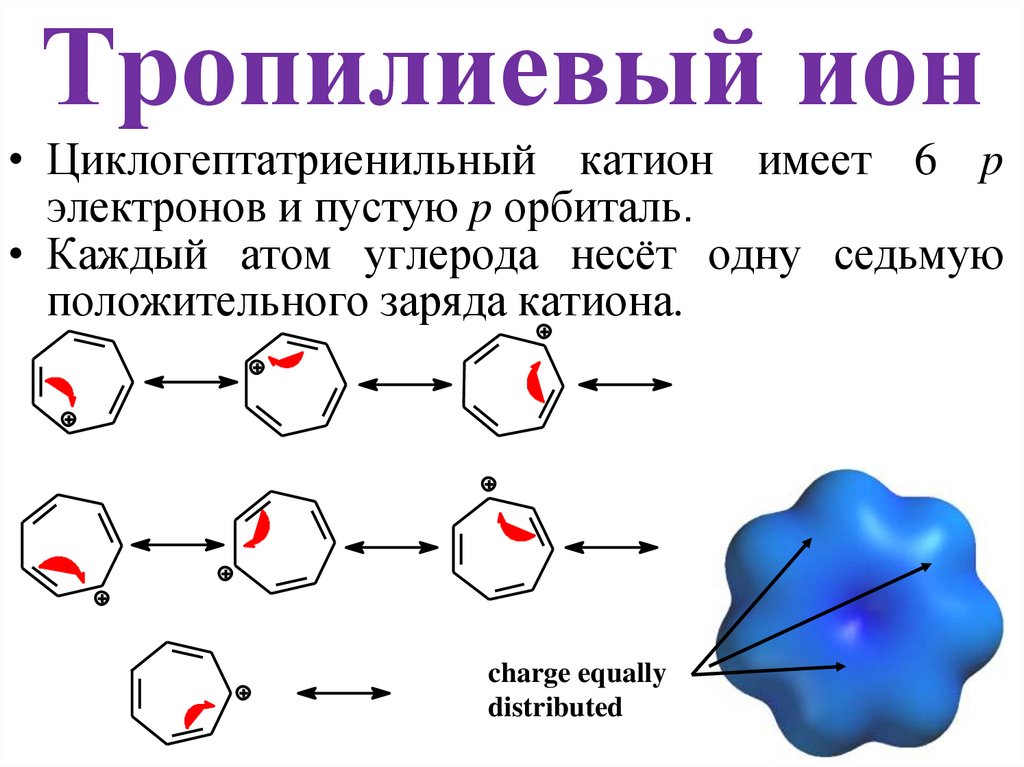
Тропилиевый ион• Циклогептатриенильный катион имеет 6 p
электронов и пустую p орбиталь.
• Каждый атом углерода несёт одну седьмую
положительного заряда катиона.
charge equally
distributed
10.
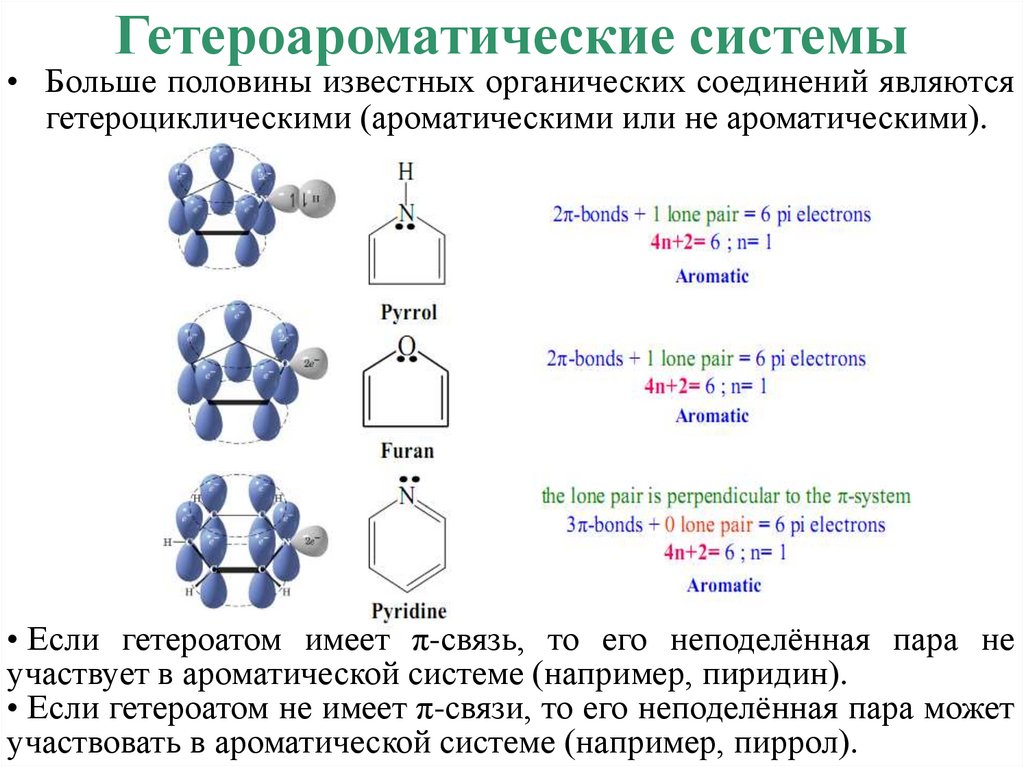
Гетероароматические системы• Больше половины известных органических соединений являются
гетероциклическими (ароматическими или не ароматическими).
• Если гетероатом имеет π-связь, то его неподелённая пара не
участвует в ароматической системе (например, пиридин).
• Если гетероатом не имеет π-связи, то его неподелённая пара может
участвовать в ароматической системе (например, пиррол).
11.
Антиароматические соединенияоксирен 1Н-азирен
1.567 Å
=
1.346 Å
Геометрия на самом деле
прямоугольная
Не стабилен выше -240 °С
• Следуя правилу Хунда, два
электрона
находятся
на
отдельных орбиталях.
• Этот бирадикал является очень
реакционноспособным.
12.
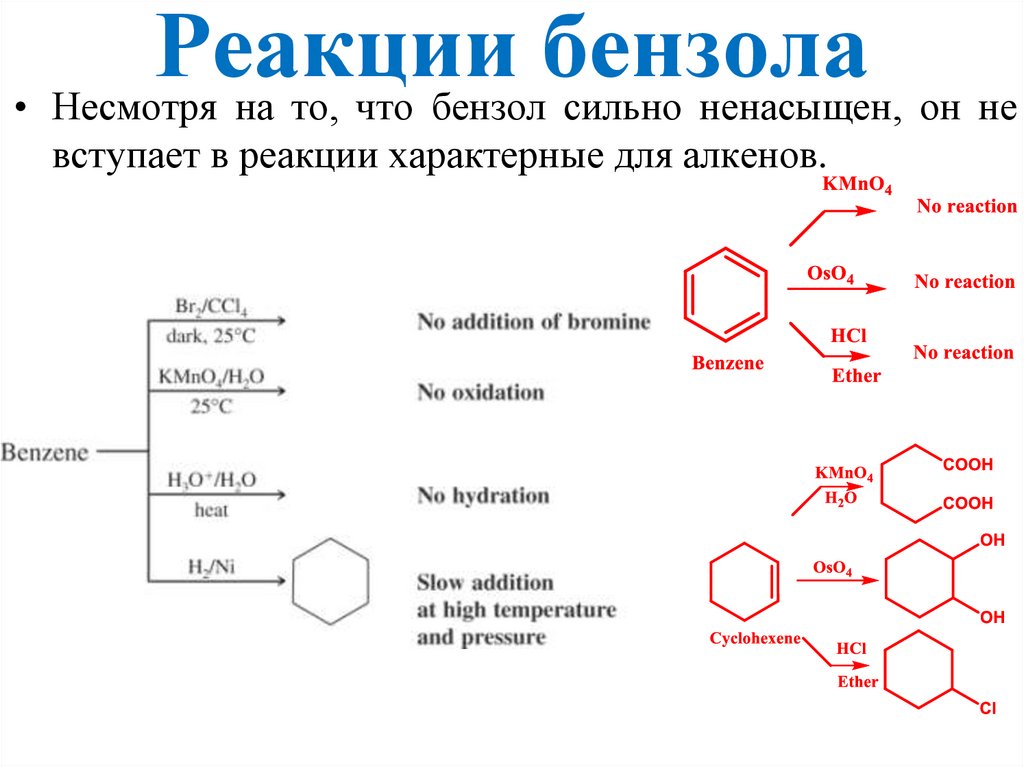
Реакциибензола
• Несмотря на то, что бензол сильно ненасыщен, он не
вступает в реакции характерные для алкенов.
13.
14.
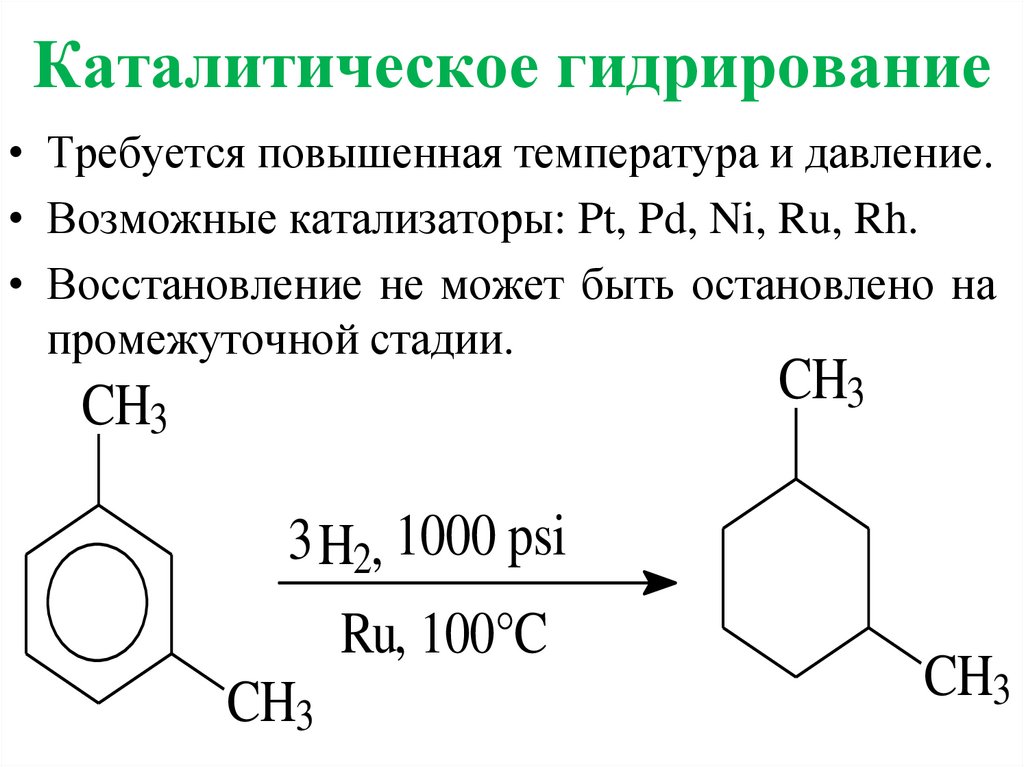
Каталитическое гидрирование• Требуется повышенная температура и давление.
• Возможные катализаторы: Pt, Pd, Ni, Ru, Rh.
• Восстановление не может быть остановлено на
промежуточной стадии.
CH
3
CH3
3 H2, 1000 psi
Ru, 100°C
CH3
CH3
15.
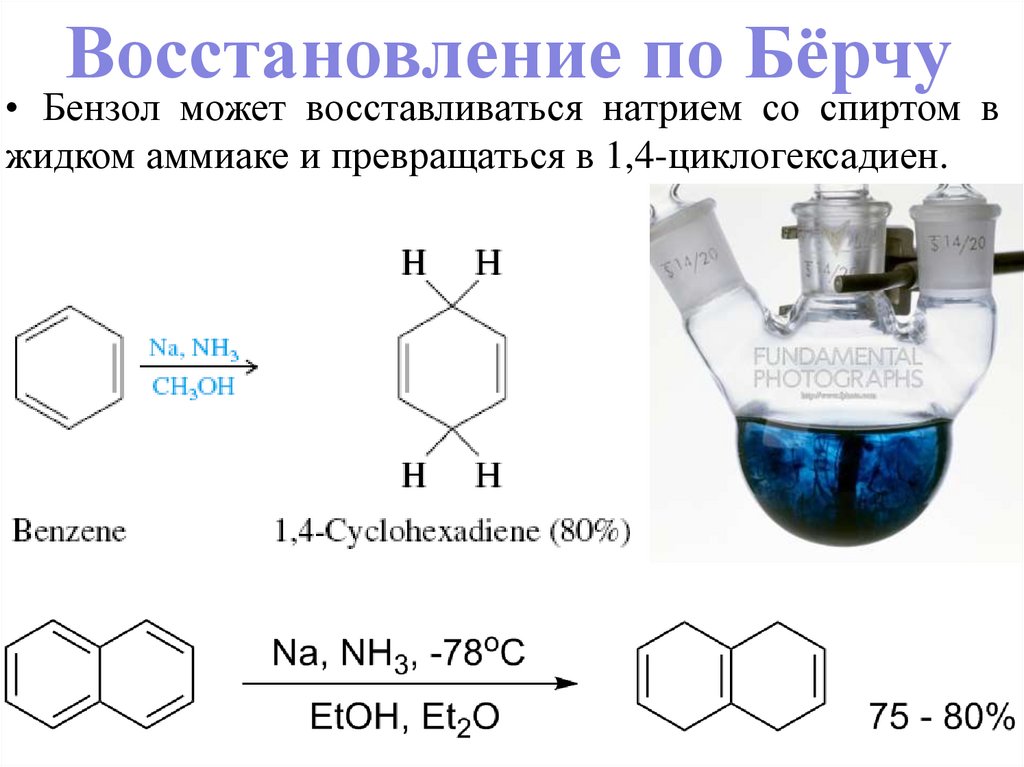
Восстановление по Бёрчу• Бензол может восставливаться натрием со спиртом в
жидком аммиаке и превращаться в 1,4-циклогексадиен.
16.
Механизм реакции Бёрча17.
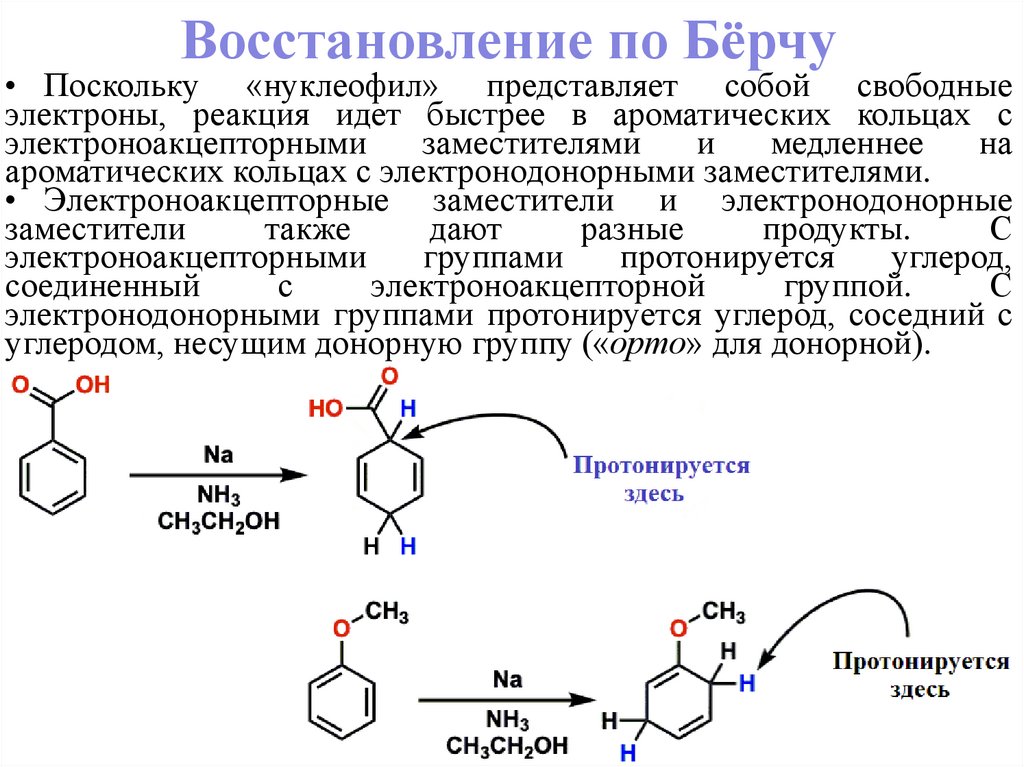
Восстановление по Бёрчу• Поскольку «нуклеофил» представляет собой свободные
электроны, реакция идет быстрее в ароматических кольцах с
электроноакцепторными
заместителями
и
медленнее
на
ароматических кольцах с электронодонорными заместителями.
• Электроноакцепторные заместители и электронодонорные
заместители
также
дают
разные
продукты.
С
электроноакцепторными
группами
протонируется
углерод,
соединенный
с
электроноакцепторной
группой.
С
электронодонорными группами протонируется углерод, соседний с
углеродом, несущим донорную группу («орто» для донорной).
18. Тропилиевый ион
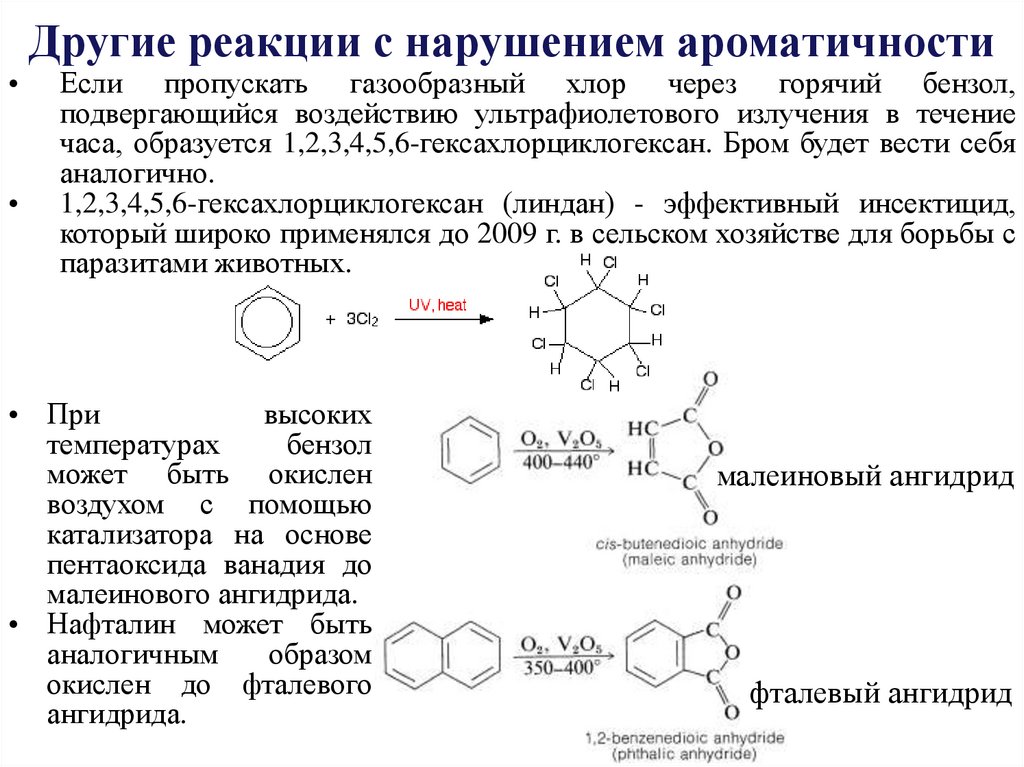
Другие реакции с нарушением ароматичности
Если пропускать газообразный хлор через горячий бензол,
подвергающийся воздействию ультрафиолетового излучения в течение
часа, образуется 1,2,3,4,5,6-гексахлорциклогексан. Бром будет вести себя
аналогично.
1,2,3,4,5,6-гексахлорциклогексан (линдан) - эффективный инсектицид,
который широко применялся до 2009 г. в сельском хозяйстве для борьбы с
паразитами животных.
• При
высоких
температурах
бензол
может быть окислен
воздухом с помощью
катализатора на основе
пентаоксида ванадия до
малеинового ангидрида.
• Нафталин может быть
аналогичным
образом
окислен до фталевого
ангидрида.
малеиновый ангидрид
фталевый ангидрид
19.
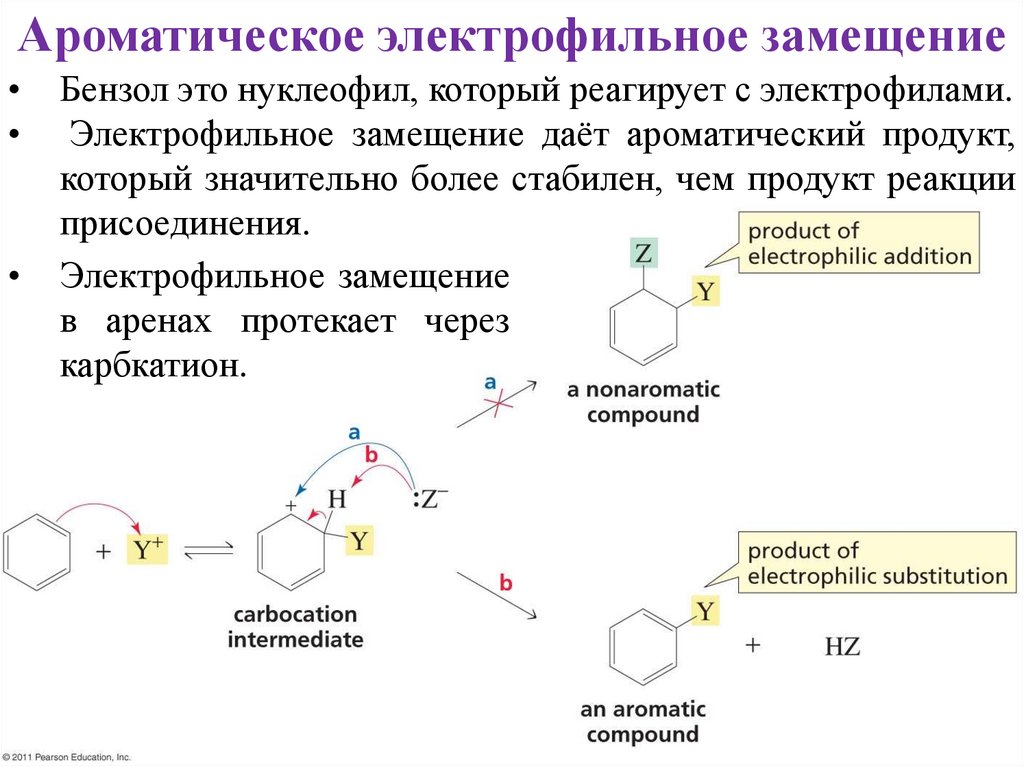
Ароматическое электрофильное замещениеБензол это нуклеофил, который реагирует с электрофилами.
Электрофильное замещение даёт ароматический продукт,
который значительно более стабилен, чем продукт реакции
присоединения.
Электрофильное замещение
в аренах протекает через
карбкатион.
20.
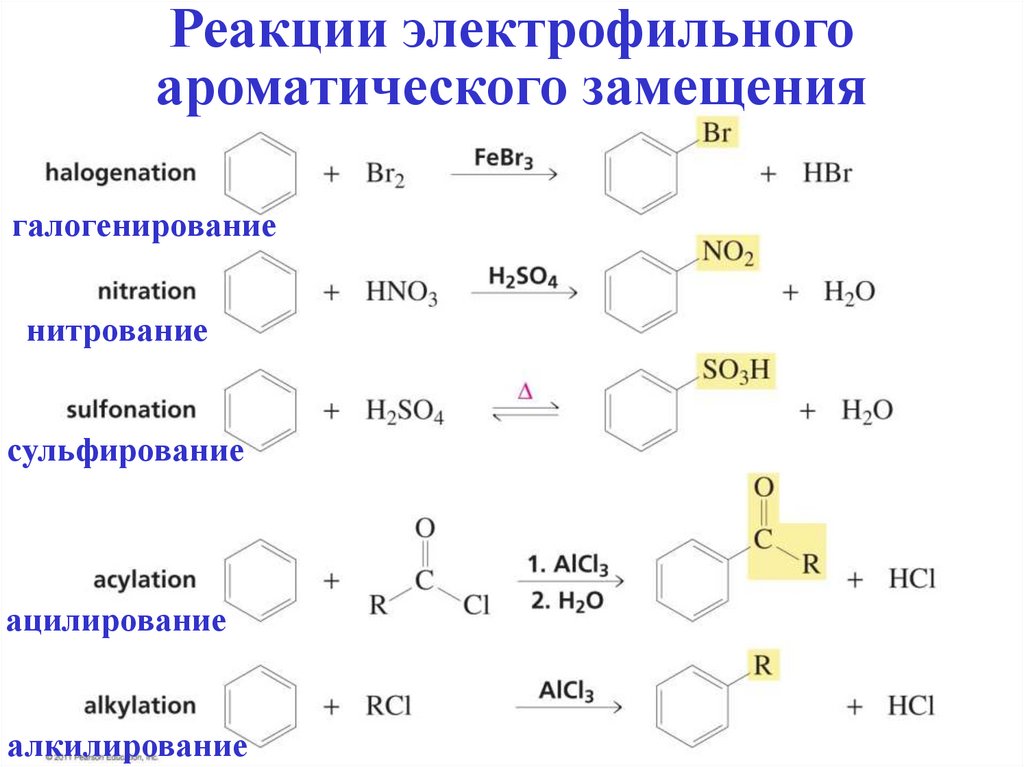
Реакции электрофильногоароматического замещения
галогенирование
нитрование
сульфирование
ацилирование
алкилирование
21.
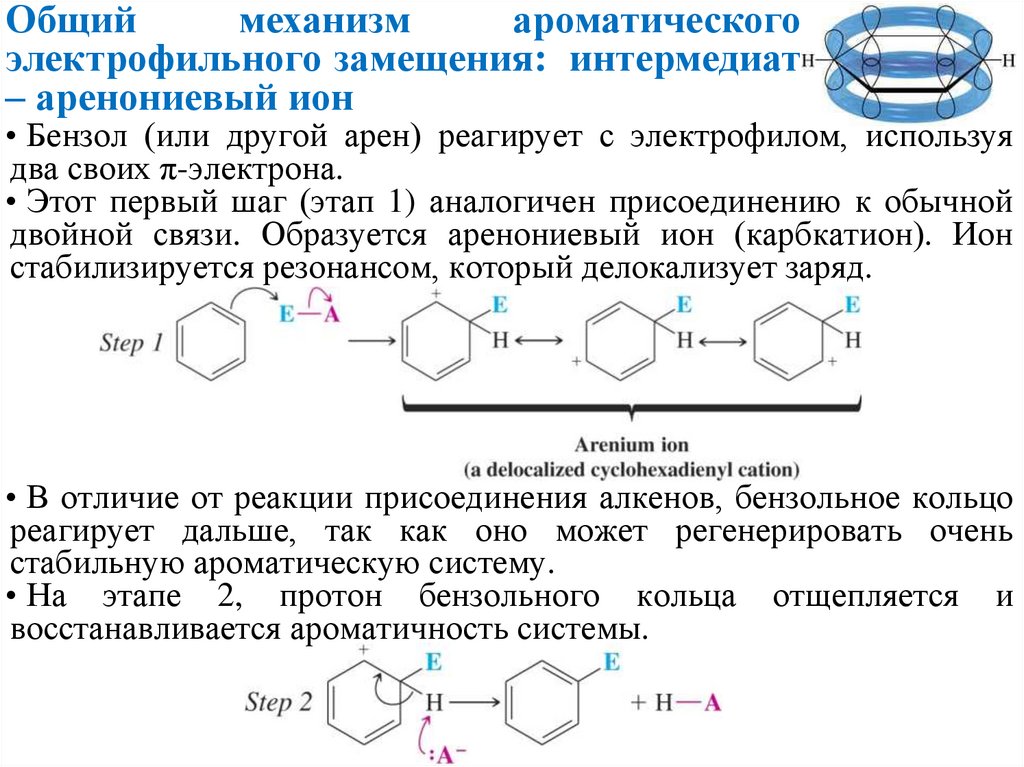
Общиймеханизм
ароматического
электрофильного замещения: интермедиат
– аренониевый ион
• Бензол (или другой арен) реагирует с электрофилом, используя
два своих π-электрона.
• Этот первый шаг (этап 1) аналогичен присоединению к обычной
двойной связи. Образуется аренониевый ион (карбкатион). Ион
стабилизируется резонансом, который делокализует заряд.
• В отличие от реакции присоединения алкенов, бензольное кольцо
реагирует дальше, так как оно может регенерировать очень
стабильную ароматическую систему.
• На этапе 2, протон бензольного кольца отщепляется и
восстанавливается ароматичность системы.
22.
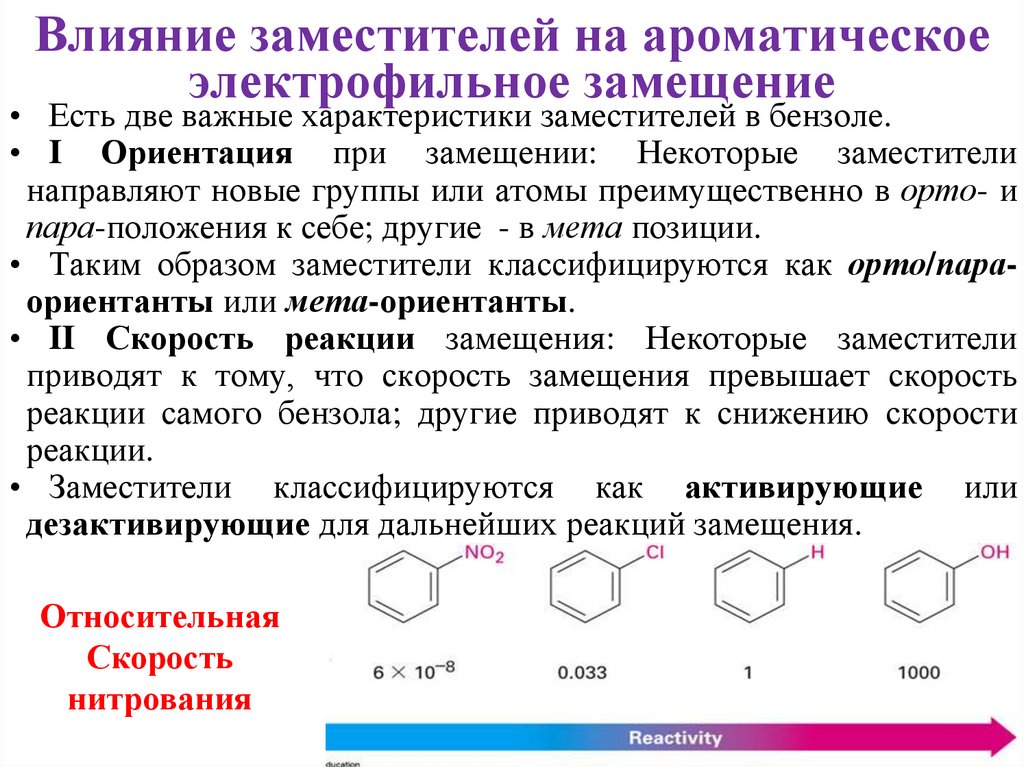
Влияние заместителей на ароматическоеэлектрофильное замещение
• Есть две важные характеристики заместителей в бензоле.
• I Ориентация при замещении: Некоторые заместители
направляют новые группы или атомы преимущественно в орто- и
пара-положения к себе; другие - в мета позиции.
• Таким образом заместители классифицируются как орто/параориентанты или мета-ориентанты.
• II Скорость реакции замещения: Некоторые заместители
приводят к тому, что скорость замещения превышает скорость
реакции самого бензола; другие приводят к снижению скорости
реакции.
• Заместители классифицируются как активирующие или
дезактивирующие для дальнейших реакций замещения.
Относительная
Скорость
нитрования
23.
Влияние заместителей на ароматическоеэлектрофильное замещение
Орто/параориентанты
Метаориентанты
Активирующие
группы
Дезактивирующие
группы
• Гидроксильная (OH);
• Алкокси (OR);
• Амино (NH2, NHR, NR2);
• Алкильная (CH3 и т.д.);
• Тио (SH, SR)
Не существуют
Галогены (F, Cl, Br, I)
• Нитро (NO2);
• Карбонильная (С=О);
• Сульфо (SO3H);
• СF3;
• Циано (CN)
• Карбоксильная
24. Реакции бензола
Природа влияния заместителейна реакции аренов
• Эффект
заместителя
является
суммой
индуктивного и резонансного эффектов.
• Индуктивный эффект – увеличение или
уменьшение электронной плотности через σсвязи = полярные ковалентные связи.
• Резонансный эффект - увеличение или
уменьшение электронной плотности из-за
перекрытия p-орбитали заместителя с pорбиталями ароматического кольца.
25.
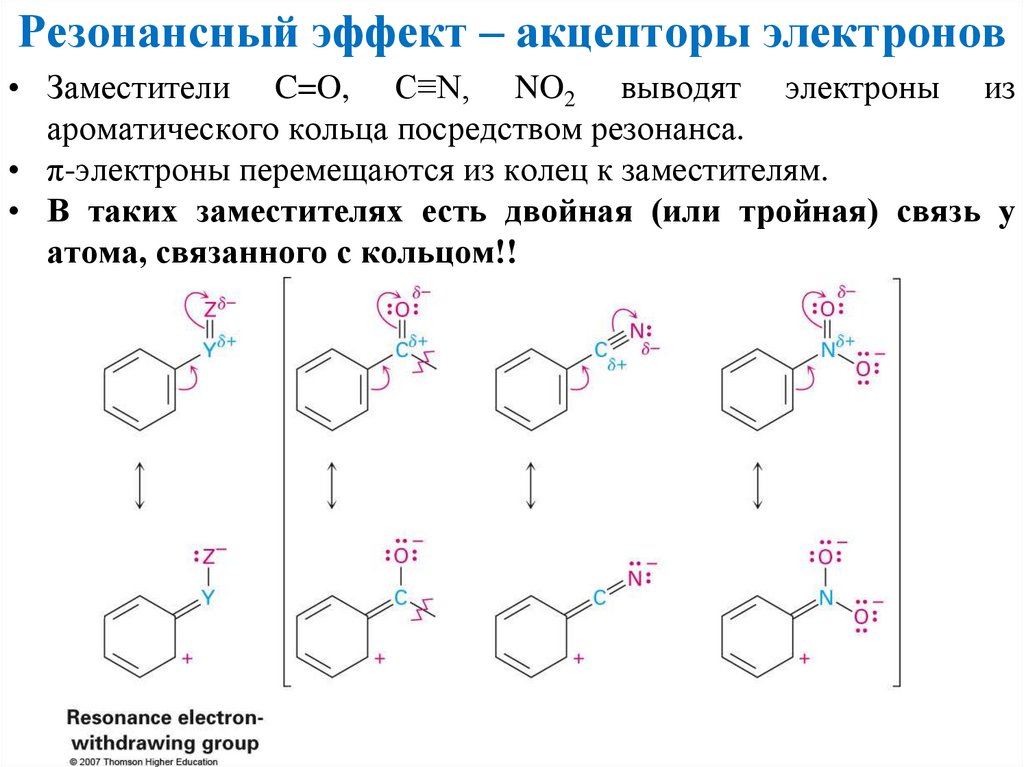
Резонансный эффект – акцепторы электронов• Заместители C=O, C≡N, NO2 выводят электроны из
ароматического кольца посредством резонанса.
• π-электроны перемещаются из колец к заместителям.
• В таких заместителях есть двойная (или тройная) связь у
атома, связанного с кольцом!!
26. Каталитическое гидрирование
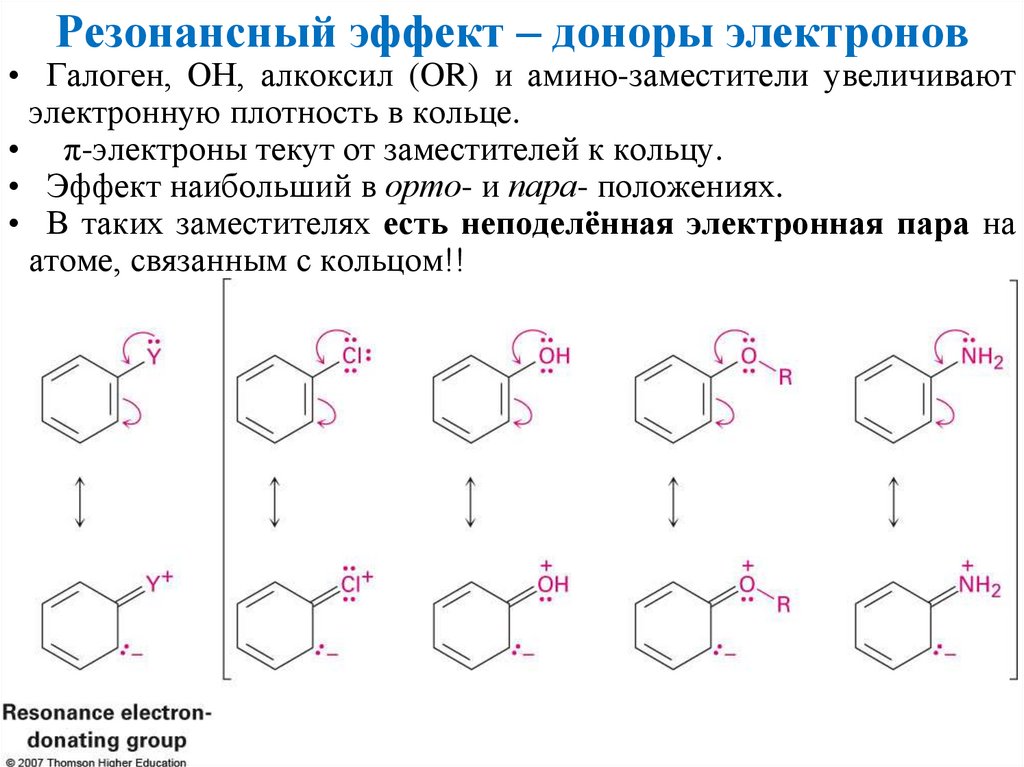
Резонансный эффект – доноры электронов• Галоген, ОН, алкоксил (OR) и амино-заместители увеличивают
электронную плотность в кольце.
• π-электроны текут от заместителей к кольцу.
• Эффект наибольший в орто- и пара- положениях.
• В таких заместителях есть неподелённая электронная пара на
атоме, связанным с кольцом!!
27.
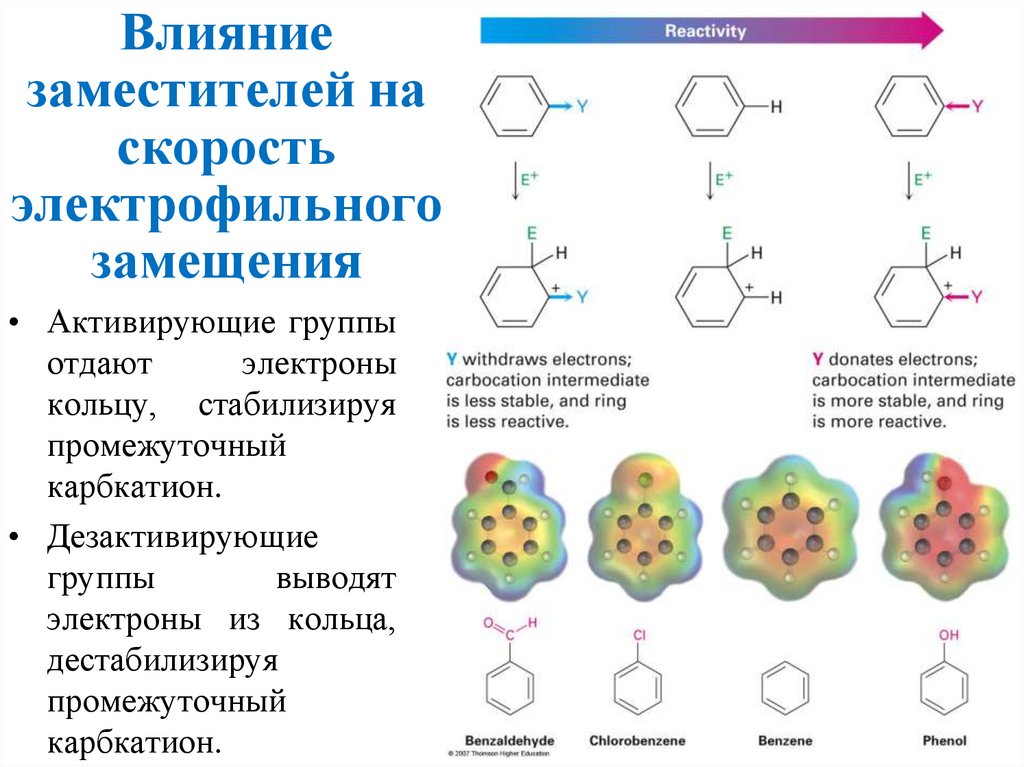
Влияниезаместителей на
скорость
электрофильного
замещения
• Активирующие группы
отдают
электроны
кольцу, стабилизируя
промежуточный
карбкатион.
• Дезактивирующие
группы
выводят
электроны из кольца,
дестабилизируя
промежуточный
карбкатион.
28. Механизм реакции Бёрча
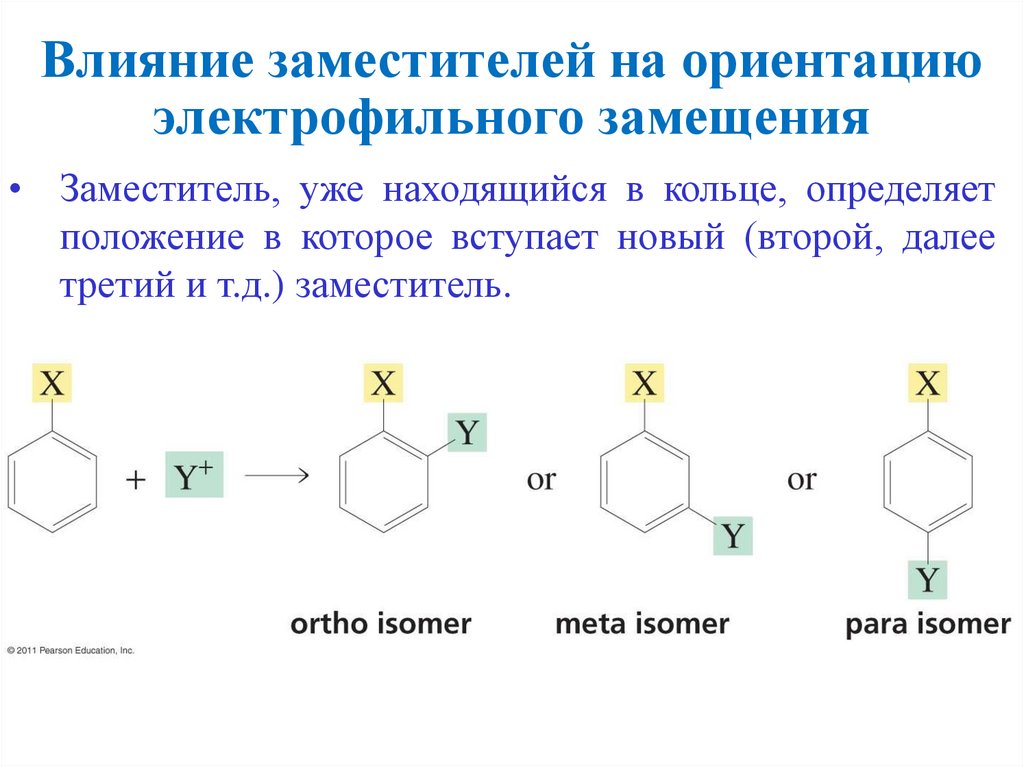
Влияние заместителей на ориентациюэлектрофильного замещения
• Заместитель, уже находящийся в кольце, определяет
положение в которое вступает новый (второй, далее
третий и т.д.) заместитель.
29.
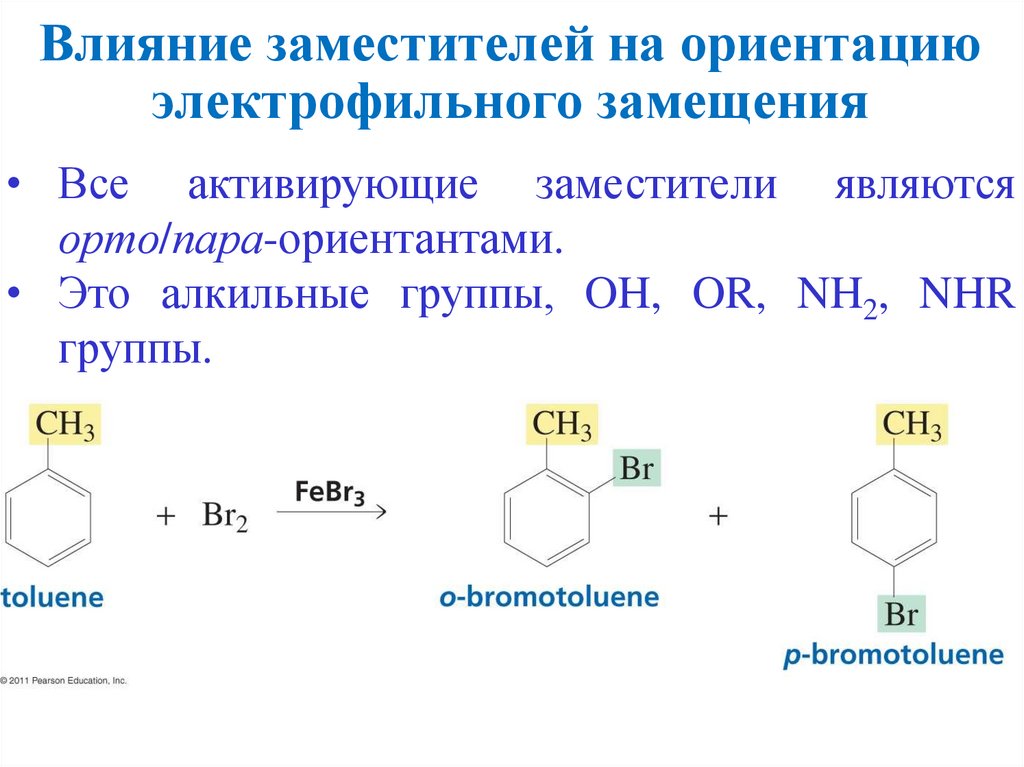
Влияние заместителей на ориентациюэлектрофильного замещения
• Все активирующие заместители являются
орто/пара-ориентантами.
• Это алкильные группы, OH, OR, NH2, NHR
группы.
30.
Влияние заместителей на ориентациюэлектрофильного замещения
• Галогены – слабо дезактивирующие группы,
также являются орто/пара-ориентантами.
31.
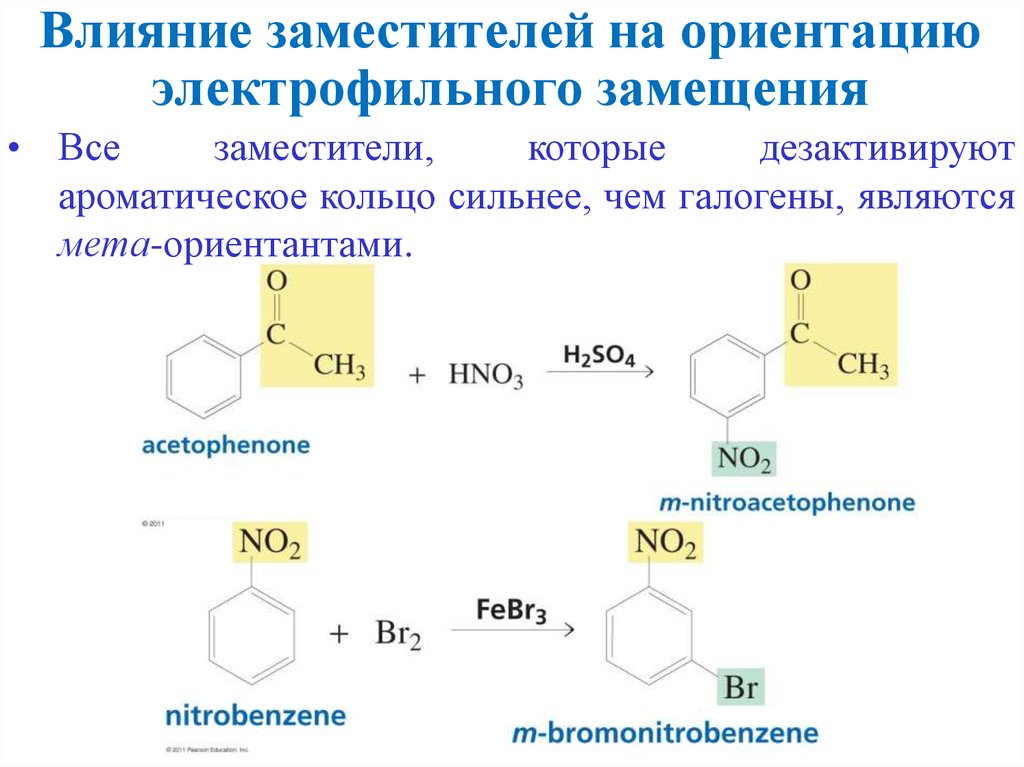
Влияние заместителей на ориентациюэлектрофильного замещения
• Все
заместители,
которые
дезактивируют
ароматическое кольцо сильнее, чем галогены, являются
мета-ориентантами.
32.
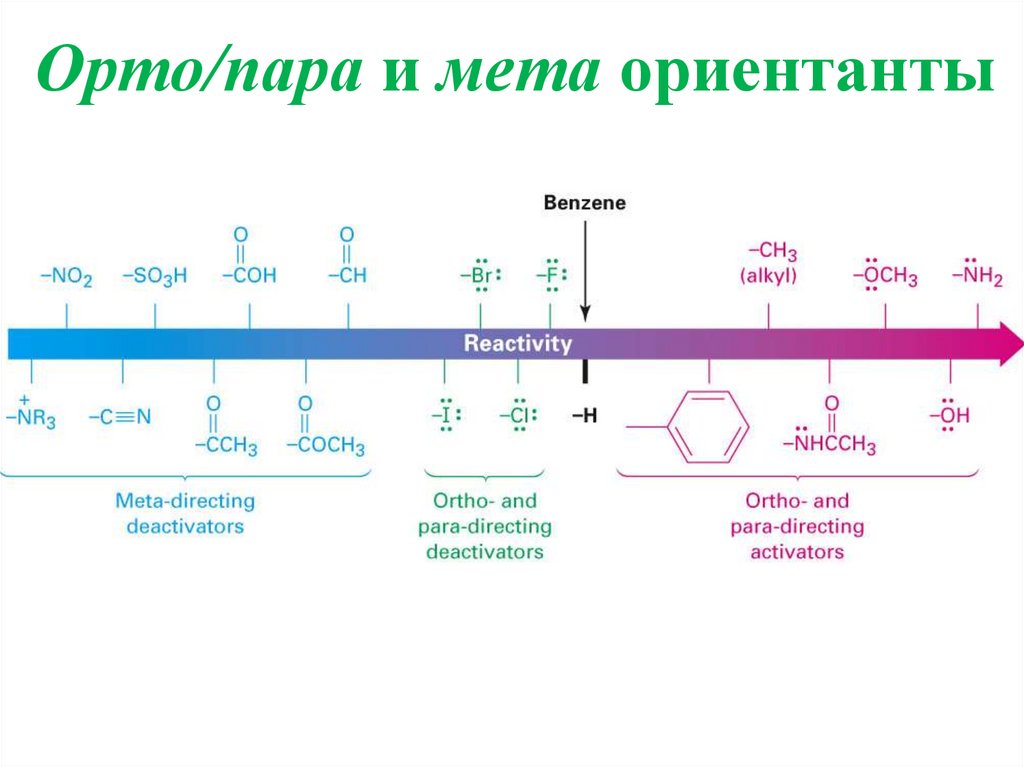
Орто/пара и мета ориентанты33.
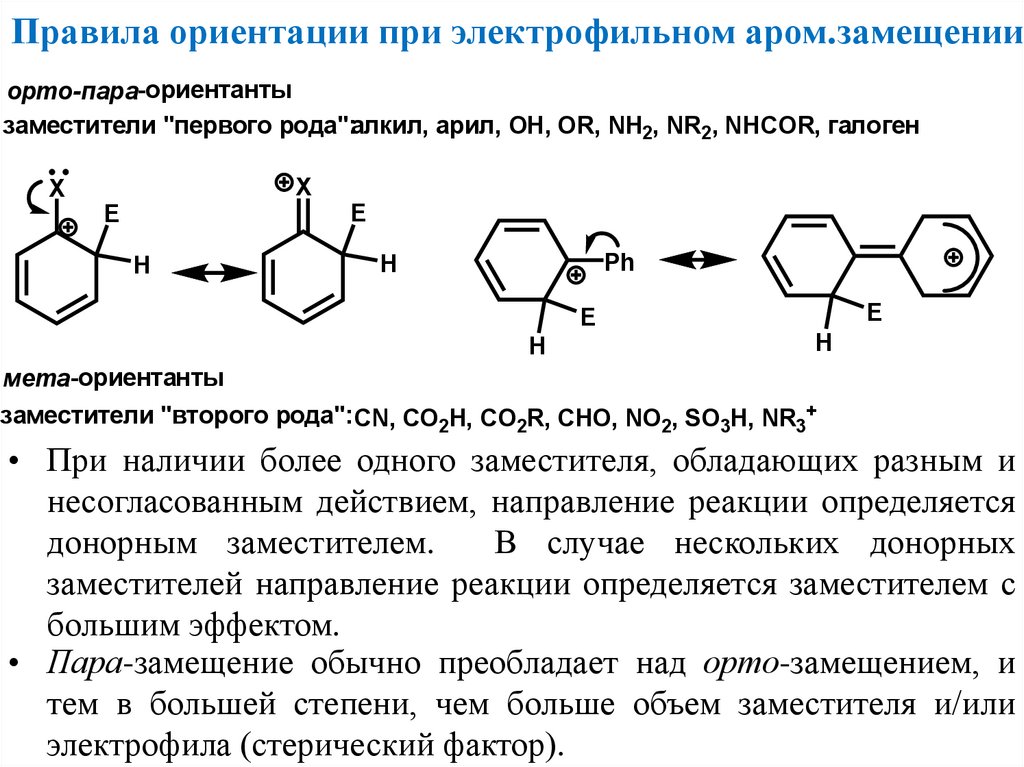
Правила ориентации при электрофильном аром.замещенииорто-пара-ориентанты
заместители "первого рода":алкил, арил, OH, OR, NH2, NR2 , NHCOR, галоген
X
X
E
E
H
Ph
H
E
E
H
H
мета-ориентанты
заместители "второго рода": CN, CO2H, CO2R, CHO, NO2, SO3H, NR3+
• При наличии более одного заместителя, обладающих разным и
несогласованным действием, направление реакции определяется
донорным заместителем.
В случае нескольких донорных
заместителей направление реакции определяется заместителем с
большим эффектом.
• Пара-замещение обычно преобладает над орто-замещением, и
тем в большей степени, чем больше объем заместителя и/или
электрофила (стерический фактор).
34.
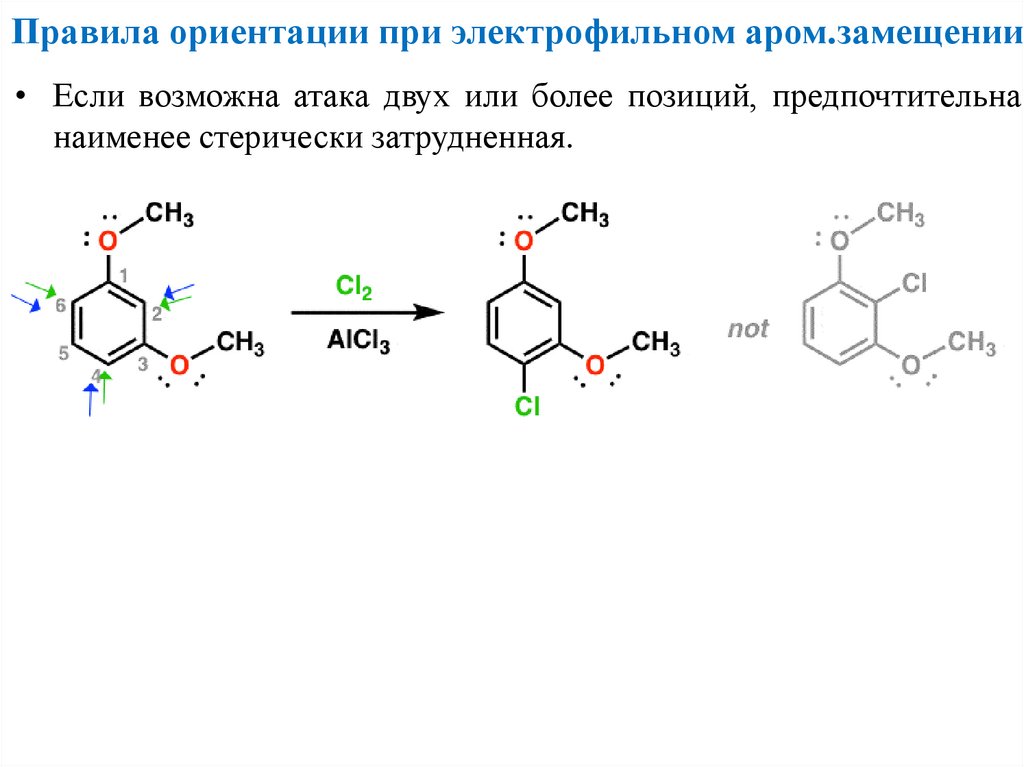
Правила ориентации при электрофильном аром.замещении• Если возможна атака двух или более позиций, предпочтительна
наименее стерически затрудненная.
35. Влияние заместителей на ароматическое электрофильное замещение
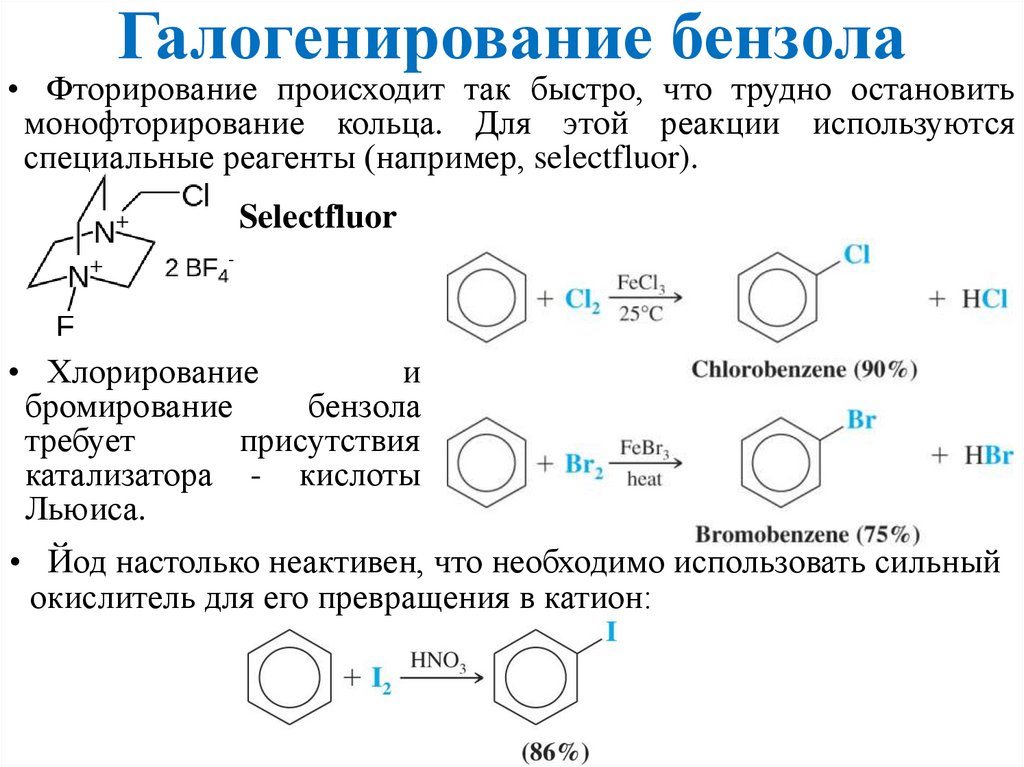
Галогенирование бензола• Фторирование происходит так быстро, что трудно остановить
монофторирование кольца. Для этой реакции используются
специальные реагенты (например, selectfluor).
Selectfluor
• Хлорирование
и
бромирование
бензола
требует
присутствия
катализатора - кислоты
Льюиса.
• Йод настолько неактивен, что необходимо использовать сильный
окислитель для его превращения в катион:
36.
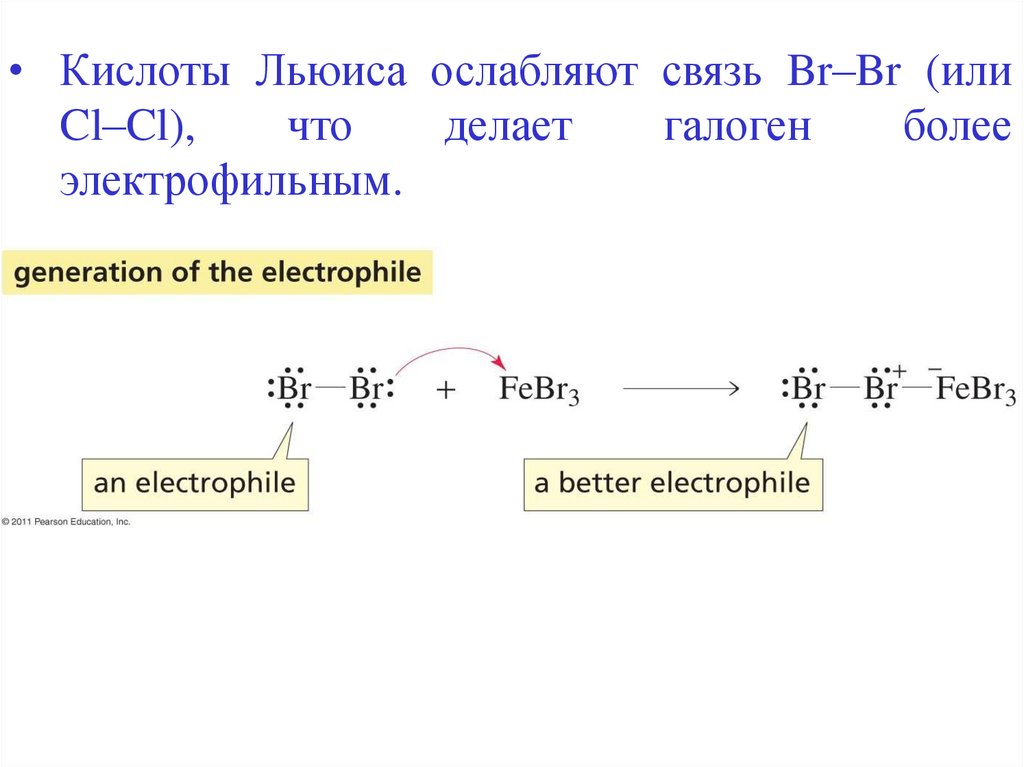
• Кислоты Льюиса ослабляют связь Br–Br (илиCl–Cl),
что
делает
галоген
более
электрофильным.
37. Природа влияния заместителей на реакции аренов
Механизм бромирования бензолаB: Бромид-анион или бензол
Катализатор регенерируется:
© 2011 Pearson Education, Inc.
38. Индуктивный эффект
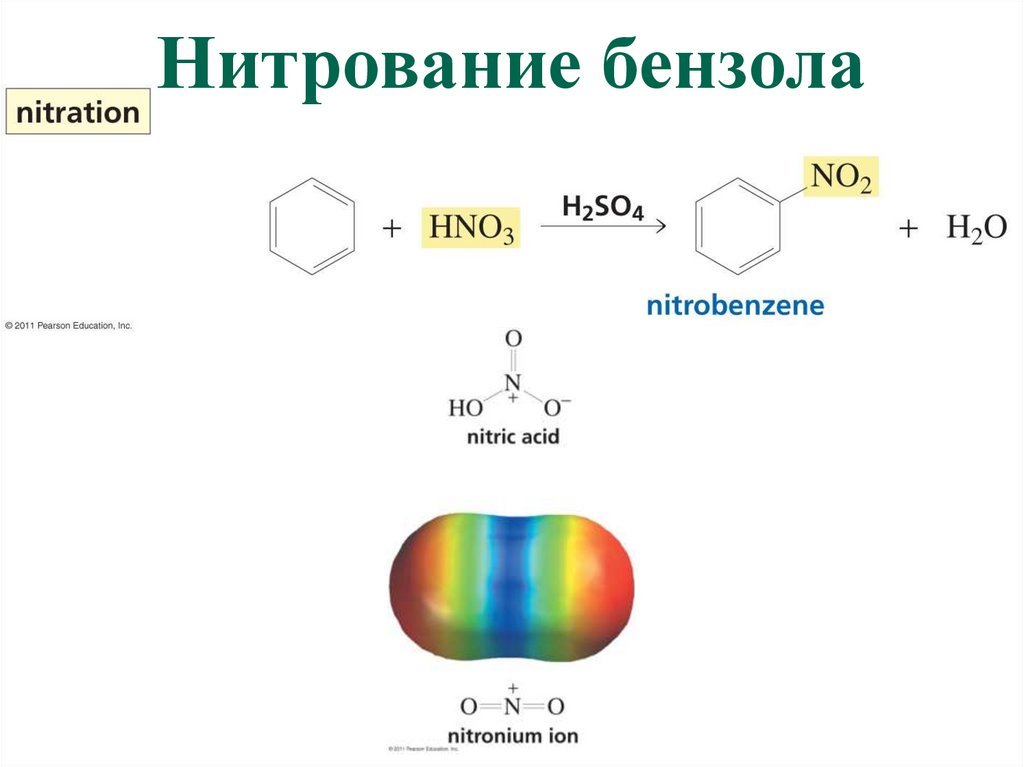
Нитрование бензола39. Резонансный эффект – акцепторы электронов
Образование нитроний-катиона:Ароматическое электрофильное замещение:
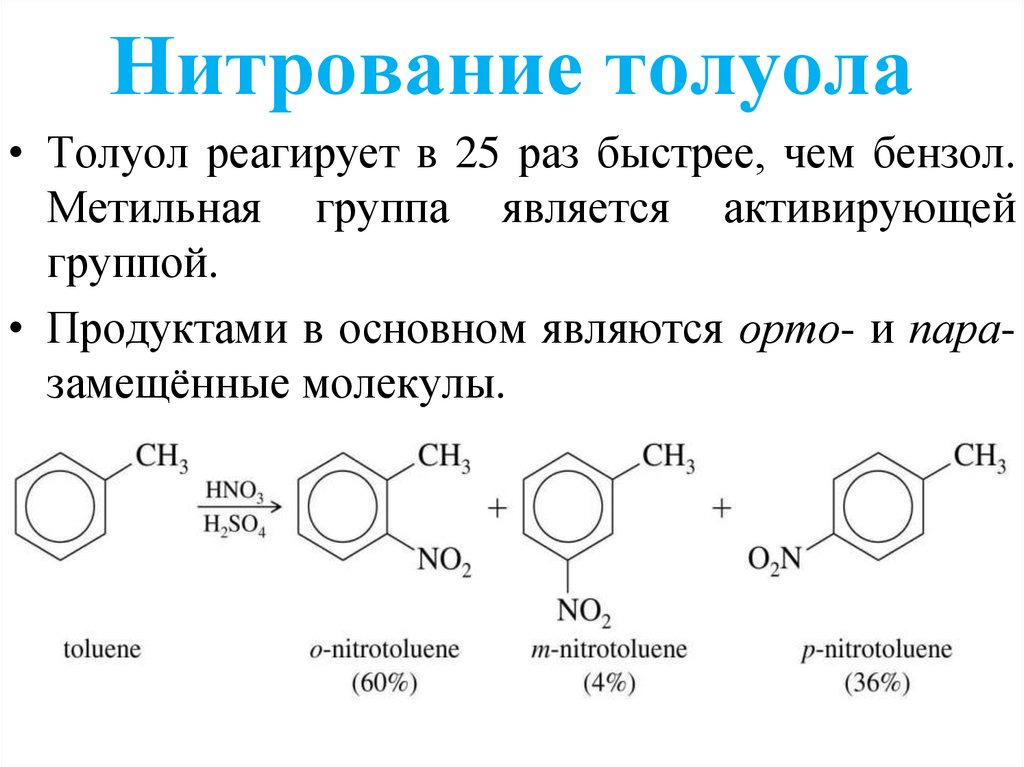
40. Резонансный эффект – доноры электронов
Нитрование толуола• Толуол реагирует в 25 раз быстрее, чем бензол.
Метильная группа является активирующей
группой.
• Продуктами в основном являются орто- и паразамещённые молекулы.
41.
Сульфирование бензола42. Влияние заместителей на скорость электрофильного замещения
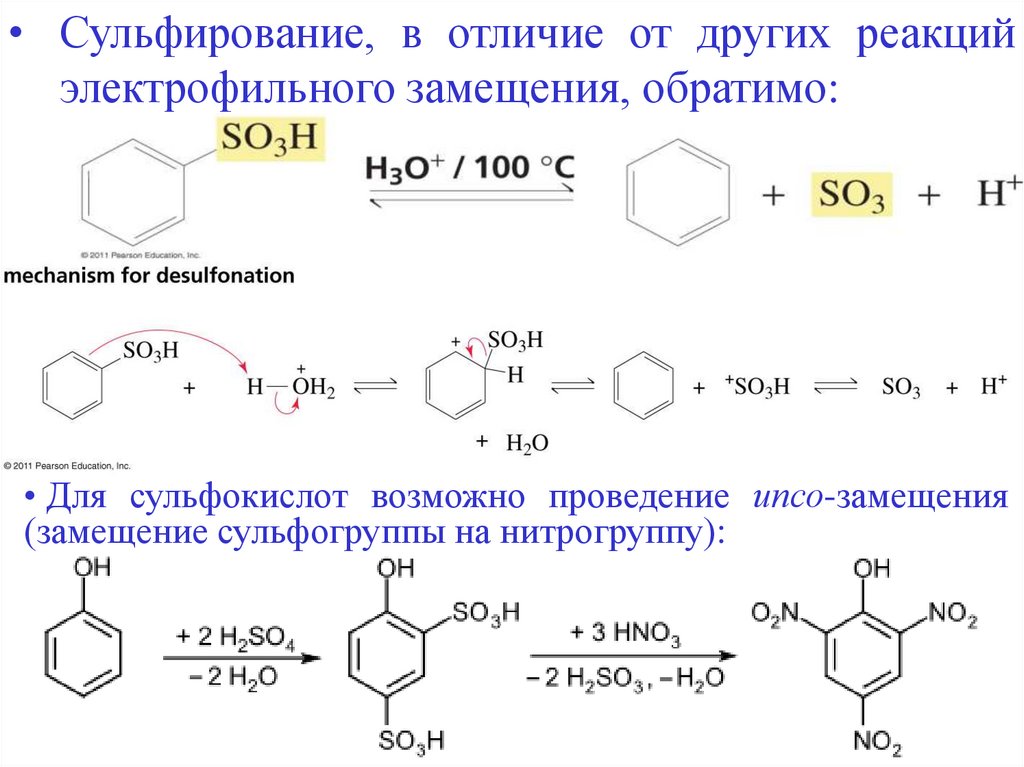
• Сульфирование, в отличие от других реакцийэлектрофильного замещения, обратимо:
• Для сульфокислот возможно проведение ипсо-замещения
(замещение сульфогруппы на нитрогруппу):
43. Результат действия индуктивного и мезомерного эффектов
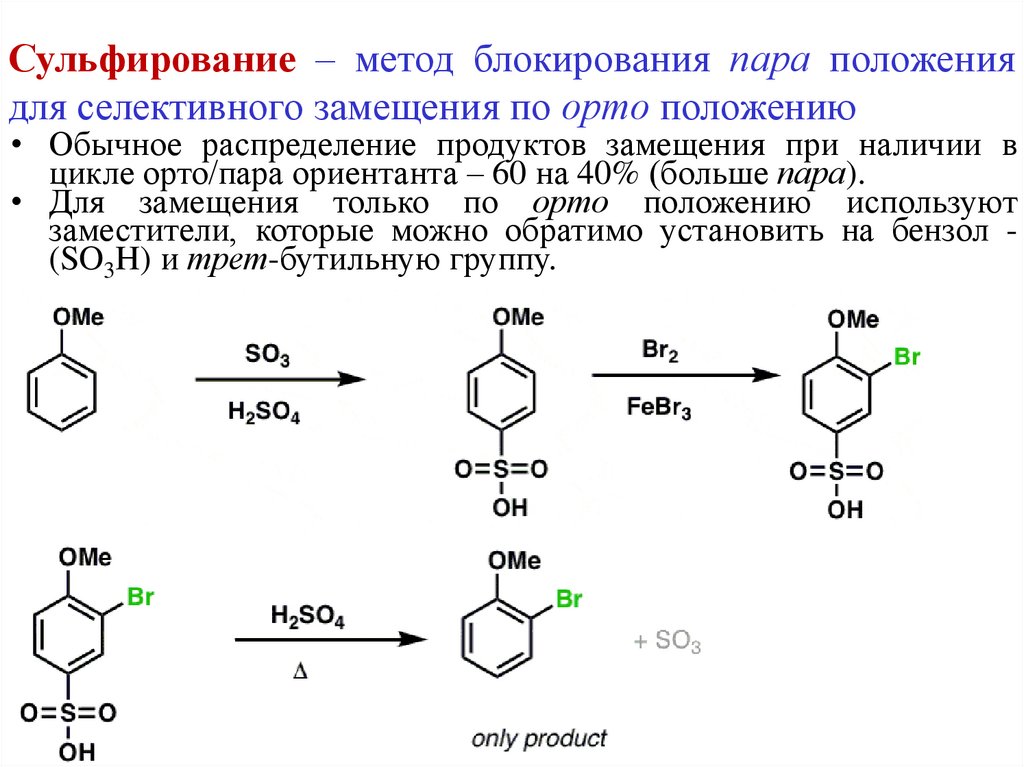
Сульфирование – метод блокирования пара положениядля селективного замещения по орто положению
• Обычное распределение продуктов замещения при наличии в
цикле орто/пара ориентанта – 60 на 40% (больше пара).
• Для замещения только по орто положению используют
заместители, которые можно обратимо установить на бензол (SO3H) и трет-бутильную группу.
44.
Алкилирование бензола(реакция Фриделя-Крафтса)
45.
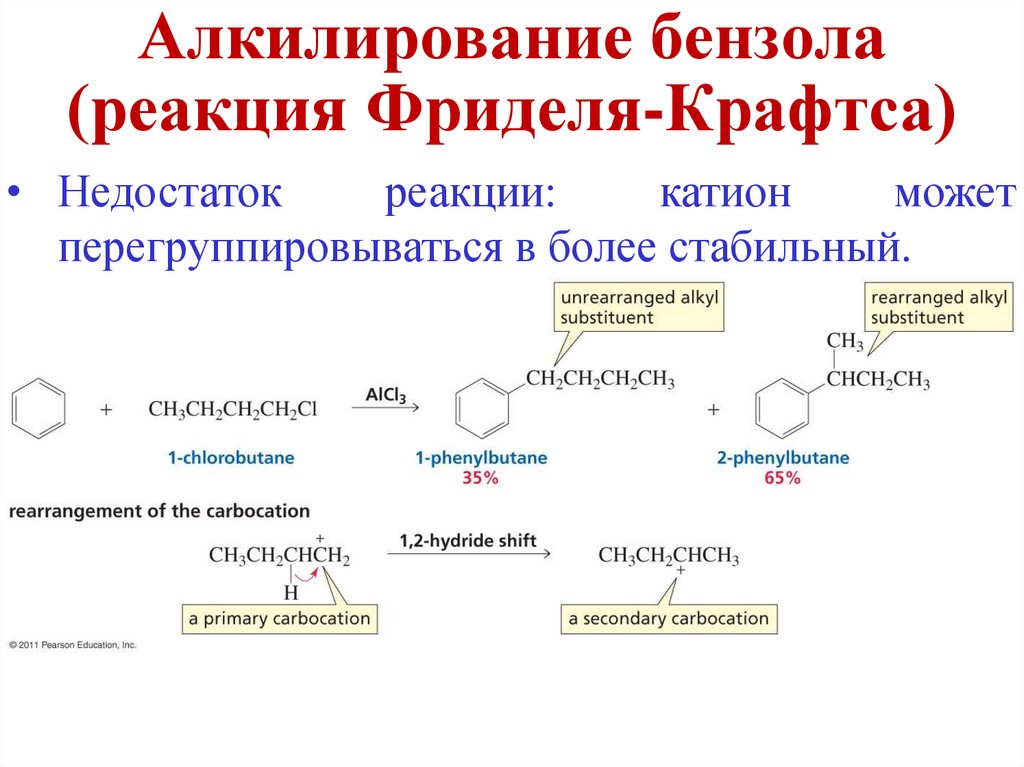
Алкилирование бензола(реакция Фриделя-Крафтса)
• Недостаток
реакции:
катион
может
перегруппировываться в более стабильный.
46.
Алкилирование бензола(реакция Фриделя-Крафтса)
• При
использовании
сильно
разветвлённых
галогеналканов преимущественно получается продукт
перегруппировки:
47.
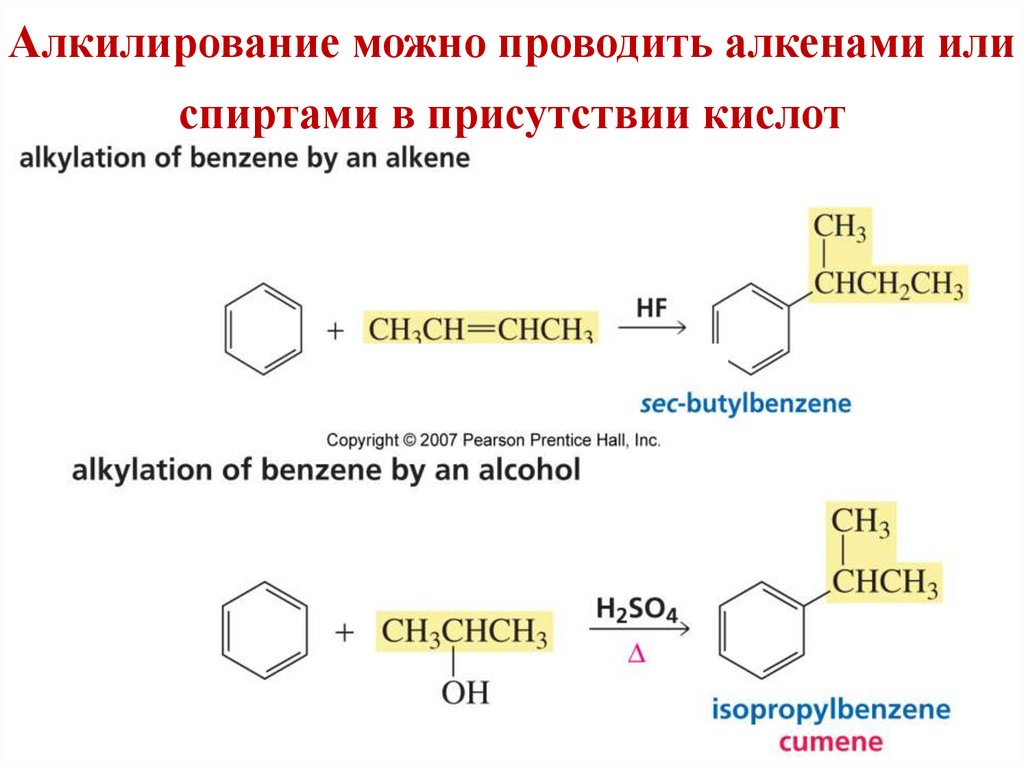
Алкилирование можно проводить алкенами илиспиртами в присутствии кислот
48.
Ограничения реакции алкилирования• Можно использовать только галогеналканы (F,Cl, I, Br).
Арилгалогениды и виниловые галогениды не реагируют (их
карбкатионы слишком нестабильны).
• Часто протекает полиалкилирование субстратов.
• Реакция не будет протекать с кольцами, содержащими
аминогруппу или сильную электроноакцепторную группу.
49.
Ацилирование по Фриделю-Крафтсу• Реакция хлорангидридов кислот (RCOCl) или ангидридов и
ароматического кольца в присутствии AlCl3 вводит ацильную
группу –COR.
• Электрофилом является ацилий-катион:
50.
Механизм реакции ацилирования• Аналогичен алкилированию.
• Электрофил: резонансно стабилизированный ацильный
катион.
• Ацильный катион не перегруппировывается!!
• Не протекает полизамещения, так как ацильная группа –
дезактивирует кольцо!!
51.
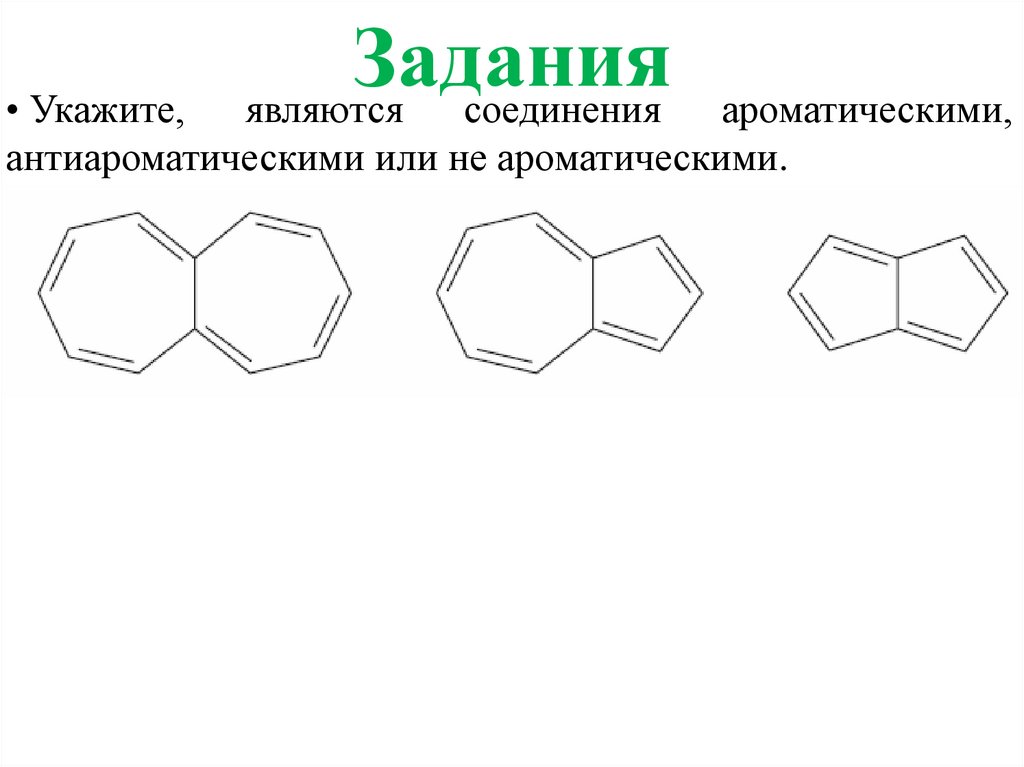
Заданияявляются
соединения
• Укажите,
ароматическими,
антиароматическими или не ароматическими.
52.
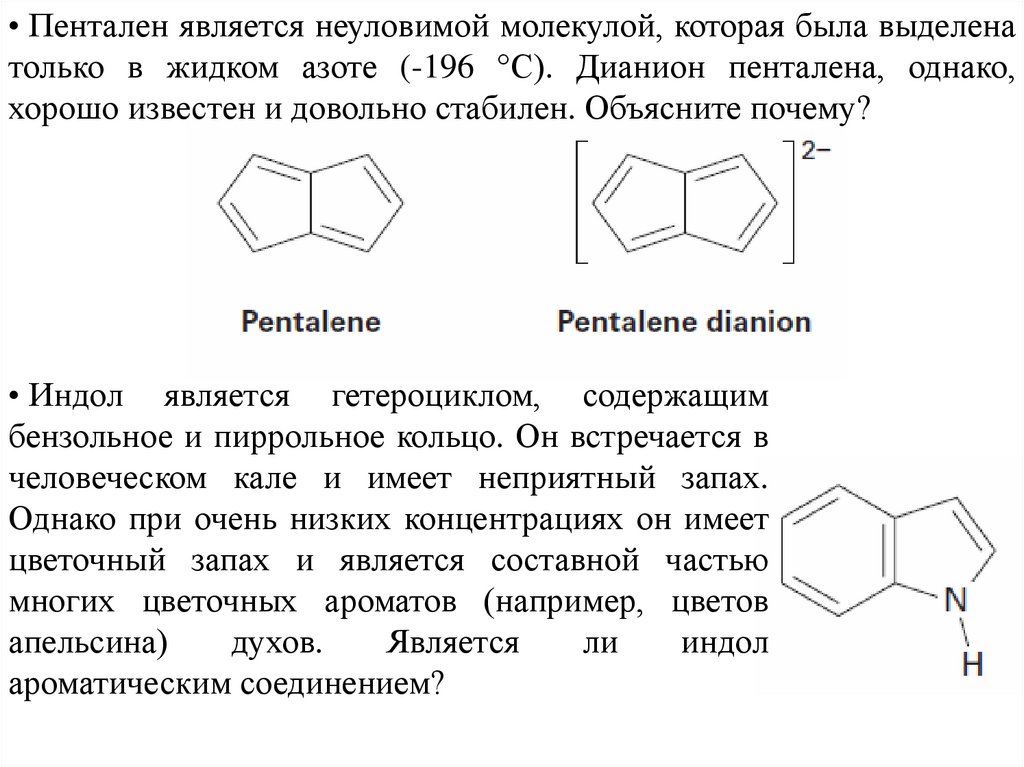
• Пентален является неуловимой молекулой, которая была выделенатолько в жидком азоте (-196 °С). Дианион пенталена, однако,
хорошо известен и довольно стабилен. Объясните почему?
• Индол является гетероциклом, содержащим
бензольное и пиррольное кольцо. Он встречается в
человеческом кале и имеет неприятный запах.
Однако при очень низких концентрациях он имеет
цветочный запах и является составной частью
многих цветочных ароматов (например, цветов
апельсина)
духов.
Является
ли
индол
ароматическим соединением?
53.
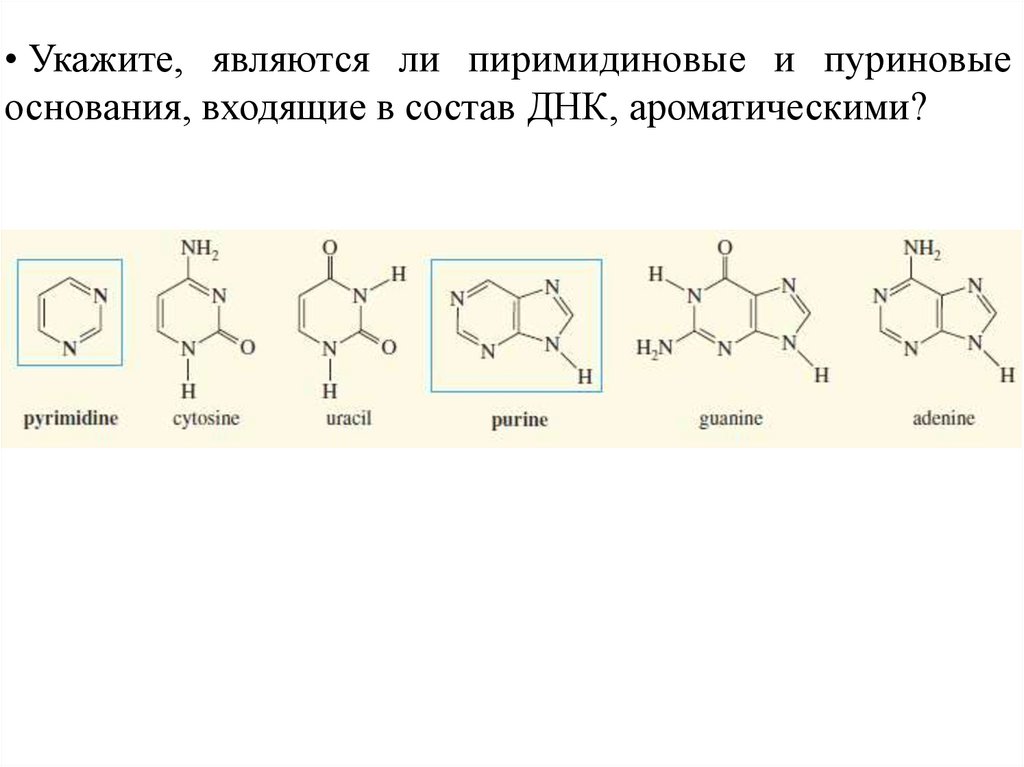
• Укажите, являются ли пиримидиновые и пуриновыеоснования, входящие в состав ДНК, ароматическими?
54.
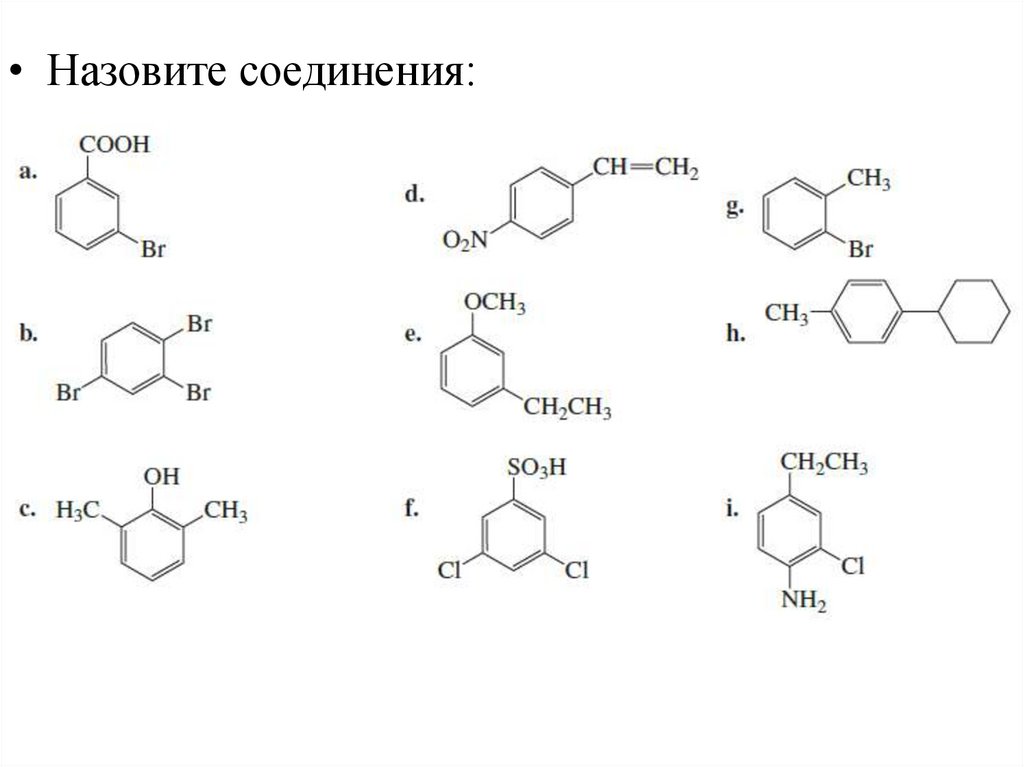
• Назовите соединения:55.
• Когда следующее соединение обрабатывают Br2 в присутствиикислоты Льюиса преобладает один продукт. Нарисуйте его
структуру.
56.
• Предскажите структуру продукта/продуктов мононитрования длянарисованных соединений:
• Предскажите
структуру
продукта
алкилирования
a)
изопропилбензола с помощью 3-хлор-2,2-диметилбутана и хлорида
алюминия (III), b) трет-бутилбензола с помощью 2-метилпропена и
HF.
57.
• Какое из соединений наименее активно в условия реакцииФриделя – Крафтса?
58.
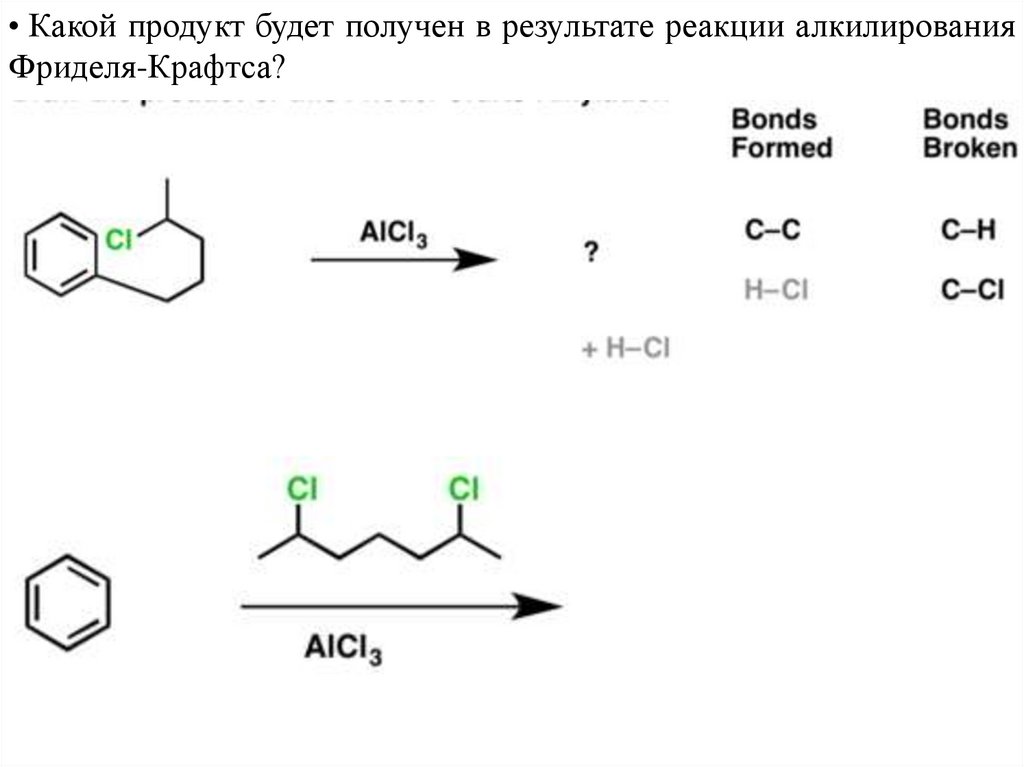
• Какой продукт будет получен в результате реакции алкилированияФриделя-Крафтса?
59.
• Напишите продукты реакций.60. Нитрование толуола
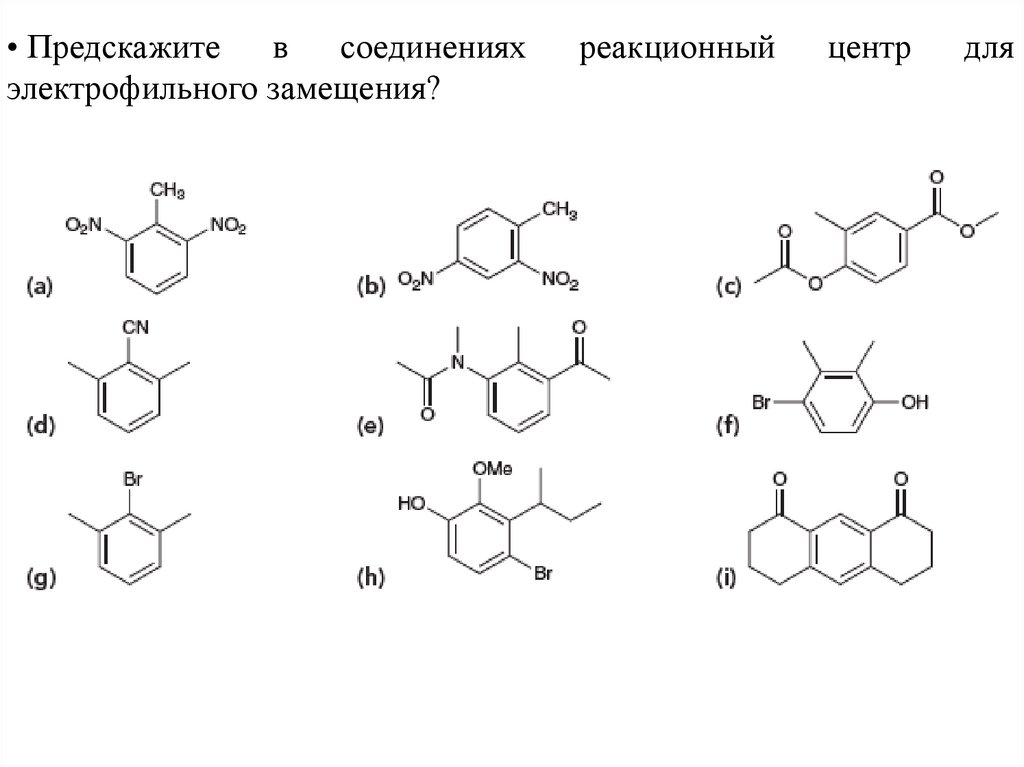
• Предскажитев
соединениях
электрофильного замещения?
реакционный
центр
для
61.
• Какова структура продукта реакций?62.
• Для каждой из следующих групп соединений определите, какиесоединение будет реагировать наиболее быстро с этилхлоридом в
присутствии трихлорида алюминия и предскажите ожидаемые
продукты реакции.
63. Аренониевый ион (σ-комплекс)
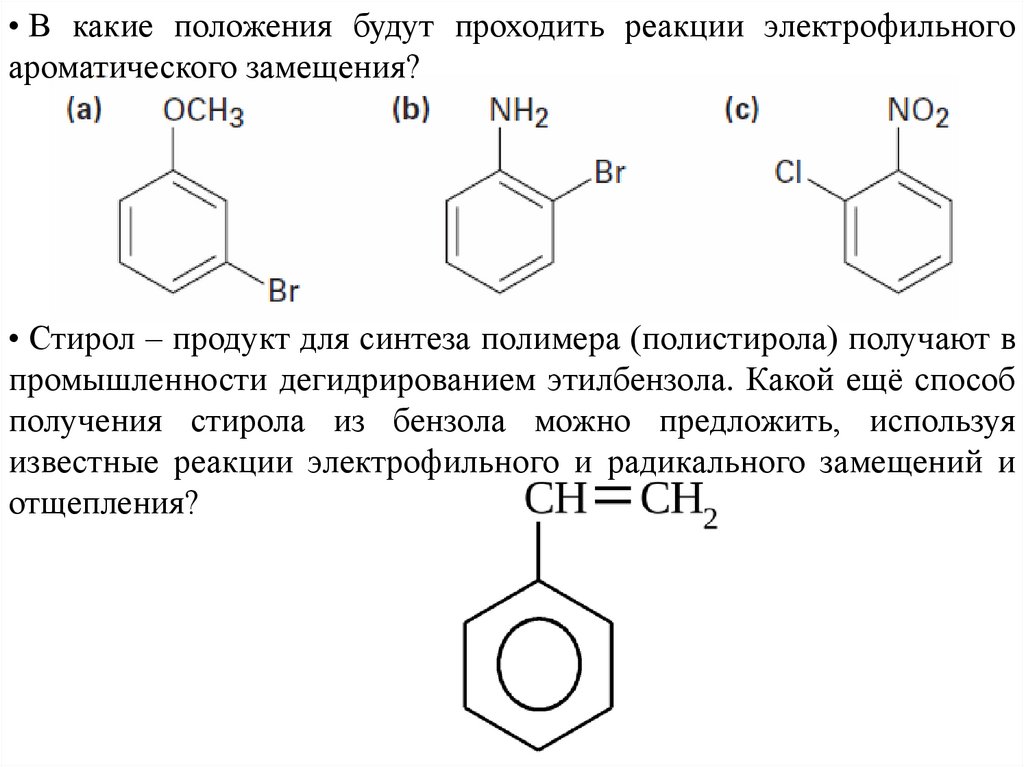
• В какие положения будут проходить реакции электрофильногоароматического замещения?
• Стирол – продукт для синтеза полимера (полистирола) получают в
промышленности дегидрированием этилбензола. Какой ещё способ
получения стирола из бензола можно предложить, используя
известные реакции электрофильного и радикального замещений и
отщепления?
64.
• 4-изопропилацетофенон используется в парфюмерии, имеетзапах фиалки. Предложите его синтез из бензола.
65.
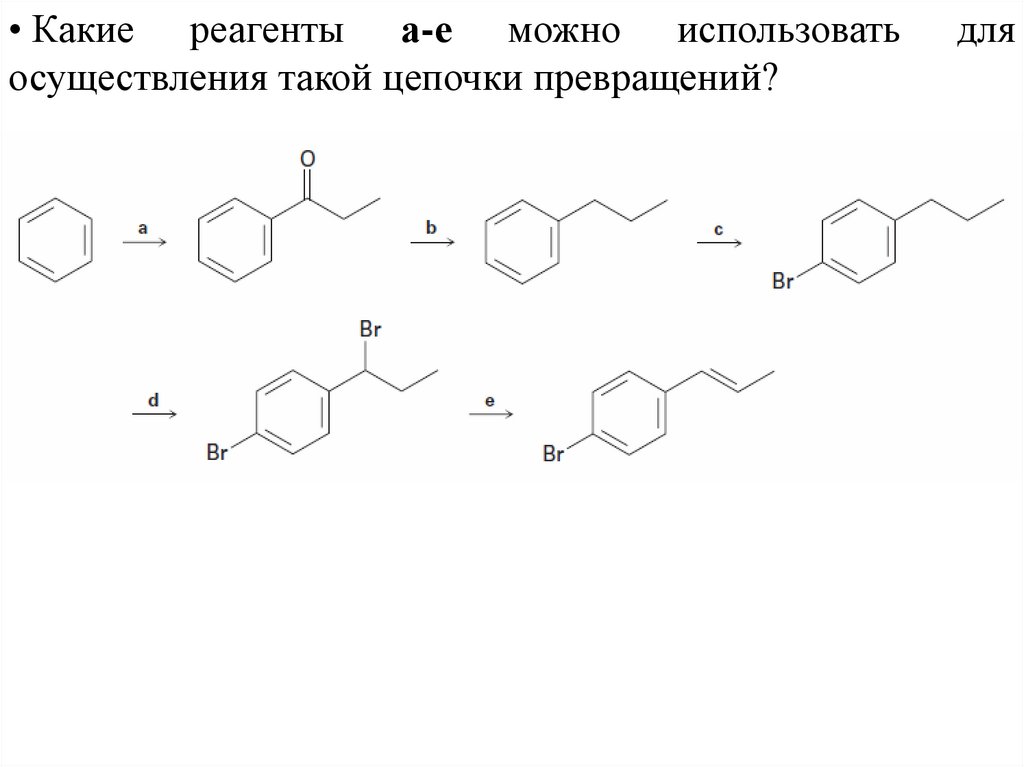
• Какие реагенты а-е можно использоватьосуществления такой цепочки превращений?
для























 Химия
Химия








