Похожие презентации:
Методы нейровизуализации при ишемических инсультах. Диагностическая значимость КТ, МРТ
1.
«Методы нейровизуализациипри ишемических инсультах.
Диагностическая значимость
КТ, МРТ»
Подготовила студентка 4 курса группы 1404
Стригун Виктория
2.
ИИ: АКТУАЛЬНОСТЬ• По данным Всемирной организации здравоохранения (ВОЗ), ежегодно
во всем мире от инсульта страдают 15 миллионов человек. Из них 5
миллионов умирают, а еще 5 миллионов остаются навсегда
нетрудоспособными.
• В РБ только в 2016 году диагноз «инсульт» был поставлен 32,5 тысячам
пациентов, около 30% из которых – люди трудоспособного возраста.
• Мужчины подвержены более высокому риску инсульта, чем
женщины; у белых мужчин частота инсультов составляет 62,8 на 100
000 человек, причем конечным результатом является смерть в 26,3%
случаев, в то время как у женщин частота инсультов составляет 59 на
100 000 человек, а уровень смертности - 39,2%.
• Хотя инсульт часто считается заболеванием пожилых людей, одна
треть инсультов происходит у лиц моложе 65 лет.
Ссылка на номер в литературе: 7
2
3.
НАРУШЕНИЯ МОЗГОВОГО КРОВООБРАЩЕНИЯВид НМК:
• А - начальные проявления недостаточности мозгового кровообращения;
• Б - преходящие нарушения мозгового кровообращения: (ПНМК), транзиторные
ишемические атаки (ТИА), гипертонические кризы, острые гипертонические энцефалопатии;
• В - инсульты: субарахноидальные кровоизлияния, внутримозговые кровоизлияния
(=геморрагические инсульты), инфаркты мозга = ишемические инсульты (тромботические,
кардиоэмболические, гемодинамические, гемореологические, лакунарные или малые
ишемические инсульты); последствия ОНМК (до 3 лет после возникновения инсульта), и
отдаленные последствия (после 3 лет НМК);
• Г - прогрессирующие НМК: хронические субдуральные гематомы и дисциркуляторные
энцефалопатии.
Инсульт – острое нарушение мозгового кровообращения, характеризующееся внезапным (в
течение нескольких минут, часов) появлением очаговой (двигательных, речевых,
чувствительных, координаторных, зрительных и других нарушений) и/или общемозговой
(изменения сознания, головная боль, рвота) неврологической симптоматики, которая
сохраняется более 24 часов или приводит к смерти больного в более короткий промежуток
времени вследствие цереброваскулярной патологии.
Кафедра
3
4.
МКБМКБ-10: I63 — Инфаркт мозга
Диагноз с кодом I63 включает 9 уточняющих диагнозов (подрубрик МКБ-10):
I63.0 — Инфаркт мозга, вызванный тромбозом прецеребральных артерий
I63.1 — Инфаркт мозга, вызванный эмболией прецеребральных артерий
I63.2 — Инфаркт мозга, вызванный неуточненной закупоркой или стенозом
прецеребральных артерий
I63.3 — Инфаркт мозга, вызванный тромбозом мозговых артерий
I63.4 — Инфаркт мозга, вызванный эмболией мозговых артерий
I63.5 — Инфаркт мозга, вызванный неуточненной закупоркой или стенозом
мозговых артерий
I63.6 — Инфаркт мозга, вызванный тромбозом вен мозга, непиогенный
I63.8 — Другой инфаркт мозга
I63.9 — Инфаркт мозга неуточненный
4
5.
ЭТИОЛОГИЯ церебральных инсультовИшемический (ИИ) – 80%
Геморрагический
= инфаркт мозга
• АГ
• Васкулиты
• Врожденные сосудистые аномалии
(аневризмы и артериовенозные
мальформации сосудов ГМ)
• Нарушения свертываемости крови
(гемофилия, передозировка антикоагулянтов,
тромболитиков, тромбоцитопения, лейкоз)
• Атеросклероз
• Тромбообразование
• Стеноз прецеребральных (чаще всего
при стенозе сонных артерий) и (или)
церебральных артерий
• Болезни сердца – кардиогенная
эмболия (мерцательная аритмия,
инфекционный эндокардит)
• Редкая сосудистая патология: болезнь
Такаясу, Мойамойа, инфекционные
артерииты и др.
• Системные факторы: АГ, аритмии,
гематологические нарушения и др.
3, 5
5
6.
ИИ: КЛАССИФИКАЦИЯ• Классификация:
атеротромботический
кардиоэмболический
лакунарный (окклюзия малой артерии)
острый инсульт с иной, определенной этиологией
(гемодинамический/гемореологический)
инсульт неустановленнной этиологии (криптогенный)
• Диагностическая визуализация играет важную роль, так как ишемический или
геморрагический инсульт не могут быть распознаны клинически (а также около
30% случаев, подобных инсульту, имеют не сосудистую причину).
• Один инфаркт на сосудистой территории с большей вероятностью может быть
атеротромботическим, чем множественные инфаркты, которые с большей
вероятностью являются эмболическими.
1, 4, 5
6
7.
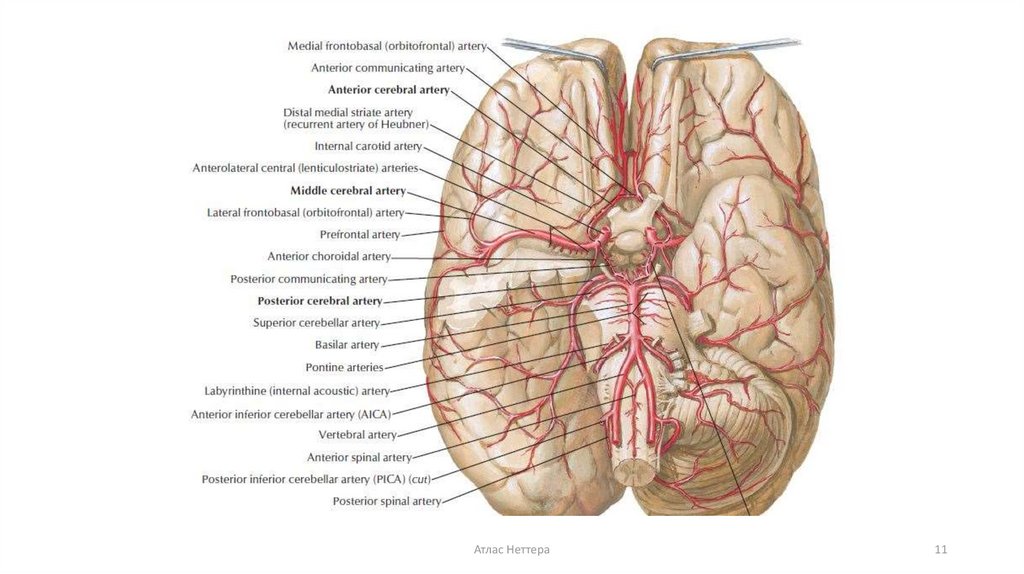
Атлас Неттера7
8.
ИИ: КЛАССИФИКАЦИЯFor the purposes of this article the following
definitions are used:
• early hyperacute: 0 to 6 hours
• late hyperacute: 6 to 24 hours
• acute: 24 hours to 1 week
• subacute: 1 to 3 weeks
• chronic: more 3 weeks
В клиническом течении инсульта выделяют
следующие периоды (А. А. Бова):
1) 1–3-и сутки –острейший период;
2) до 28 суток (4 недели) – острый период;
3) до 6 месяцев – ранний восстановительный
период;
4) до 2-х лет – поздний восстановительный период;
5) после 2-х лет - период остаточных явлений.
1, 6, 11
The vascular territory affected will determine exact
symptoms and clinical behaviour of the lesion:
anterior circulation infarct
• anterior cerebral artery infarct (АСА)
• middle cerebral artery infarct (МСА)
• lacunar infarct
• striatocapsular infarct
posterior circulation infarct
• posterior cerebral artery infarct (РСА)
• cerebellar infarct
• brainstem infarct:
• midbrain infarct
• pontine infarct
• medullary infarct
8
9.
ИИ: КЛАССИФИКАЦИЯПо локализации:
• В системе внутренней сонной артерии (ВСА): кора лобной, теменной, височной
долей, подкорковое белое вещество, внутренняя капсула.
• В бассейне передней мозговой артерии (ПМА): поверхностные ветви - медиальная
поверхность лобной и теменной долей, парацентральная долька, частично
глазничная часть лобной доли, наружная поверхность верхней лобной извилины,
передние 2/3 мозолистого тела; глубокие – переднее бедро внутренней капсулы,
скорлупа, бледный шар, частично гипоталамическая область.
• В бассейне средней мозговой артерии (СМА) часто!: большая часть подкорковых
узлов и внутренней капсулы, кора височной и теменной долей.
• В вертебро-базилярной система (ВБС): ствол мозга, лабиринт, мозжечок,
затылочные доли, медиобазальные отделы височных долей.
• В бассейне задней мозговой артерии (ЗМА): затылочная доля, задняя 1/3 таламуса
и гипоталамической области, лучистость Грациоле, медиобазальные отделы
височной доли, задняя 1/3 мозолистого тела.
5
9
10.
Table 1. Vascular Supply to the BrainVASCULAR TERRITORY
Structures Supplied
Anterior Circulation (Carotid)
Anterior Cerebral Artery
Cortical branches: medial frontal and parietal lobe
Medial lenticulostriate branches: caudate head, globus pallidus, anterior
limb of internal capsule
Middle Cerebral Artery
Cortical branches: lateral frontal and parietal lobes, lateral and anterior
temporal lobe
Lateral lenticulostriate branches: globus pallidus and putamen, internal
capsule
Anterior Choroidal Artery
Optic tracts, medial temporal lobe, ventrolateral thalamus, corona radiata,
posterior limb of the internal capsule
Posterior Circulation (Vertebrobasilar)
Posterior Cerebral Artery
Cortical branches: occipital lobes, medial and posterior temporal and
parietal lobes
Perforating branches: brainstem, posterior thalamus and midbrain
Posterior Inferior Cerebellar Artery
Inferior vermis; posterior and inferior cerebellar hemispheres
Anterior Inferior Cerebellar Artery
Anterolateral cerebellum
Superior Cerebellar Artery
Superior vermis; superior cerebellum
7
10
11.
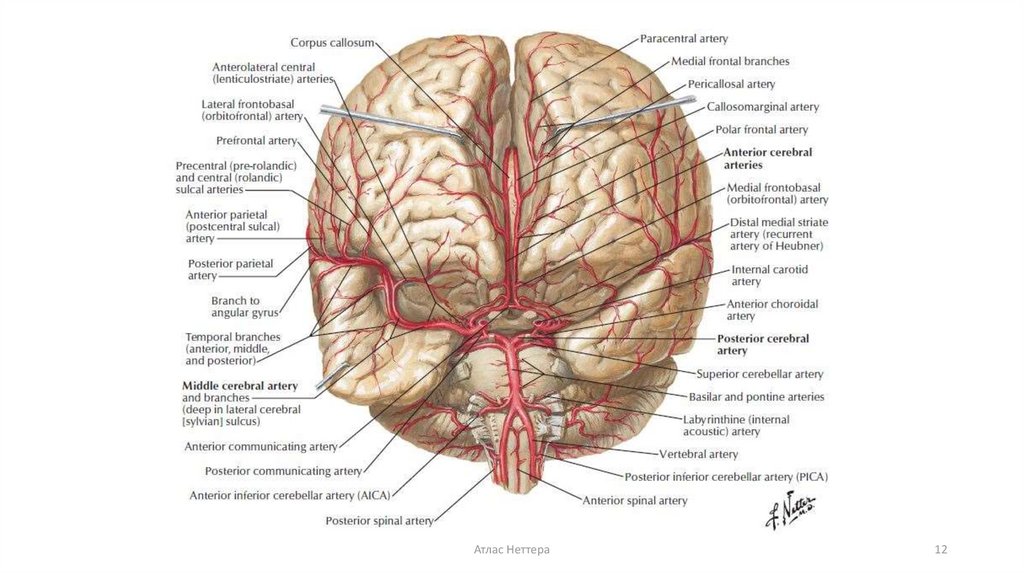
Атлас Неттера11
12.
Атлас Неттера12
13.
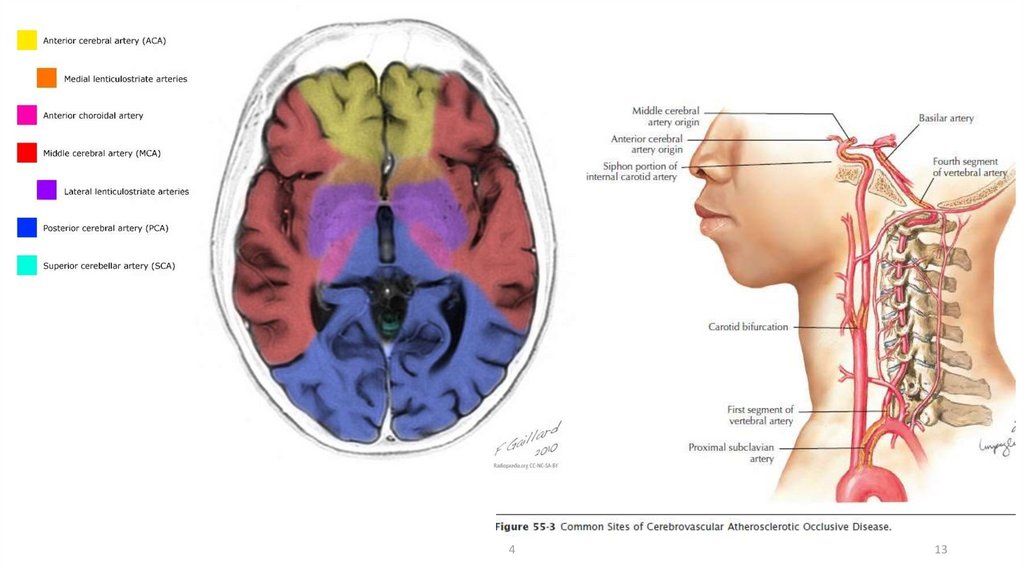
413
14.
Атлас Неттера14
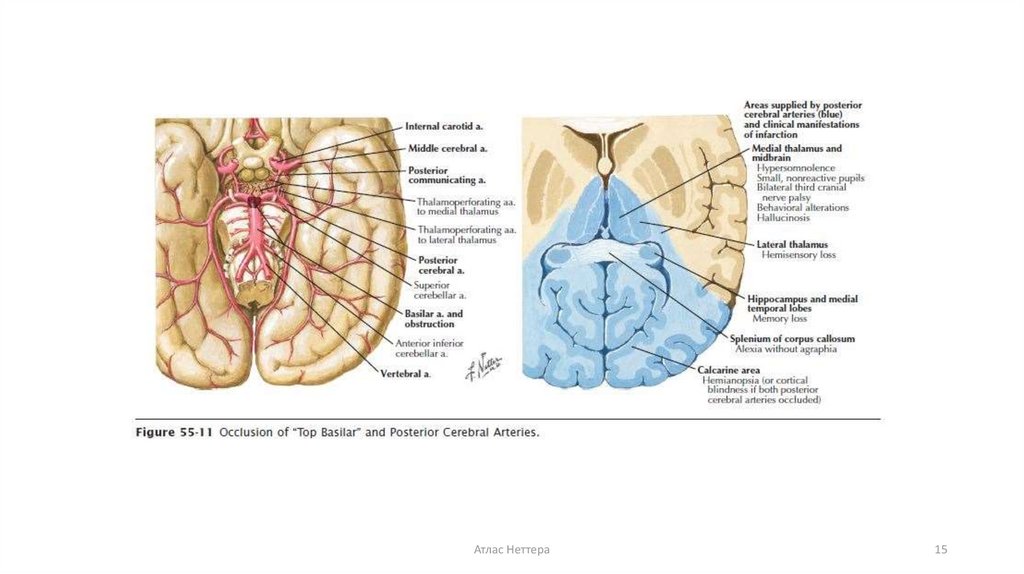
15.
Атлас Неттера15
16.
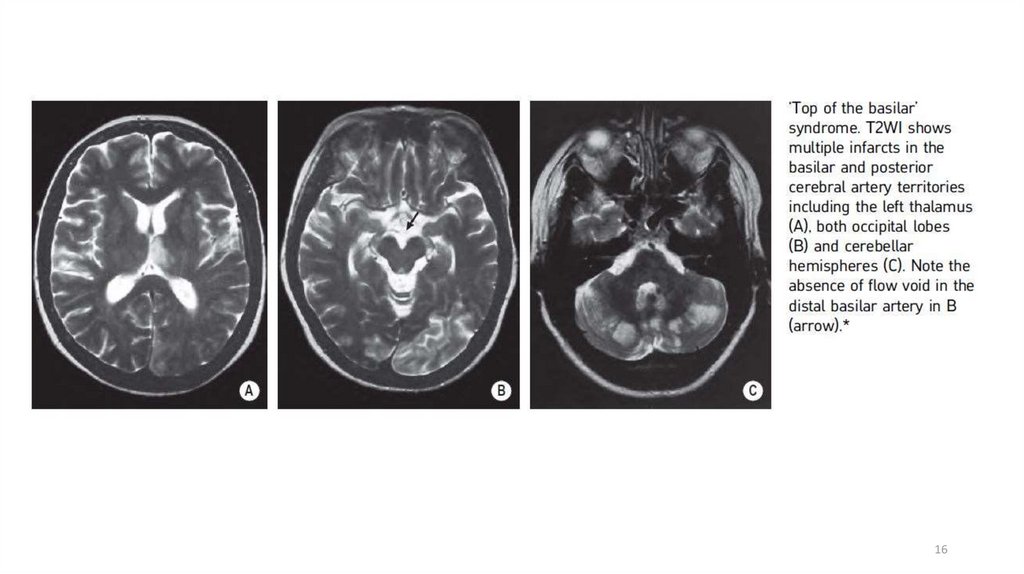
1617.
Атлас Неттера17
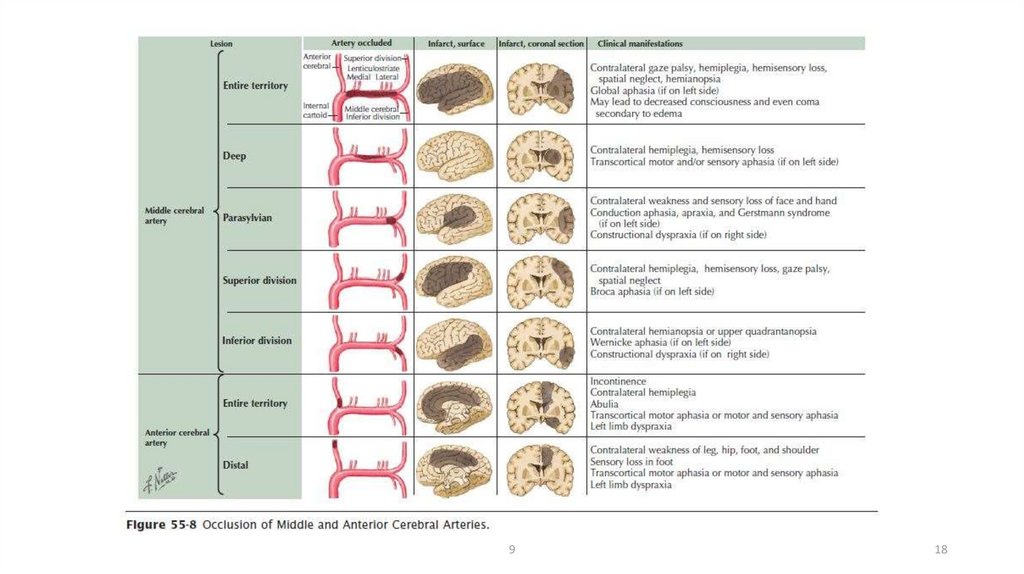
18.
918
19.
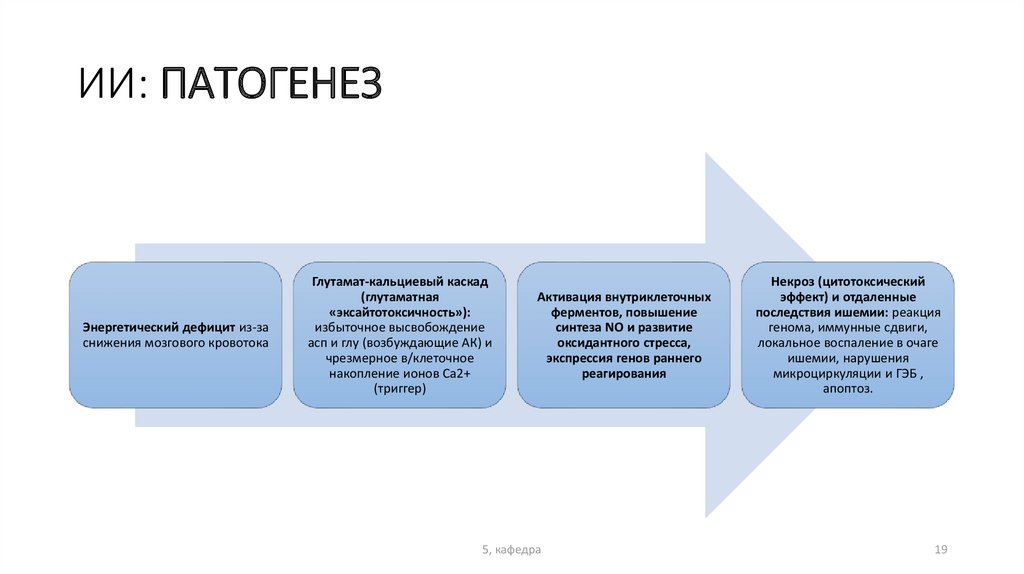
ИИ: ПАТОГЕНЕЗЭнергетический дефицит из-за
снижения мозгового кровотока
Глутамат-кальциевый каскад
(глутаматная
«эксайтотоксичность»):
избыточное высвобождение
асп и глу (возбуждающие АК) и
чрезмерное в/клеточное
накопление ионов Са2+
(триггер)
Активация внутриклеточных
ферментов, повышение
синтеза NO и развитие
оксидантного стресса,
экспрессия генов раннего
реагирования
5, кафедра
Некроз (цитотоксический
эффект) и отдаленные
последствия ишемии: реакция
генома, иммунные сдвиги,
локальное воспаление в очаге
ишемии, нарушения
микроциркуляции и ГЭБ ,
апоптоз.
19
20.
ИИ: ПАТОФИЗИОЛОГИЯ• Нейрональная ишемия быстро истощает внутриклеточный аденозинтрифосфат
(АТФ), что приводит к нарушению мембраносвязанных АТФ-зависимых ионных
каналов, ответственных за нейрональные покоящиеся мембранные потенциалы и
генерацию потенциалов действия. Эта метаболическое нарушение приводит к
накоплению внутриклеточных ионов (включая ионы кальция), создавая
внутриклеточный градиент, ответственный за внутриклеточное накопление воды
(то есть цитотоксический отек).
• Эндотелиальные клетки головного мозга более устойчивы к ишемии, чем нейроны
и нейроглиальные клетки. Приблизительно через 3-4 часа после начала ишемии
целостность гематоэнцефалического барьера нарушается, и белки плазмы могут
проникать во внеклеточное пространство. Внутрисосудистая вода поступает в ткани,
когда происходит реперфузия (вазогенный отек); этот процесс начинается через 6
часов после начала инсульта и достигает максимума через 2-4 дня после начала
инсульта. Реперфузия также может сопровождаться геморрагической
трансформацией инфаркта, которая обычно связана с объемом и локализацией
инфаркта, чаще встречаясь у крупных корковых инфарктов.
4
20
21.
ИИ:ПАТОФИЗИОЛОГИЯ
• Ядерная зона («сердцевина» инфаркта): ее формирование завершается через 5-8
мин с момента ОНМК. Сerebral blood flow of lower than 10 mL/100 g of tissue/min.
• «Ишемическая полутень» (пенумбра): область мозга окружающая ядерную зону,
это потенциально жизнеспособная зона в которой снижен кровоток, но в целом
сохранен энергетический метаболизм и присутствуют функциональные, а не
структурные изменения. Сerebral blood flow < 25 mL/100g of tissue/min.
• Формирование 50% окончательного V инфаркта происходит в течение первых 90
мин (1,5 часа) с момента развития инсульта, 80% - в течение 360 мин (6 часов), т.е.
первые 3-6 часов – «терапевтическое окно» - спасение пенумбры!
5, 7
21
22.
ИИ: Лакунарные инсульты• Лакунарные инсульты составляют 13–20% всех ишемических инсультов. Это
небольшие глубокие церебральные инфаркты – рез-т окклюзии проникающих
ветвей MCA (СМА), лентикулостриатных артерий или проникающих ветвей
Виллизиева круга (Willis' circle), позвоночной артерии или основной артерии.
• Общие места для этих поражений включают базальные ганглии, внутреннюю
капсулу, таламус, ствол мозга и мозжечок.
• Размеры не превышают 1,5 см.
• Подавляющее большинство лакунарных инсультов связано с гипертонической
ангиопатией церебральных артерий (плазморрагии, фибриноидный некроз,
облитерирующий гиалиноз, тромбоз): дисфункция эндотелия/нарушение
гемореологии, гемостаза, фибринолиза – кризовое повышение АД – острая
окклюзия интрацеребральной артерии – очаговая ишемия мозга.
• Causes of lacunar infarcts include the following: Microatheroma, Lipohyalinosis, Fibrinoid
necrosis secondary to hypertension or vasculitis, Hyaline arteriosclerosis, Amyloid
angiopathy, Microemboli.
4, 7, кафедра
22
23.
КТ (компьютерная томография)• РКТ (СТ) - рентгенологическое исследование, при котором
изображение слоя исследуемого объекта получают путем
компьютерной обработки результатов его просвечивания
рентгеновским лучом при движении рентгеновской трубки по
окружности.
• Проходя через тело пациента, рентгеновское излучение ослабляется
соответственно плотности и атомному составу исследуемых тканей.
При этом пучок рентгеновских лучей фиксируется специальной
системой детекторов, которые преобразуют энергию излучения в
электрические сигналы (по принципу цифровой рентгенологии).
• ГИПЕРДЕНСИВНЫЙ/ГИПОДЕНСИВНЫЙ
• non-enhanced computed tomography = NECT
8
23
24.
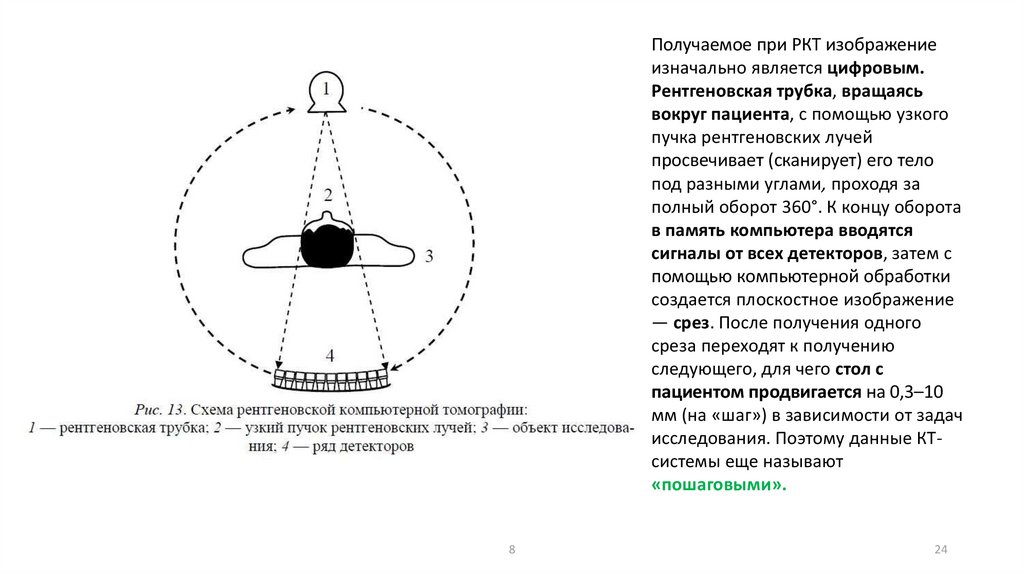
Получаемое при РКТ изображениеизначально является цифровым.
Рентгеновская трубка, вращаясь
вокруг пациента, с помощью узкого
пучка рентгеновских лучей
просвечивает (сканирует) его тело
под разными углами, проходя за
полный оборот 360°. К концу оборота
в память компьютера вводятся
сигналы от всех детекторов, затем с
помощью компьютерной обработки
создается плоскостное изображение
— срез. После получения одного
среза переходят к получению
следующего, для чего стол с
пациентом продвигается на 0,3–10
мм (на «шаг») в зависимости от задач
исследования. Поэтому данные КТсистемы еще называют
«пошаговыми».
8
24
25.
КТ• Участки среза, которые ослабляют рентгеновское излучение, выглядят
светлыми, а пропускающие рентгеновские лучи — темными (по
принципу обычной рентгенографии).
• Но особенно важным является получение количественной
характеристики плотности тканей, которая измеряется в условных
единицах — единицах Хаунсфилда (HU). За нулевую отметку
принимается плотность воды — 0 HU, плотность воздуха составляет –
1000 UH, плотность костной ткани — +1000 HU. Остальные ткани
человеческого тела принимают промежуточные значения. Поскольку
все зоны плотности нельзя одновременно отобразить на дисплее, во
время исследования врач выбирает определенный диапазон по шкале
Хаунсфилда, так называемое «окно». Выбирается «окно» в
зависимости от планируемой зоны осмотра и предполагаемой
патологии.
8
25
26.
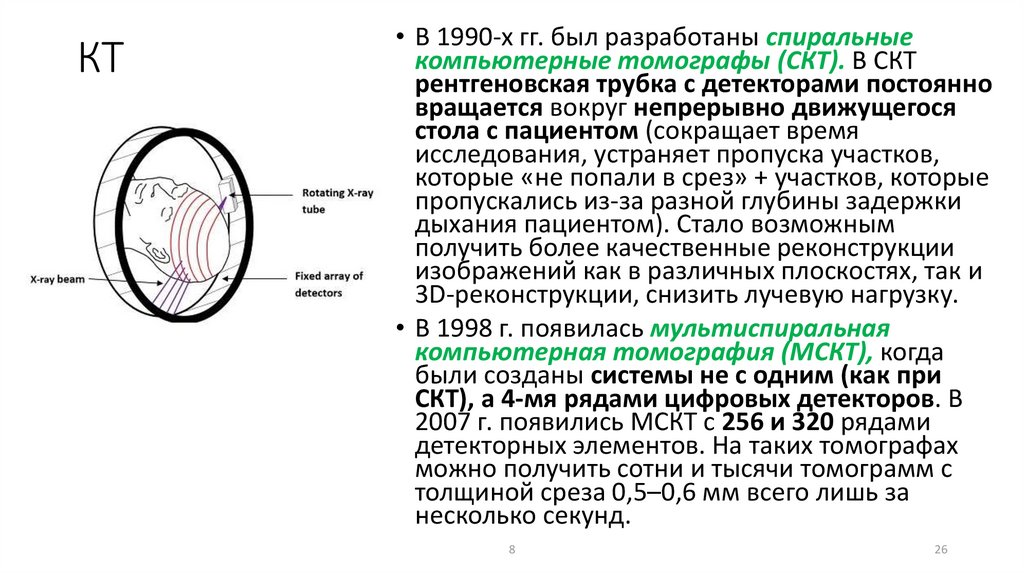
КТ• В 1990-х гг. был разработаны спиральные
компьютерные томографы (СКТ). В СКТ
рентгеновская трубка с детекторами постоянно
вращается вокруг непрерывно движущегося
стола с пациентом (сокращает время
исследования, устраняет пропуска участков,
которые «не попали в срез» + участков, которые
пропускались из-за разной глубины задержки
дыхания пациентом). Стало возможным
получить более качественные реконструкции
изображений как в различных плоскостях, так и
3D-реконструкции, снизить лучевую нагрузку.
• В 1998 г. появилась мультиспиральная
компьютерная томография (МСКТ), когда
были созданы системы не с одним (как при
СКТ), а 4-мя рядами цифровых детекторов. В
2007 г. появились МСКТ с 256 и 320 рядами
детекторных элементов. На таких томографах
можно получить сотни и тысячи томограмм с
толщиной среза 0,5–0,6 мм всего лишь за
несколько секунд.
8
26
27.
Атлас Неттера27
28.
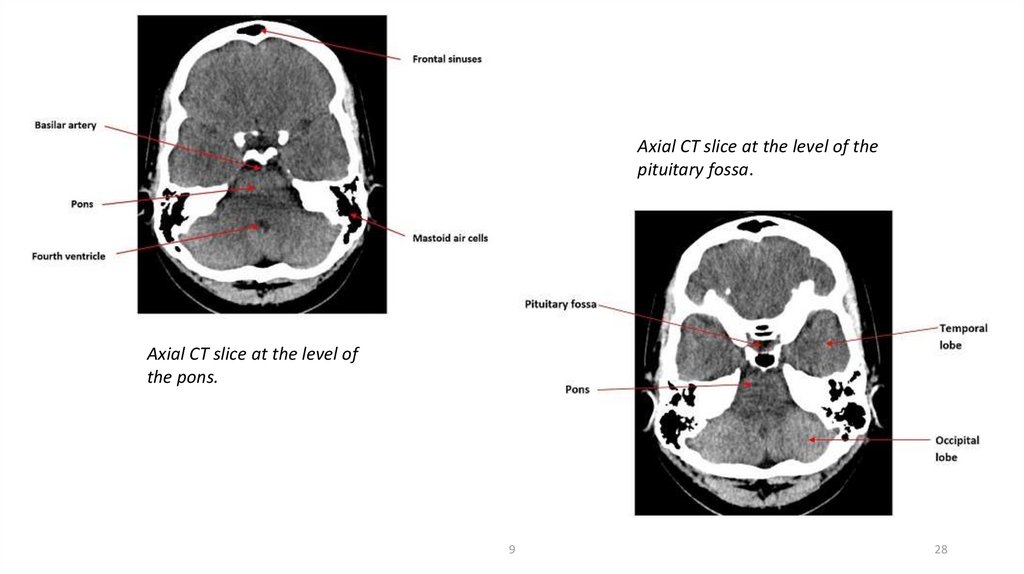
Axial CT slice at the level of thepituitary fossa.
Axial CT slice at the level of
the pons.
9
28
29.
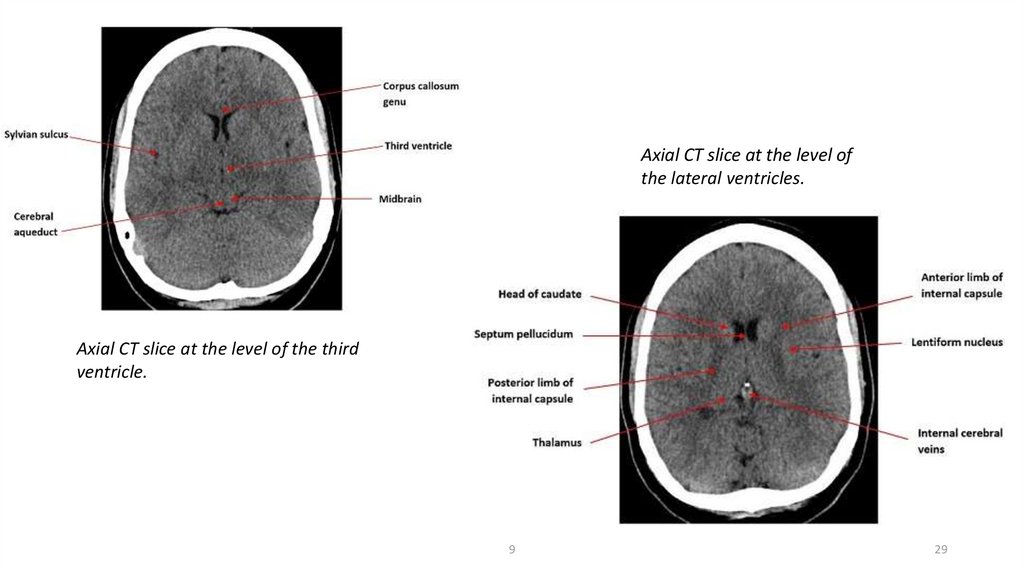
Axial CT slice at the level ofthe lateral ventricles.
Axial CT slice at the level of the third
ventricle.
9
29
30.
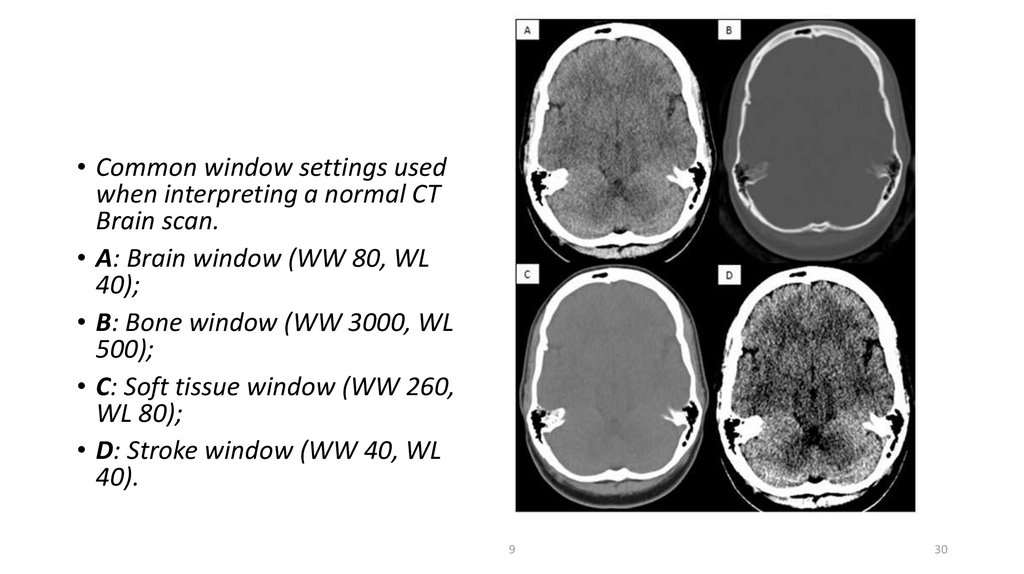
• Common window settings usedwhen interpreting a normal CT
Brain scan.
• A: Brain window (WW 80, WL
40);
• B: Bone window (WW 3000, WL
500);
• C: Soft tissue window (WW 260,
WL 80);
• D: Stroke window (WW 40, WL
40).
9
30
31.
КТ (NECT)/ИШЕМИЧЕСКИЙ ИНСУЛЬТ• Международный стандарт при постановке диагноза ОНМК.
• Частота выявления зоны поражения методом КТ зависит от длительности промежутка времени
между клиническим дебютом инсульта и КТ-исследованием, а также от характера поражения
(наличие геморрагической трансформации), величины и локализации инфаркта.
• Выявляет зоны ишемии не менее 2 часов после начала гипоперузии. Повтор исследования (или
МРТ) через 24 часа, если первое изменений не выявило. Наличие выраженной неврологической
клиники и отсутствие изменений при КТ (в первые 3-6 часов) указывают на ишемическое
повреждение. К исходу первых суток ишемические очаги обычно становятся видимыми на КТ. Это
обусловлено физическими свойствами рентгеновского излучения, не позволяющего отобразить
фокальный цитотоксический отек мозга, слабо отличающийся по плотностным характеристикам от
неизмененного вещества головного мозга в первые минуты и часы развития ИИ.
• Цели КТ в острой обстановке:
исключить внутричерепное кровоизлияние, которое исключает тромболизис.
искать какие-либо "ранние" признаки ишемии.
исключить другие внутричерепные патологии, которые могут имитировать инсульт, такие как
опухоль.
5, 6
31
32.
КТ/ИИ• Полушарная локализация с вовлечением коры: изменения могут выявляться через
3 ч от начала заболевания, к концу первых суток – частота визуализации КТизменений 60 %, к 7-ому дню – 100 % всех выявляемых при данном исследовании
ИМ.
• Ишемические повреждения мозга в структурах ЗЧЯ при КТ выявляются хуже по
сравнению с полушарной локализацией данных изменений (из-за небольшого
объема поражений и наличия артефактов при КТ-сканировании данной области).
• Наиболее ранним КТ-признаком ишемического повреждения с системе СМА
является отсутствие визуализации чечевицеобразного ядра или коры островка в
связи с развитием в зоне поражения цитотоксического отека.
• При больших полушарных инфарктах в течение первых часов инсульта еще до
появления гиподенсивных изменений в веществе мозга выявляется локальный
объемный эффект (масс-эффект) в виде сужения корковых борозд в зоне
поражения и сдавления бокового желудочка на стороне поражения. Аналогичные
изменения могут наблюдаться при больших инфарктах мозжечка.
5
32
33.
КТ/ИИ• В остром периоде: доминирующий тип тканевых изменений в зоне
ишемического повреждения - цитотоксический отек, к которому обычно
присоединяется и вазогенный отек при поражении МЦР.
• Первая неделя заболевания - равномерно гиподенсивный участок,
оказывающий объемный эффект на окружающие структуры мозга. В
большинстве случаев данный участок соответствует определенному
сосудистому бассейну и имеет клиновидную форму с основанием наружу.
• В ряде случаев в качестве ранних изменений выявляется гиперденсивность
участков средней, реже – задней мозговой артерий на стороне поражения,
что свидетельствует о наличии тромбоза или эмболии данных сосудов - КТангиография + КТ-перфузия.
• Могут выявляться различные сосудистые изменения, потенциально
способные вызывать ишемические повреждения мозга: кальцификаты в
атеросклеротических бляшках в стенках артерий, извитость и расширение
сосудов, церебральные сосудистые мальформации.
5
33
34.
КТ/ИИ• Начиная с конца первой недели: повышение плотности до изоденсивного, а иногда и
слабогиперденсивного состояния, что связано с развитием реактивного неовазогенеза и
восстановлением иногда избыточного кровотока. Данный феномен определяется как
эффект «затуманивания», он затрудняет выявление истинных границ зоны ишемического
повреждения.
• В течение второй недели: обычно регрессирует положительный эффект объемного
воздействия, позже начинает проявляться эффект утраты вещества мозга.
• Через 1,5 – 2 месяцев: выявляются гиподенсивные изменения, соответствующие
формирующейся постинфарктной кисте.
• При КТ хорошо выявляется геморрагическая трансформация в зоне острого ишемического
повреждения, которая может быть по типу пропитывания кровью вещества мозга или в
виде формирования кровоизлияния. Соответственно наблюдаются умеренно выраженные
или выраженные гиперденсивные изменения в зонах геморрагической трансформации
(диагностика такой трансформации по типу пропитывания – сложная задача по сравнению с
диагностикой внутримозговой гематомы: отсутствие однородности показателей тканевой
плотности в зоне кровоизлияния, которая располагается внутри или по краю зоны
пониженной плотности, соответствующей инфаркту).
5
34
35.
Noncontrast computed tomography(CT) scan in a 52-year-old man with a
history of worsening right-sided
weakness and aphasia demonstrates
diffuse hypodensity and sulcal
effacement with mass effect involving
the left anterior and middle cerebral
artery territories consistent with acute
infarction. There are scattered
curvilinear areas of hyperdensity noted
suggestive of developing petechial
hemorrhage in this large area of
infarction.
7
35
36.
3637.
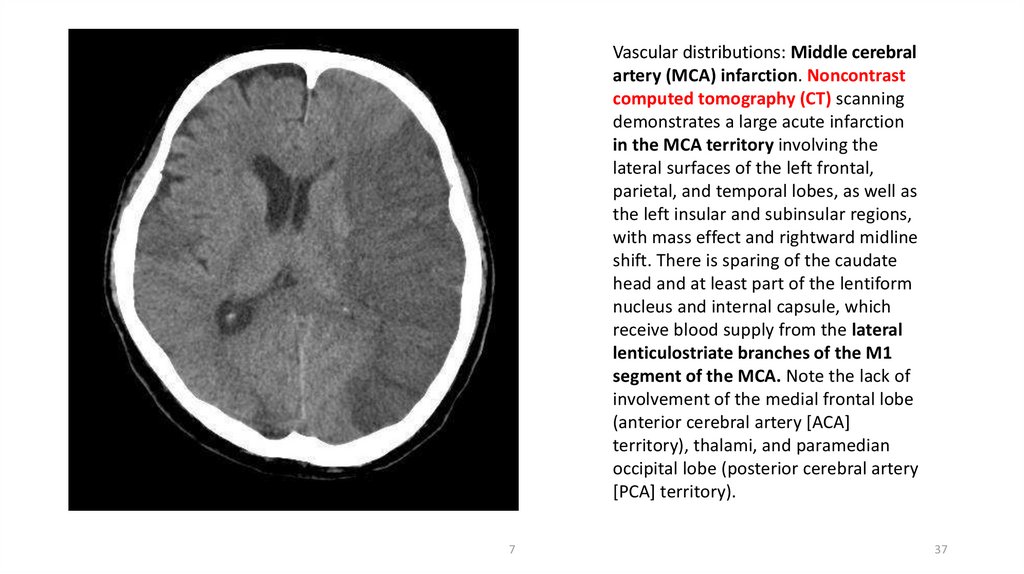
Vascular distributions: Middle cerebralartery (MCA) infarction. Noncontrast
computed tomography (CT) scanning
demonstrates a large acute infarction
in the MCA territory involving the
lateral surfaces of the left frontal,
parietal, and temporal lobes, as well as
the left insular and subinsular regions,
with mass effect and rightward midline
shift. There is sparing of the caudate
head and at least part of the lentiform
nucleus and internal capsule, which
receive blood supply from the lateral
lenticulostriate branches of the M1
segment of the MCA. Note the lack of
involvement of the medial frontal lobe
(anterior cerebral artery [ACA]
territory), thalami, and paramedian
occipital lobe (posterior cerebral artery
[PCA] territory).
7
37
38.
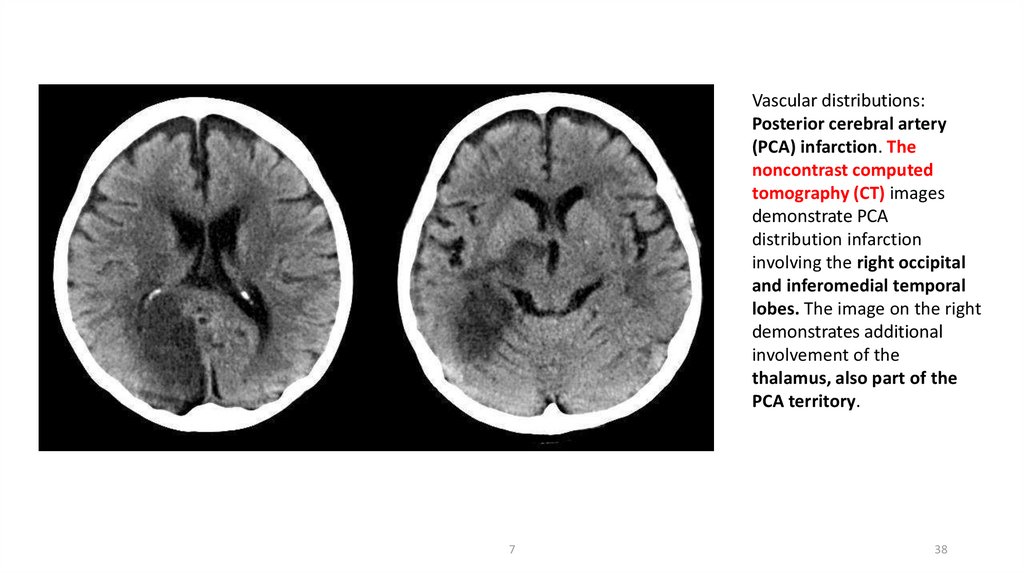
Vascular distributions:Posterior cerebral artery
(PCA) infarction. The
noncontrast computed
tomography (CT) images
demonstrate PCA
distribution infarction
involving the right occipital
and inferomedial temporal
lobes. The image on the right
demonstrates additional
involvement of the
thalamus, also part of the
PCA territory.
7
38
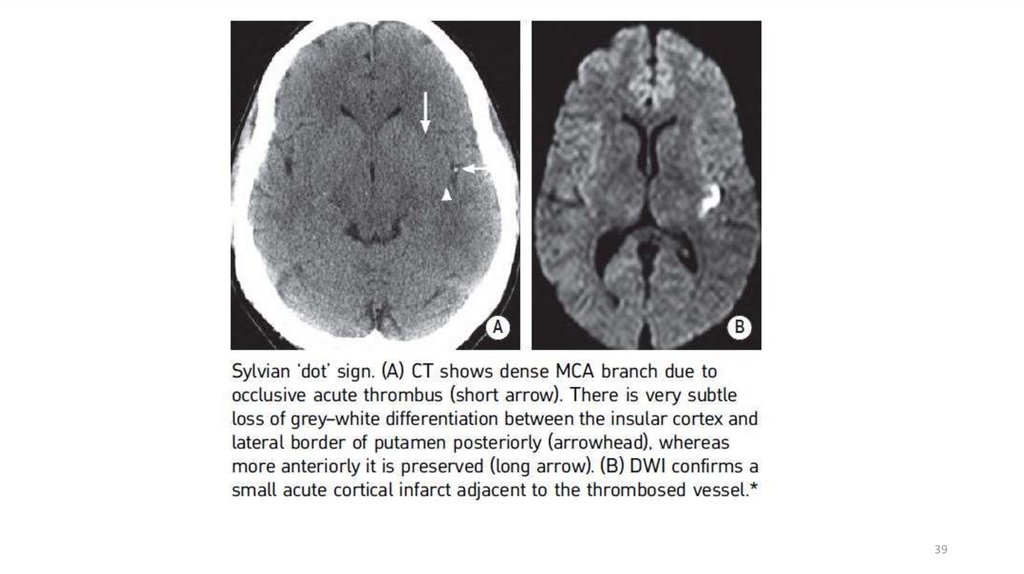
39.
3940.
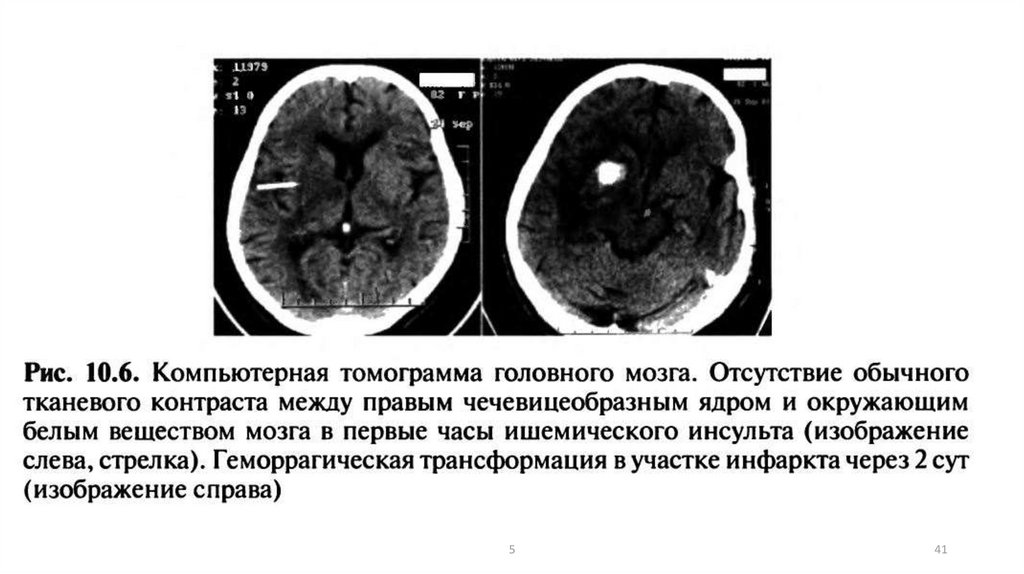
4041.
541
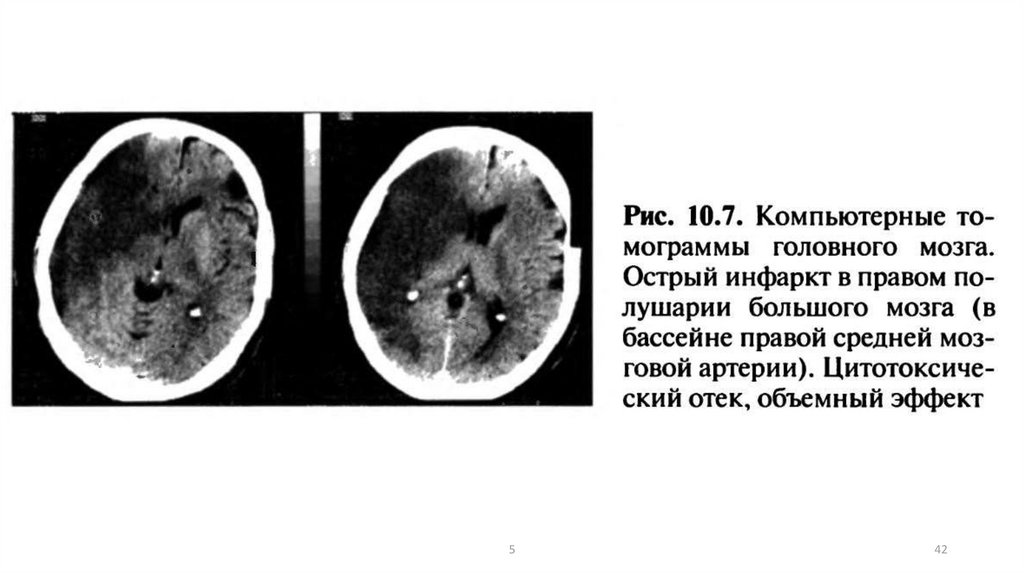
42.
542
43.
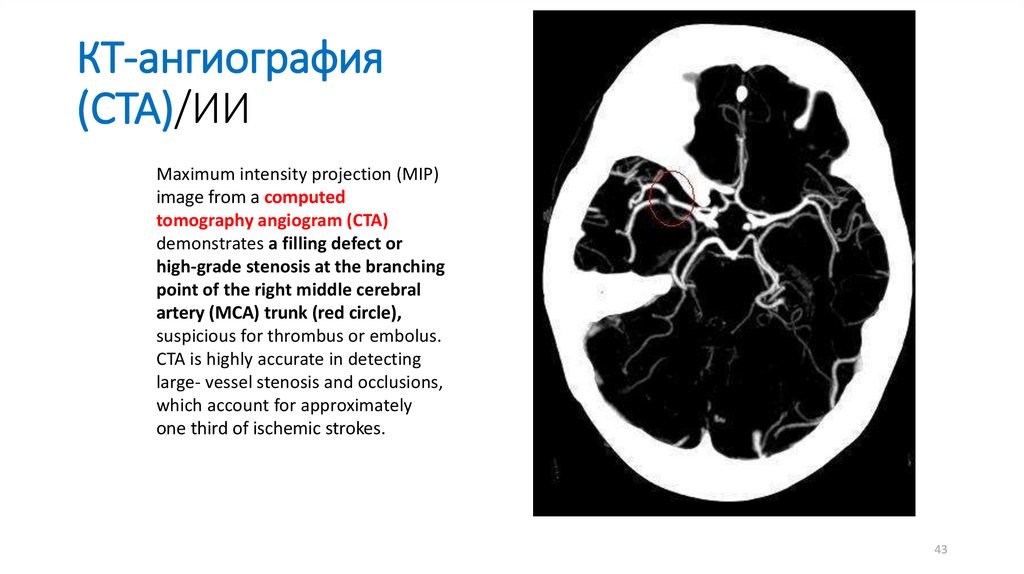
КТ-ангиография(CTA)/ИИ
Maximum intensity projection (MIP)
image from a computed
tomography angiogram (CTA)
demonstrates a filling defect or
high-grade stenosis at the branching
point of the right middle cerebral
artery (MCA) trunk (red circle),
suspicious for thrombus or embolus.
CTA is highly accurate in detecting
large- vessel stenosis and occlusions,
which account for approximately
one third of ischemic strokes.
43
44.
4445.
КТ-перфузия (pCT)/ИИ• Большая часть КТ-перфузиионных исследований связана с отбором пациентов с
ишемическим инсультом (ИИ) для тромболизиса (ТЛТ) и реваскуляризации. К тому
же КТ-перфузия в остром периоде ИИ является эффективным средством
мониторинга жизнеспособности вещества мозга и прогнозирования исхода
заболевания.
• КТ-перфузия позволяет определить истинную зону ишемии головного мозга, в том
числе (что важно для терапевтических мероприятий) ее обратимый (пенумбра) и
необратимый (ядро некроза) компоненты (объемы). Обратимый может служить
мишенью для терапевтического воздействия (ТЛТ), т.е. минимизировать размер
зоны деструкции ткани мозга.
• Понимая эту ситуацию, рентгенологи многих стран предложили и стали широко
использовать методики КТ в комплексе, включающем нативную КТ головного мозга,
КТ-ангиографию (КТА) экстра- и интракраниальных артерий, КТ-перфузию головного
мозга. Длительность подобного исследования составляет не более 5 минут.
12
45
46.
КТ-перфузия/ИИ• КТ-перфузия может быть выполнена на любом МСКТ с установленным соответствующим
программным обеспечением. Метод КТ-перфузии основан на внутривенном введении контрастного
вещества (КВ), прохождение которого по церебральной сети капилляров отслеживается при помощи
серии КТ-срезов. Церебральная перфузия оценивается по картам, построенным для каждого из
параметров, а также по их абсолютным и относительным значениям в соответствующих областях
головного мозга. При этом метод КТ-перфузии предоставляет информацию о состоянии мозгового
кровотока при помощи совокупности следующих параметров:
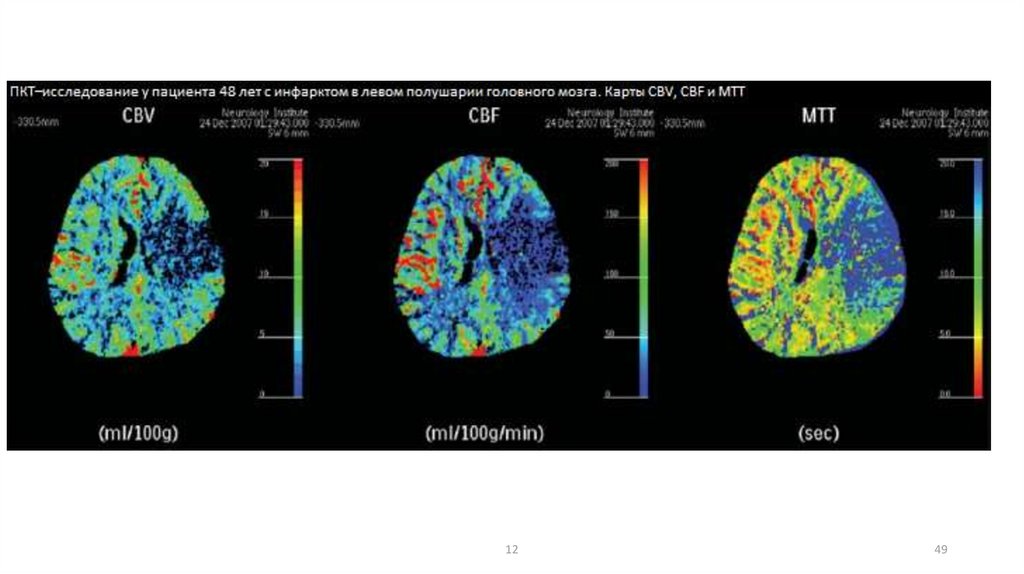
[1] церебральный объем крови - cerebral blood volume, CBV (или «объем мозгового кровотока»,
ОМК) - общий объем крови в выбранном участке мозговой ткани; это понятие включает кровь как в
капиллярах, так и в более крупных сосудах - артериях, артериолах, венулах и венах; данный
показатель измеряется в миллилитрах крови на 100 г мозгового вещества (мл/100 г);
[2] церебральный кровоток - cerebral blood flow, CBF (или «скорость мозгового кровотока», СМК) скорость прохождения определенного объема крови через заданный объем ткани мозга за единицу
времени; CBF измеряется в миллилитрах крови на 100 г мозгового вещества в минуту (мл/100 г х мин);
[3] среднее время прохождения - mean transit time, MTT (или «среднее время транзита», СВТ) среднее время, за которое кровь (контрастный препарат) проходит по сосудистому руслу выбранного
участка мозговой ткани, измеряется в секундах (сек).
12
46
47.
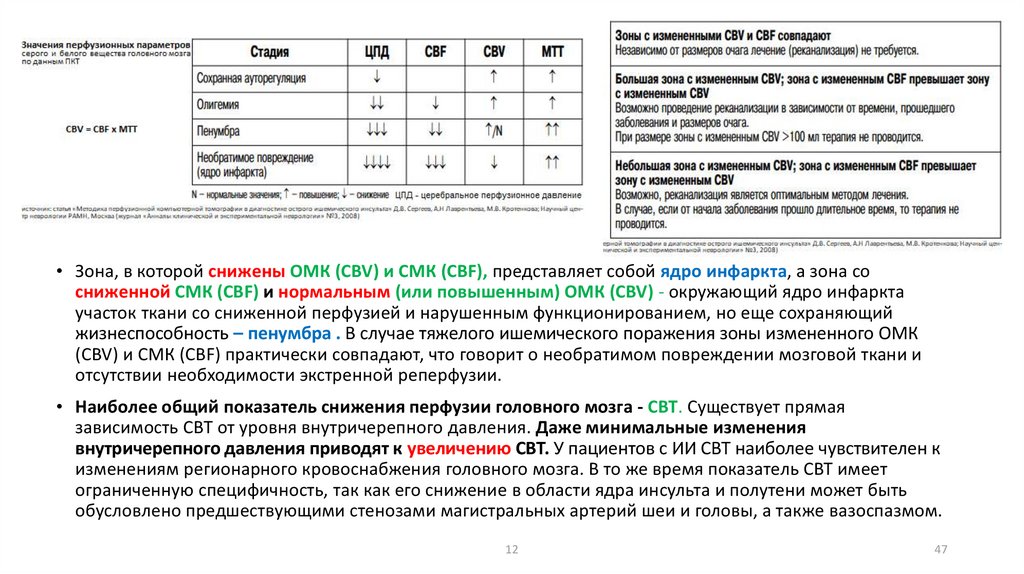
• Зона, в которой снижены ОМК (CBV) и СМК (CBF), представляет собой ядро инфаркта, а зона сосниженной СМК (CBF) и нормальным (или повышенным) ОМК (CBV) - окружающий ядро инфаркта
участок ткани со сниженной перфузией и нарушенным функционированием, но еще сохраняющий
жизнеспособность – пенумбра . В случае тяжелого ишемического поражения зоны измененного ОМК
(CBV) и СМК (CBF) практически совпадают, что говорит о необратимом повреждении мозговой ткани и
отсутствии необходимости экстренной реперфузии.
• Наиболее общий показатель снижения перфузии головного мозга - СВТ. Существует прямая
зависимость СВТ от уровня внутричерепного давления. Даже минимальные изменения
внутричерепного давления приводят к увеличению СВТ. У пациентов с ИИ СВТ наиболее чувствителен к
изменениям регионарного кровоснабжения головного мозга. В то же время показатель СВТ имеет
ограниченную специфичность, так как его снижение в области ядра инсульта и полутени может быть
обусловлено предшествующими стенозами магистральных артерий шеи и головы, а также вазоспазмом.
12
47
48.
КТ-перфузия/ИИ• КТ-перфузия применяется не только с целью быстрой диагностики ИИ в острейший период, но и для
быстрой оценки эффективности селективной ТЛТ. Кроме того, выявление обширных поражений
головного мозга позволяет сделать вывод о невозможности проведения активной тромболитической
терапии, в первую очередь в связи с развитием вторичных геморрагических осложнений в очаге
ишемии.
• Основными проблемами, связанными с внедрением КТ-перфузии, являются использование
рентгеновского излучения и КВ, а также и ограниченность зоны охвата головного мозга. В настоящее
время разрабатываются сканеры с большим массивом детекторов, способные выполнять «объемное»
сканирование с ориентировочной оценкой перфузии всего мозга. Кроме того, в связи с наличием
костных артефактов КТ-перфузию нельзя использовать для исследования ишемических очагов в
задней черепной ямке. Необходима стандартизация техники получения данных (например, выбор
зоны артерии и вены, от которого зависят количественные значения параметров), а также изучение
воспроизводимости и возможности сравнения данных в зависимости от сканера и оператора.
• Несомненными достоинствами КТ-перфузии являются возможность количественной оценки
перфузионных показателей с созданием параметрических карт CBF, CBV и МТТ, отсутствие
потребности в специальном аппаратном обеспечении и радиофармпрепаратах, широкая
распространенность мультидетекторной и спиральной КТ. Кроме того, имеется возможность
сочетания различных методик КТ (в частности, КТА). К положительным моментам относятся также
быстрота выполнения методики и относительно низкая чувствительность к движениям пациента, что
особенно важно в ургентных условиях.
12
48
49.
1249
50.
5051.
Digital Subtraction Angiography (DSA)• Цифровая субтракционная ангиография (digital subtraction angiography,
DSA) — контрастное исследование сосудов с последующей
компьютерной обработкой. Оно позволяет получить снимки высокого
качества с выделением отдельных сосудов из общей картины, при этом
можно уменьшить количество вводимого контрастного вещества и это
вещество можно вводить внутривенно, не прибегая к катетеризации
артерии, что менее травматично для пациента. Трёхмерная цифровая
субстракционная ангиография (3D-DSA) и цветная цифровая
субстракционная ангиография (Color-DSA) — методы обработки для
DSA, позволяющие получить соответственно трёхмерную реконструкцию
изображений с ангиографа и совместить изображение артериального
кровотока, венозного кровотока и перфузии на одном изображении с
применением техники цветового кодирования.
51
52.
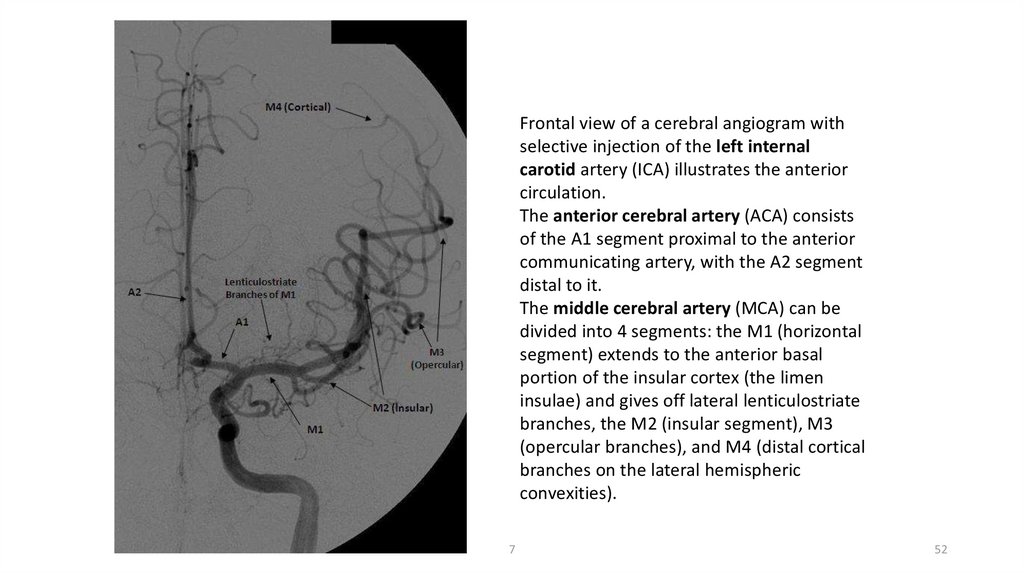
Frontal view of a cerebral angiogram withselective injection of the left internal
carotid artery (ICA) illustrates the anterior
circulation.
The anterior cerebral artery (ACA) consists
of the A1 segment proximal to the anterior
communicating artery, with the A2 segment
distal to it.
The middle cerebral artery (MCA) can be
divided into 4 segments: the M1 (horizontal
segment) extends to the anterior basal
portion of the insular cortex (the limen
insulae) and gives off lateral lenticulostriate
branches, the M2 (insular segment), M3
(opercular branches), and M4 (distal cortical
branches on the lateral hemispheric
convexities).
7
52
53.
Lateral view of a cerebral angiogramillustrates the branches of the
anterior cerebral artery (ACA) and
Sylvian triangle. The pericallosal
artery has been described to arise
distal to the anterior communicating
artery or distal to the origin of the
callosomarginal branch of the ACA.
The segmental anatomy of the ACA
has been described as follows: the
A1 segment extends from the
internal carotid artery (ICA)
bifurcation to the anterior
communicating artery; A2 extends to
the junction of the rostrum and genu
of the corpus callosum; A3 extends
into the bend of the genu of the
corpus callosum; A4 and A5 extend
posteriorly above the callosal body
and superior portion of the
splenium. The Sylvian triangle
overlies the opercular branches of
the middle cerebral artery (MCA),
with the apex representing the
Sylvian point.
53
54.
Frontal projection from a right vertebralartery angiogram illustrates the posterior
circulation.
The vertebral arteries join to form the basilar
artery.
The posterior inferior cerebellar arteries
(PICAs) arise from the distal vertebral arteries.
The anterior inferior cerebellar arteries
(AICAs) arise from the proximal basilar artery.
The superior cerebellar arteries (SCAs) arise
distally from the basilar artery prior to its
bifurcation into the posterior cerebral arteries
(PCAs).
7
54
55.
5556.
5657.
5758.
МРТ (магнитно-резонансная томография)• МРТ — способ получения томографических изображений для исследования
внутренних органов и тканей с использованием явления ядерного
магнитного резонанса.
• Способ основан на измерении электромагнитного отклика ядер атомов
водорода, а именно, на возбуждении их определённым сочетанием
электромагнитных волн в постоянном магнитном поле высокой
напряжённости.
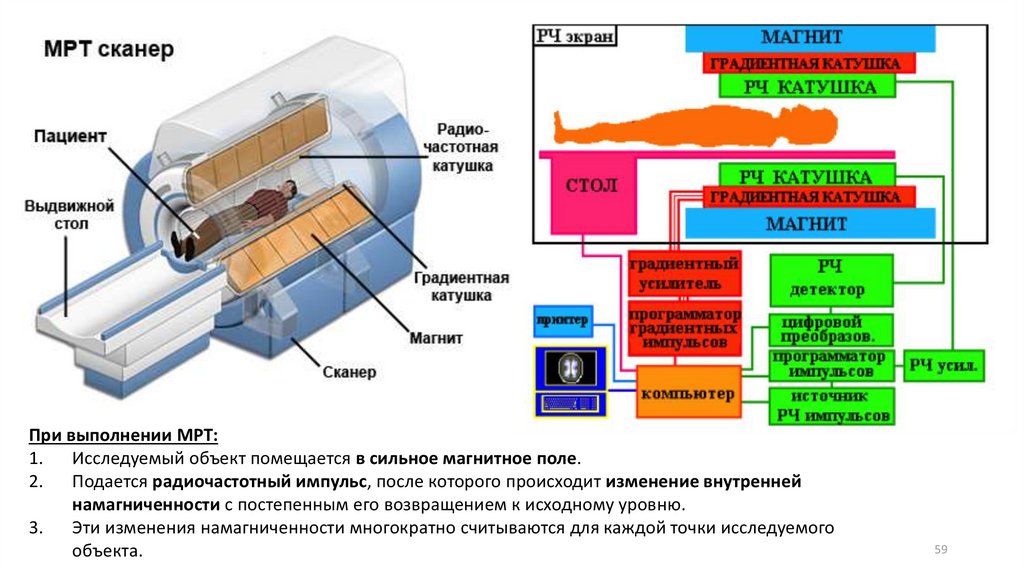
• Основные компоненты любого МР-томографа:
1. Магнит (постоянное гомогенное магнитное поле)
2. Градиентные катушки
3. Радиочастотные катушки (радиочастотный сигнал, который изменяет
магнитное поле)
4. Блок обработки информации (компьютер)
58
59.
При выполнении МРТ:1. Исследуемый объект помещается в сильное магнитное поле.
2. Подается радиочастотный импульс, после которого происходит изменение внутренней
намагниченности с постепенным его возвращением к исходному уровню.
3. Эти изменения намагниченности многократно считываются для каждой точки исследуемого
объекта.
59
60.
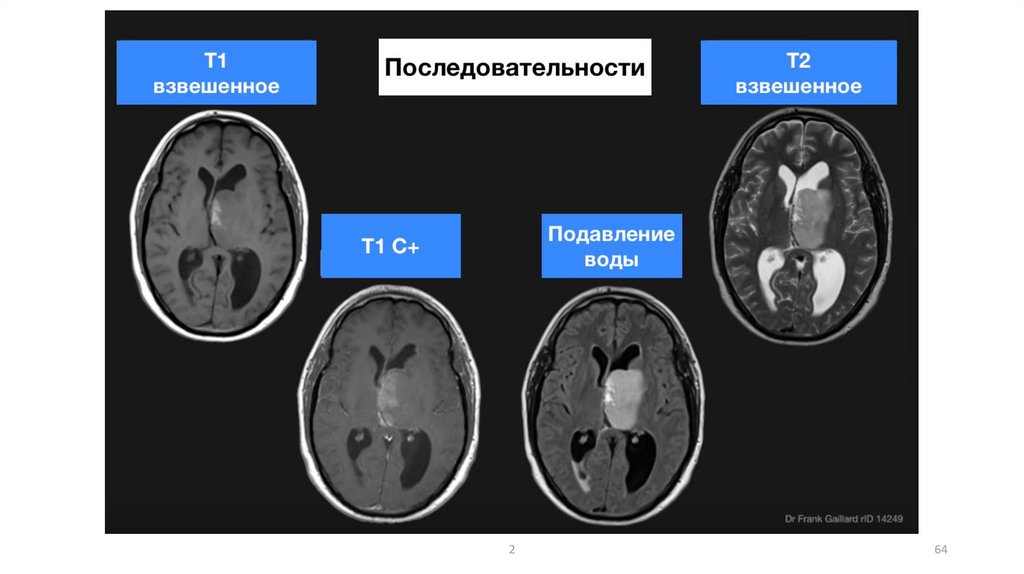
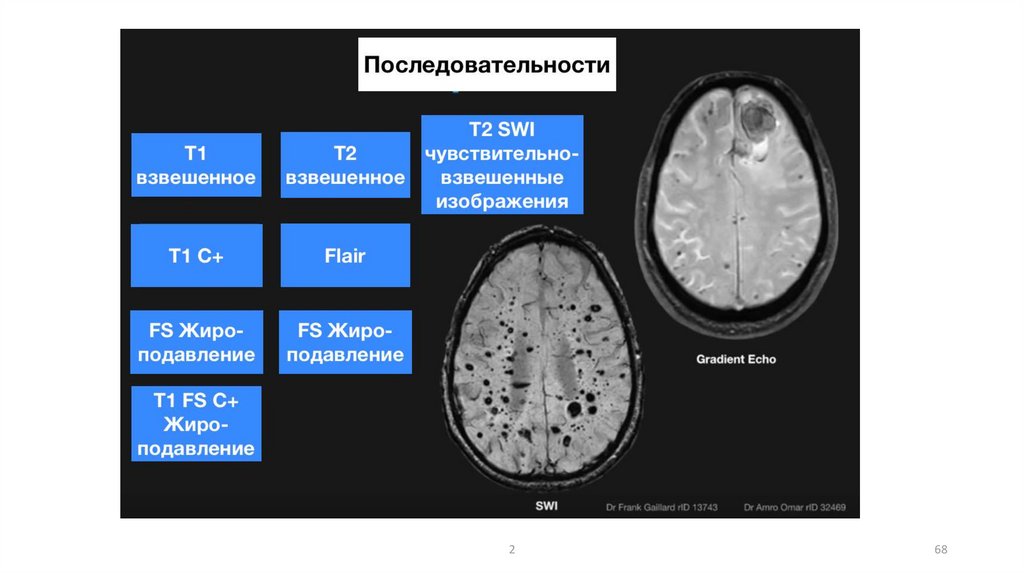
МРТЧасто используемые методы МРТ:
• T1-взвешенная визуализация (T1-WI), в которой спинномозговая жидкость (CSF) имеет
низкую интенсивность сигнала по отношению к ткани мозга
• T2-взвешенная визуализация (T2-WI), в которой CSF имеет высокую интенсивность сигнала
по отношению к ткани мозга
• Спин-взвешенная визуализация, при которой CSF имеет плотность, аналогичную ткани
мозга
• Градиентное эхо-изображение, которое обладает наибольшей чувствительностью при
выявлении ранних геморрагических изменений
• Диффузионно-взвешенная визуализация (DWI), в которой изображения отражают
микроскопическое случайное движение молекул воды
• Визуализация с перфузионным взвешиванием (PWI), в которой гемодинамически
взвешенные МР-последовательности основаны на прохождении МР-контраста через ткань
мозга
• ГИПОИНТЕНСИВНЫЙ/ГИПЕРИНТЕНСИВНЫЙ
4
60
61.
МРТТ1WI и Т2WI
• Когда пациент находится в магнитном поле, магнитные моменты атомов водорода, находящихся в
воде тканей его тела выстраиваются вдоль магнитного поля. В результате действия радиочастотного
импульса магнитные моменты атомов водорода меняют свое направление (отклоняются от
первоначального направления “по полю” на некоторый угол а) – возбуждаются, при выключении
радиочастотного импульса происходит восстановление первоначального направления “по полю”. Этот
процесс восстановления называется — релаксацией.
• Это самое время релаксации или другими словами — быстрота восстановления направления
магнитных моментов атомов водорода к первоначальному направления “по полю” изменяется от
одного типа ткани к другому. Это различие времен релаксации используется в МРТ, чтобы отличить
нормальные и патологические ткани. Каждая ткань характеризуется двумя временами (константами)
релаксации: T1 — время продольной релаксации и Т2 — время поперечной релаксации.
• Время эхо (TE или Echo Time) – интервал между радиочастотным импульсом и пиком сигнала (эхо),
индуцированного в катушке. Измеряется в миллисекундах. Степень T2 релаксации определяется через
TE. Так же TE значительно влияет на контраст изображения во всех типах последовательностей.
• Время повторения (TR или repetition time) — интервал между двумя радиочастотными импульсами.
В SE – между двумя 90° импульсами, в GE – между двумя α импульсами и в IR – между двумя 180°
импульсами. Определяет насколько продольная намагниченность успевает восстанавливаться до
применения следующего импульса. Влияет на степень релаксации Т1. Измеряется в миллисекундах.
• Базовые характеристики Т1: TR: короткое и TE: короткое.
• Базовые характеристики Т2: TR: длинное, TE: длинное, угол переворота: менее важен чем при T1
взвешенности.
2
61
62.
6263.
МРТТ1+С
• На Т1-взвешенных постконтрастных изображениях Т1+С
кровеносные сосуды (например, артерии и вены в
мозгу, шее, груди, животе, верхних и нижних
конечностях) выглядят гиперинтенсивно. Кровеносные
сосуды и патологии с высокой васкуляризацией
гиперинтенсивнее на Т1-взвешенных постконтрастных
изображениях.
• Патологии с гиперваскуляризацией выглядят
гиперинтенсивными на Т1-взвешенных
постконтрастных изображениях (например, опухоли, как
гемангиома, лимфангиома, гемангиоэндотелиома,
саркома Капоши, ангиосаркома, гемангиобластома и
т.д., а также воспалительные процессы, такие как
дисцит, менингит, синовит, артрит, остеомиелит и т.д.).
Патологические процессы не имеющие кровеносных
сосудов остаются неизменными.
• В большинстве случаев при получении Т1-взвешенных
постконтрастных изображений используется
жироподавление (Fat Sat), кроме исследований
головного мозга.
2
63
64.
264
65.
МРТПоследовательности восстановления с инверсией:
FLAIR/STIR
• Последовательности восстановления с
инверсией используются, чтобы получить изображения
взвешенные по T1, но при этом кривые T1 релаксации
тканей «разведены друг от друга», чтобы создать
большее различие в Т1 контрасте.
Flair или Fluid attenuation inversion recovery (FLAIR)
• Представляет собой последовательность инверсиивосстановления с длинным T1 используемая для
устранения влияния жидкости в получаемом
изображении.
• Патологические процессы, при которых увеличивается
содержание воды в тканях, как правило,
гиперинтенсивные на FLAIR изображениях.
• FLAIR последовательность полезна при следующих
заболеваниях центральной нервной системы: инфаркт,
рассеянный склероз, субарахноидальное
кровоизлияние, ЧМТ, постконтрастные FLAIR
изображения включены в протоколы для оценки
лептоменингеальных заболеваний, таких как менингит.
2
65
66.
МРТSTIR или Short tau inversion recovery
• Последовательность инверсиявосстановление спинового эха (STIR),
так же называемая инверсиейвосстановление с коротким Т1.
• Пространства заполненные жидкостью
(например, спинномозговая жидкость в
желудочках мозга и позвоночном
канале, свободная жидкость в
брюшной полости, жидкость в желчном
пузыре и общем желчном протоке,
синовиальная жидкость в суставах,
жидкость в мочевом канале и мочевом
пузыре, отек или любая другая
патологическая жидкость в организме)
выглядят гиперинтенсивными, а жир
очень гипоинтенсивным.
• Патологические процессы, при которых
увеличивается содержание воды в
тканях, как
правило, гиперинтенсивные на
STIR изображениях.
2
66
67.
МРТГрадиентное эхо
• Быстрое градиентное эхо (Fast Gradient Echo, fastGRE): ткани дают
низкий сигнал и низкий контраст, а получение изображения занимает
менее 1 с.
SWI
• Получают изображения, взвешенные по неоднородности магнитного
поля (SWI). Эта особая форма сбора информации и обработки
изображений дает изображение повышенной контрастности,
чувствительное к венозной крови, кровоизлияниям и накоплениям
железа.
• Клиническое применение: основное применение визуализация мелких
кровоизлияний до 5 мм в диаметре, а также продуктов крови и
кальция.
2
67
68.
268
69.
МРТПротон (PD)-взвешенное
изображение
• На PD-взвешенных
изображениях сигнал от
жидкости практически
идентичен сигналу от жира.
Жидкость обычно выглядит
серовато-белой, почти
аналогично по внешнему виду,
жиру в организме.
• На PD-взвешенных изображениях
с насыщением жира, жировая
ткань (области, содержащие
жировую ткань, например,
подкожно-жировая клетчатки и
жир в костном мозге) выглядят
гипоинтенсивными. Все
остальные характеристики PDвзвешенных изображений
остаются теми же.
2
69
70.
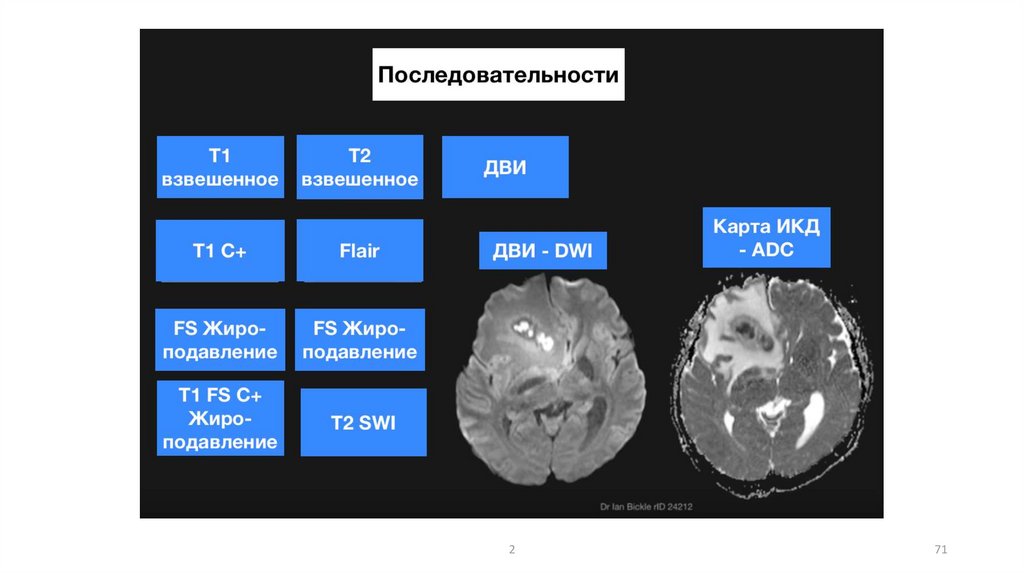
МРТДиффузионно-взвешенная визуализация (DWI)
• Обнаруживает хаотическое или направленное (МР-трактография) движение
молекул воды (диффузию).
• Диффузия более свободна в жидкостях и более ограничена в тканях.
• В тканях диффузия более свободна в межклеточных пространствах и более
ограничена внутри клеток (мембранными и клеточными органеллами). Чем шире
межклеточные пространства, тем свободнее диффузия.
• Выявляет ишемию (цитотоксический отек) в течение нескольких минут после
развития неврологической симптоматики.
• 2 этапа анализа ДВИ: 1) – качественный – визуальная оценка интенсивности
сигнала на диффузионных изображениях; 2) – количественный – определение
измеряемого коэффициента диффузии (ИКД) на реконструированных картах
ИКД.
• Повышенный сигнал на диффузионных изображениях + сниженный сигнал на карте
ИКД = ограничение (снижение) диффузии.
70
71.
271
72.
МРТВизуализация с перфузионным взвешиванием (PWI)
• Перфузионной МРТ в настоящее время называют методы оценки перфузии при прохождении болюса
контрастного вещества.
• По мере прохождения болюса контрастного вещества по сосудистой системе многократно
регистрируют изображение одного и того же среза (обычно это 10 разных уровней или срезов). Само
сканирование занимает 1-2 мин. График снижения интенсивности МР-сигнала при прохождении
болюса контрастного вещества даёт зависимость «интенсивность сигнала — время» в каждом
пикселе среза. Форма этой кривой в артерии и вене определяет артериальную и венозную функции,
с помощью которых рассчитывают гемодинамические тканевые параметры.
• PWI позволяет обнаруживать гипоперфузионные участки ГМ. В участках, расположенных дистальнее
артериальной окклюзии, поступление контрастного вещества или маркирующих водных молекул
может быть замедленным. Результирующая кривая «сигнал-время» может превратиться в кривую
«концентрация-время», по которой можно определить функции, которые отображают региональную
перфузию. Интенсивность сигнала уменьшается, когда контрастный материал проходит через
инфарктную область и возвращается к нормальному состоянию, когда он выходит из этой области.
Кривая получается из этих данных отслеживания (то есть кривая вымывания сигнала), которая
представляет и оценивает объем церебральной крови (CBV).
• Для получения ПВ MP-изображения используют разные контрастные вещества, которые содержат
хелаты гадолиния. В частности, чаще всего применяют гадолиний, учитывая эффект восприимчивости,
возникающий в прилегающих тканях и снижающий время Т2-взвешенного изображения, которое
определяется низким сигналом при соответствующих последовательностях.
2
72
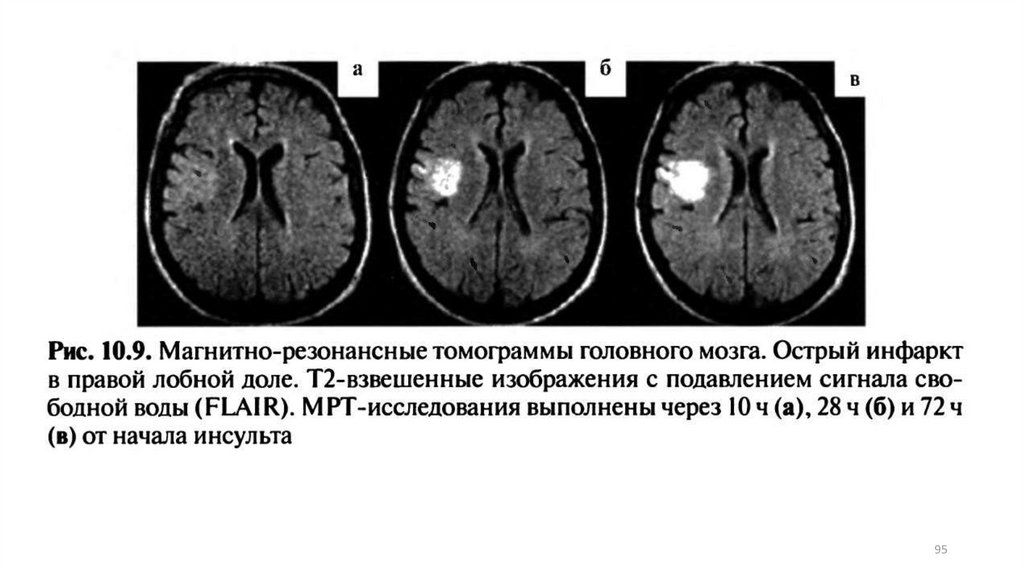
73.
МРТ/ИИ• На Т1-ВИ снижение сигнала в зоне инфаркта умеренное и в первые сутки
инсульта для диагностики малоинформативное.
• На Т2-ВИ повышение интенсивности сигнала в зоне инфаркта может
наблюдаться через 3 ч от начала инсульта, через 8 ч изменения на МРизображениях отмечается у 15% больных и через 24 ч – у 90% пациентов.
• Определение объема поражения при инфаркте, а также выявление мелких
участков ишемического повреждения мозга вблизи ликворных пространств
на обычных Т2-ВИ затруднено в связи с высоким сигналом от СМЖ. В этих
случаях имеют преимущество изображения, полученные на режиме с
подавлением сигнала свободной воды (FLAIR).
• Отражая динамику развития отека мозга (цитотоксического и
развивающегося вслед за ним вазогенного), интенсивность сигнала на Т2-ВИ
и протон-взвешенных изображениях в зоне инфаркта увеличивается к 4-7м суткам инсульта, затем снижается к 10-14 суткам заболевания.
5
73
74.
МРТ/ИИ• Имеются описания отдельных наблюдений выраженного снижения интенсивности
сигнала на Т2-ВИ к концу 2 недели инсульта, когда очаг инфаркта становился
практически изоинтенсивным по отношению к нормальному веществу мозга, на
основании чего был предложен термин «МР-затуманивание», по аналогии с
эффектом при КТ.
• Наряду с изменением интенсивности сигнала появляется и нарастает объемный
эффект, проявляющийся сглаженностью рисунка борозд и извилин мозга,
сдавлением наружных и внутренних ликворных пространств. Данные изменения
при МРТ-исследовании выявляются более точно и надежно по сравнению с КТ в
связи с возможностью получения изображений в различных проекциях.
• Для геморрагической трансформации повышение сигнала на Т1-ВИ, связанное с
появлением метгемоглобина во внеклеточном пространстве, является основным
диагностическим критерием. Данный признак начинает выявляться через 5-7 дней
от момента развития геморрагической трансформации и сохраняется в течение
нескольких недель, когда КТ-признаки данного осложнения инфаркта уже
регрессируют.
5
74
75.
МРТ/ИИ• В процессе организации инфаркта наблюдаются 2 основных типа тканевых
изменений в зоне поражения – формирование кистозных полостей, заполненных
ликвороподобной жидкостью (кистозная трансформация), и пролиферация глии
(глиозная трансформация).
• Дифференцировка данных типов тканевых изменений затруднена как на КТизображениях, так и на обычных Т2-ВИ и Т1-ВИ, так как в участках глиозной
трансформации общее содержание воды также повышено, хотя и в меньшей
степени, чем в постинфарктных кистах.
• На изображениях, полученных при использовании режима с подавлением
свободной воды (FLAIR), участки глиозной трансформации гиперинтенсивные, так
как вода в клетках глии связанная, в отличии от этого постинфарктные кисты будут
гипоинтенсивными, так как содержат в основном свободную воду. Использование
данного режима позволяет надежно определять соотношение двух указанных
типов тканевых изменений в зоне хронического ИМ и соответственно изучать
влияние на них различных факторов, в том числе и терапевтических воздействий.
5
75
76.
МРТ• Flair или Fluid attenuation inversion recovery (FLAIR)
представляет собой последовательность инверсиивосстановления с длинным T1 используемая для
устранения влияния жидкости в получаемом
изображении.
• Т1 время в данной последовательности подобрано
равным времени релаксации вещества/ткани которую
необходимо подавить. Импульс инверсии приложен
так, что T1-релаксация жидкости достигает
пересечения с нулевым значением в момент TI,
приводя к «стиранию» сигнала.
• Патологические процессы, при которых увеличивается
содержание воды в тканях, как правило,
гиперинтенсивные на FLAIR изображениях.
• FLAIR последовательность полезна при следующих
заболеваниях центральной нервной системы: инфаркт,
рассеянный склероз, субарахноидальное
кровоизлияние, ЧМТ, постконтрастные FLAIR
изображения включены в протоколы для оценки
лептоменингеальных заболеваний, таких как менингит.
2
76
77.
МРТ/ИИ• Применение PWI может предоставить дополнительную информацию в диагностике ИМ.
Гадолиний сокращает время Т1 релаксации, что приводит к появлению сигнала
повышенной интенсивности на Т1-ВИ в местах его накопления.
• Различают 2 основных типа контрастного усиления – внутрисосудистое и паренхиматозное.
Внутрисосудистый тип накопления контрастного препарата отражает, как правило,
замедление тока крови в очаге поражения и может быть одним из самых ранних признаков
ишемии мозга, предшествуя изменениям интенсивности сигнала на Т2-ВИ и Т1-ВИ.
Паренхиматозный тип контрастного усиления связан с повреждением ГЭБ и выходом
контрастного препарата из сосудистого русла в вещество мозга.
• В 60-78% случаев у большинства больных с ИИ в первые сутки заболевания наблюдается
эффект внутрисосудистого контрастного усиления, причем чаще при большом объеме и
корковой локализации очага поражения, паренхиматозный тип контрастного усиления в
это время встречается значительно реже – в 26% случаев.
• Однако к 6-7 суткам заболевания фактически у всех отмечается паренхиматозный тип и
лишь в трети случаев – внутрисосудистый. В дальнейшем эффект контрастного усиления
ИМ снижается.
5
77
78.
МРТ/ИИ• Использование диффузно-взвешенных (ДВИ) и перфузионных МР-изображений!
• ДВИ: участки ИМ выявляются через несколько минут в связи с тем, что молекулы
воды из внеклеточного пространства перемещаются в клетки в зоне развития
цитотоксического отека мозга – отчетливые гиперинтенсивные изменения.
• Перфузионные МР-изображения: участки гипоперфузии мозга. Сопоставление
распространенности данных изменений с величиной гиперинтенсивных участков из
ДВИ позволяет дифференцировать зону необратимых ишемических
повреждений вещества мозга от пенумбры. У взрослых пациентов на обратимость
изменений в зоне гипоперфузии указывает отсутствие признаков цитотоксического
отека, т.е. гиперинтенсивных изменений на ДВИ. У детей появление последних
может не сопровождаться развитием необратимых изменений в зоне
гипоперфузии.
• Визуализация острой фокальной ишемии мозга возможна уже через несколько мин
от ее начала при помощи ДВИ и ПВИ.
5
78
79.
379
80.
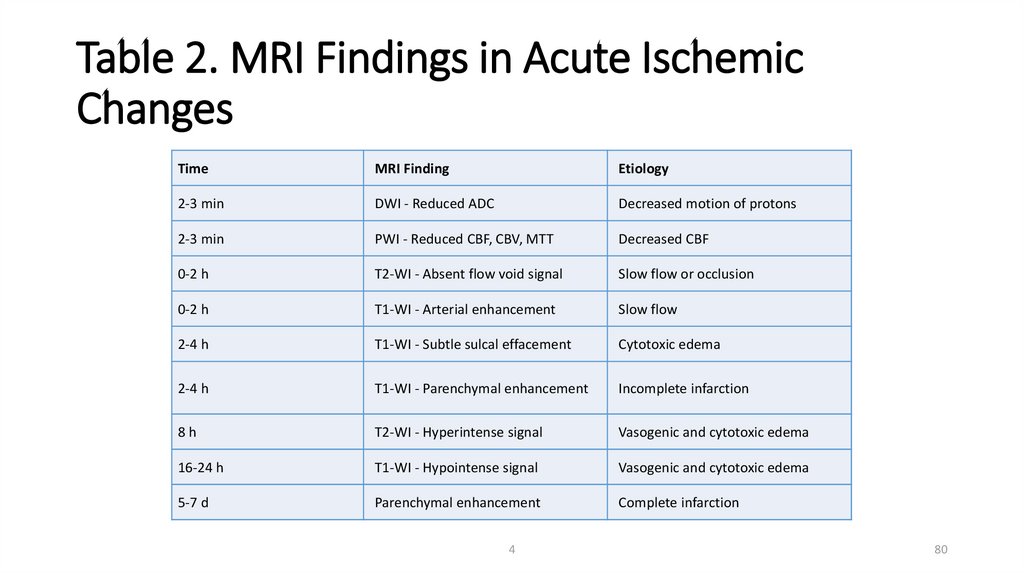
Table 2. MRI Findings in Acute IschemicChanges
Time
MRI Finding
Etiology
2-3 min
DWI - Reduced ADC
Decreased motion of protons
2-3 min
PWI - Reduced CBF, CBV, MTT
Decreased CBF
0-2 h
T2-WI - Absent flow void signal
Slow flow or occlusion
0-2 h
T1-WI - Arterial enhancement
Slow flow
2-4 h
T1-WI - Subtle sulcal effacement
Cytotoxic edema
2-4 h
T1-WI - Parenchymal enhancement
Incomplete infarction
8h
T2-WI - Hyperintense signal
Vasogenic and cytotoxic edema
16-24 h
T1-WI - Hypointense signal
Vasogenic and cytotoxic edema
5-7 d
Parenchymal enhancement
Complete infarction
4
80
81.
МРТ/ИИ/Ранний острейший инсульт (0-6 часов)МРТ/ИИ/Поздний острейший период (6-24 часа)
T1: изоинтенсивный сигнал (через 2-4 часа T1-WI
показывает тонкое стирание бороздок вследствие
цитотоксического отека)
PWI Т1:
• в первые 2 часа может встречаться артериальное
накопление контрастного вещества
• паренхимальное накопление контраста в
незавершенном инсульте может возникать на 2-4 часа
T2:
• изоинтенсивный сигнал
• может возникать феномен пустоты потока в
ипсилатеральной внутренней сонной артерии в
первые 2 часа в случае обширного инсульта
FLAIR:
• интенсивность сигнала варьирует
• обычно интенсивность сигнала повышается после 6
часов, но иногда встречается повышение МР сигнала и
в первые 2 часа
DWI: высокая интенсивность сигнала
Карты ИДК: низкая интенсивность сигнала
SWI или последовательности градиентного эха: в первые
12 часов может быть геморрагическая трансформация
(наименее вероятно)
T1: гипоинтенсивный сигнал через примерно 16
(до 24) часов после начала (из-за
цитотоксического и вазогенного отека)
PWI Т1:
• может возникать артериальное накопление
контрастного вещества
• кортикальное усиление в незавершенном
инсульте
• возможно менингеальное накопление
T2: интенсивность сигнала варьирует, обычно
гипер- через 8 часов от начала инсульта (из-за
цитотоксического и вазогенного отека)
FLAIR: обычно гиперинтенсивный сигнал
DWI: высокая интенсивность сигнала
Карты ИДК: низкая интенсивность сигнала
SWI или последовательности градиентного эха: в
первые 12 часов может быть геморрагическая
трансформация (наименее вероятно)
81
82.
МРТ/ИИ/Острый период (24 часа-1 неделя) –сигналы МРТ становятся более заметными и
хорошо разграниченными.
МРТ/ИИ/Подострый период (1-3 недели)
T1:
• гипоинтенсивный сигнал
• гиперинтенсивность при кортикальном некрозе
(3-5 день)
PWI Т1:
• артериальный и менингеальный паттерны
накопления;
• в случае завершенного инфаркта
паренхиматозный паттерн возникает на 5-7 день
T2: гиперинтенсивный сигнал
FLAIR: обычно высокая интенсивность сигнала
DWI: высокая интенсивность сигнала
Карты ИДК: низкая интенсивность сигнала
SWI или последовательности градиентного эха:
геморрагическая трансформация после 48 часов до 5
дня
T1:
• гипоинтенсивный сигнал
• гиперинтенсивность при кортикальном некрозе (после 2
недели)
PWI Т1: паренхимальный паттерн накопления в случае
завершенного инсульта; обычно приходится на 1-8 недели
T2: гиперинтенсивный сигнал;
"затемнение/затуманивание" может наблюдаться на 1-4
неделе с пиком на 2-3 неделе (1-4 неделе с пиком на ) –
изоинтенсивный сигнал.
FLAIR: высокая интенсивность сигнала
DWI:
• высокая интенсивность сигнала на 10-14 день
• после гипо- или изоинтенсивность
• гиперинтенсивность в случае феномена Т2
просвечивания
Карты ИДК:
• низкая интенсивность сигнала на 7-10 сутки;
• возможна псевдонормализация на 10-15 день с
последуюшим повышением интенсивности сигнала
SWI или последовательности градиентного эха:
82
геморрагическая трансформация не характерна
83.
МРТ/ИИ/Хронический период (>3 недели)T1:
• гипоинтенсивный сигнал
• может быть гиперинтенсивность при кортикальном некрозе (после 2 недели)
PWI Т1: паренхимальный паттерн накопления с 8 недели и до 4-го месяца
T2: гиперинтенсивный сигнал
FLAIR: гипер-/гипоинтенсивность сигнала в случае глиоза/кистозной энцефаломаляции
DWI:
• интенсивность сигнала варьирует
• может быть изоинтенсивность
• гиперинтенсивность в случае феномена Т2 просвечивания
• гипоинтенсивность в случае кистозной энцефаломаляции
Карты ИДК: высокая интенсивность сигнала
SWI или последовательности градиентного эха: микрокровоизлияния и геморрагическая
трансформация
1
83
84.
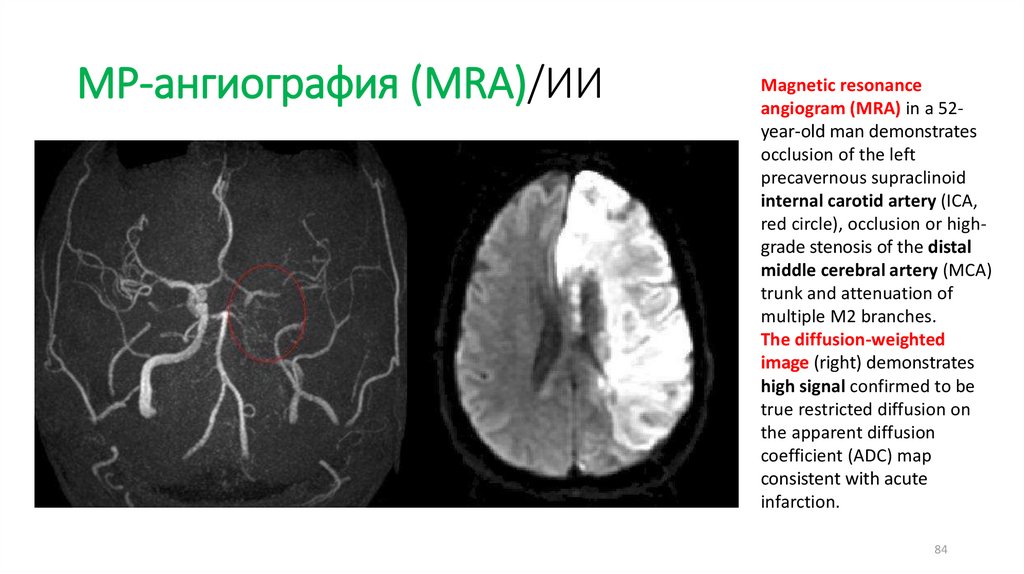
МР-ангиография (MRA)/ИИMagnetic resonance
angiogram (MRA) in a 52year-old man demonstrates
occlusion of the left
precavernous supraclinoid
internal carotid artery (ICA,
red circle), occlusion or highgrade stenosis of the distal
middle cerebral artery (MCA)
trunk and attenuation of
multiple M2 branches.
The diffusion-weighted
image (right) demonstrates
high signal confirmed to be
true restricted diffusion on
the apparent diffusion
coefficient (ADC) map
consistent with acute
infarction.
84
85.
МРТ/ИИNB! ПРОБЛЕМЫ:
• Ограничения МРТ заключаются в более длительном времени и более
высокой стоимости исследования, невозможности исследования пациентов
с металлическими телами в полости черепа и кардиостимуляторами.
• В первые сутки заболевания с целью дифференциальной диагностики между
ишемическим поражением и геморрагическим инсультом, поскольку в
первые сутки выявляемость кровоизлияний при КТ выше, чем при МРТ.
• Рекомендации 2013 года по раннему лечению острого ишемического
инсульта рекомендуют, что хотя в большинстве случаев КТ предоставляет
необходимую информацию, МРТ может использоваться перед
внутривенным введением ТРА для исключения ICH (абсолютного
противопоказания) и для определения наличия гиперинтенсивности
ишемии при МРТ (класс I Уровень доказанности А).
4, 5
85
86.
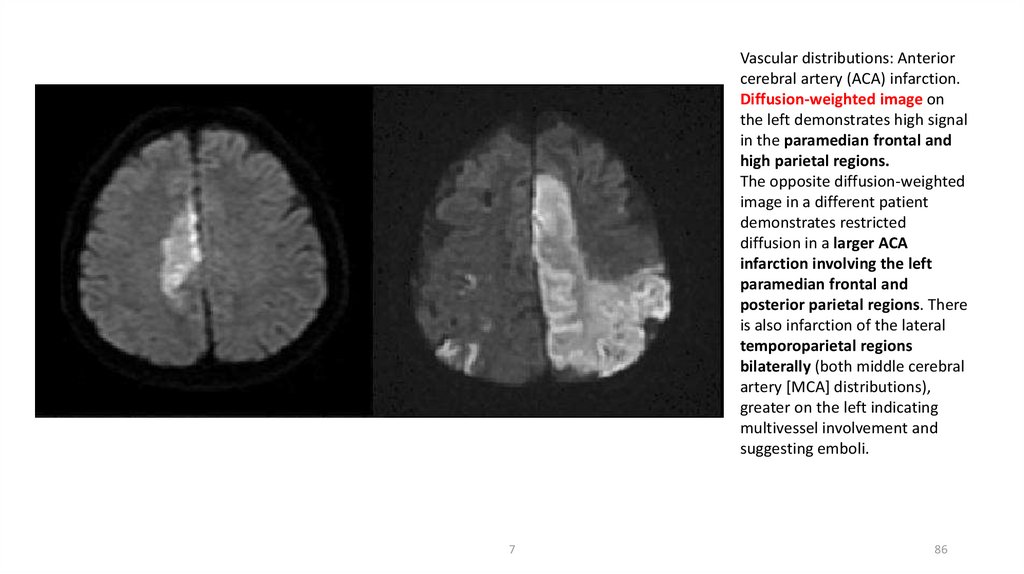
Vascular distributions: Anteriorcerebral artery (ACA) infarction.
Diffusion-weighted image on
the left demonstrates high signal
in the paramedian frontal and
high parietal regions.
The opposite diffusion-weighted
image in a different patient
demonstrates restricted
diffusion in a larger ACA
infarction involving the left
paramedian frontal and
posterior parietal regions. There
is also infarction of the lateral
temporoparietal regions
bilaterally (both middle cerebral
artery [MCA] distributions),
greater on the left indicating
multivessel involvement and
suggesting emboli.
7
86
87.
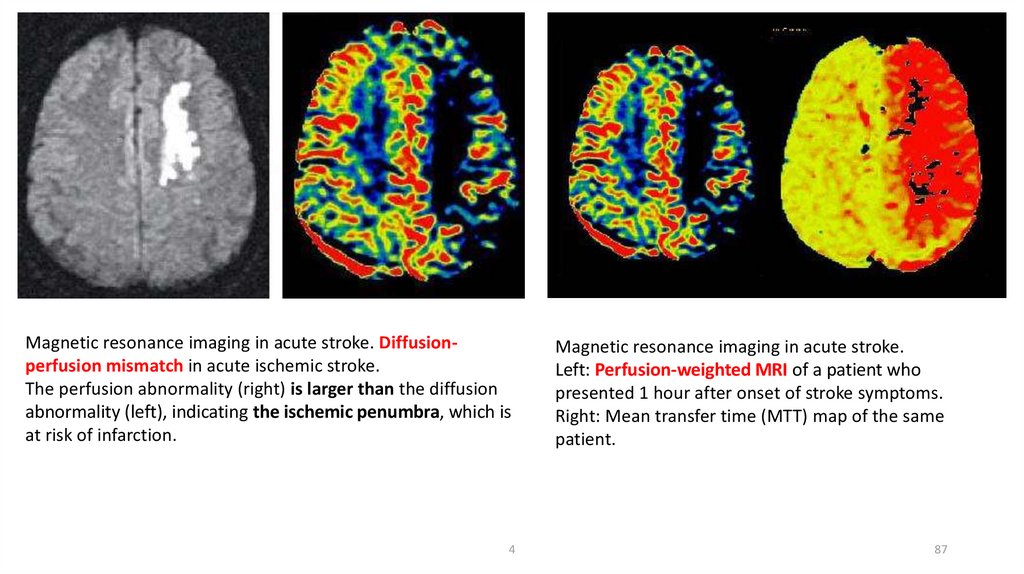
Magnetic resonance imaging in acute stroke. Diffusionperfusion mismatch in acute ischemic stroke.The perfusion abnormality (right) is larger than the diffusion
abnormality (left), indicating the ischemic penumbra, which is
at risk of infarction.
Magnetic resonance imaging in acute stroke.
Left: Perfusion-weighted MRI of a patient who
presented 1 hour after onset of stroke symptoms.
Right: Mean transfer time (MTT) map of the same
patient.
4
87
88.
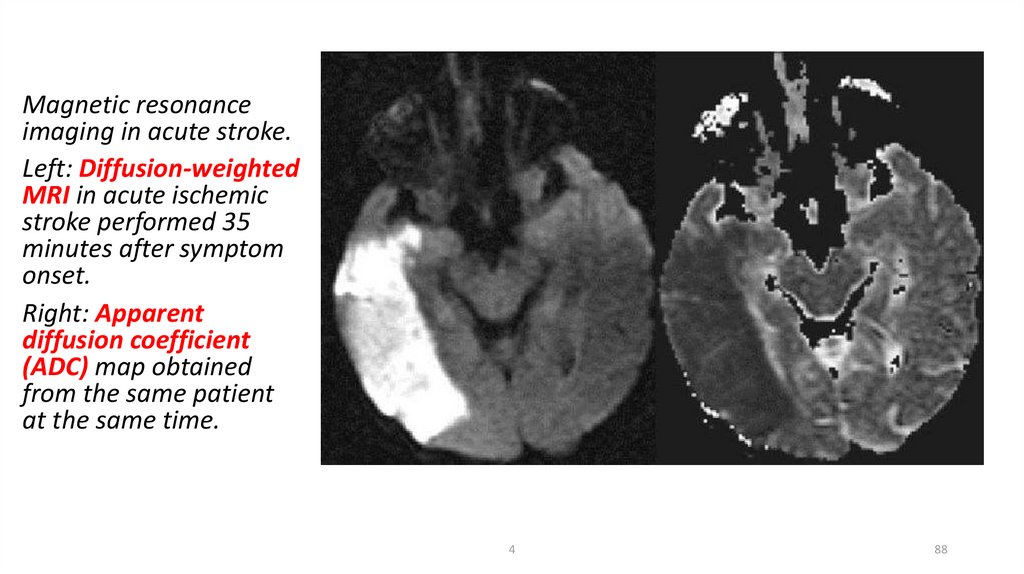
Magnetic resonanceimaging in acute stroke.
Left: Diffusion-weighted
MRI in acute ischemic
stroke performed 35
minutes after symptom
onset.
Right: Apparent
diffusion coefficient
(ADC) map obtained
from the same patient
at the same time.
4
88
89.
Magnetic resonance imaging(MRI) scan was obtained in a 62year-old man with hypertension
and diabetes and a history of
transient episodes of right-sided
weakness and aphasia.
The fluid-attenuated inversion
recovery (FLAIR) image (left)
demonstrates patchy areas of high
signal arranged in a linear fashion
in the deep white matter,
bilaterally. This configuration is
typical for deep border-zone, or
watershed, infarction, in this case
the anterior and posterior middle
cerebral artery (MCA) watershed
areas.
The left-sided infarcts have
corresponding low signal on the
apparent diffusion coefficient
(ADC) map (right), signifying
acuity. An old left posterior
parietal infarct is noted as well.
89
90.
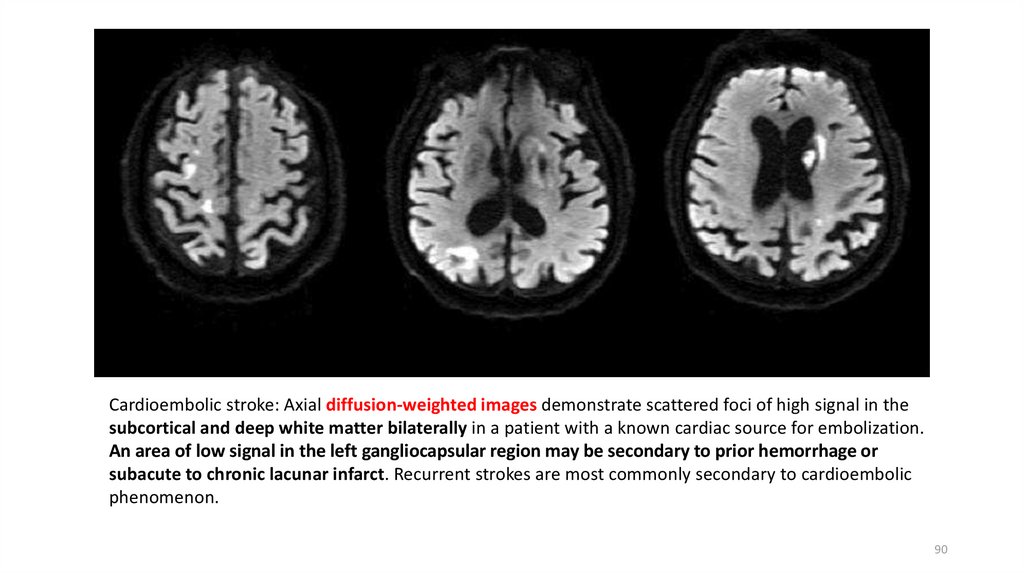
Cardioembolic stroke: Axial diffusion-weighted images demonstrate scattered foci of high signal in thesubcortical and deep white matter bilaterally in a patient with a known cardiac source for embolization.
An area of low signal in the left gangliocapsular region may be secondary to prior hemorrhage or
subacute to chronic lacunar infarct. Recurrent strokes are most commonly secondary to cardioembolic
phenomenon.
90
91.
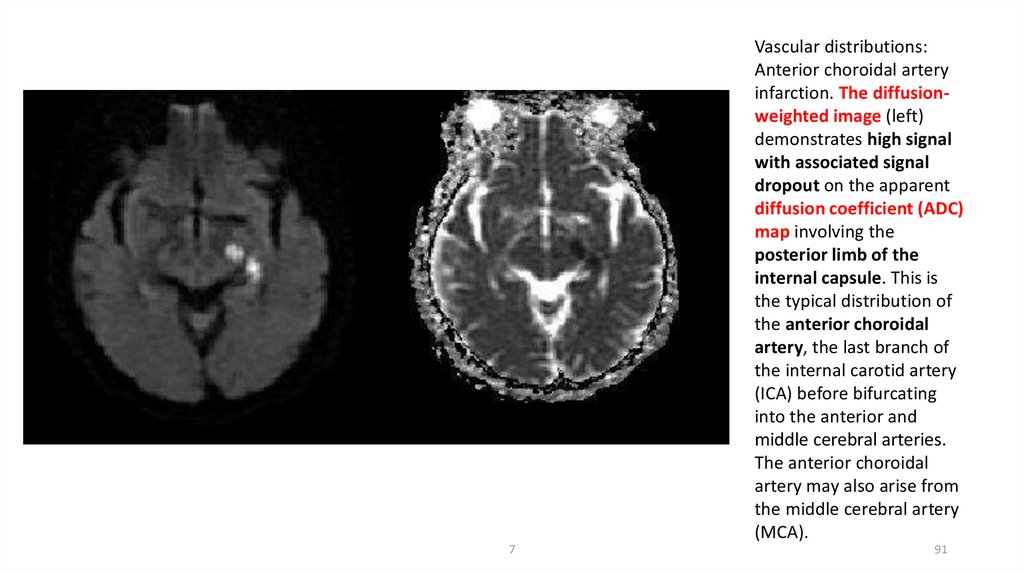
Vascular distributions:Anterior choroidal artery
infarction. The diffusionweighted image (left)
demonstrates high signal
with associated signal
dropout on the apparent
diffusion coefficient (ADC)
map involving the
posterior limb of the
internal capsule. This is
the typical distribution of
the anterior choroidal
artery, the last branch of
the internal carotid artery
(ICA) before bifurcating
into the anterior and
middle cerebral arteries.
The anterior choroidal
artery may also arise from
the middle cerebral artery
(MCA).
7
91
92.
The diffusion-weighted MRIreveals a region of hypointensity
in the distribution of the right
middle cerebral artery. Flanking
the anterior and posterior
regions of this abnormality are
regions of hyperintensities,
which represent regions of new
infarct. The contiguity of these
regions suggests that they are
extensions of the old infarct.
4
92
93.
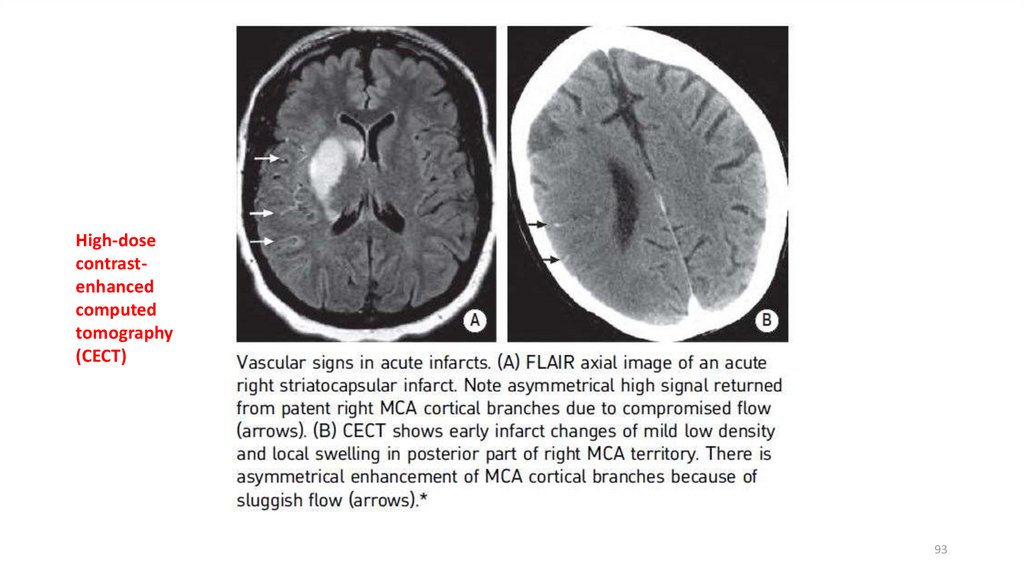
High-dosecontrastenhanced
computed
tomography
(CECT)
93
94.
9495.
9596.
9697.
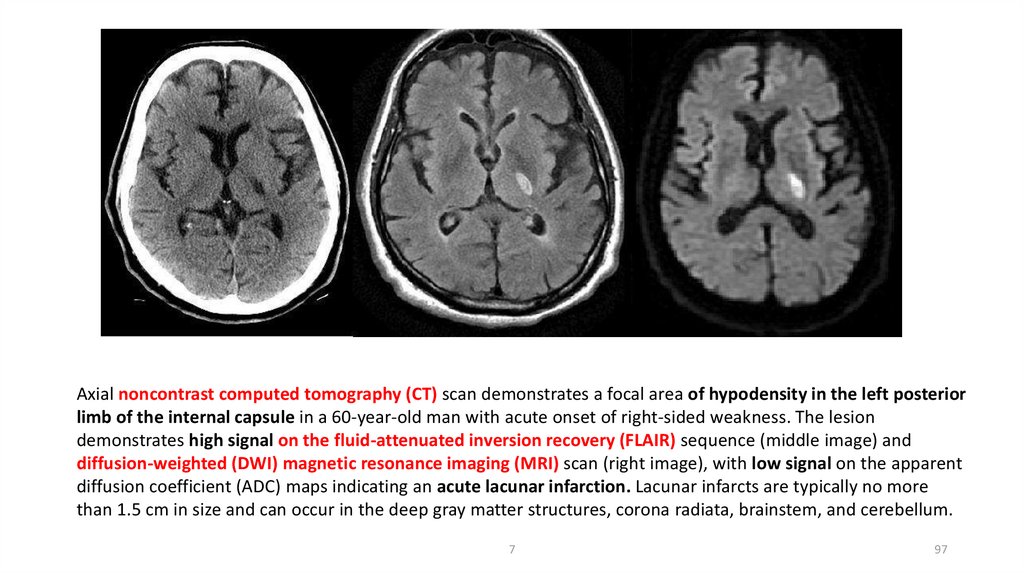
Axial noncontrast computed tomography (CT) scan demonstrates a focal area of hypodensity in the left posteriorlimb of the internal capsule in a 60-year-old man with acute onset of right-sided weakness. The lesion
demonstrates high signal on the fluid-attenuated inversion recovery (FLAIR) sequence (middle image) and
diffusion-weighted (DWI) magnetic resonance imaging (MRI) scan (right image), with low signal on the apparent
diffusion coefficient (ADC) maps indicating an acute lacunar infarction. Lacunar infarcts are typically no more
than 1.5 cm in size and can occur in the deep gray matter structures, corona radiata, brainstem, and cerebellum.
7
97
98.
Рекомендациях Американской ассоциации сердца/Американской ассоциации инсульта(American Heart Association/American Stroke Association) по раннему уходу за пациентами
с острым ишемическим инсультом, опубликованных в журнале «Stroke» в марте 2018 г.
• Визуализирующие методы исследования головного мозга
1. Всем пациентам, госпитализированным предположительно с острым инсультом, сразу же после доставки в клинику
рекомендуется выполнить визуализирующее исследование головного мозга с оценкой полученных результатов. В
большинстве случаев для принятия решения о дальнейшем лечении достаточно оценки результатов неконтрастной
компьютерной томографии. (I; B-NR)
2. Работу в клинике рекомендуется организовать таким образом, чтобы результаты визуализирующего исследования
головного мозга могли быть получены в течение 20 мин после доставки по крайней мере у 50% пациентов, которым,
возможно, понадобится внутривенное введение альтеплазы или выполнение механической тромбэктомии. (I; B-NR)
3. В текущее время нет достаточных доказательств для определения пороговых значений жесткости гипоаттенюации
(проницаемости) компьютерно-томографического исследования у пациентов с ишемическим инсультом, поэтому она не
может рассматриваться в качестве критерия для отсрочки внутривенного применения альтеплазы. (III: не рекомендуется; B-R)
4. Признаки гиперденсивности средних мозговых артерий по данным компьютерной томографии не являются критерием
несвоевременного назначения внутривенного введения альтеплазы пациентам, соответствующим другим критериям этого
назначения. (III: не рекомендуется; B-R)
5. Рутинное использование магнитно-резонансной визуализации для исключения микроизлияний в мозге после
внутривенного применения альтеплазы не рекомендуется. (III: не рекомендуется; B-NR)
6. Использование критериев визуализирующих исследований в целях отбора пациентов для лечения с внутривенным
введением альтеплазы при инсульте, время начала которого неизвестно (наступивший во сне), вне пределов научных
исследований не рекомендуется. (III: не рекомендуется; B-NR)
98
99.
7. Выполнение мультимодальной компьютерной томографии и магнитно-резонансного исследования недолжно задерживать начало внутривенного введения альтеплазы. (III: вредно; B-NR)
8. Пациентам, соответствующим критериям назначения эндоваскулярной терапии, рекомендуется
проводить неинвазивное внутричерепное сосудистое исследование во время первичной оценки данных
визуализирующего исследования, но при этом не следует задерживать внутривенное введение
альтеплазы. (І; А)
9. Компьютерную ангиографию для выявления окклюзии крупных сосудов рекомендовано проводить
пациентам, соответствующим критериям эндоваскулярной терапии, не дожидаясь определения уровня
креатинина в сыворотке крови, если в анамнезе отсутствует почечная недостаточность. (IIа; B-NR)
10. Визуализирующее исследование экстракраниальных отделов внутренних сонных артерий и
позвоночных артерий, помимо внутричерепного кровообращения, рекомендовано для планирования
механической тромбэктомии и оценки пригодности пациентов. (IIa; C-EO)
11. Использование прочих методов визуализации, помимо компьютерной томографии и ангиографии
или магнитно-резонансной томографии и ангиографии (таких как перфузионное исследование), для
отбора претендентов для механической тромбэктомии менее чем за 6 ч до проведения вмешательства
не рекомендуется. (III: не рекомендуется; B-R)
12. При остром ишемическом инсульте с окклюзией крупных сосудов бассейна сонной артерии между 6м и 24-м часом с начала развития симптомов диффузионно-взвешенную магнитно-резонансную
томографию, компьютерную томографическую перфузию или магнитно-резонансную перфузию
рекомендуется проводить исключительно со вспомогательной целью, для отбора пациентов на
выполнение механической тромбэктомии при условии, что правила проведения стандартной
визуализации и других критериев отбора, эффективность которых подтверждена в рандомизированных
клинических исследованиях, были строго соблюдены. (I; A)
13. Оценка состояния коллатерального кровообращения может быть критерием пригодности пациентов
к выполнению механической тромбэктомии. (IIb; C-LD)
99
100.
100101.
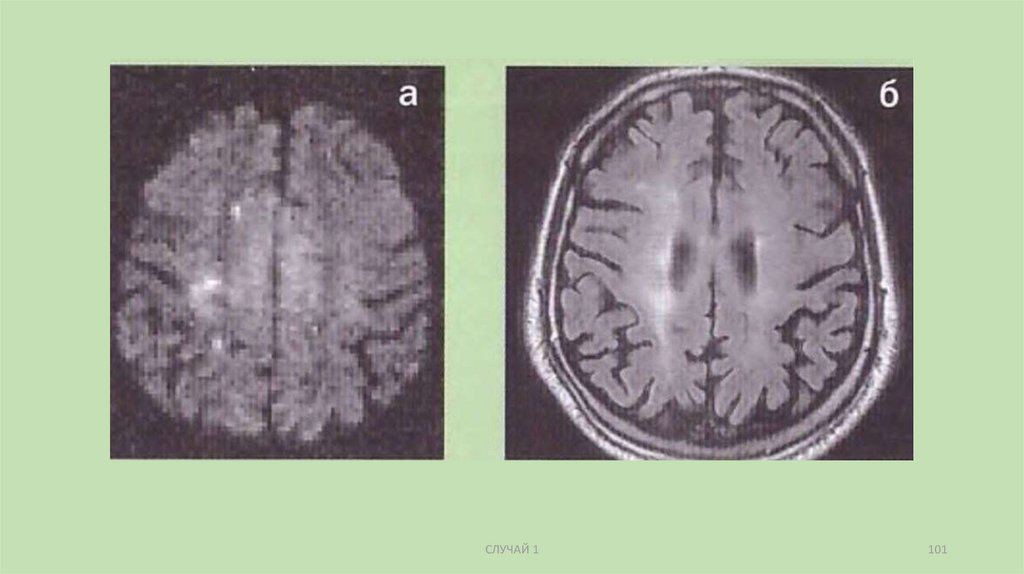
СЛУЧАЙ 1101
102.
СЛУЧАЙ 1102
103.
СЛУЧАЙ 2103
104.
СЛУЧАЙ 2104
105.
СЛУЧАЙ 2105
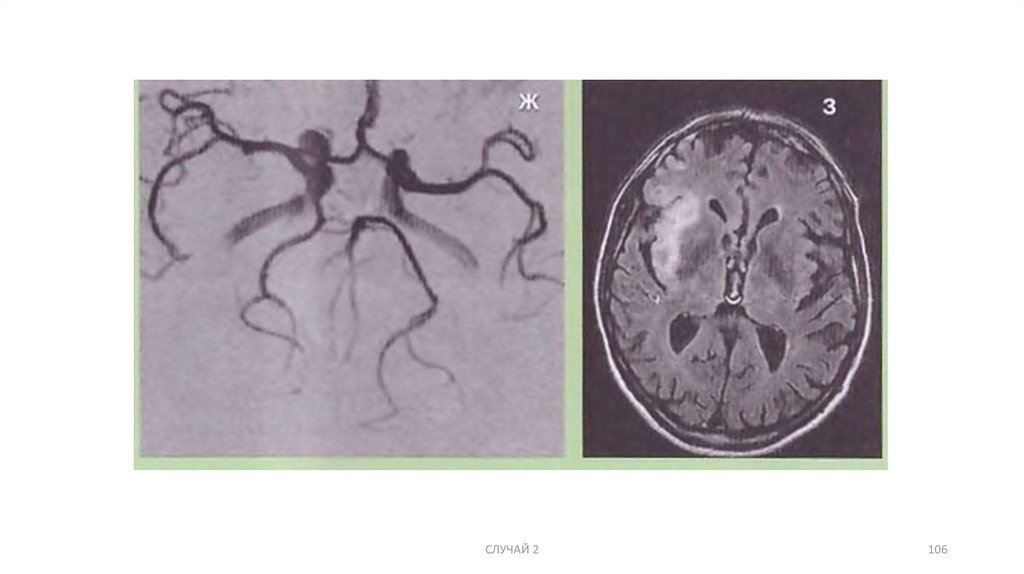
106.
СЛУЧАЙ 2106
107.
МРТ/PWI• Изображения с контрастным усилением показывают усиление артерии с последующим усилением паренхимы.
Артериальное усиление может быть очень ранним (у> 50% пациентов) и связано с медленным кровотоком; обычно он
исчезает через 1 неделю.
• Паренхиматозное усиление отличается полным и неполным инфарктом.
При полном инфаркте он начинается через 5-7 дней после инсульта и сохраняется в течение нескольких месяцев.
При неполном инфаркте он может наблюдаться в течение 2-4 часов и, как правило, более интенсивно, чем при полном
инфаркте.
• Хотя обычные последовательности МРТ чаще всего не показывают признаков инсульта в острой фазе, обычная МРТ может
показывать признаки внутрисосудистого тромба, такие как отсутствие кровотока на T2-WI, гиперинтенсивность сосудов на
FLAIR и гипоинтенсивный сосудистый признак на gradient-recalled echo sequence.
• На контрастных изображениях артериальное усиление обычно сохраняется в течение острой фазы, в то время как
усиление паренхимы обычно оценивается в конце этой фазы при полном инфаркте. При неполном инфаркте усиление
паренхимы обычно происходит раньше.
• В течение этого периода происходит реперфузия и наблюдаются петехиальные и явные кровоизлияния, обычно через 2448 часов после начала инсульта. Обычно петехиальные кровоизлияния вызывают явление «запотевания» из-за продуктов
распада гемоглобина, которое маскирует инфаркт на T1-WI и T2-WI.
• На изображениях с контрастным усилением артериальное усиление обычно разрешается к этому времени, и усиление
паренхимы обычно сохраняется на протяжении этой фазы.
• Усиление паренхимы коры, как правило, имеет форму гириформы, тогда как подкорковое усиление обычно представляет
собой однородную центральную структуру.
4
107
108.
ЛИТЕРАТУРА1.
https://radiographia.info/article/ishemicheskiy-insult-golovnogo-mozga (Laura M. Allen, Anton N. Hasso, Jason Handwerker,
Hamed Farid, RadioGraphics 2012; 32:1285–1297; doi: 10.1148/rg.325115760)
2.
http://24radiology.ru
3.
Diagnostic Radiology Essensials, Grant, Griffin 2013
4.
https://emedicine.medscape.com/article/1155506-overview
5.
Гусев, Коновалов, Скворцова Том 1. Неврология 4-ое издание дополненное, 2015
6.
https://radiopaedia.org/articles/ischaemic-stroke?lang=gb
7.
https://emedicine.medscape.com/article/1916852-overview
8.
Основы и принципы лучевой диагностики : учеб.-метод. пособие / А. И. Алешкевич [и др.]. – Минск: БГМУ, 2015. – 60 с.
9.
http://www.southsudanmedicaljournal.com/archive/august-2016/how-to-interpret-an-unenhanced-ct-brain-scan.-part-1basic-principles-of-computed-tomography-and-relevant-neuroanatomy.html
10.
Топический диагноз в неврологии по Петеру Дуусу, 2016
11.
Бова: Ишемические инсульты, статья
12.
https://laesus-de-liro.livejournal.com/47372.html
108































































 Медицина
Медицина








