Похожие презентации:
Оксиды. Классификация и химические свойства
1. Тема: «Оксиды. Классификация и химические свойства».
2. Оксиды-это сложные вещества, которые состоят из двух элементов, одним из которых является кислород.
Общая формула оксидов:ЭnOm
3.
4.
5. Несолебразующими называют такие оксиды, которые не взаимодействуют ни с кислотами, ни с щелочами и не образуют солей.
Примеры несолеобразующихоксидов: NO; N2O; CO; SiO.
6.
Солеобразующиминазываются оксиды,
которые взаимодействуют с
кислотами или с щелочами
с образованием соли и
воды.
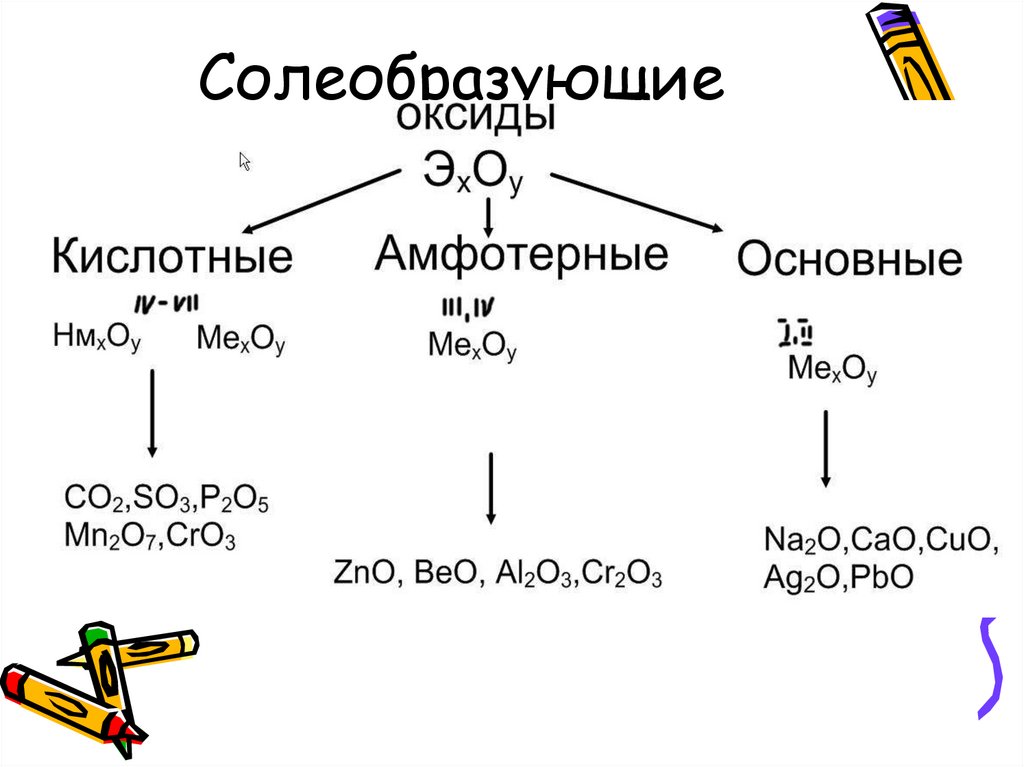
7. Солеобразующие оксиды:
8. Кислотные оксиды-это такие оксиды, которым соответствуют кислоты (оксиды неМе или металлов с валентностью 3-7) CO2 - H2CO3
SO2-H2SO3Mn2O7-HMnO4
9.
Нерастворимый в водекислотный оксид
SiO2
10. Типичные реакции кислотных оксидов
Кислотный оксид +щёлочь→соль + вода (реакция
обмена).
SO3+2KOH→K2SO4+H2O
CO2+Ca(OH)2→CaCO3+H2O
Кислотный оксид +
вода→кислота
(реакция соединения)
11. Основные оксиды-это такие оксиды, которым соответствуют основания (Ме с валентностью- 1 и 2)
K2O – KOHLi2O-LiOH
Sr(OH)2
BaO- Ba(OH)2
SrO-
12. Типичные реакции основных оксидов
• Основный оксид + кислота→соль +вода
(реакция обмена)
CuO + H2SO4→CuSO4 + H2O
K2O +2HCl→2KCl + H2O
Основный оксид +
вода→щёлочь
(реакция соединения)
13. Общие свойства оксидов:
Основный оксид + кислотныйоксид→ соль
(реакция соединения)
Li2O + CO2 → Li2CO3
SO2 + MgO → MgSO3
14. Задания для закрепления изученной темы:
1).Какие из перечисленных веществявляются оксидами?
КОН; SiO2; H2SO4; CaO; NaCl; N2O3;
Fe2O3; Zn(OH)2; Al2O3.
2)Какие из перечисленных веществ
являются основными и
кислотными оксидами? Дать им
названия.
Li2O; SO3; FeO; Mn2O7;CO2; BaO; SiO2
15. Задание 3:Осуществить следующие превращение:
алюминий→оксид алюминия→гидроксид
алюминия→бромид
алюминия→алюминий.
Напишите уравнения реакций.














 Химия
Химия








