Похожие презентации:
Азотсодержащие гетероциклические соединения
1. Азотсодержащие гетероциклические соединения
2.
Азотсодержащие гетероциклическиесоединения - органические соединения, содержащие в
своих молекулах циклы, в образовании которых принимают
участие неуглеродные атомы (гетероатомы).
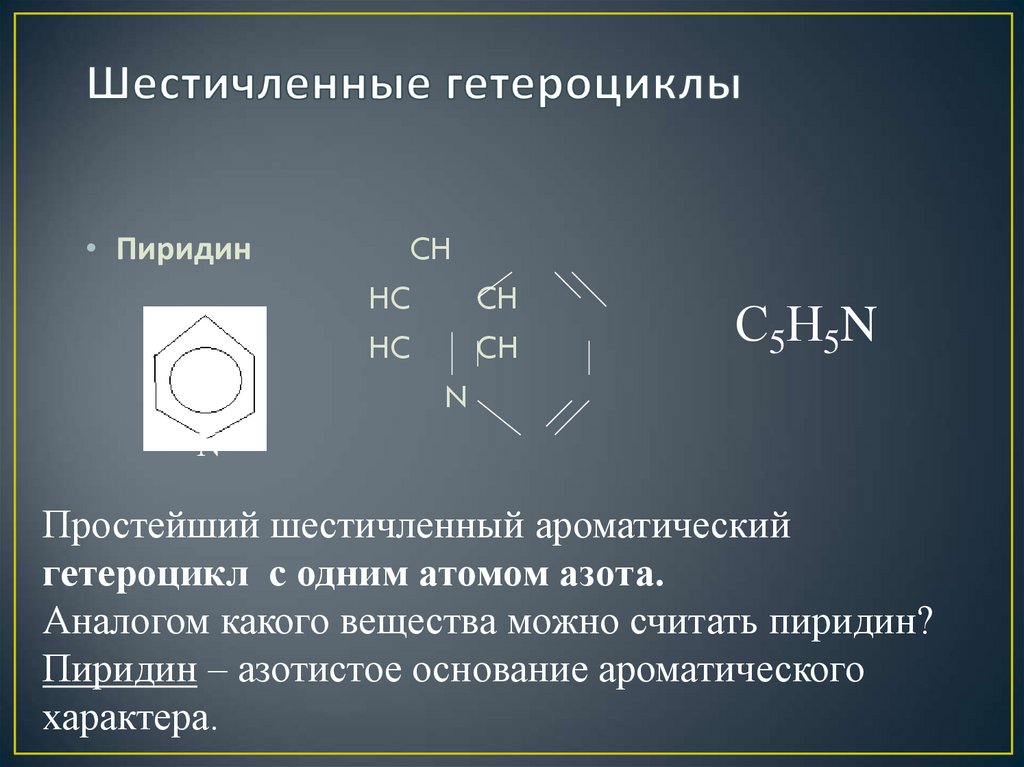
3. Шестичленные гетероциклы
• ПиридинCH
HC
CH
HC
CH
N
С5Н5N
N
Простейший шестичленный ароматический
гетероцикл с одним атомом азота.
Аналогом какого вещества можно считать пиридин?
Пиридин – азотистое основание ароматического
характера.
4. Строение пиридина
• По электронному строению напоминает бензол. Всеатомы в sp2-гибридизации. Шесть негибридных
электронов (по одному от каждого атома) образуют пэлектронную ароматическую систему.
• Две гибридные орбитали атома азота образуют связи с
атомами углерода, а третья содержит неподеленную
электронную пару.
• Какими свойствами может обладать пиридин?
5. Физические свойства и получение пиридина
бесцветная жидкость,
немного легче воды,
с резким неприятным запахом,
с водой смешивается в любых соотношениях.
выделяют из каменноугольной смолы.
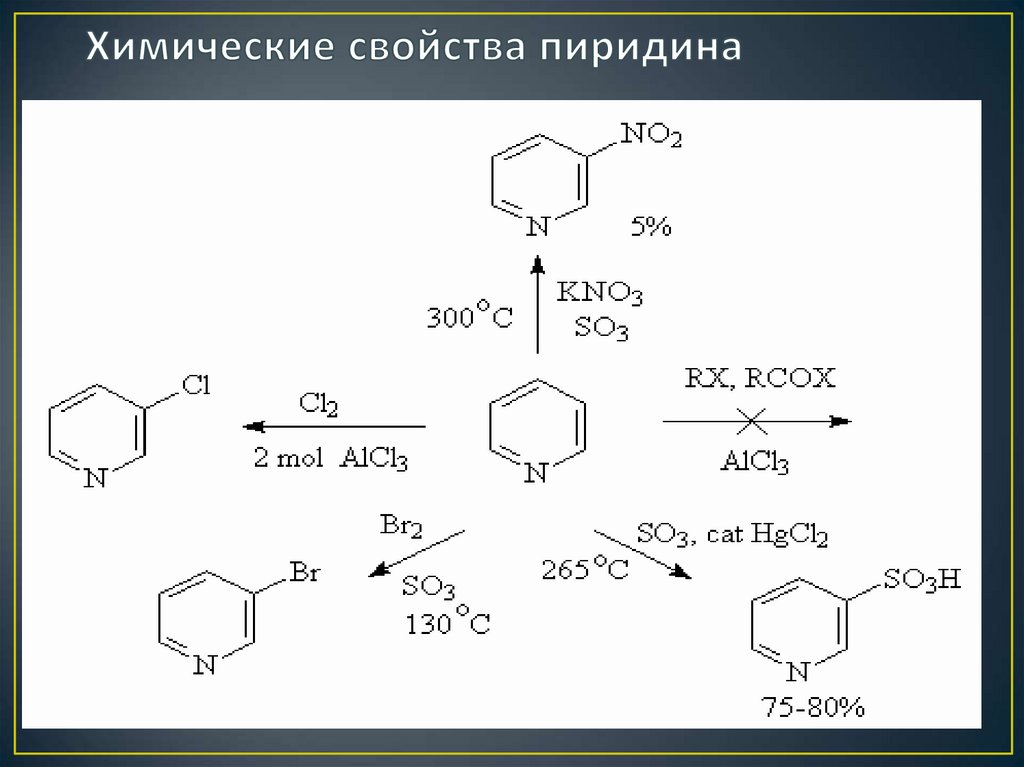
6. Химические свойства пиридина
• Чем определяются химические свойства пиридина?• Наличием ароматической системы – реакции
электрофильного замещения и гидрирования.
• Наличием атома азота с неподеленной электронной
парой – основные свойства.
7. Химические свойства пиридина
8. Основные свойства пиридина
• Более слабое основание, чем алифатические амины.Водный раствор окрашивает лакмус в синий цвет.
• C5H5N+H2O —> [C5H5NH]OH
гидроксид пиридина
• При взаимодействии с сильными кислотами образует
соли пиридиния.
• C5H5N+HCl —> [C5H5NH]Cl
хлорид пиридина
9. Ароматические свойства пиридина
• Активность в реакциях электрофильного замещения ниже,чем бензола из-за большой электроотрицательности атома
азота.
• Нитруется при 300 0С с низким выходом.
• C5H5N+H2SO4 —> [C5H4N]HSO3+H2O
сульфопиридин
• C5H5N+HNO3 —> [C5H4N]NO2+H2O
нитропиридин
10. Ароматические свойства пиридина
• При гидрировании пиридина образуется пиперидин, которыйпредставляет собой циклический вторичный амин и является
гораздо более сильным основанием, чем пиридин.
• C5H5N + 3H2 —> C5H11N пиперидин
• Гексагидропиридин, шестичленный насыщенный цикл с
одним атомом азота.
Бесцветная жидкость с аммиачным запахом, смешивается с
водой, а также с большинством органических растворителей,
образует азеотропную смесь с водой (35% воды по массе,
Tкип 92.8°C) Входит в виде структурного фрагмента в
фармацевтические препараты и алкалоиды. Получил своё
название от латинского названия черного перца Piper nigrum, из
которого впервые был выделен.
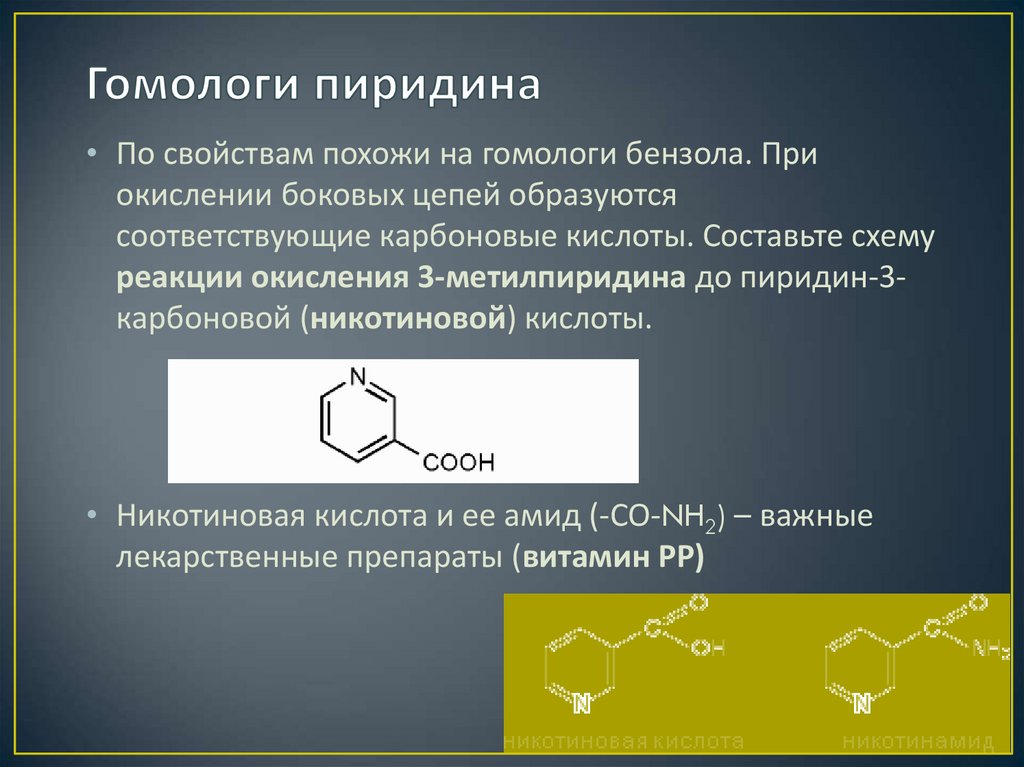
11. Гомологи пиридина
• По свойствам похожи на гомологи бензола. Приокислении боковых цепей образуются
соответствующие карбоновые кислоты. Составьте схему
реакции окисления 3-метилпиридина до пиридин-3карбоновой (никотиновой) кислоты.
• Никотиновая кислота и ее амид (-СО-NH2) – важные
лекарственные препараты (витамин РР)
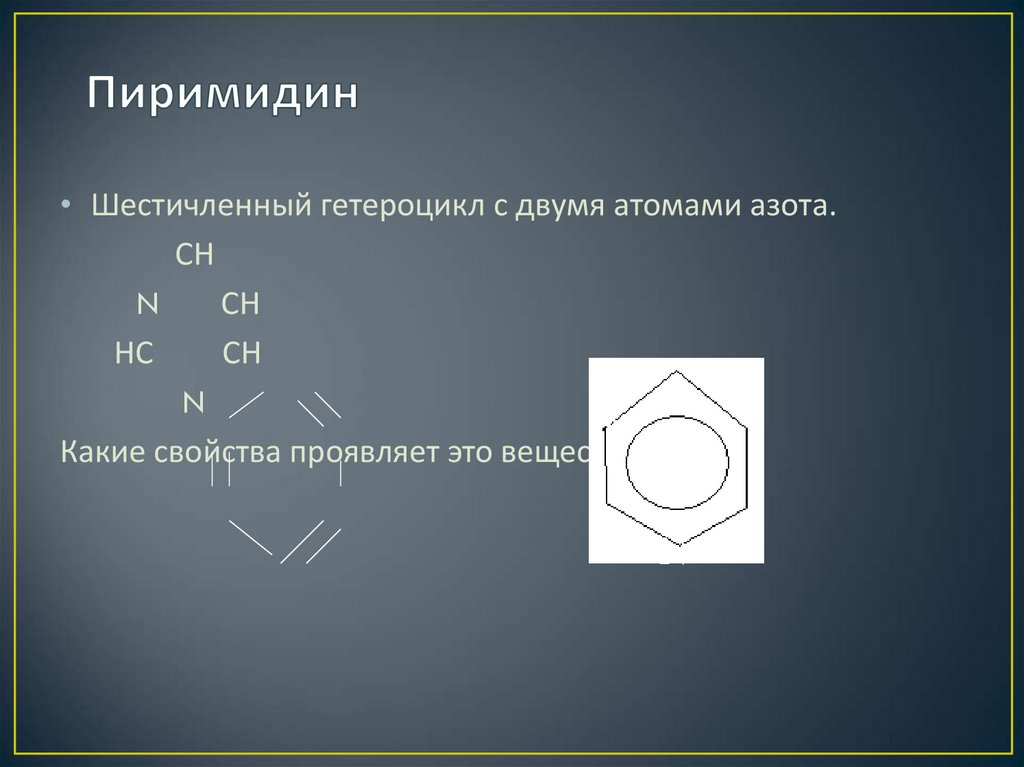
12. Пиримидин
• Шестичленный гетероцикл с двумя атомами азота.СН
N
СН
НС
СН
N
N
Какие свойства проявляет это вещество?
N
13. Свойства пиримидина
• Благодаря наличию в кольце двухэлектроотрицательных атомов азота, пиридин менее
активен в реакциях электрофильного замещения, чем
пиридин.
• Его основные свойства выражены слабее, чем у
пиридина.
• Основное значение – родоначальник класса
пиримидиновых оснований!
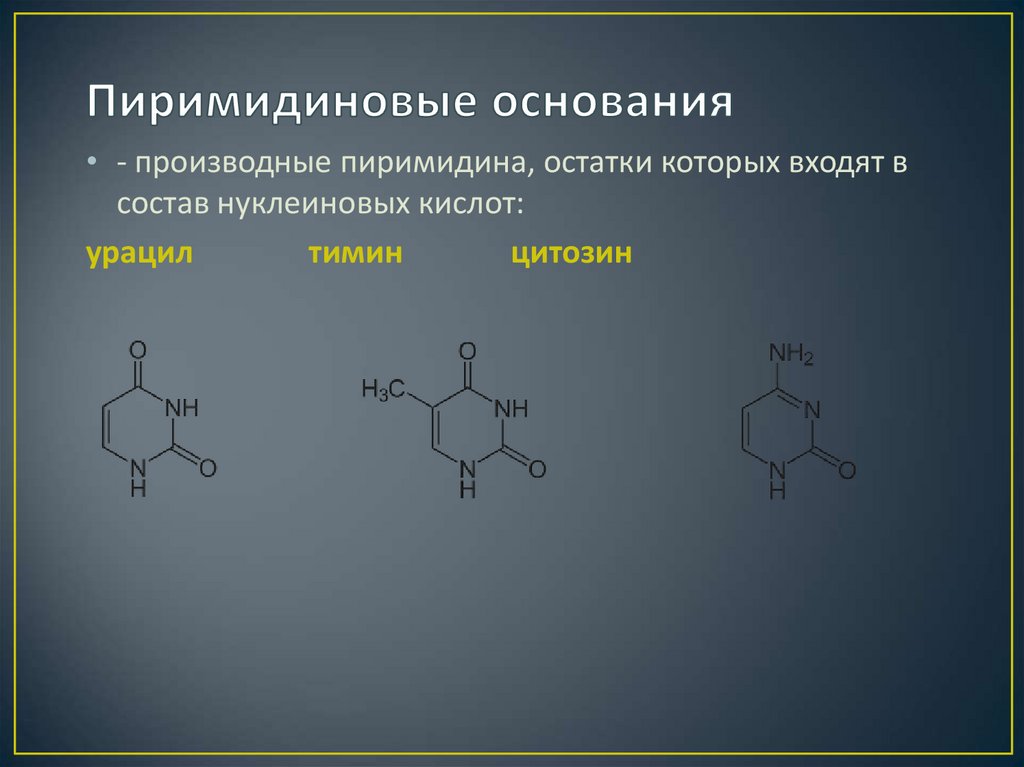
14. Пиримидиновые основания
• - производные пиримидина, остатки которых входят всостав нуклеиновых кислот:
урацил
тимин
цитозин
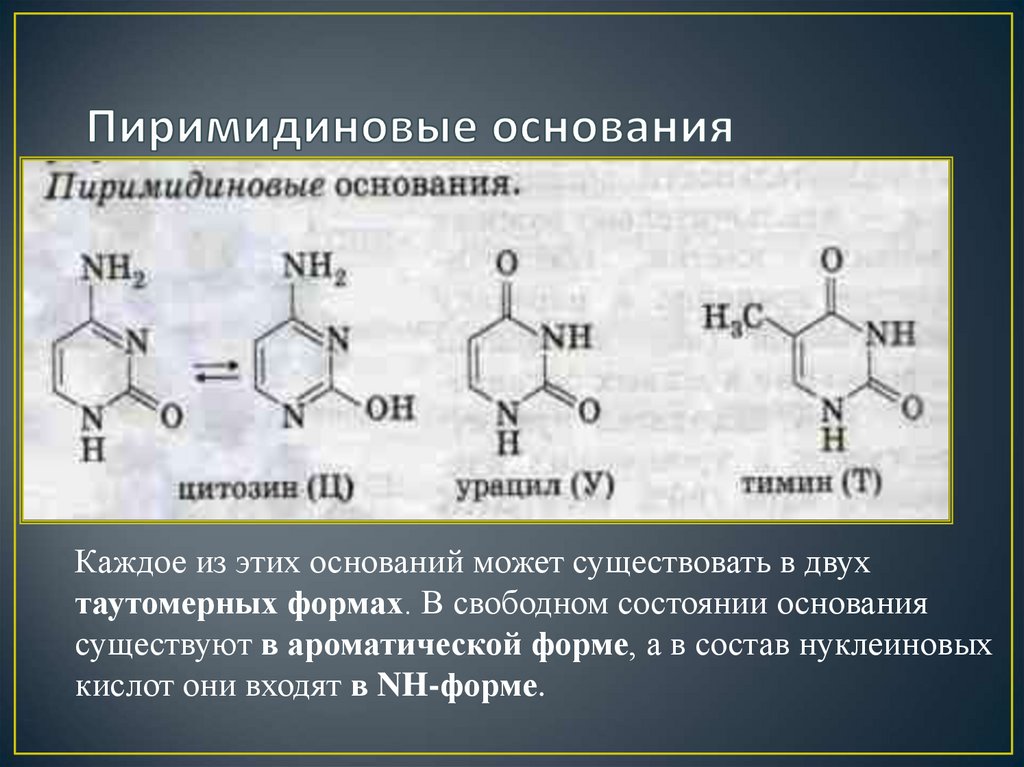
15. Пиримидиновые основания
Каждое из этих оснований может существовать в двухтаутомерных формах. В свободном состоянии основания
существуют в ароматической форме, а в состав нуклеиновых
кислот они входят в NH-форме.
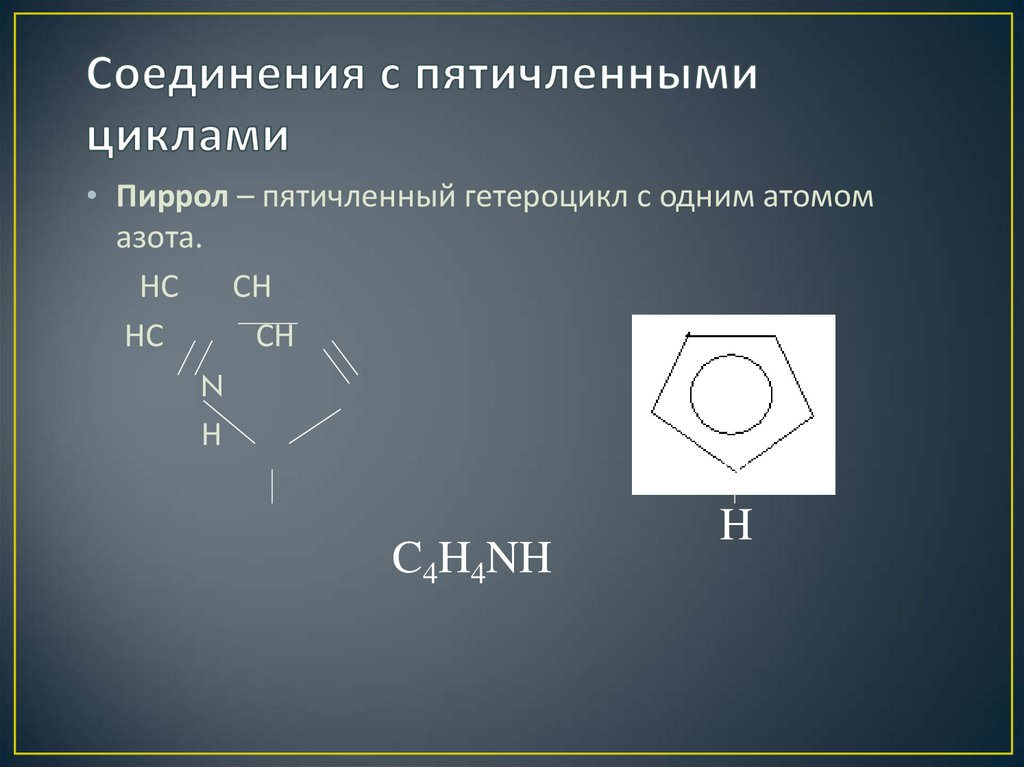
16. Соединения с пятичленными циклами
• Пиррол – пятичленный гетероцикл с одним атомомазота.
НС
СН
НС
СН
N
Н
C4H4NH
N
H
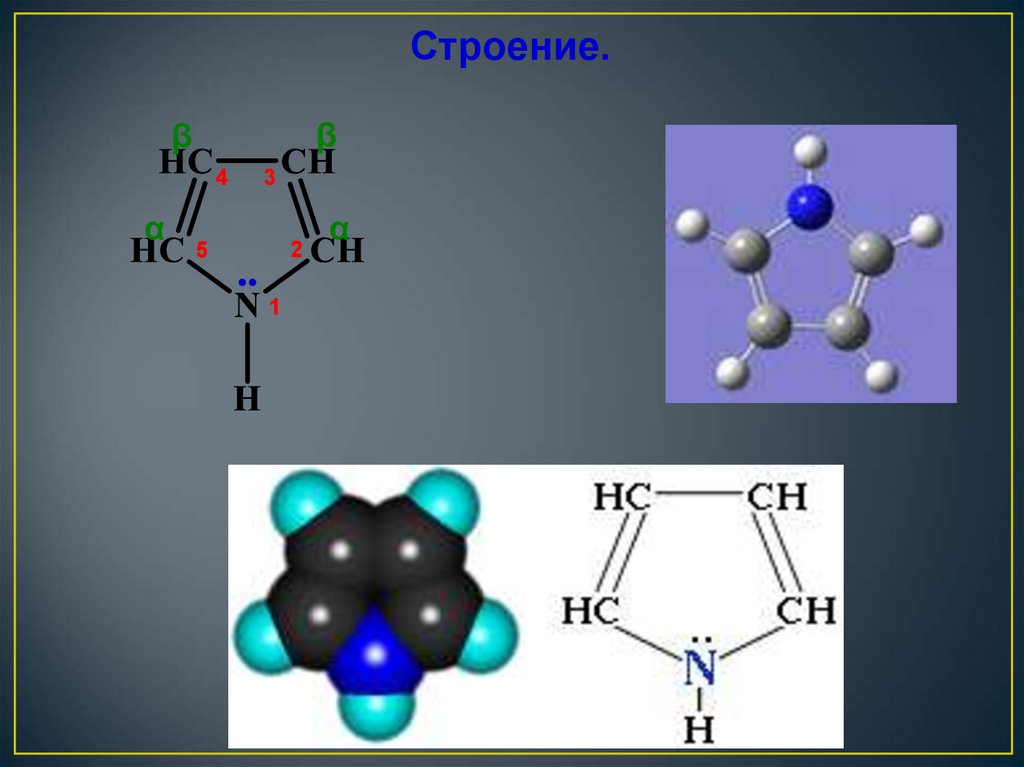
17. Строение молекулы пиррола
• Атомы углерода и атом азота находятся в состоянии в sp2гибридизации. Четыре негибридизованных электрона атомауглерода и неподелённая электронная пара атома азота образуют
п-электронную ароматическую систему.
• Электронная пара атома азота в пирроле входит в состав
ароматической системы, поэтому пиррол практически лишен
основных свойств.
18.
Строение.β
β
4
α
3
2
5
●
1
α
19. Физические свойства пиррола
Бесцветная жидкость
Запах напоминает запах хлороформа
Слабо растворим в воде (<6%)
Растворим в органических растворителях
На воздухе быстро окисляется и темнеет
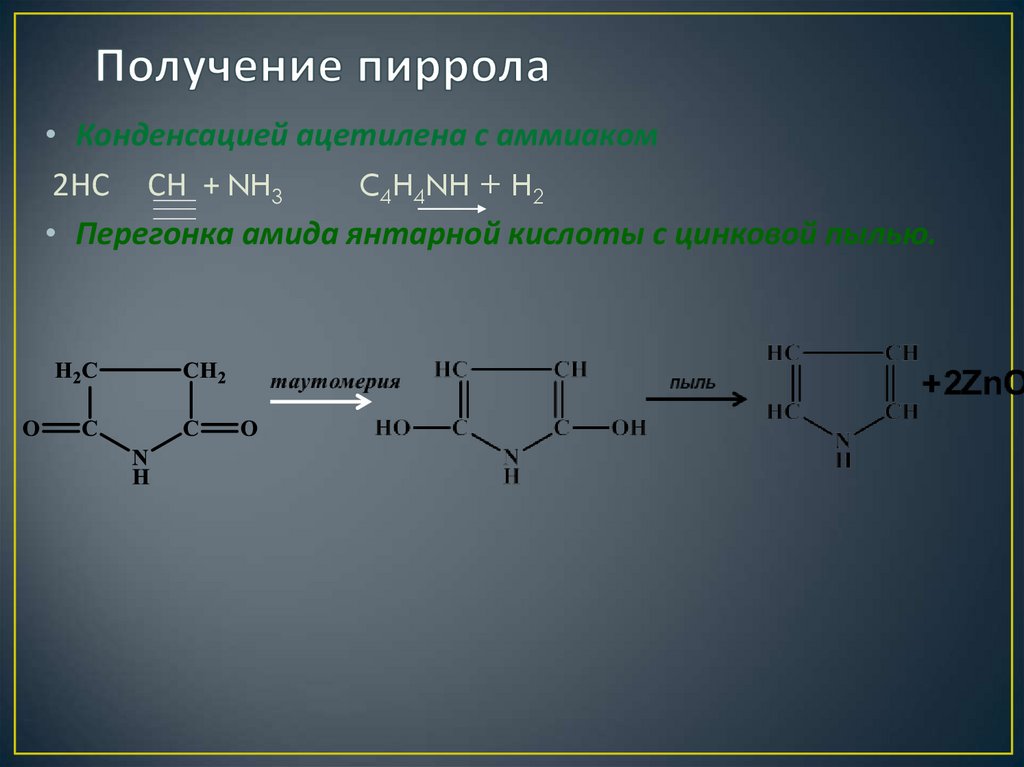
20. Получение пиррола
• Конденсацией ацетилена с аммиаком2НС СН + NH3
C4H4NH + H2
• Перегонка амида янтарной кислоты с цинковой пылью.
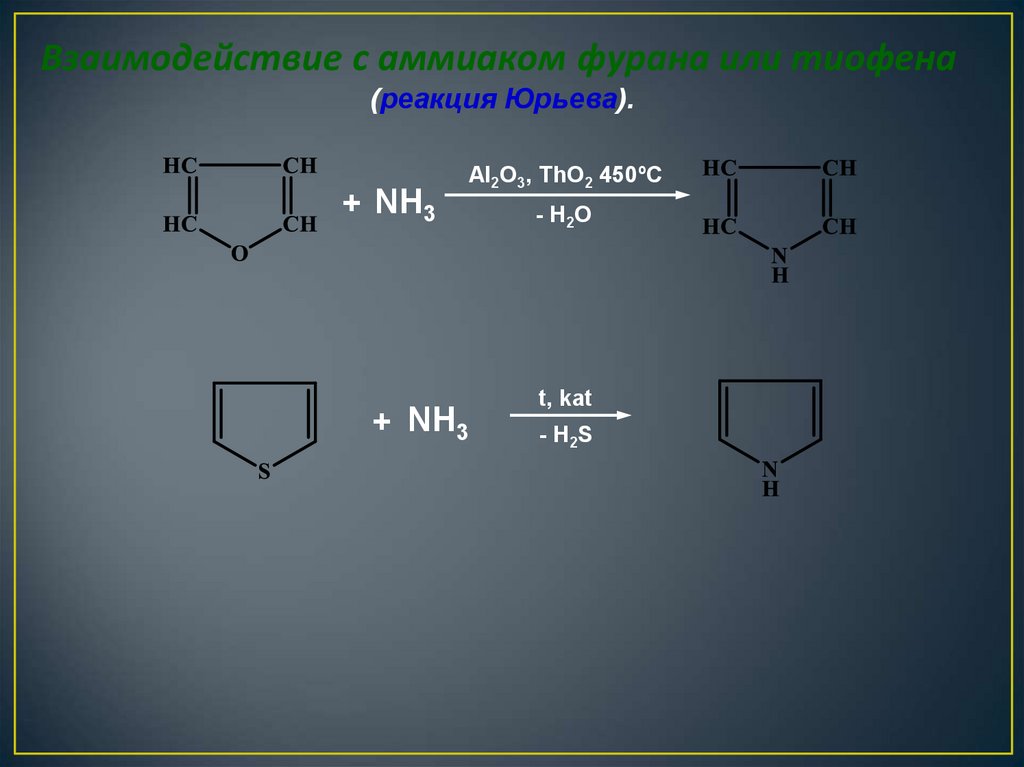
21.
Взаимодействие с аммиаком фурана или тиофена(реакция Юрьева).
+ NH3
Al2O3, ThO2 450ºC
+ NH3
- H2O
t, kat
- H2S
22. Химические свойства пиррола
• В кислой среде неустойчив: сильные минеральныекислоты могут вытягивать электронную пару атома
азота из ароматической системы.
• Проявляет свойства очень слабой кислоты. Реагирует с
калием, образуя пиррол-калий.
• 2C4H4NH+2K —> 2C4H4NK+H2
пиррол калий
• Как ароматическое соединение вступает в реакции
электрофильного замещения у альфа-атома углерода.
• C4H4NH+4I2 —> C4I4NH++4 HI
тетраиод пиррол
• Йодол, антисептик
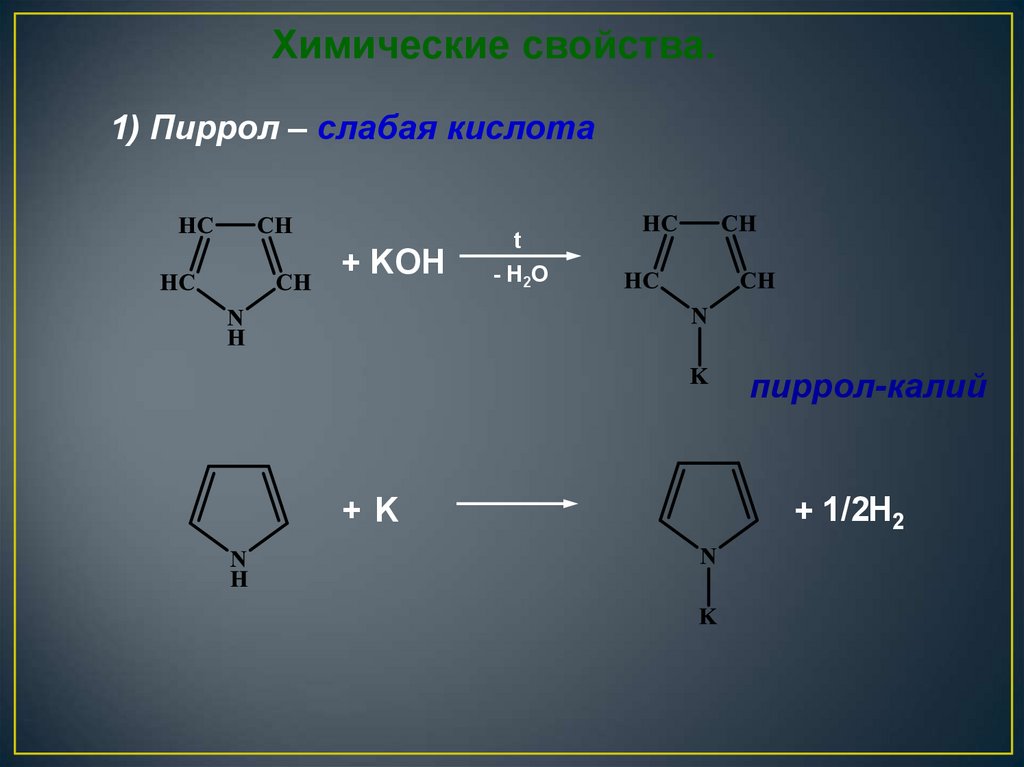
23.
Химические свойства.1) Пиррол – слабая кислота
+ KOH
t
- H2O
пиррол-калий
+K
+ 1/2H2
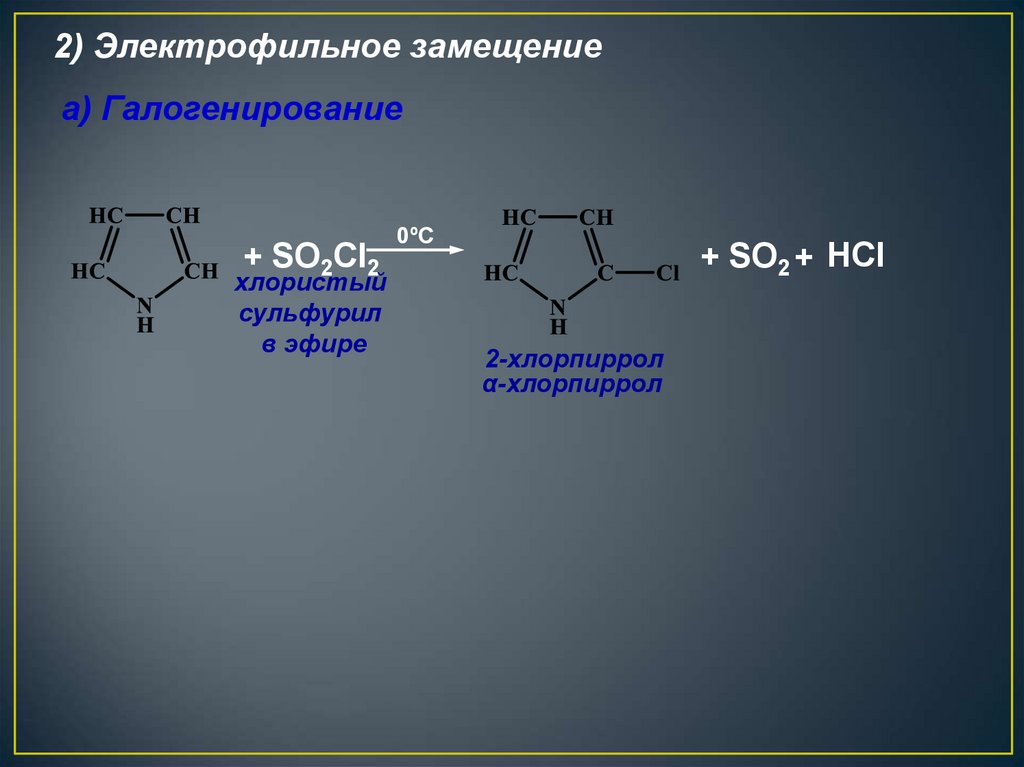
24.
2) Электрофильное замещениеа) Галогенирование
+ SO2Cl2
хлористый
сульфурил
в эфире
0ºС
+ SO2 + HCl
2-хлорпиррол
α-хлорпиррол
25.
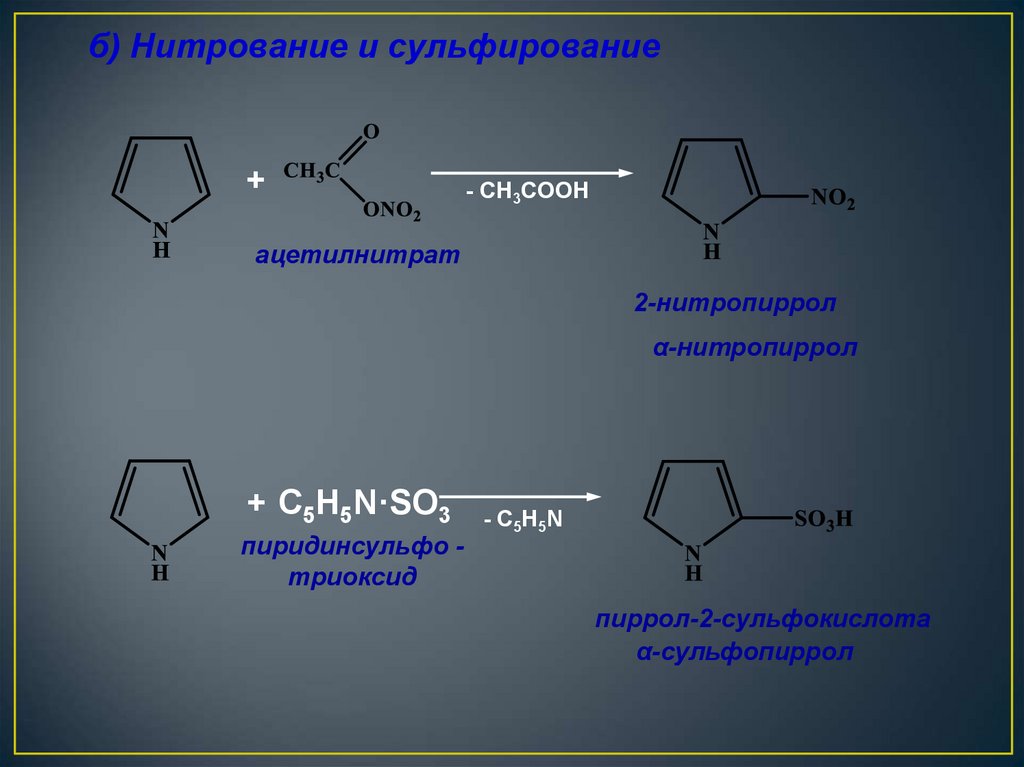
б) Нитрование и сульфирование+
- CH3COOH
ацетилнитрат
2-нитропиррол
α-нитропиррол
+ C5H5N·SO3
пиридинсульфо триоксид
- C5H5N
пиррол-2-сульфокислота
α-сульфопиррол
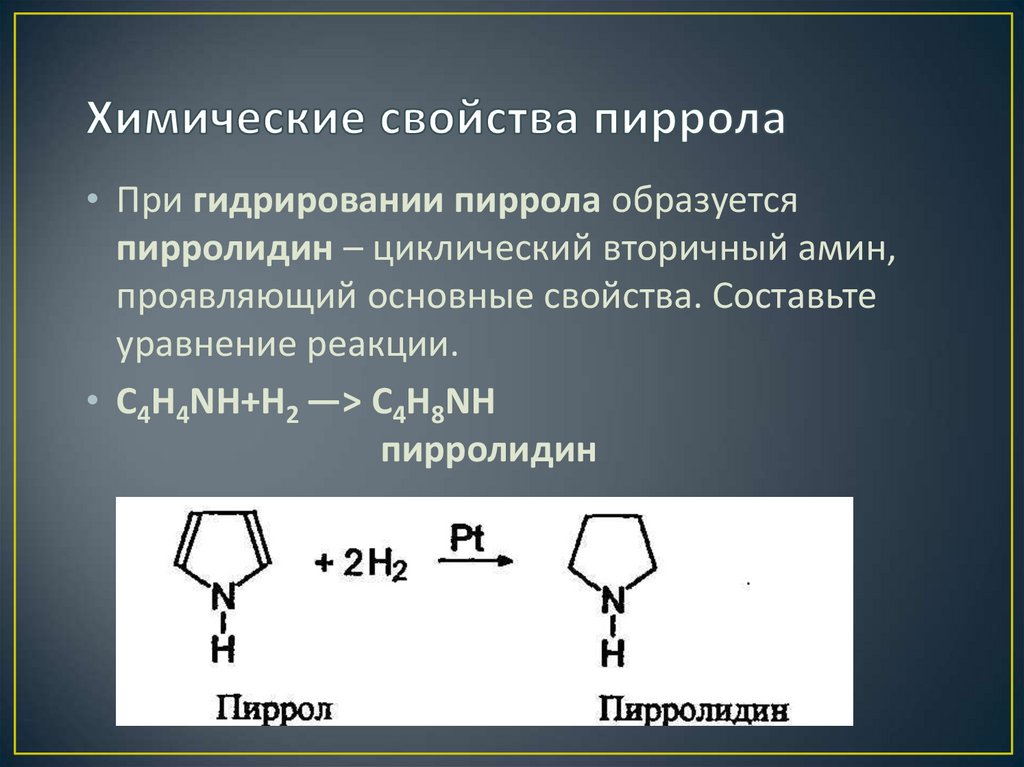
26. Химические свойства пиррола
• При гидрировании пиррола образуетсяпирролидин – циклический вторичный амин,
проявляющий основные свойства. Составьте
уравнение реакции.
• C4H4NH+H2 —> C4H8NН
пирролидин
27.
Взаимопревращения гетероциклических соединенийРеакции Юрьева
Al2O3, ThO2
450-500°С
H2O
H2S
NH3
H2O
H2S
NH3
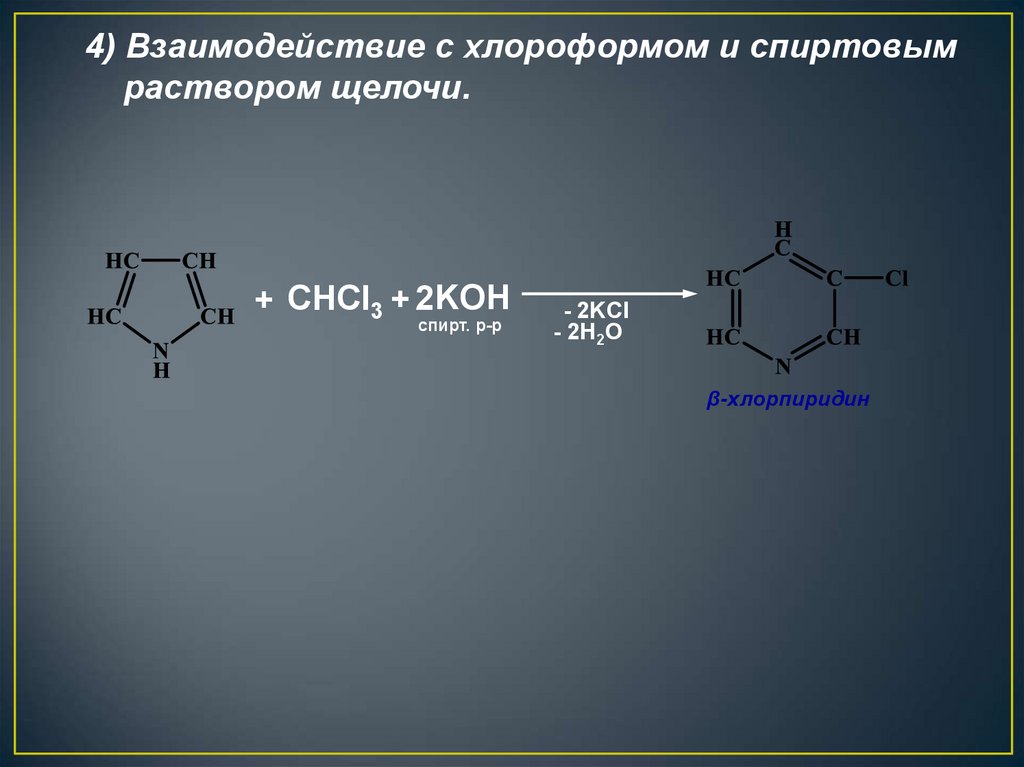
28.
4) Взаимодействие с хлороформом и спиртовымраствором щелочи.
+ CHCl3 + 2KOH
спирт. р-р
- 2KCl
- 2H2O
β-хлорпиридин
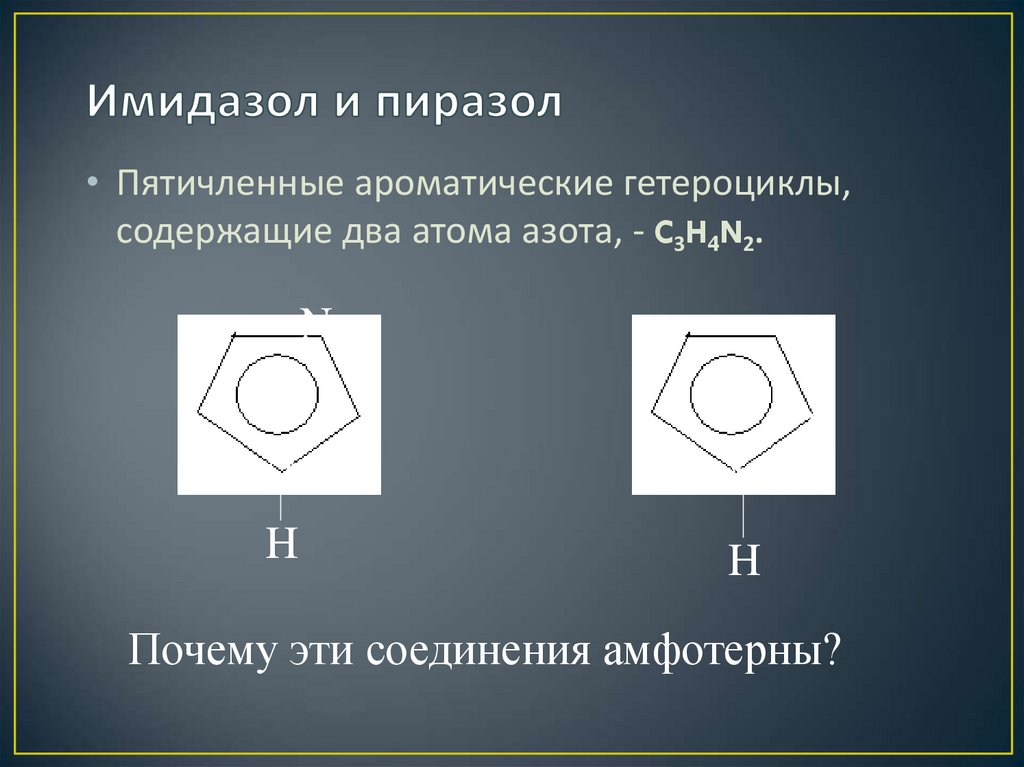
29. Имидазол и пиразол
• Пятичленные ароматические гетероциклы,содержащие два атома азота, - C3H4N2.
N
N
N
N
H
H
Почему эти соединения амфотерны?
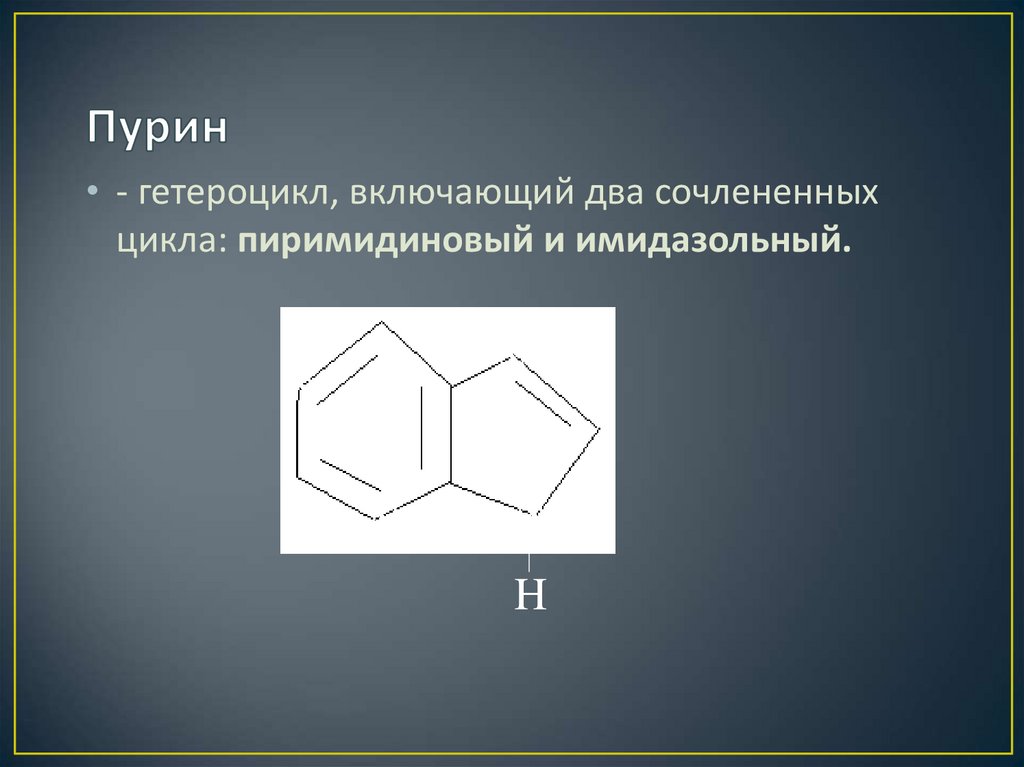
30. Пурин
• - гетероцикл, включающий два сочлененныхцикла: пиримидиновый и имидазольный.
N
N
N
N
H
31. Строение и свойства пурина
• Ароматическая система пурина включает в себя 10 пиэлектронов (8 электронов двойных связей и дванеподеленных пиррольного атома азота).
• Пурин –амфотерное соединение. Почему?
• Основные свойства – атомы азота шестичленного
цикла, кислотные свойства – группа NH пятичленного
цикла.
• Основное значение пурина – родоначальник класса
пуриновых оснований!
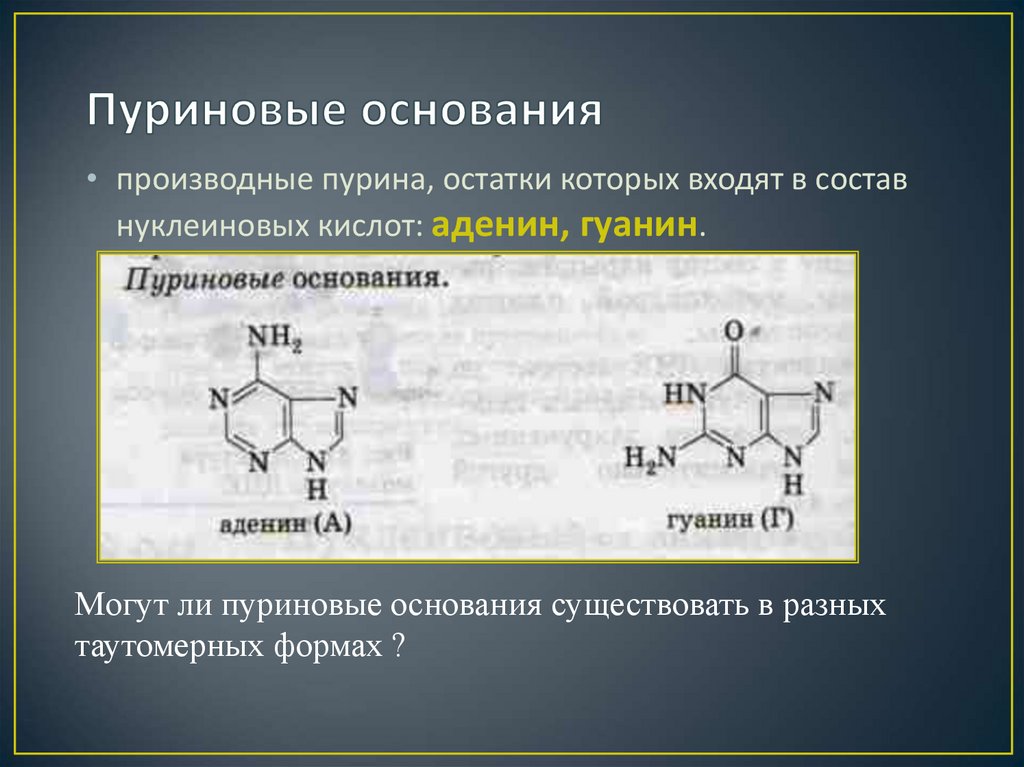
32. Пуриновые основания
• производные пурина, остатки которых входят в составнуклеиновых кислот: аденин, гуанин.
Могут ли пуриновые основания существовать в разных
таутомерных формах ?
33.
• Домашнее задание: прочитать пар.39, записатьопределение АГС. Найти применение
пиридина в интернете и записать в тетрадь
(кратко).















 Химия
Химия








