Похожие презентации:
Приготовление раствора сахара
1.
2.
Раствор — это однородная система,состоящая из частиц растворённого вещества,
растворителя и продуктов их взаимодействия.
3.
cахарcахароза
(С12Н22О11)
4.
5.
Отношение массы растворённого вещества к общеймассе раствора называют массовой долей
растворённого вещества.
6.
Проведём\ опыт
200 мл
20
70 мл
5
7.
Проведём\ опыт
=
+
70 мл
25 г
8.
Расчёт массовой доли\ сахара в растворе
=
+
70 мл
Дано:
25 г
Решение.
V(H2O) = 70 мл
m(С12Н22О11) = 25 г
w(С12Н22О11) — ?
m(p-p) = m(С12Н22О11) + m(Н2О).
m(Н2О) = V(Н2О) ∙ ρ(Н2О), ρ(Н2О) = 1 г/мл.
m(Н2О) = 70 мл ∙ 1 г/мл = 70 г.
m(р-р) = m(С12Н22О11) + m(Н2О) = 25 г + 70 г = 95 г.
Ответ: w(С12Н22О11) = 0,26, или 26%.
9.
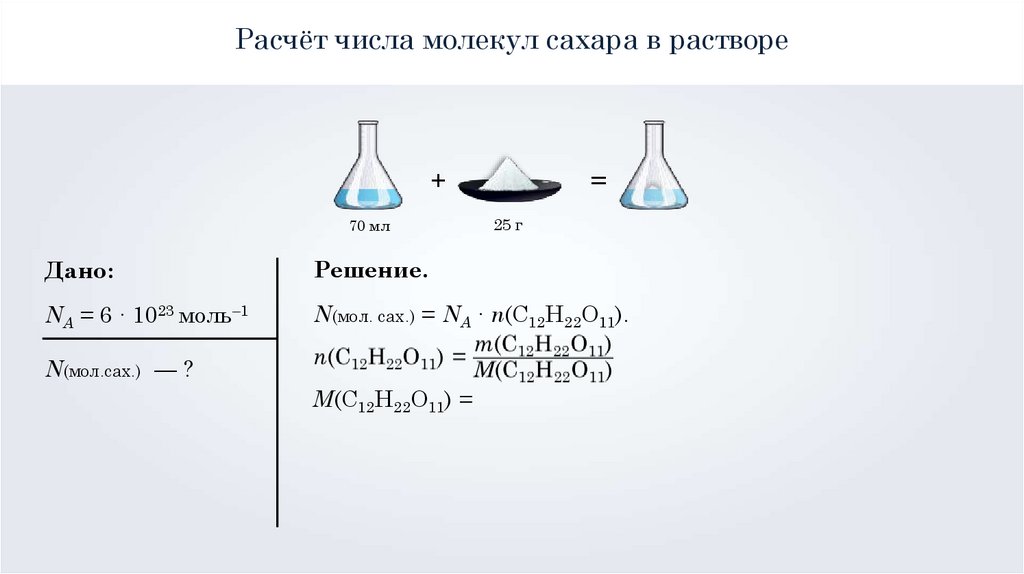
Расчёт числа молекул\ сахара в растворе
=
+
70 мл
25 г
Дано:
Решение.
NA = 6 ∙ 1023 моль–1
N(мол. сах.) = NA ∙ n(С12Н22О11).
N(мол.сах.) — ?
M(С12Н22О11) =
10.
M(С12Н22О11) = 12 ∙ 12 + 1 ∙ 22 + 16 ∙ 11 = 342 г/моль.11.
Расчёт числа молекул\ сахара в растворе
=
+
70 мл
25 г
Дано:
Решение.
NA = 6 ∙ 1023 моль–1
N(мол. сах.) = NA ∙ n(С12Н22О11).
N(мол.сах.) — ?
M(С12Н22О11) = 12 ∙ 12 + 1 ∙ 22 + 16 ∙ 11 = 342 г/моль.
n(С12Н22О11) = 25 г : 342 г/моль = 0,07 моль.
N(мол. сах.) = 6 ∙ 1023 ∙ 0,07 = 42 ∙ 1021.
Ответ: N(мол. сах.) = 42 ∙ 1021.










 Химия
Химия








