Похожие презентации:
Диамины
1.
Лекция 122.2.3 Диамины
Диамины — углеводороды (алифатические и ароматические), у
которых два атома водорода замещены аминогруппами
H2N CH2 x NH C CH2 y C OH
O
O
Гексаметилендиамин (ГМД)
(1,6-диаминогексан) H2N(CH2)6NH2
Наиболее распространенным промышленным способом получения
гексаметилендиамина является превращение адипиновой кислоты по
следующей схеме:
HOC(CH2)4COH + NH3
NH2C(CH2)4CNH2
-H2O
-H2O
O
O
O
O
+H2
N C(CH2)4C N
H2N(CH2)6NH2
Гексаметилендиамин получают также из бутандиена, который
хлорируют до 1,4-дихлорбутена. Последний обработкой цианистым
натрием переводят в 1,4-дицианбутен, гидрированием которого
получают гексаметилендиамин:
+NaCN
CH2 CH CH CH2 + Cl2
ClCH2 CH CH CH2Cl
-NaCl
NCCH2 CH CH CH2CN
+H2
H2N(CH2)6NH2
2.
Химические свойстваС органическими и неорганическими кислотами
гексаметилендиамин легко образует соли.
Аминогруппы в гексаметилендиамине могут быть
замещены другими функциональными группами,
например, под действием азотистой кислоты образуется
1,6-гексаметиленгликоль
HNO2
H2N CH2 6 NH2
HO CH2 6 OH
Гексаметилендиамин вступает в реакции конденсации и
поликонденсации с альдегидами, кетонами, одно- и двухосновными кислотами.
n H2N CH2 6 NH2 + n HO C CH2 4 C OH
O
O
n H3N+(CH2)6N+H3-OOC(CH2)4COON CH2 N C CH2 4 C
+ 2n H2O
6
H
H O
O n
3.
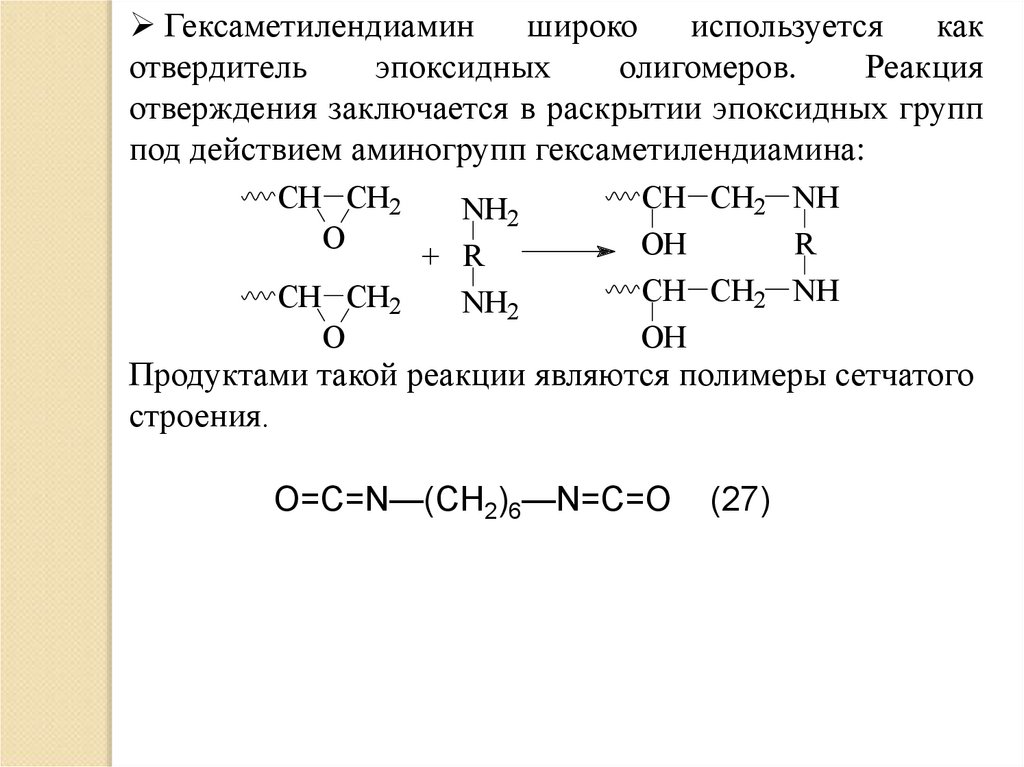
Гексаметилендиаминшироко
используется
как
отвердитель
эпоксидных
олигомеров.
Реакция
отверждения заключается в раскрытии эпоксидных групп
под действием аминогрупп гексаметилендиамина:
CH CH2
O
NH2
+ R
CH CH2
NH2
O
CH CH2 NH
OH
R
CH CH2 NH
OH
Продуктами такой реакции являются полимеры сетчатого
строения.
O=C=N—(CH2)6—N=C=О
(27)
4.
2.3. Мономеры для получения поликарбонатовПоликарбонаты — сложные полиэфиры
угольной кислоты общей формулы
O R O C
O n
Угольная кислота не устойчивое соединение легко
распадается на оксид углерода (IV) и воду
Для синтеза поликарбанатов используют производные
угольной кислоты
1. дихлорангидрид угольной кислоты – фосген Cl C Cl
O
Его получают из угарного газа (оксида углерода (II)) и
хлора на активном угле в качестве катализатора (на свету
при нагревании).
СO + Cl2
Cl C Cl
O
5.
Химические свойстваГазообразный фосген очень медленно гидролизуется парами
воды:
Cl C Cl + H2O
2 HCl + CO2
O
В жидкой фазе гидролиз происходит быстро. Сильные
щелочи мгновенно расщепляют фосген:
2 NaCl + CO2 + H2O
2 NaOH + Cl C Cl
O
Энергично реагирует с аммиаком с
образованием карбамида и хлорида аммония:
Cl C Cl + 4 NH3
H2N C NH2 + 2 NH4Cl
O
O
Реакцией фосгена с диаминами получают диизоцианаты,
которые применяются как мономеры в производстве
полиуретанов:
H2N R NH2 + 2 Cl C Cl
Cl C HN R NH C Cl
-2HCl
-2HCl
O
O
O
O C N R N C O
(27)
6.
С солями карбоновых кислот фосген реагирует собразованием соответствующих ангидридов:
2 RC ONa + Cl C Cl
O
O
O
RC
RC
O
O + 2 NaCl + CO2
Как мономер фосген находит применение при
получении поликарбонатов и полимочевин.
Поликарбонаты образуются поликонденсацией фосгена с
дифенилолпропаном
Для получения полимочевин проводят взаимодействие
фосгена с диаминами:
n H2N R NH2 + n Cl C Cl
O
HN R NH C + 2n HCl
O n
7.
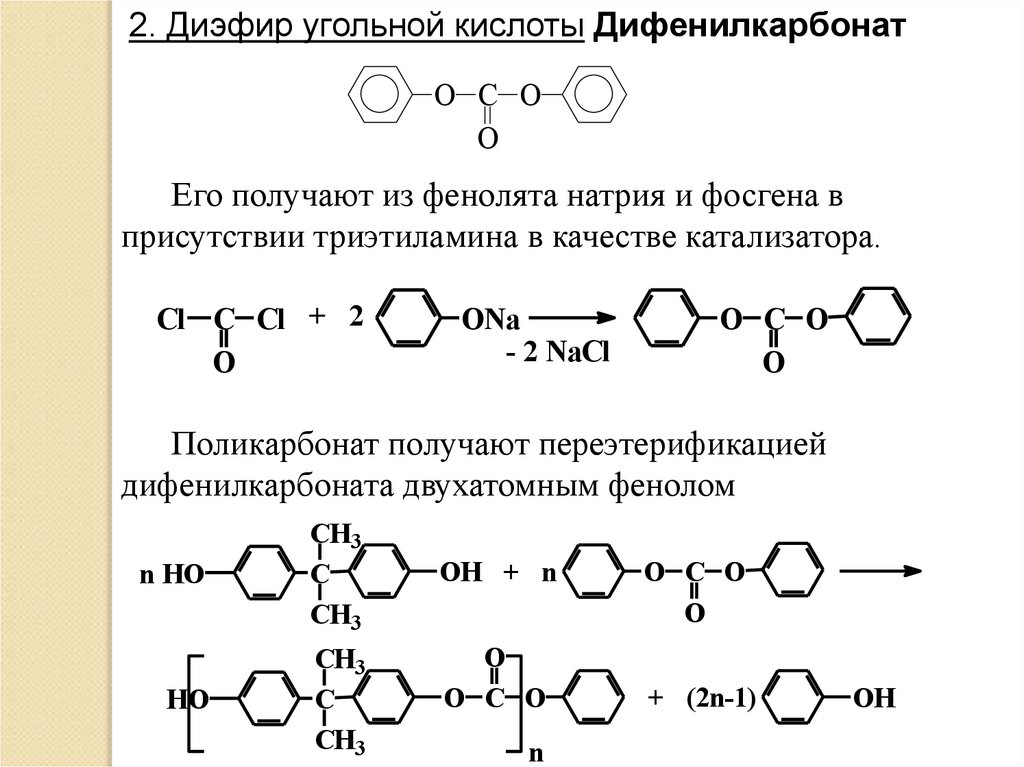
2. Диэфир угольной кислоты ДифенилкарбонатO C O
O
Его получают из фенолята натрия и фосгена в
присутствии триэтиламина в качестве катализатора.
Cl C Cl + 2
O
ONa
- 2 NaCl
O C O
O
Поликарбонат получают переэтерификацией
дифенилкарбоната двухатомным фенолом
n HO
CH3
C
CH3
HO
CH3
C
CH3
OH + n
O
O C O
n
O C O
O
+ (2n-1)
OH
8.
2.4. Мономеры для гомополиконденсацииГидроксикислоты и аминокислоты
HO R COOH
H2N R COOH
9.
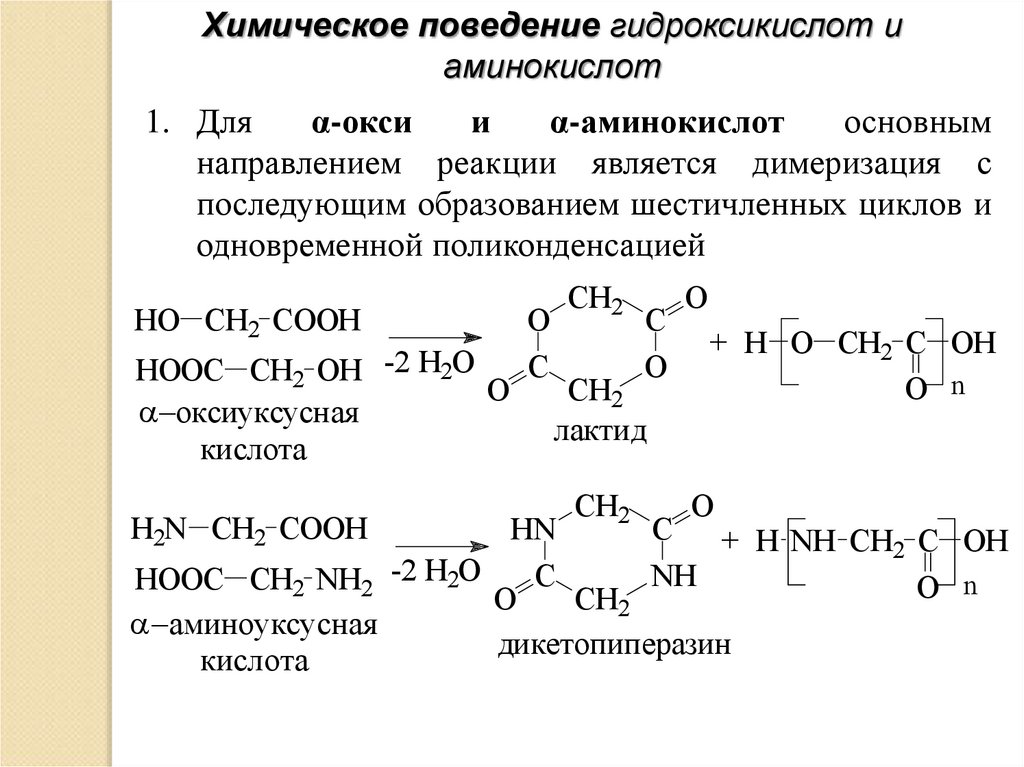
Химическое поведение гидроксикислот иаминокислот
1. Для
α-окси
и
α-аминокислот
основным
направлением реакции является димеризация с
последующим образованием шестичленных циклов и
одновременной поликонденсацией
HO CH2 COOH
HOOC CH2 OH -2 H2O
O
оксиуксусная
кислота
H2N CH2 COOH
O
C
CH2
C
O
CH2
лактид
CH2
O
+ H O CH2 C OH
O n
O
HN
C + H NH CH C OH
2
C
NH
HOOC CH2 NH2 -2 H2O
O n
O
CH2
аминоуксусная
дикетопиперазин
кислота
10.
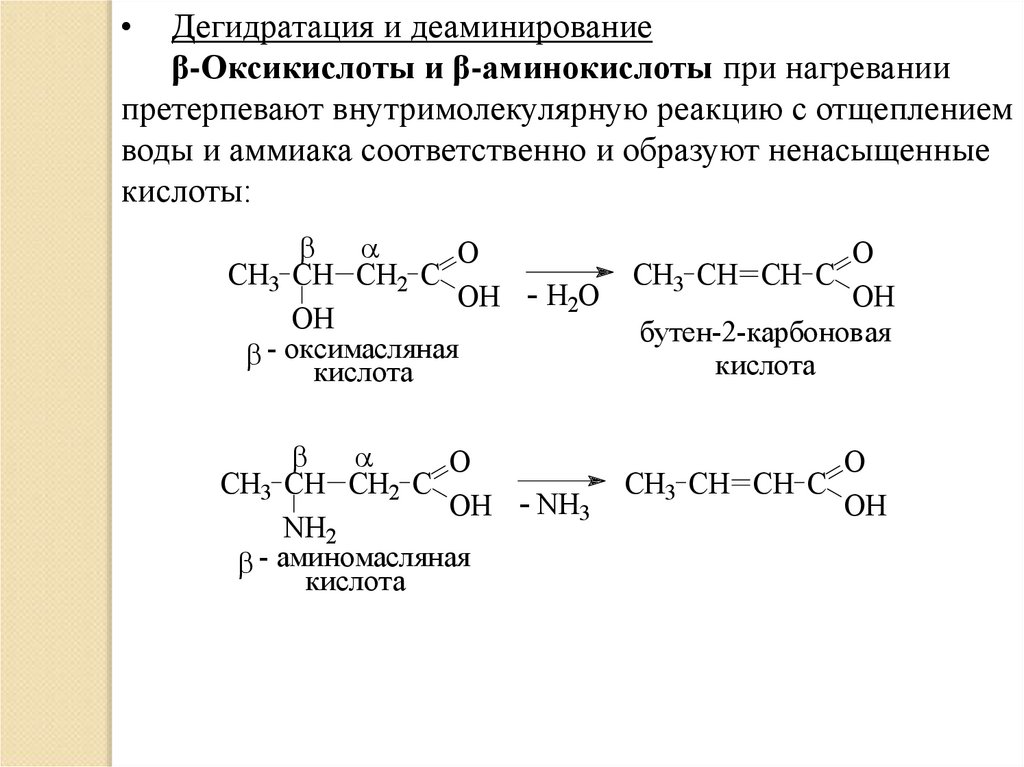
Дегидратация и деаминирование
β-Оксикислоты и β-аминокислоты при нагревании
претерпевают внутримолекулярную реакцию с отщеплением
воды и аммиака соответственно и образуют ненасыщенные
кислоты:
O
СH3 CH CH2 C
OH - H2O
OH
- оксимасляная
кислота
O
СH3 CH CH C
OH
бутен-2-карбоновая
кислота
O
СH3 CH CH2 C
OH - NH3
NH2
- аминомасляная
кислота
O
СH3 CH CH C
OH
11.
3. γ-Окси и γ-аминокислоты образуют устойчивыепятичленные циклы:
O
CH3 СH CH2 CH2 C
OH - H2O
OH
- оксивалериановая
кислота
CH3 СH CH2 CH2 C
O
лактон
O
O
O
СH
CH
CH
C
СH
CH
CH
C
CH3
CH3
2
2
2
2
OH - H2O
NH2
NH
лактам
-аминовалериановая
кислота
4. δ-Аминокислоты образуют устойчивые шестичленные
циклы и в обычных условиях не образуют полимеров.
δ-Оксикислоты
циклизуются
с
одновременной
поликонденсацией.
12.
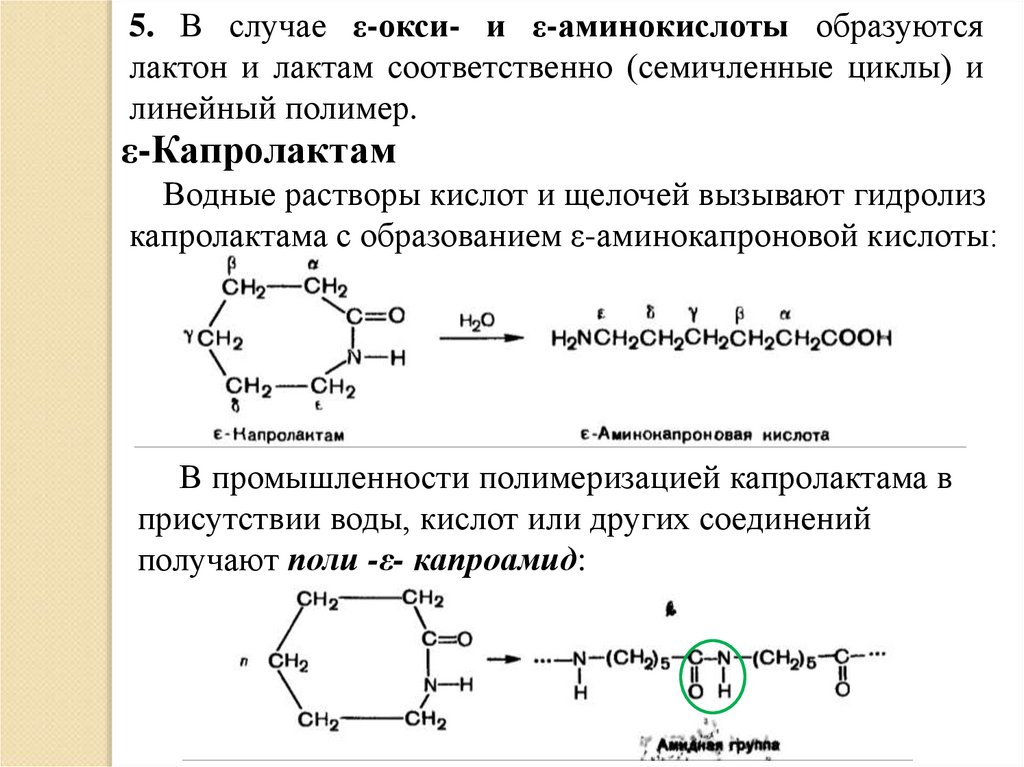
5. В случае ε-окси- и ε-аминокислоты образуютсялактон и лактам соответственно (семичленные циклы) и
линейный полимер.
ε-Капролактам
Водные растворы кислот и щелочей вызывают гидролиз
капролактама с образованием ε-аминокапроновой кислоты:
В промышленности полимеризацией капролактама в
присутствии воды, кислот или других соединений
получают поли -ε- капроамид:
13.
14.
6. Если между функциональными группами больше 6метиленовых групп, как в (ζ-окси и ζ-аминокислотах, то
восьмичленные циклы не образуются, а происходит
только поликонденсация (например, 9-аминононановая и
11-аминоундекановая аминокислоты, по существу,
образуют только полимеры).









 Химия
Химия








