Похожие презентации:
Основы иммунотерапии
1. Государственное бюджетное образовательное учреждение высшего профессионального образования «ПЕРВЫЙ САНКТ-ПЕТЕРБУРГСКИЙ ГОСУДАРСТВЕНН
Государственное бюджетное образовательное учреждениевысшего профессионального образования
«ПЕРВЫЙ САНКТ-ПЕТЕРБУРГСКИЙ ГОСУДАРСТВЕННЫЙ
МЕДИЦИНСКИЙ
УНИВЕРСИТЕТ ИМЕНИ АКАДЕМИКА И.П. ПАВЛОВА»
МИНИСТЕРСТВА ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
КАФЕДРА ИММУНОЛОГИИ
2 ЦИКЛ - КЛИНИЧЕСКАЯ ИММУНОЛОГИЯ
ЗАНЯТИЕ № 11
ОСНОВЫ ИММУНОТЕРАПИИ
2. фронтальный опрос -вопросы
1.Что такое иммунотерапия?
2.
Что такое активная и пассивная иммунотерапия, приведите примеры.
3.
В каких случаях требуется иммунотерапия?
4.
В каких случаях иммунотерапия противопоказана?
5.
Каковы механизмы действия иммунотропных препаратов?
6.
Какие иммунотропные препараты вам известны?
7.
Что такое иммуномодуляторы?
8.
Что такое иммуностимуляторы?
9.
Что такое иммунодепрессанты?
10. Как
оценить эффективность иммунотерапии?
3. Развитие многих заболеваний и нарушение жизненно-важных процессов связано с нарушениями функционирования иммунной системы
10Развитие многих заболеваний и нарушение жизненно-важных
процессов связано с нарушениями функционирования
иммунной системы
иммунная система
9
8
онкология
7
атеросклероз
6
коморбидные заболевания
5
аутоиммунные заболевнаие
4
3
2
1
Эмбриональный
0
период
бластоциста
рождение
Постэмбриональный период
юность
зрелость
старение
4. Основные термины
Иммунотерапия –способ лечения
заболеваний человека с
помощью
фармакологических
средств, направленных
на усиление,
подавление или
замещение функций
иммунной системы
Таргентрая терапия
направлена на
конкретную мишень,
играющую важную
роль в патогенезе
заболевания
(цитокины, рецепторы
и т.д.)
5.
Иммунотропная терапияпрофилактическая
вакцинотерапия.
имуномодуляторы/
иммуностимуляторы.
заместительная
терапия.
Цель проведения терапии:
повышение эффективности
этиотропной
противоинфекционной терапии.
увеличение длительности
периодов ремиссии при
хронических инфекционновоспалительных заболеваниях.
профилактика инфекционных
осложнений при использовании
иммуносупрессивной терапии.
6. Показания к назначению иммунотерапии
ПИДи ВИД
Аллергия
(ограничения)
Аутоиммунитет
Онкология (в
том
числе
лимфопролифератив
ные заболевания)
Инфекционные заболевания
(например, хронические
вирусные инфекции,
микозы и др.).
Профилактика реакций
отторжения трансплантата
Заболевания,
сопровождающиеся
нарушением регенерации.
7. Цель иммунотерапиии
Стабилизацияхронических
процессов.
Замедление
прогрессирования
хронических
заболеваний.
Улучшение
качества
жизни пациентов с
хроническими
воспалительными
заболеваниями.
8. Принципы назначения иммунотерапии
NB:Снижение
показателей
иммунитета у
практически здорового
человека не является
основанием для
назначения
иммунотропных
препаратов.
9. Основные термины
Иммуностимуляторы –
лекарственные
средства,
активирующие:
функции системы
клеточного и/или
гуморального
иммунитета,
иммунные
реакции или
отдельные их
звенья.
Иммунодепрессанты (или
иммуносупрессоры) –
лекарственные средства,
подавляющие иммунные ответ,
применяются для обеспечения
искусственного угнетения
иммунитета (иммуносупрессии).
Назначаются при аутоиммунных
заболеваниях, онкопатологии,
при трансплантации.
10. Основные термины
Иммуномодуляторы-препараты различного
происхождения, обладающие
специфической способностью
стимулировать иммунные
процессы и активировать
клетки моноцитарномакрофагального ряда,
Т и В-лимфоциты.
Иммуномодуляторы способны
восстанавливать функции
иммунной системы.
Действие иммуномодуляторов
зависит от исходного
состояния иммунной
системы пациента и может
быть разнонаправленным:
они нормализуют как
пониженные, так и
повышенные иммунные
показатели.
11. Основные термины
Специальные видылечения и профилактики
заболеваний включают:
Иммунозаместительную
терапию (введение
иммуноглобулинов при
ИД)
АСИТ
(аллергенспецифическую
иммунотерапию –лечение
этиологически
значимыми аллергенами)
Иммунопрофилактику
(вакцины, сыворотки).
12. Механизмы действия иммунотропных средств
Воздействие наодин механизм
иммунной
системы может
привести к
каскаду изменений
во всех ее звеньях.
Не все механизмы
действия
иммунотропных
препаратов
изучены.
Наиболее полно изучены механизмы действия
следующих иммунотропных препаратов:
Создание активного иммунитета с
помощью вакцин.
Создание пассивного иммунитета с
помощью препаратов иммуноглобулинов.
Стимуляция или угнетение синтеза
цитокинов.
Сочетанное иммуномодулирующее
действие и прямое действие на антиген
(противовирусные препараты).
Стимуляция гемопоэза (КСФ)
Таргентная терапия
13.
1885 — Л. Пастер получилвакцину против бешенства
14. Недостатки существующих вакцин
Недостаточная эффективность.Многократность введения.
Побочные реакции.
«Шприцевые» инфекции.
Небольшой срок годности.
Сложность прививочных компаний.
15. Требования к «идеальной» вакцине
Компонентывакцины (антигены),
адъюванты и пр. должны иметь
точно установленную структуру.
Вакцина
должна вводиться один раз.
Вакцина
должна быть комплексной
и создавать иммунитет ко многим
инфекциям.
Вакцина
должна обеспечивать
пожизненный иммунитет у 100%
привитых.
Вакцина
должна быть безопасной и
не обладать побочными действиями.
Вакцина
должна вводиться
неинвазивным методом,
удобным для медицинского
персонала.
Вакцина должна быть
стабильной, иметь
длительный срок хранения.
Технология изготовления
вакцины должна отвечать
современным требованиям.
Вакцина не должна быть
дорогой.
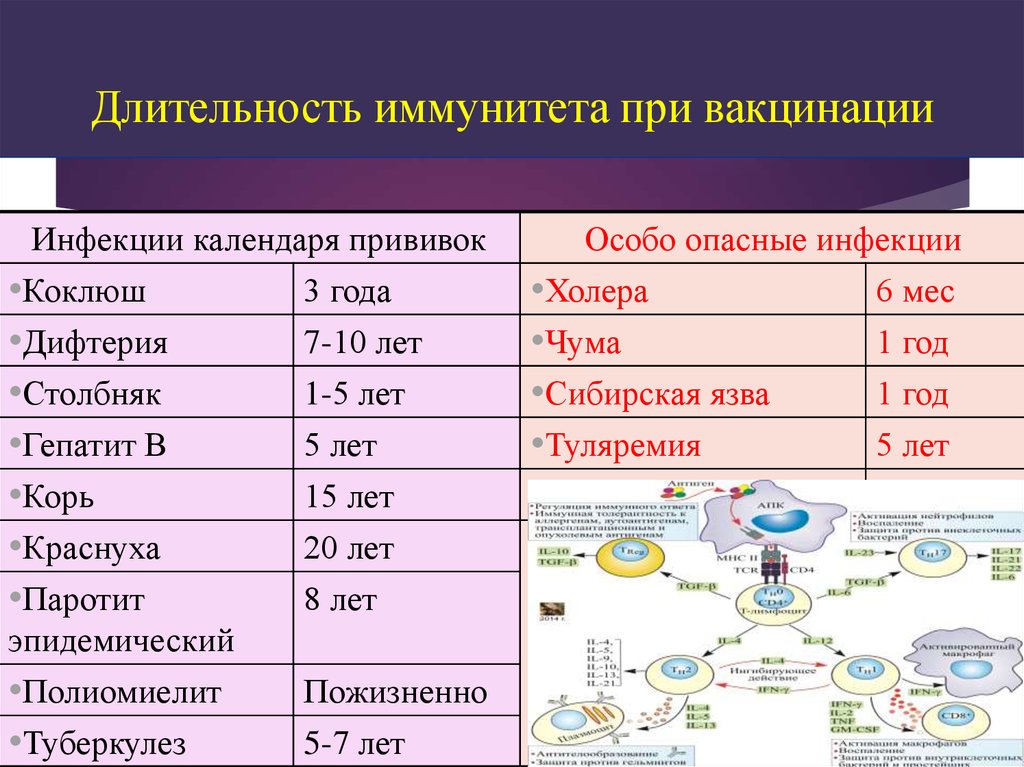
16. Длительность иммунитета при вакцинации
Инфекции календаря прививок•Коклюш
•Дифтерия
•Столбняк
•Гепатит В
•Корь
•Краснуха
•Паротит
3 года
7-10 лет
1-5 лет
5 лет
15 лет
20 лет
8 лет
эпидемический
•Полиомиелит
•Туберкулез
Пожизненно
5-7 лет
Особо опасные инфекции
•Холера
•Чума
•Сибирская язва
•Туляремия
•Бруцеллез
6 мес
1 год
1 год
5 лет
1-2 года
17. Иммунологические механизмы действия вакцин
В основе вакцинации лежитиммунологический феномен,
называемый иммунологической
памятью.
Этот феномен используется во
всех программах вакцинации –
для формирования длительно
живущей популяция лимфоцитов
памяти,
либо достигается персистенция в
организме уровня антигена,
который продолжает
рестимулировать
антигеспецифические
лимфоциты.
Формирование иммунного ответа на
вакцины, имитирует,
инфекционный процесс и
представлено следующими этапами:
- захват АПК антигенов вакцин,
-расщепление и представление на
клеточной поверхности эпитопов
антигенов в комплексе с
молекулами МНС класса I и II;
- распознование антигенов Т- и Влимфоцитами;
- активация, дифференцировка и
пролиферация клонов клеток,
появление регуляторных ,
эффекторных и клеток памяти,
антител.
18. Вакцины содержат патоген-ассоциирован ные молекулярные паттерны (PAMPs) или индуцируют локальный выход DAMPs. Эти PAMPs и DAMPs обнаруживаются патер
Вакцинысодержат
патогенассоциирован
ные
молекулярные
паттерны
(PAMPs) или
индуцируют
локальный
выход DAMPs.
Эти PAMPs и
DAMPs
обнаруживаются
патерраспознающими
рецепторами
(PRRs),
дендритных
клеток (DCs),
что активирует
DC, они
мигрируют в
лимфоузлы.
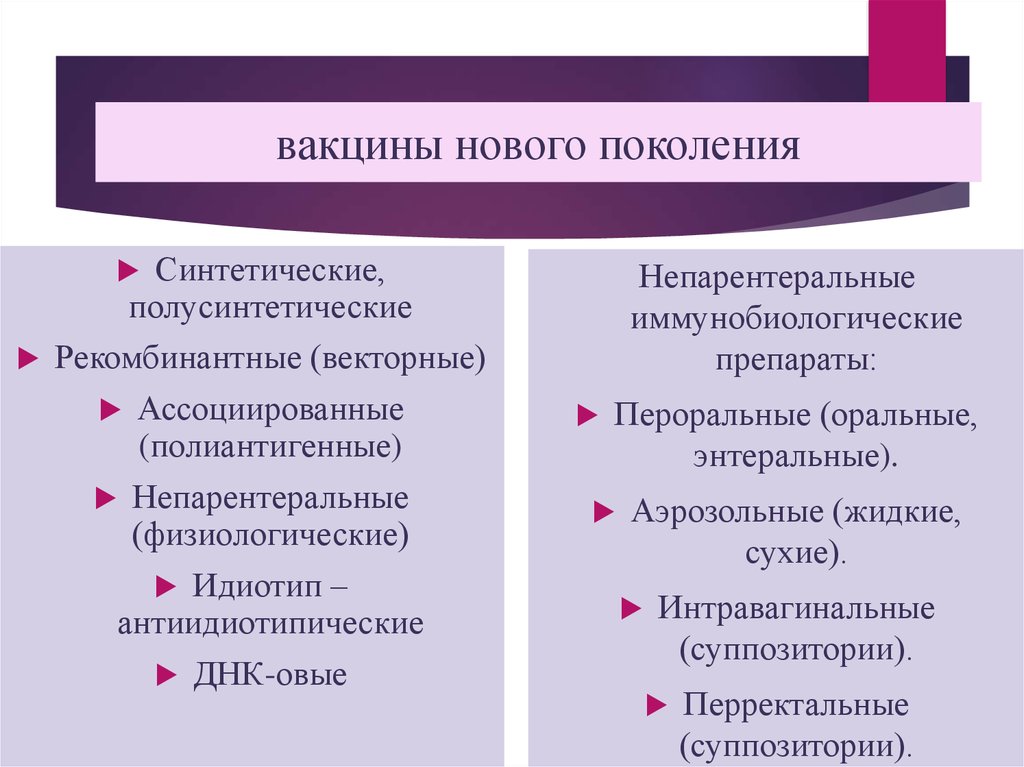
19. вакцины нового поколения
Синтетические,полусинтетические
Рекомбинантные (векторные)
Ассоциированные
(полиантигенные)
Непарентеральные
(физиологические)
Идиотип –
антиидиотипические
ДНК-овые
Непарентеральные
иммунобиологические
препараты:
Пероральные (оральные,
энтеральные).
Аэрозольные (жидкие,
сухие).
Интравагинальные
(суппозитории).
Перректальные
(суппозитории).
20. Синтетический дипептид пидотимод: механизм действия
Пидотимод стимулирует экспрессию дендритными клетками, покрайней мере, 2-х рецепторов врожденного иммунитета: TLR2 и
TLR4, а также трансдукцию TLR-ассоциированного сигнального пути
посредством стимуляции NFκB.
Благодаря этому Имунорикс восстанавливает естественный ход
иммунного ответа на патогены.
1. Xiaofang Hu et al. The detailed analysis of the changes of murine DC induced by thymic
peptide pidotimod., Humen Vaccines& Immunotherapeutics, 2012; 8 (9): 1250-1258
2. Zuccotti GV et al. Immunomodulating activity of Pidotimod in children with Down syndrome , J
Biol Regul Homeost Agents. 2013;27(1):253-8
21. Пути вакцинации с учетом феномена хоминга лимфоцитов
22.
АССОЦИИРОВАННАЯ С ЖКТ ЛИМФОИДНАЯ ТКАНЬ(GALT)
Пищевод
Желудок
Толстая
кишка
Тонкая кишка
Время контакта со слизистой
оболочкой АГ:
Пищевод - 5-6 секунд;
Желудок - 2-4 часа (pH 1-2);
Тонкая кишка - 5-6 часов
50% иммунных клеток
находятся в MALT
23. Стимуляция адаптивного иммунитета при разных путях введения лигандов рецепторов врожденного иммунитета: индукция синтеза IgA в разных био
Стимуляция адаптивного иммунитета при разных путях введения лигандоврецепторов врожденного иммунитета: индукция синтеза IgA в разных
биотопах организма
Сублингвально
Интраназально
Перорально
Верхние дыхат. пути
+++
+++
+/++
Нижние дыхат. пути
+++
+ до +++
+/++
Желудок
+/+++
-
+/+++
Тонкая кишка
++
-
+++
Толстая кишка
?
-
±
Прямая кишка
?
-
±
Половые пути
+++
++
-
Кровь
++
+++
+
Czerkinsky C. et al. Sublingual vaccination // Human vaccines, 2011.
24. Выбор сублингвального пути: преимущества
Слизистая оболочка подъязычной зоныпредставляет собой тонкий
многослойный эпителий толщиной
100-200 мкм, что меньше толщины
слизистой оболочки в других
участках полости рта.
В подъязычной области выявляется
большое число антигенпредставляющих клеток: клетки
Лангерганса (непосредственно в
среди эпителиоцитов) и другие дендритные клетки (в собственной
пластинке слизистой и подслизистой
основе), которые после захвата
антигенов и активации способны
мигрировать к дренирующим
лимфатическим узлам, в первую
очередь к шейным.
Слизистые оболочки полости рта и
подъязычной зоны вызвали интерес
в качестве места доставки
лекарственных препаратов,
поскольку здесь не происходит
распад белков/пептидов, с чем
сопряжено введение препаратов
через желудочно-кишечный тракт, а
кроме того они богаты антигенпредставляющими клетками, что
делает их важными мишенями с
точки зрения места иммунизации.
Czerkinsky C et al. Sublingual
vaccination // Human vaccines, 2011.
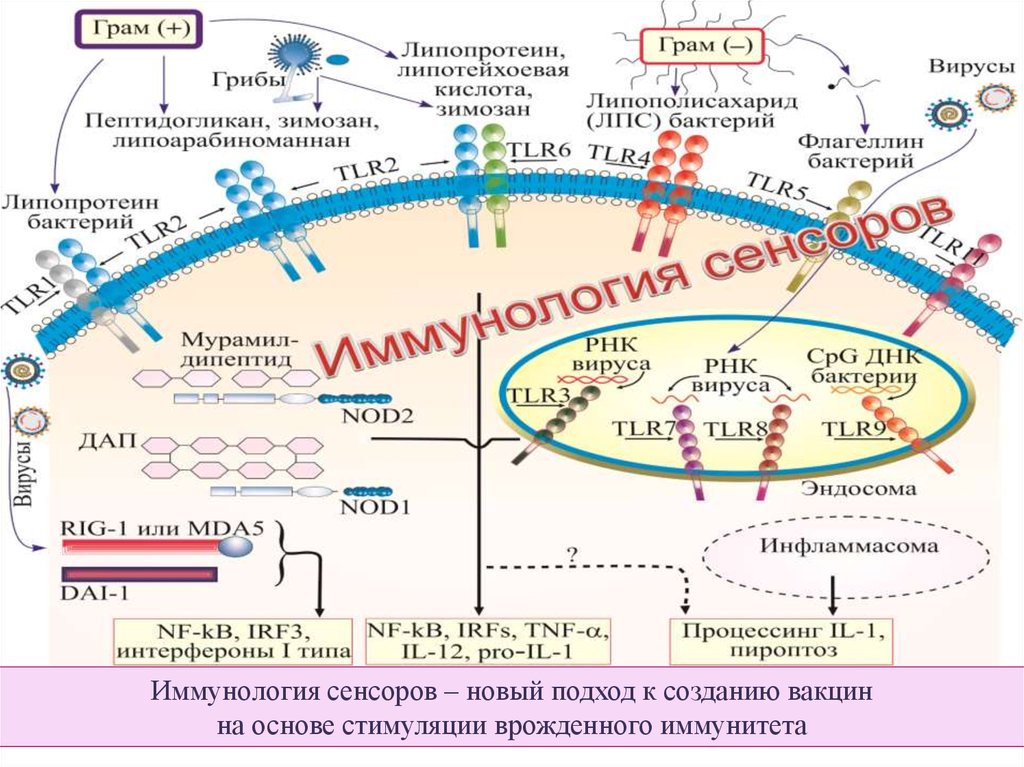
25.
Иммунология сенсоров – новый подход к созданию вакцинна основе стимуляции врожденного иммунитета
26. Классификация состояния гиперчувствительности
ГиперчувствительностьАллергическая
гиперчувствительность
(иммунологические механизмы)
IgE опосредованная
неатопия
атопия
Атопия
инсектная аллергия
Неаллергическая гиперчувствительность
(неиммунологические механизмы,
например, аспириновая)
Не опосредованная IgE
Т-клетки:
контактный дерматит
Эозинофилы:
гастроэнтеропатия
гельминты
IgG: аллергический
альвеолит
лекарства
другие
другие
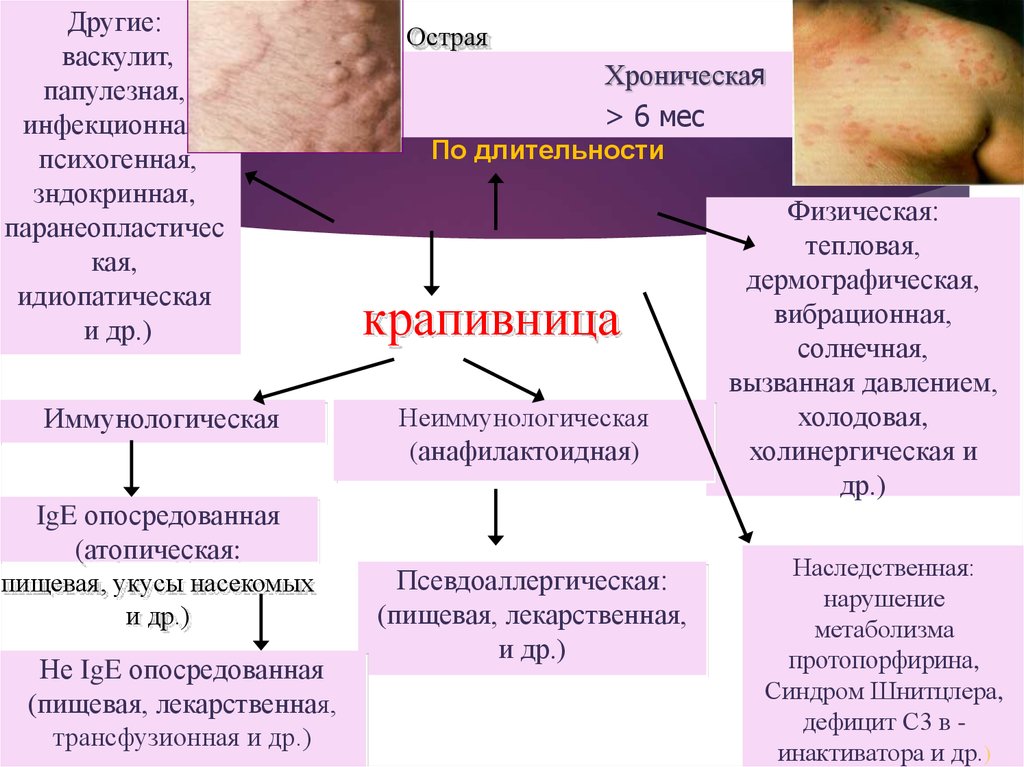
27. Физическая: тепловая, дермографическая, вибрационная, солнечная, вызванная давлением, холодовая, холинергическая и др.)
Другие:васкулит,
папулезная,
инфекционная,
психогенная,
зндокринная,
паранеопластичес
кая,
идиопатическая
и др.)
Иммунологическая
IgE опосредованная
(атопическая:
пищевая, укусы насекомых
и др.)
Не IgE опосредованная
(пищевая, лекарственная,
трансфузионная и др.)
Острая
Хроническая
> 6 мес
По длительности
крапивница
Неиммунологическая
(анафилактоидная)
Псевдоаллергическая:
(пищевая, лекарственная,
и др.)
Физическая:
тепловая,
дермографическая,
вибрационная,
солнечная,
вызванная давлением,
холодовая,
холинергическая и
др.)
Наследственная:
нарушение
метаболизма
протопорфирина,
Синдром Шнитцлера,
дефицит С3 в инактиватора и др.)
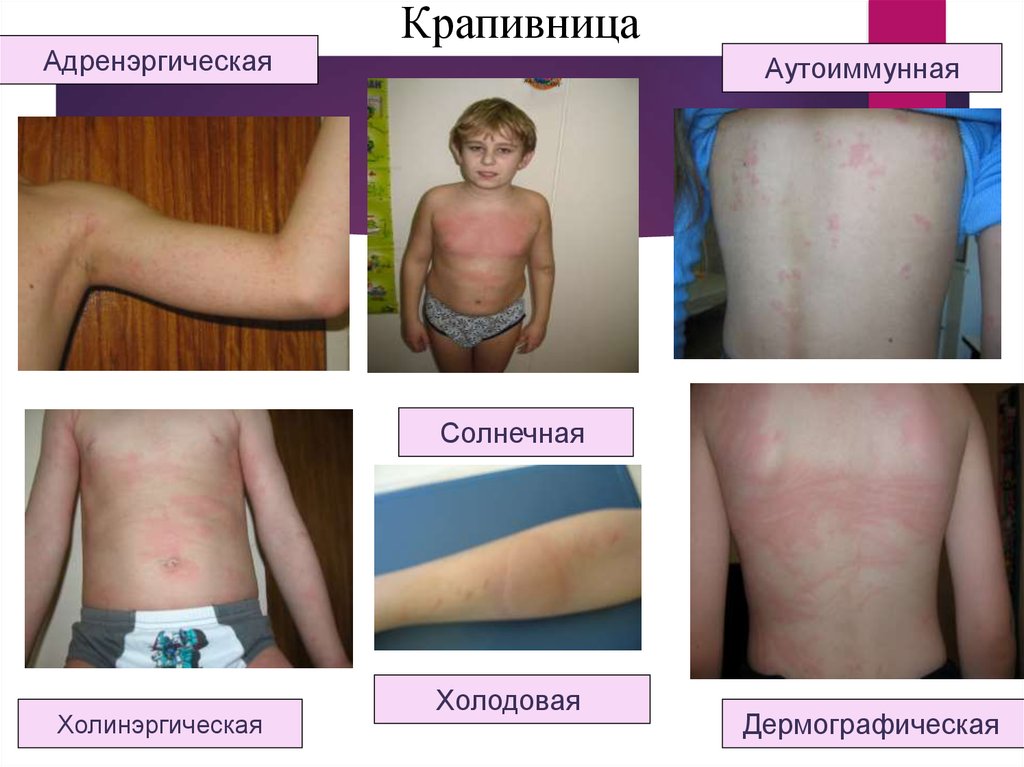
28. Крапивница
АдренэргическаяКрапивница
Аутоиммунная
Солнечная
Холинэргическая
Холодовая
Дермографическая
29. Псевдоаллергия - определение
Псевдоаллергия (греч. pseudēsложный) –
патологический процесс, по
клиническим проявлениям похожий
на аллергию, но не имеющий
иммунологической стадии развития.
Конечные стадии истинной аллергии
совпадают с псевдоаллергией :
патохимическая стадия освобождение
(и образование de novo ) медиаторов;
патофизиологическая стадия реализация клинических симптомов.
Неиммунный механизм дегрануляции
тучных клеток –
факторы (не IgE), приводящие к
дестабилизации мембраны тучной
клетки и к ее дегрануляции .
30.
Гистаминспазм гладких
мышц
расширение
артериол и венул
увеличение
проницаемости
стенок капилляров
Раздражение
нервных
окончаний
экссудация
отек окружающих
тканей
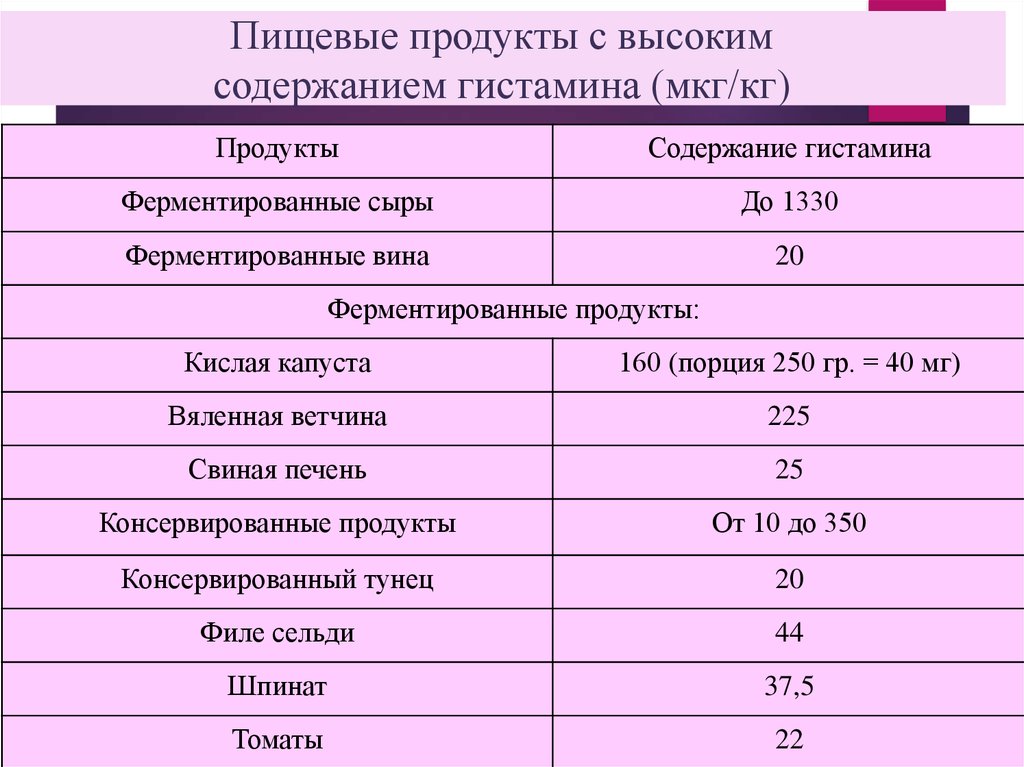
31. Пищевые продукты с высоким содержанием гистамина (мкг/кг)
ПродуктыСодержание гистамина
Ферментированные сыры
До 1330
Ферментированные вина
20
Ферментированные продукты:
Кислая капуста
160 (порция 250 гр. = 40 мг)
Вяленная ветчина
225
Свиная печень
25
Консервированные продукты
От 10 до 350
Консервированный тунец
20
Филе сельди
44
Шпинат
37,5
Томаты
22
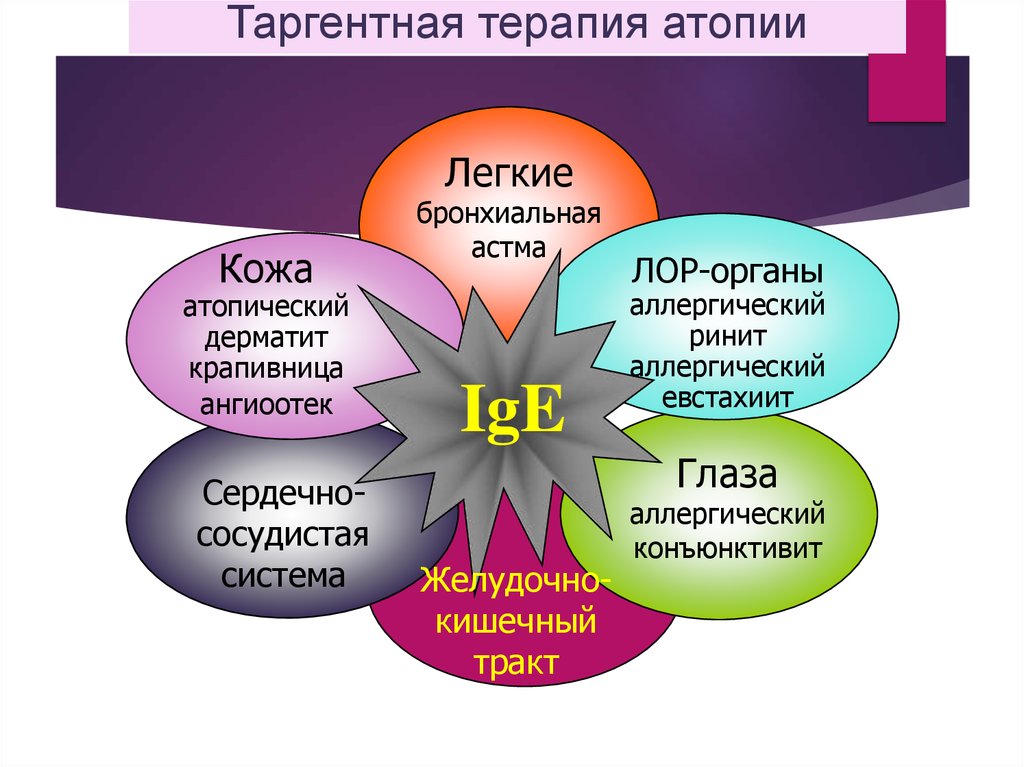
32.
Таргентная терапия атопииЛегкие
Кожа
атопический
дерматит
крапивница
ангиоотек
Сердечнососудистая
система
бронхиальная
астма
IgE
ЛОР-органы
аллергический
ринит
аллергический
евстахиит
Глаза
Желудочнокишечный
тракт
аллергический
конъюнктивит
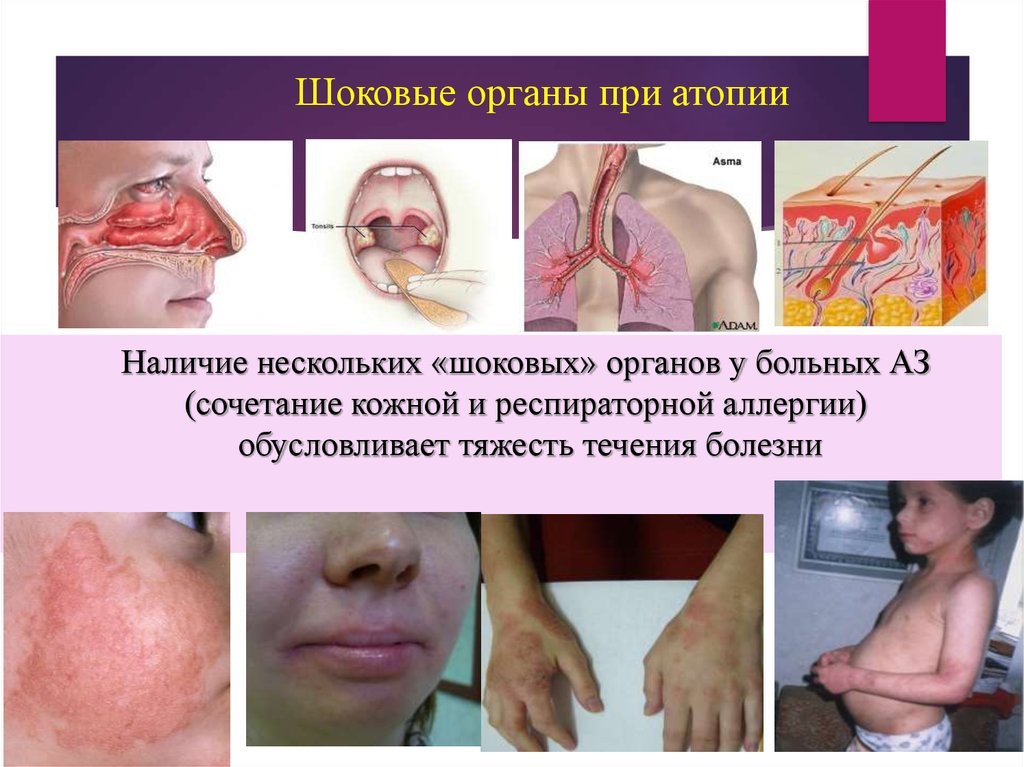
33. Шоковые органы при атопии
Наличие нескольких «шоковых» органов у больных АЗ(сочетание кожной и респираторной аллергии)
обусловливает тяжесть течения болезни
34. Аллергические заболевания ЛОР органов
Аллергический ринитАллергический риносинусит
Полипозный аллергический ринит
Аллергический отит
Аллергический ларингит, трахеит
35. «Атопический марш»
У 80% детей, заболевшихутопическим дерматитом в
раннем детстве,
впоследствии клинически
проявляется атопический
ринит.
10-20% из них заболевает
бронхиальной астмой.
Феномен
«качелей»: при
появлении
респираторных
проявлений
улучшается
течение кожного
процесса.
36. «Атопический марш»
•Бронхиальная астма•Круглогодичный аллергический
риноконъюнктивит
•Поллиноз
•Атопический дерматит
Возраст - годы
0 1 2
6
Пищевая аллергия
12
Пыльцевая аллергия
Бытовая аллергия
14
37.
«Атопический марш»В 45-65% в структуре атопических
заболеваний (в зависимости от возраста)
встречаются сочетанные проявления атопии
с поражением кожи, ЛОР-органов и органов
респираторного тракта.
Естественный ход «атопического марша», т.е.
естественного течения атопии,
характеризуется возрастной
последовательностью развития клинических
симптомов и сенсибилизации
(атопическмй дерматит –
атопический ринит –
атопическая бронхиальная астма)
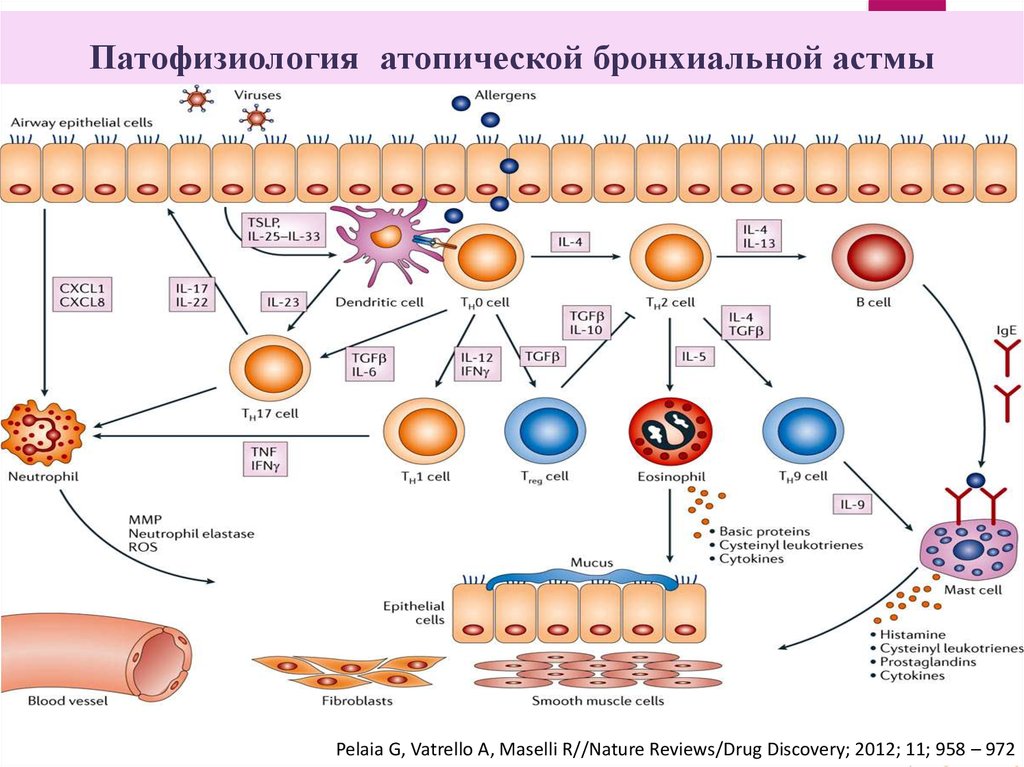
38.
Патофизиология атопической бронхиальной астмыPelaia G, Vatrello A, Maselli R//Nature Reviews/Drug Discovery; 2012; 11; 958 – 972
39. Омализумаб: профиль безопасности
Данные по безопасности собраны у более чем 7,500 пациентов(>5,000 получивших омализумаб)1
Частота нежелательных явлений (НЯ) была сопоставимой на терапии
омализумабом и иной терапии (контроль)
Большинство НЯ были легкими или средне-тяжелыми и непродолжительными
Частота НЯ, приведших к отказу от терапии составляет 1.3% для омализумаба и
1.5% для плацебо
В исследованиях, оценивающих реакцию в месте инъекции препарата, общая
частота реакций была сопоставимой:
омализумаб: 45%; плацебо: 43%
Не было найдено увеличения частоты злокачественных новообразований.
Сводный анализ двойных слепых плацебо-контролируемых РКИ не выявил
повышения риска малигнизации на терапии омализумабом2
Исследование EXCELS показало что терапия омализумабом не связана с
увеличенным риском малигнизации3
EXCELS – исследование, в котором в течение 5 лет наблюдались 7,836 пациентов
и целью которого было оценить риск малигнизации.
1. Corren J, Casale TB, Lanier B, et al. Safety and tolerability of omalizumab. Clin Exp Allergy 2009;39:788–97. 2. Busse W,
Buhl R, Vidaurre DF, et al. Omalizumab and the risk of malignancy: results from a pooled analysis. J Allergy Clin Immunol
2012;129:983–9. 3. Long A, Rahmaoui A, Rothman KJ, et al. Incidence of malignancy in patients with moderate-to severe
asthma treated with or without omalizumab. J Allergy Clin Immunol 2014;134:560-7.
40. Иммуноопосредованное воспаление при астме : мишени для таргентной терапии
Бокаловидная клетка
Дендрит
ная
клетка
Аллергены
Гельминты
Вирусы
Тollподобные
рецепторы
(TLR)
Поврежд
ение
эпителия
Гладкие мышцы бронхов
Участие в развитии Th2-воспаления
В-клетки Тучные клетки
Дендритные
клетки
CD8- T клетки
Омализумаб
Лигелизумаб
Меполизумаб
Реслизумаб
Бенрализумаб
(связывание IL-4Rα)
Наивные
T клетки
CD4- T клетки
NK- T клетки
Дупилумаб
(связывание IL-4Rα)
Базофилы
Эозинофилы
Тралокинумаб
Лебрикизумаб
(рецептор)
Mitchell P.D., El-Gammal A.I., O’Byrne P.M.//Clin Pharmacol Ther; 2015; ‘Accepted Article’, doi: 10.1002/cpt.284
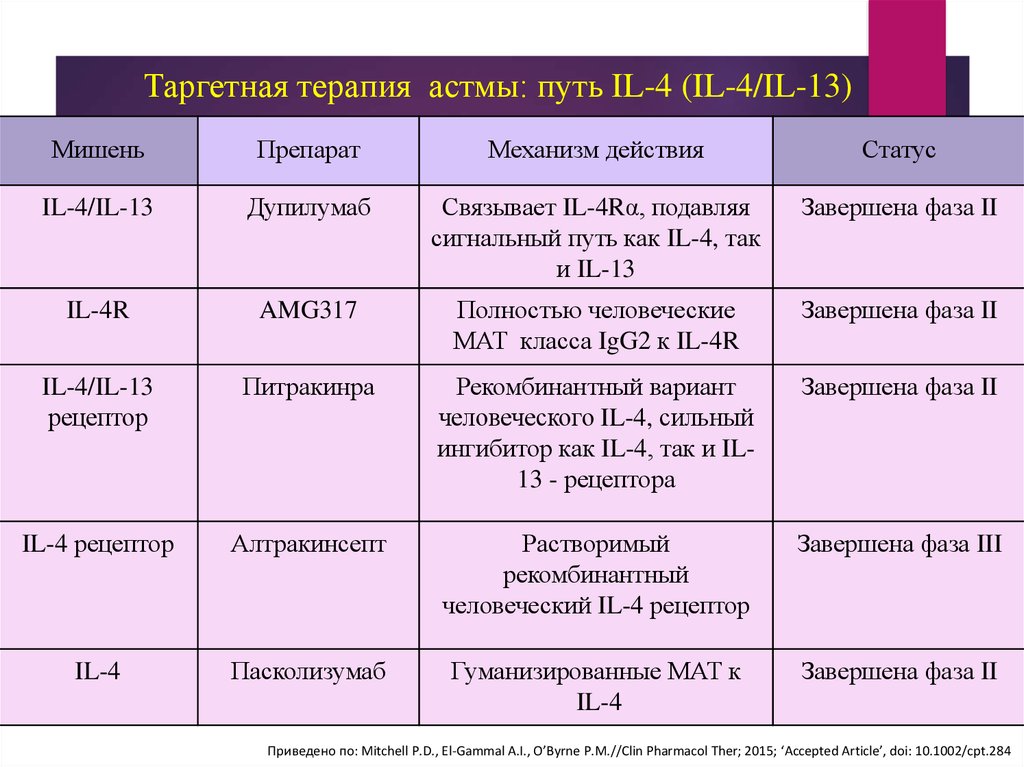
41. Таргетная терапия астмы: путь IL-4 (IL-4/IL-13)
МишеньПрепарат
Механизм действия
Статус
IL-4/IL-13
Дупилумаб
Связывает IL-4Rα, подавляя
сигнальный путь как IL-4, так
и IL-13
Завершена фаза II
IL-4R
AMG317
Полностью человеческие
МАТ класса IgG2 к IL-4R
Завершена фаза II
IL-4/IL-13
рецептор
Питракинра
Рекомбинантный вариант
человеческого IL-4, сильный
ингибитор как IL-4, так и IL13 - рецептора
Завершена фаза II
IL-4 рецептор
Алтракинсепт
Растворимый
рекомбинантный
человеческий IL-4 рецептор
Завершена фаза III
IL-4
Пасколизумаб
Гуманизированные МАТ к
IL-4
Завершена фаза II
Приведено по: Mitchell P.D., El-Gammal A.I., O’Byrne P.M.//Clin Pharmacol Ther; 2015; ‘Accepted Article’, doi: 10.1002/cpt.284
42. Мишени для таргетной терапии астмы:IL-13
МишеньПрепарат
Механизм действия
Статус
IL-13
Лебрикизумаб
Гуманизированные МАТ
IgG4 с высокой
аффинностью к IL-13
Завершена фаза II,
исследование
продолжается
IL-13
Тралокинумаб
Человеческие МАТ,
нейтрализующие IL-13
Продолжается
фаза III
IL-13
Анрукинзумаб
(IMA-638 и
IMA-026)
Полностью
гуманизированные МАТ,
которые связываются с
разными эпитопами и
нейтрализуют IL-13
Завершена фаза II
Приведено по: Mitchell P.D., El-Gammal A.I., O’Byrne P.M.//Clin Pharmacol Ther; 2015; ‘Accepted Article’, doi: 10.1002/cpt.284
43. Стимуляция созревания и миграции эозинофилов при астме
ВЛКТучная клетка
Костный мозг
Предшественник
эозинофила
Меполизумаб
Реслизумаб
IL-5 (активация
и выживание
эозинофилов)
Повреждение
тканей
Инфекция
Аллергены
IL-25, IL-33,
TSLP
β-субъединица
IL-5Rα
IL-4
ДК
RANTES
и эотаксин
Th2
хемоаттракция
β-субъединица
IL-5Rα
Эозинофил
ВЛК – врождённая лимфоидная клетка
Бенрализумаб
ДК – дендритная клетка
RANTES – хемокин, экспрессируемый
Базофил
и секретируемый Т-клетками при
активации
Адаптировано из: Patterson M.F., Borish L., Kennedy J.L.//J Asthma Allrergy; 2015; 8; 125 - 134
44. Мишени для таргетной терапии астмы: IL-5
МишеньПрепарат
Механизм действия
Статус
IL-5
Меполизумаб
Гуманизированные МАТ к
IL-5 (IgG1)
Одобрен в США
04.11.15, в Европе
02.12.15
IL-5
Реслизумаб
Гуманизированные IgG1
МАТ к IL-5 (IgG4/k)
Завершена фаза III
IL-5
Бенрализумаб
Гуманизированные
афукозилированные МАТ к
IL-5Rα, индуцируют
апоптоз эозинофилов
Завершена фаза II,
исследования
продолжаются
Приведено по: Mitchell P.D., El-Gammal A.I., O’Byrne P.M.//Clin Pharmacol Ther; 2015; ‘Accepted Article’, doi: 10.1002/cpt.284
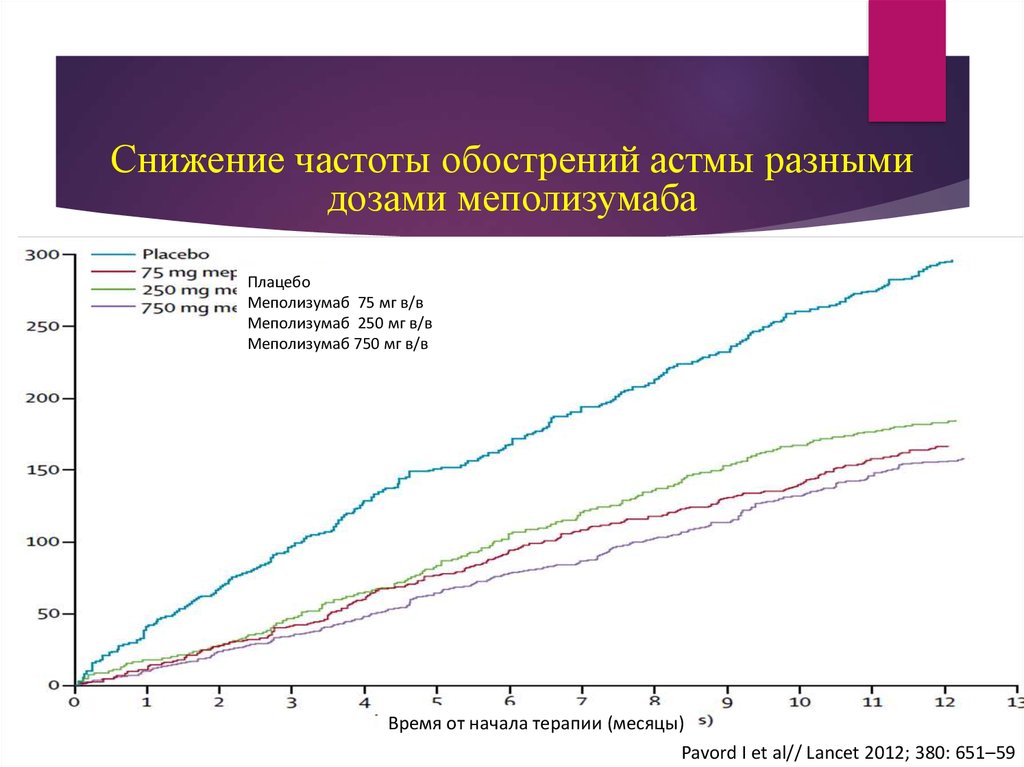
45.
Снижение частоты обострений астмы разнымидозами меполизумаба
Плацебо
Меполизумаб 75 мг в/в
Меполизумаб 250 мг в/в
Меполизумаб 750 мг в/в
Время от начала терапии (месяцы)
Pavord I et al// Lancet 2012; 380: 651–59
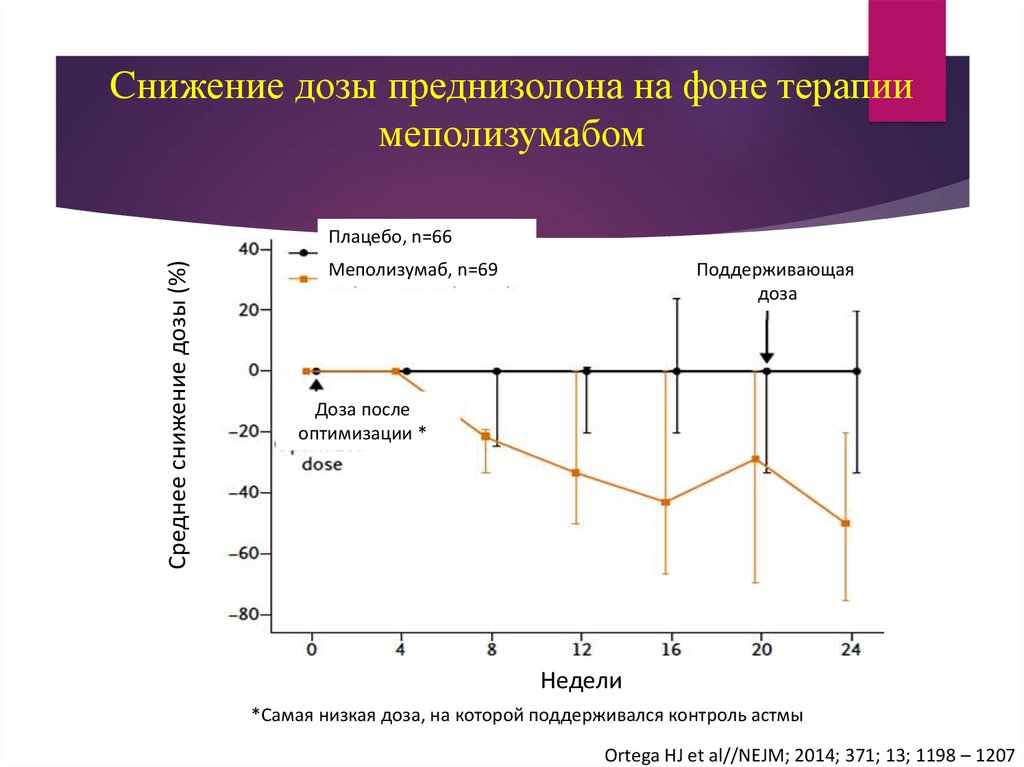
46. Cнижение дозы преднизолона на фоне терапии меполизумабом
Среднее снижение дозы (%)Плацебо, n=66
Меполизумаб, n=69
Поддерживающая
доза
Доза после
оптимизации *
Недели
*Самая низкая доза, на которой поддерживался контроль астмы
Ortega HJ et al//NEJM; 2014; 371; 13; 1198 – 1207
47. Показатели и маркёры эффективности биопрепаратов, действующих на путь Th2
Эозинофилиякрови и
мокроты
Снижение частоты
обострений
Блокада
эффектов IL-5
Улучшение контроля астмы
Блокада
эффектов IL-13
Повышение ОФВ1
Блокада
эффектов IL-4
Снижение уровня IgE
Периостин (регуляторный
белок)
Адаптировано из: Chung K.F.// Lancet 2015; 386: 1086–96
48. ЛЕЧЕБНОЕ ПРИМЕНЕНИЕ ПРЕПАРАТОВ ИЛ-1(проф.Симбирцев А.С.)
СИСТЕМНОЕДействие на уровне
организма
Активация разных
механизмов развития
защитных реакций
МЕСТНОЕ
Высокая локальная
концентрация
Отсутствие
системных
побочных эффектов
49.
INFαIL-6
IL-1β
IL-12,IL-23
TNFα
TNFα
IL-8
IL-8
Синтез цитокинов
Регуляция
температуры,
поведения,
синтеза гормонов
Активация лимфоцитов
IL-1
Экспрессия молекул
адгезии на эндотелиоцитах,
прокоагулянтная активность,
синтез цитокинов
Продукция белков
острой фазы воспаления
NO
PG
Активация
кроветворения
LT
Активация фагоцитоза
Активация iNOS и метаболизма
арахидоновой кислоты
50. Механизмы местного иммуностимулирующего и ранозаживляющего действия ИЛ-1
Механизмы местного иммуностимулирующего иранозаживляющего действия ИЛ-1
Функций нейтрофилов
Числа макрофагов
Роста грануляционной
ткани
Эпителизации
Изменения продукции
провоспалительных
цитокинов
ИЛ-1
(Singer A.J., Clark R.A.F. N Engl J Med, 1999, V.341, P. 738-746)
ИЛ-8
51. Динамика изменения площадей ран при применении ИЛ-1
РАНОЗАЖИВЛЯЮЩЕЕ ДЕЙСТВИЕРЕКОМБИНАНТНОГО ИНТЕРЛЕЙКИНА-1 бета
100
*
% от исходной площади
Динамика изменения площадей ран
при применении ИЛ-1
Плацебо
80
*
*
*
60
*
ИЛ-1
40
20
* - p<0,05
0
Дни:0
3
5
7
11
13
Беспородные SPF мыши (C.River, Венгрия)
Модель осложненного течения раневого процесса на фоне иммуносупрессии у мышей
52.
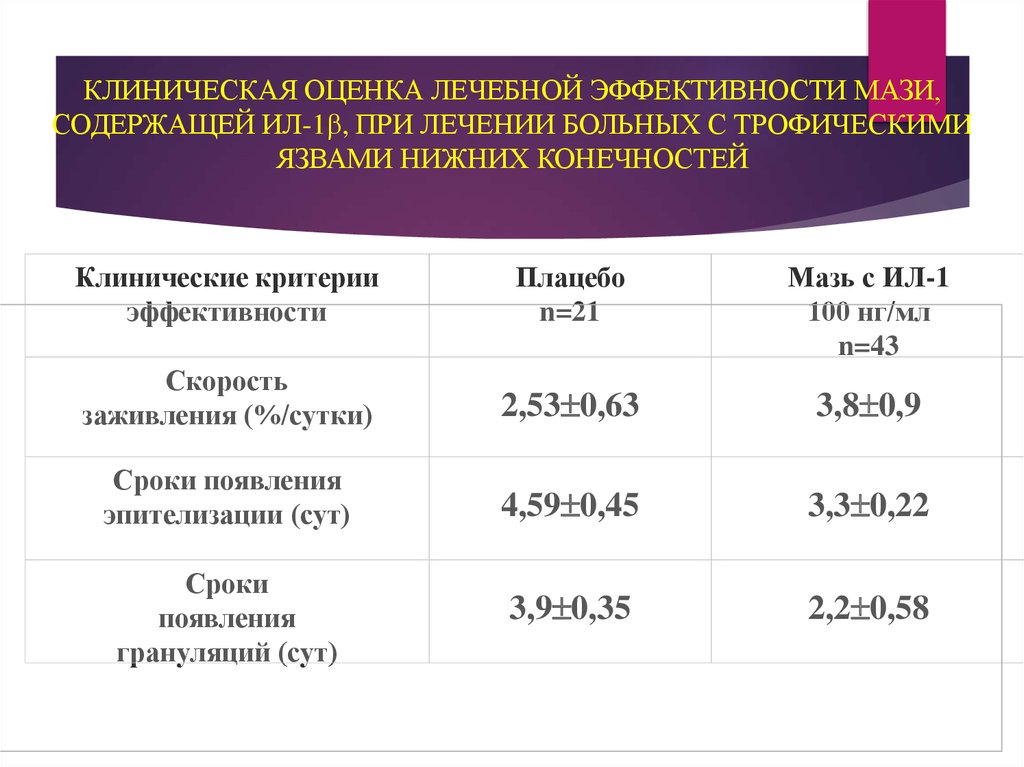
КЛИНИЧЕСКАЯ ОЦЕНКА ЛЕЧЕБНОЙ ЭФФЕКТИВНОСТИ МАЗИ,СОДЕРЖАЩЕЙ ИЛ-1 , ПРИ ЛЕЧЕНИИ БОЛЬНЫХ С ТРОФИЧЕСКИМИ
ЯЗВАМИ НИЖНИХ КОНЕЧНОСТЕЙ
Клинические критерии
эффективности
Плацебо
n=21
Мазь с ИЛ-1
100 нг/мл
n=43
Скорость
заживления (%/сутки)
2,53 0,63
3,8 0,9
Сроки появления
эпителизации (сут)
4,59 0,45
3,3 0,22
Сроки
появления
грануляций (сут)
3,9 0,35
2,2 0,58
53. ПРЕИМУЩЕСТВА ЛЕЧЕБНОГО ПРИМЕНЕНИЯ ЦИТОКИНОВ
ВозможностьПрименение
рекомбинантных
препаратов
идентичных
эндогенным
цитокинам.
Полностью
охарактеризованный
механизм действия.
сочетания с
химиотерапией и
терапией
антибиотиками.
Высокая
эффективность
лечения по сравнению
с традиционными
методами.
54.
Использование иммуноглобулинов вклинической практике
Профилактикаа
Специфические
иммуноглобулины:
Перед контактом с инфекцией
Введение в зоне эпидемии
Лечение
Иммуномодулирующая
терапия
Заместительная терапия
(восполнение дефицита
антител)
Острые ситуации
Хронические
состояния
55. Убедительно доказано эффективное применение ВВИГ при следующих ВИД
Гипогаммаглобулинемия.Профилактика инфекций при хроническом
лимфолейкозе.
Профилактика цитомегаловирусной инфекции при
аллогенной пересадке КМ и других органов .
Синдром отторжения при аллогенной пересадке КМ.
СПИД.
Хронические демиелинизирующие воспалительные
полинейропатии.
Острая и хроническая тромбоцитопеническая пурпура
(ИТП), в том числе у детей связанная с ВИЧ-инфекцией.
Аутоиммунная тромбоцитопения.
56. Обоснования для применения ИГ при сепсисе и тяжелых инфекциях
Наличии широкогоспектра
высокоаффинных
антител,
вызывающих
комплемент опосредованное
уничтожение
возбудителя и
повышение
активности
фагоцитоза.
Нейтрализации
эндотоксинов,
экзотоксинов и
суперантигенов.
2)
Модулировании системных
воспалительных реакций
1) ингибирование
провоспалительных
цитокинов.
стимуляция высвобождения
противовоспалительных
цитокинов.
Модулировании действия
комплемента путем
нейтрализации его
активированных факторов
С3b bC4b.
57. Применение ВВИГ при сепсисе и тяжелых инфекциях (принципиальное условие лечения – эрадикация патогена)
ВВИГ - это препаратыпатогенетической терапии
тяжёлых
бактериальных инфекций.
ВВИГ не эффективны в
лечении септического шока,
поэтому включение их в
комплекс терапии необходимо
своевременно, а не когда
возникла катастрофа:
септический шок.
Абсолютным показаниям
является снижение уровня
белка (особенно γ – фракции)
500 мг/дл
Рекомендовано раннее
включение ВВИГ у больных
тяжелыми бактериальными
инфекциями в сочетании с
лейкопенией, абсолютной
лимфопенией, я
агранулоцитозов, у больных,
получающих
иммуносупресивную
терапию.
58.
Требования к препаратам ВВИГ• Сохранение максимально
физиологичных значений
концентрации подклассов
IgG.
Концентрации IgA и IgM
должны составлять
наименьшие значения для
профилактики
анафилактических
реакций.
• Современный препарат
ВВИГ должен быть
максимально
физиологичным:
- Не содержать глюкозу.
- Содержать минимально
возможное содержание солей.
- Иметь оптимальный уровень
рН.
- Осмолярность близкую к
физиологической.
• Использование готовых к
инфузии растворов
минимизирует технические
ошибки при приготовлении
раствора ВВИГ мед.
персоналом.
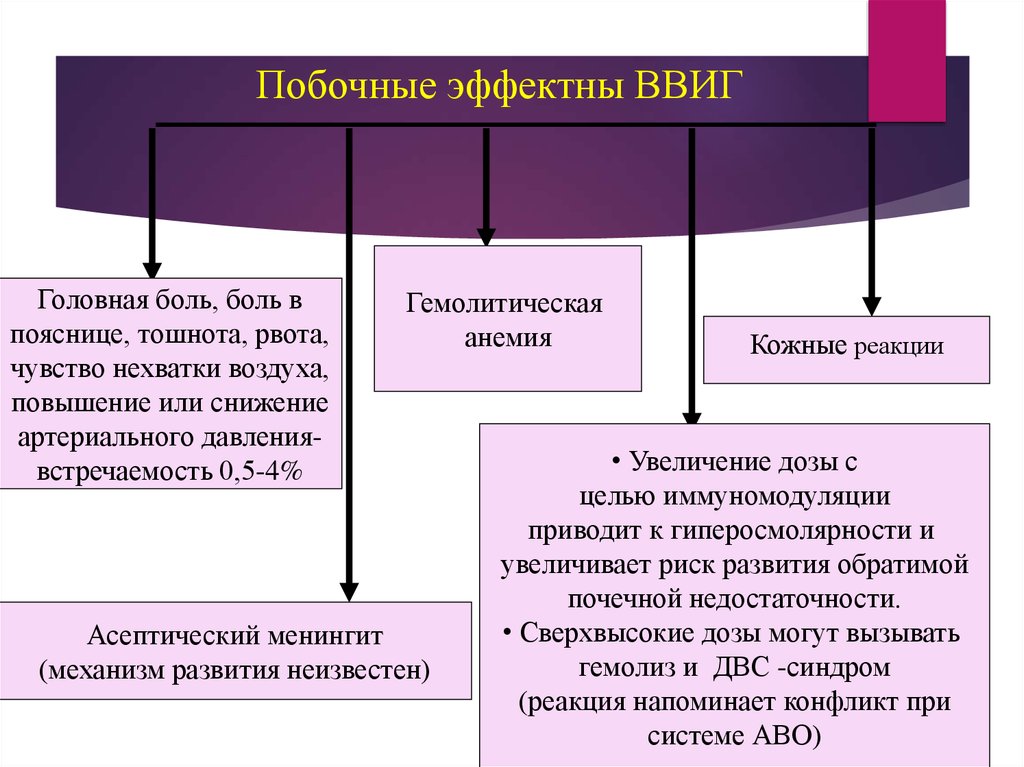
59. Побочные эффектны ВВИГ
Головная боль, боль впояснице, тошнота, рвота,
чувство нехватки воздуха,
повышение или снижение
артериального давлениявстречаемость 0,5-4%
Гемолитическая
анемия
Асептический менингит
(механизм развития неизвестен)
Кожные реакции
• Увеличение дозы с
целью иммуномодуляции
приводит к гиперосмолярности и
увеличивает риск развития обратимой
почечной недостаточности.
• Сверхвысокие дозы могут вызывать
гемолиз и ДВС -синдром
(реакция напоминает конфликт при
системе АВО)
60.
Снижение риска развития побочных эффектовВВИГ
Введение ВВИГ
Ступенчатое изменение скорости при первом введении
При необходимости при первом введении – премедикация
Учет сопутствующей патологии (риск развития тромбозов, сердечная
и почечная недостаточность)
При высоком риске тромбозов:
надлежащая гидратация
антиагреганты
61. Иммуномодуляторы
Основная мишень большинстваиммуномодуляторов в организме
– активация клеток моноцитарномакрофагального ряда
Активация:
Фагоцитоза
Внутриклеточного уничтожения
бактерий
Продукции провоспалительных
цитокинов
Стимуляции гуморального и
клеточного иммунных ответов
Классификация
иммунорегуляторов по
происхождению:
Микробные
Тимические
Костно-мозговые
Цитокины
Нуклеиновые кислоты
Растительные
Химически чистые
Синтетические пептиды
62. Иммуномодуляторы
Сочетанное действие имонотерапия
Наиболее разработаны:
Принципы
применения
иммуномодуляторов
у больных с
недостаточным
противоинфекцион
ной защитой.
Используются в комплексной
терапии с другими
препаратами.
Используются в виде
монотерапии - при проведении
иммунореабилитационных
мероприятий (при неполном
выздоровлении, после
перенесенного острого
инфекционного заболевания).
63.
Все люди разные и на лекарства они «отвечают» поразному: это важно для иммуномодуляторовдля
иммуномодуляторов
различной природы
- нужна
персонализация
Стандартизированны
й подход на основе
доказательной
медицины
(стандарты, протоколы,
клинические
рекомендации)
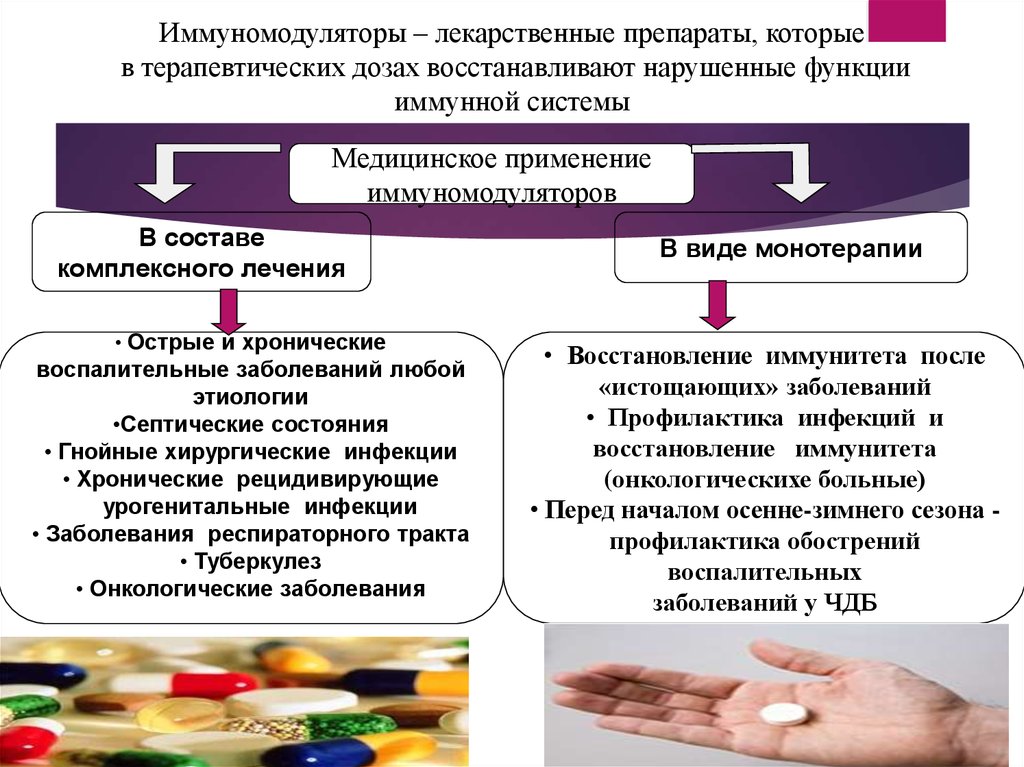
64. Иммуномодуляторы – лекарственные препараты, которые в терапевтических дозах восстанавливают нарушенные функции иммунной системы
Иммуномодуляторы – лекарственные препараты, которыев терапевтических дозах восстанавливают нарушенные функции
64
иммунной системы
Медицинское применение
иммуномодуляторов
В составе
комплексного лечения
• Острые и хронические
воспалительные заболеваний любой
этиологии
•Септические состояния
• Гнойные хирургические инфекции
• Хронические рецидивирующие
урогенитальные инфекции
• Заболевания респираторного тракта
• Туберкулез
• Онкологические заболевания
В виде монотерапии
• Восстановление иммунитета после
«истощающих» заболеваний
• Профилактика инфекций и
восстановление иммунитета
(онкологическихе больные)
• Перед началом осенне-зимнего сезона профилактика обострений
воспалительных
заболеваний у ЧДБ
65.
МОДУЛЯТОРЫ БАКТЕРИАЛЬНОГО ПРОИСХОЖДЕНИЯ– ЗАЩИТАСЛИЗИСТЫХ ОТ ПАТОГЕНОВ – ТРИУМФ 70 И 80-х годов
В начале заболевания –
• предотвращение развития осложнений,
• ускорение процессов выздоровления,
• уменьшения клинических проявлений воспалительного процесса,
• снижение потребности в антибиотиках
При прогрессировании заболевания – ограничение дальнейшей
гененрализации и профилактика хронического воспаления
В стадии реабилитации –
• ускорение репаративных процессов
• замедление окислительного метаболизма нейтрофилов и макрофагов
• профилактика рецидивов
Караулов А.В., Ликов В.Ф. и др.
66.
Ликопид - результат оригинальногоисследования российских ученых,
которое проводилось параллельно
с разработкойаналогов МДП
западными специалистами.
Из гидролизата Lactobacillus
bulgaricus ученые выделили
компонент клеточной стенки этих
бактерий - N-ацетилглюкозаминилN-ацетилмурамил-L-аланил-Dизоглютамин (ГМДП),
обладающий высокой
иммуностимулирующей
активностью и слабой
пирогенностью.
Т.М. Андронова,
E. Lederer, Institut Pasteur, France
E. Lederer - синтез и
описание молекулы
МДП (мурамилдипептида),
Т.М. Андронова - синтез и
описание
молекулы
ГМДП
67.
Общие противопоказания к назначению ИМ-ранний возраст (до 6 мес)
-беременность
-лактация
-повышенная индивидуальная чувствительность
Сопутствующая патология:
- Аутоиммунные заболевания (тироидит и др.)
-Состояния при заболеваниях, сопровождающихся
высокой лихорадкой или гипертермией (>38 °C)
С осторожностью следует применять у больных с
атопическими заболеваниями иммуномодулирующие
препараты из тимуса крупного рогатого скота, а также
созданные
на основе растительных экстрактов
68. Применение иммуномодуляторов у детей с атопическими заболеваниями
При назначениииммуномодуляторов
следует учитывать, что они
не обладают избирательной
способностью ингибировать
Th2-клеточный ответ.
Слишком частое назначение
курсов
иммуномодулирующей
терапии не всегда ведет к
повышению
терапевтического эффекта.
68
Больным с тяжелой
аллергической патологией
лечение иммуномодуляторами
следует проводить при
динамическом
иммунологическом
исследовании.
Назначение иммуномодуляторов
должно проводится с большой
осторожностью больным с
поливалентной лекарственной
аллергией и при наличии
непереносимости бактериальных
и вирусных вакцин.
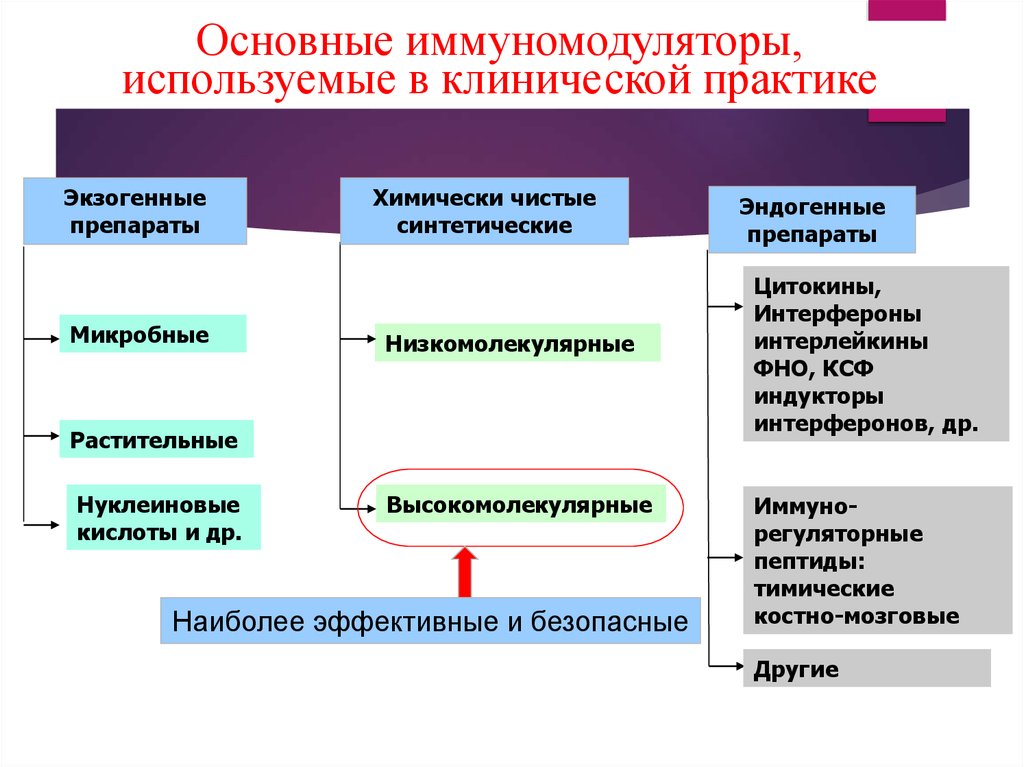
69.
Основные иммуномодуляторы,используемые в клинической практике 69
Экзогенные
препараты
Микробные
Химически чистые
синтетические
Низкомолекулярные
Растительные
Нуклеиновые
кислоты и др.
Высокомолекулярные
Наиболее эффективные и безопасные
Эндогенные
препараты
Цитокины,
Интерфероны
интерлейкины
ФНО, КСФ
индукторы
интерферонов, др.
Иммунорегуляторные
пептиды:
тимические
костно-мозговые
Другие
70. При нарушениях Т-клеточных и макрофагально-моноцитарных реакций
При нарушениях Т-клеточных и макрофагально70моноцитарных реакций
рекомендовано назначение экзогенных иммуномодуляторов
Классификация иммуномодуляторов (Р.М.Хаитов, Б.В.Пинегин, 2003)
Группа
Подгруппа
Название
Состав
Экзогенные
Микробные
Естественные
Рибомунил
Бронхо-мунал,
Иммудон, ИРС-19
Ликопид
Рибосомы бактерий
Лизаты бактерий
Лизаты бактерий
Полусинтетические
Глюкозаминилмурамилдипептид
Одной из основных причин частого возникновения ОРВИ и более тяжелого течения
инфекционно-воспалительных заболеваний у детей является несостоятельность
системы местной защиты, препятствующей проникновению патогенных
микроорганизмов в организм человека, в связи с чем важное место занимают
иммуномодуляторы местного действия.
В настоящее время существует несколько типов иммуномодуляторов местного
действия:
препараты на основе компонентов клеточной стенки бактерий, бактериальные лизаты
(Имудон, ИРС19),препараты на основе нуклеиновых кислот, полимерные
(полиоксидоний)
71. Основные эффекты этих препаратов
71увеличение числа антителопродуцирующих клеток в слизистой
оболочке
индукция синтеза антиген-специфических секреторных
антител
формирование на слизистых защитной пленки из секреторных
иммуноглобулинов
стимуляция процессов фагоцитоза, активация Т регуляторных клеток,
усиление продукции противовоспалительных цитокинов, развитие
адъювантного эффекта
72. Аллергенспецифическая иммунотерапия (АСИТ)
Одиниз методов
патогенетического
лечения атопических
заболеваний.
Введение
в организм
пациента
возрастающих доз
причинно-значимого
аллергена.
73. АСИТ : механизмы действия
Генерация Трегуляторных
лимфоцитов и развитие
толегрогенных ответов на
причинно-значимый
аллерген.
Подавление
цитокинового и
пролиферативного
ответов на этиологически
значимый антиген.
Подавление миграции
эффекторных клеток в
очаг воспаления.
Торможение
аллергенспецифической
реакции.
Угнетение тканевой
гиперреактивности.
74. АСИТ – аллергенспецифическая иммунотерапия
АСИТ –: иммунотерапия
аллергенспецифическая
Показания:
легкие и среднетяжелые формы течения заболеваний:
Атопический
сезонный/круглогоди
чный ринит.
Атопический
сезонный/круглогоди
чный
риноконъюктивит.
Атопический
дерматит.
Контролируемая
атопическая
бронхиальная
астма.
75. Известные в России препараты для АСИТ
Водно-солевые экстракты аллергенов отечественногопроизводства для подкожного введения
Адъювантные аллергены (Сталлержен, Франция) для подкожного
введения (ИР)
Сублингвальные аллергены «Сталораль» (Сталлержен, Франция)
Сублингвальные аллергены ( Севафарма, Чехия) Весенняя смесь
ранняя, капли
Сублингвальные аллергоиды (Лофарма, Италия), таблетки «Лайс
Грасс» (LAIS Grass) и «Лайс Дерматофагоидес» (LAIS
Dermatophagoides) 1000АЕ №30 и 300АЕ №40.
Аллергенная Единица (АЕ) и Индекс реактивности - единицы
стандартизации.
Одна единица эквивалентна 1/40 провоцирующей дозы
соответствующего немодифицированного аллергена, оцениваемая
по назальному провоцирующему тесту у сенсибилизированных
добровольцев
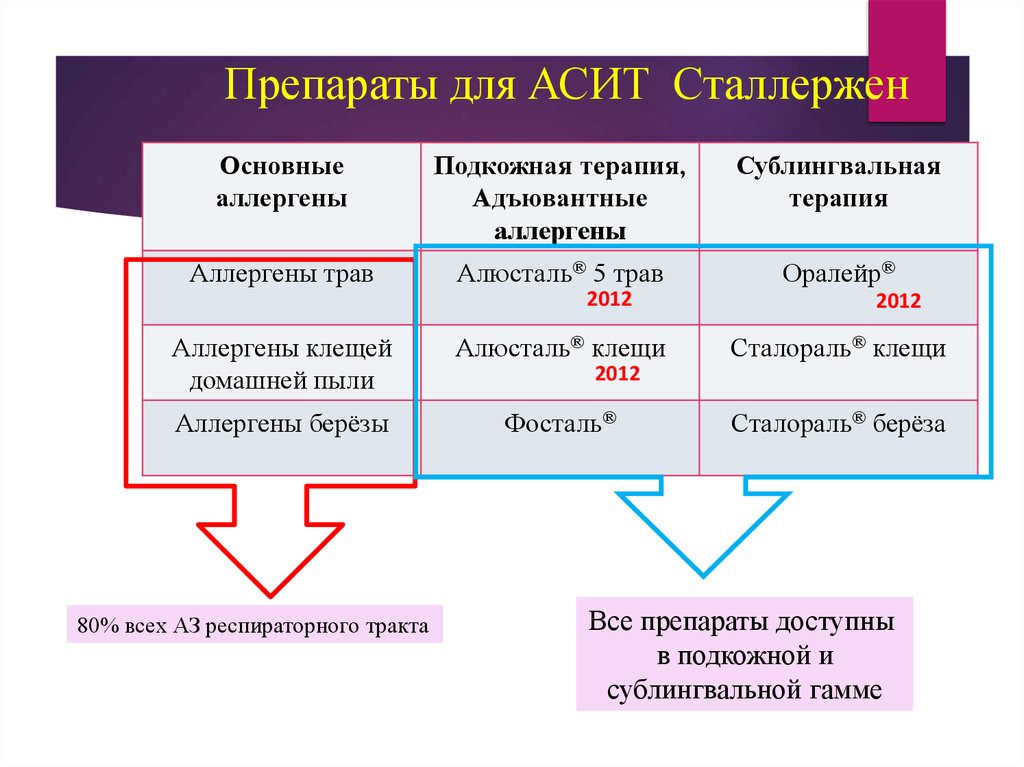
76. Препараты для АСИТ Сталлержен
Основныеаллергены
Подкожная терапия,
Адъювантные
аллергены
Сублингвальная
терапия
Аллергены трав
Алюсталь® 5 трав
Оралейр®
2012
Аллергены клещей
домашней пыли
Алюсталь® клещи
Аллергены берёзы
Фосталь®
80% всех АЗ респираторного тракта
2012
Сталораль® клещи
2012
Сталораль® берёза
Все препараты доступны
в подкожной и
сублингвальной гамме
77. АСИТ –характеристика эффективности
Своевременнопроведенная АСИТ
предупреждает переход
более легких форм
атопических заболеваний в
более тяжелые (например,
атопического ринита в
бронхиальную астму).
Положительный
клинический эффект от
проведенной АСИТ может
сохраняться в течение
многих лет.
Клиническое
лечебное действие
АСИТ
достигается при
завершении
повторных курсов
(3-5 курсов
лечения),
улучшение может
наблюдаться уже
после 1 курса.
78. АСИТ – противопоказания к проведению
Тяжелыеимунопатологические
состояния и ИД.
Онкологические
заболевания.
Тяжелые психические
расстройства.
Лечение β-блокаторами.
Неконтролируемая
атопическая бронхиальная
астма.
Сердечно-сосудистые
заболевания. при которых
возможны осложнения при
использовании
адреналина.
Наличие в анамнезе
анафилактического шока.
Дети младше 5 лет (для
подкожной АСИТ).
Беременность, лактация.
79. Схемы проведения АСИТ
АСИТ проводится только в условияхспециализированных
аллергологических кабинетов
специалистами аллергологамииммунологами.
Для АСИТ отбираются причиннозначимые аллергены, элиминация
которых невозможна (домашняя
пыль, клещи домашней пыли,
пыльца растений).
Схемы проведения АСИТ включают 2
этапа:
1 этап –достижение максимальной
терапевтической дозы
2 этап – поддерживающая терапия
(фаза основной терапии).
В зависимости от схемы
проведения АСИТ бывает:
Предсезонной.
Предсезонно-сезонной.
Круглогодичной.
Методы введения аллергена
включают:
Инъекционные (подкожное
введение аллергена)
Неинъекционные
(сублингвальные –
рассасывание, или оральные проглатывание).
80.
ИР/мл - Индекс Реактивности – биологическая единица стандартизацииАЛЮСТАЛЬ® Аллерген клещей
Экстракт аллергенов 50% Dermatophagoides farinae + 50% Dermatophagoides
pteronyssinus
Стандартизированые экстракты
Нет риска заражения вирусами
Собственная запатентованная культура
клещей компании Сталлержен, крупнейшего
производителя аллергенов клещей в мире
(700кг/год)
0,01 ИР 0,1 ИР
1 ИР
10 ИР
Начальный курс 4 флакона
10 ИР
Поддерживающий курс 1 флакон
81. Осложнения АСИТ
Местные:проявляются в местевведения аллергена, могут
отмечаться:
Системные :проявляются вне зоны
введения аллергена, могут
отмечаться уже через 30 минут:
Покраснение,
легкие системные реакции
(заложенность носа, зуд, чихание,
слезотечение, першение в горле,
сухой кашель).
Зуд,
Отек
Подобные появления могут
сохраняются от 1 до 3 суток, для их
минимизирования назначают
антигистаминные препараты.
При сублингвальном применении
местные реакции редко
развиваются и проходят
самостоятельно.
Среднетяжелые системные
реакции (затрудненное дыхание,
кожный зуд, высыпания по телу).
Тяжелые системные проявления
(бронхоспазм, генерализованная
крапивница, отек гортани,
анафилактический шок).
82. ВОПРОСЫ
1. Что такое иммунотерапия?2. Что такое иммунологический мониторинг?
3. Каковы виды иммунотерапии вам известны?
4. Перечислите основные принципы действия иммунотропных средств.
5. Какова классификация иммуномодуляторов?
6. Дайте характеристику иммунотропным препаратам по происхождению.
7. Перечислите основные показания к назначению иммунотерапии.
8. Перечислите основные противопоказания к назначению
иммунотерапии.
9. Что такое аллергенспецифическая иммунотерапия?
10. Каковы показания и противопоказания к проведению АСИТ?
83. Тестовые вопросы
Иммунтерапия-ЭТО:К иммунотропным средствам
относятся:
Усиление функций иммунной
системы
Подавление функций иммунной
системы
Группа препаратовиммуномодуляторов
Замещение функций иммунной
системы
Группа препаратовиммунодепрессантов
Группа препаратовиммуностимуляиторов
Группа препаратов
иммуномодуляторов,
иммуноститмуляторов,
иммунодепрессантов
Группа ганглиоблокаторов
Опосредованное влияние на
иммунную систему путем пересадки
стволовых клеток
Использование фармакологических
средств, направленных на усиление,
подавление или замещение функций
иммунной системы.
84. Тестовые вопросы
Противопоказаниями дляпроведения АСИТ являются:
К серьезным
осложнениям АСИТ
относят:
Тяжелые
иммунопатологические
состояния и иммунодефициты
Тяжелые психические
расстройства
Выраженный
бронхоспазм
Неконтролируемая
бронхиальная астма
Генерализованная
крапивница
Отек гортани
Анафилактический шок
Все перечисленное
Онкологические заболевания
Все перечисленное
85. Тестовые вопросы
Какие группыиммунотропных
препаратов выделяют:
По происхождению
иммунотропные
препараты разделяют:
Иммуностимуляторы
На микробные
Иммунодепрессанты
Нуклеиновые кислоты
Иммуноглобулины
Тимические
Вакцины, сыворотки
Костно-мозговые
Все перечисленное
Все перечисленное
86. Тестовые вопросы
Показания к назначениюиммунотерапии:
Первичные
иммунодефициты
Приобретенные
(вторичные)
иммунодефициты
Аллергопатология
Аутоиммунные заболевания
Аритмия
В зависимости от схемы
лечения АСИТ может
быть:
Предсезонной
Предсезонно-сезонной
Круглогодичной
Сезонной
Все
перечисленное
87. Тестовые вопросы
Сколько этаповпроведения АСИТ
включает в себя
любая схема:
Два
Три
Четыре
Пять
Один
АСИТ может быть назначена:
Пациентам с контролируемой
атопической бронхиальной астмой
(легкая и среднетяжелая формы)
Пациентам, страдающим атопическим
дерматитом легкого и среднетяжелого
течения с высокой степенью
сенсибилизации
Пациентам, страдающим сезонным
аллергическим ринитом (поллинозом)
Пациентам, страдающим неатопической
бронхиальной астмой
Все перечисленное верно
88.
Тетрадь (альбом) Занятие № 11Дата
Тема занятия: «Основы иммунотерапии»
1. Краткие ответы на развернутые вопросы (1 -10)
Дополнительные задания к занятию № 9:
2. укажите, какие типы терапии относятся к активной иммунотерапии,
какие- к активной, и почему?
3. Проверьте свой альбом за 2 цикл «Клиническая иммунология»
Альбом следует принести на зачетное занятие№ 12 и предъявить для
проверки.
89. Домашнее задание к занятию № 12 –повторение тем занятий 2 цикла:
Зачетное занятие по курсу «Клиническая иммунология» включает:Наличие альбома по иммунологии с выполненными заданиями
ответы на 10 тестовых заданий (1 тест-1 балл),
Ответы на 3 вопроса ( 1 вопрос-10 баллов)
Ответы на устные вопросы преподавателя по всем пройденным темам 2
цикла
Максимальный балл за зачет -40,
Минимальный балл -25.
Желаем успехов!!!








































































 Медицина
Медицина








