Похожие презентации:
Растворение. Растворимость веществ в воде
1. Растворение. Растворимость веществ в воде.
8 класс2. Растворы
1. Жидкие (водный, спиртовой,лекарственные настойки и т.д.)
2. Твердые (сплавы)
3. Газообразные (воздух)
3. Растворение. Растворы.
Физическая теория(Вант-Гофф, Оствальд,
Аррениус)
Химическая теория
(Менделеев, Каблуков,
Кистяковский)
• Растворениеэто процесс
диффузии.
• Растворы- это
однородные
смеси
• Растворение- это процесс
химического взаимодействия
растворяемого вещества с
водой – процесс гидратации
• Растворы- это соединения –
гидраты.
• Гидраты- это непрочные
соединения веществ с водой,
существующие в растворе.
4. Современная теория (физико-химическая теория)
• Растворение – это физикохимический процесс• Растворы- это однородная
(гомогенная) система, состоящая из
частиц растворенного вещества,
растворителя и продуктов их
взаимодействия- гидратов.
5. Состав гидратов
1. Непостоянный в растворах.2. Постоянный состав в кристаллогидратах:
Медный купорос – CuSO4. 5H2O
Глауберова соль- Na2SO4.10H2O
Сода кристаллическая- Na2CO4.10H2O
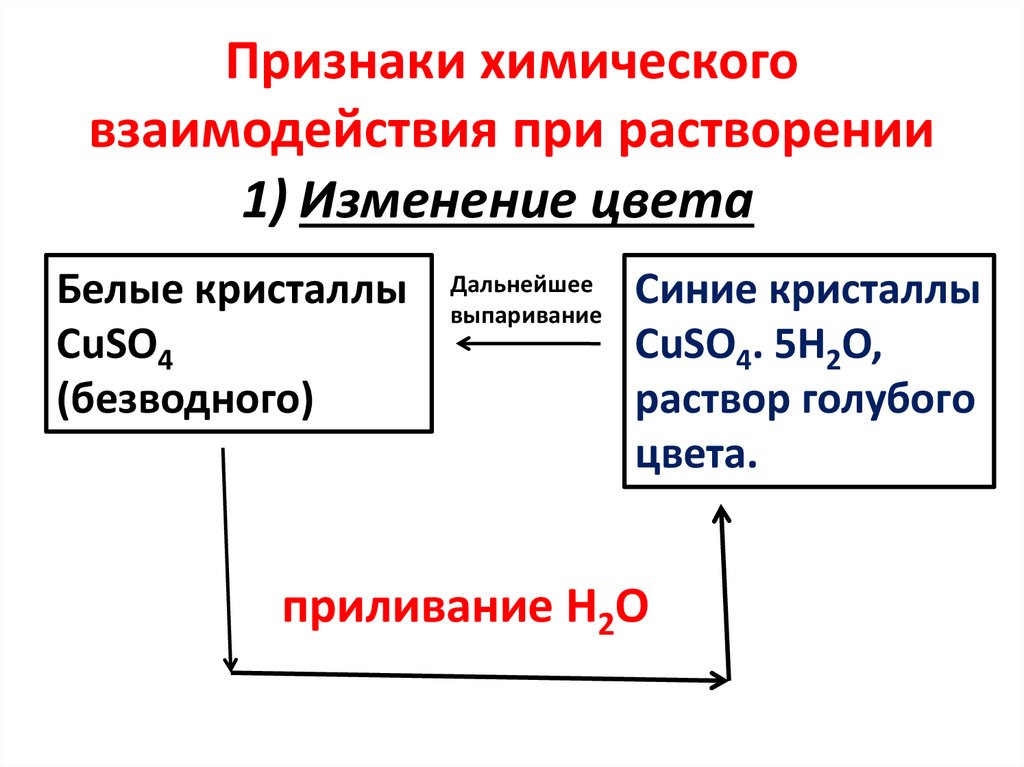
6. Признаки химического взаимодействия при растворении
1) Изменение цветаБелые кристаллы
CuSO4
(безводного)
Дальнейшее
выпаривание
Синие кристаллы
CuSO4. 5H2O,
раствор голубого
цвета.
приливание H2O
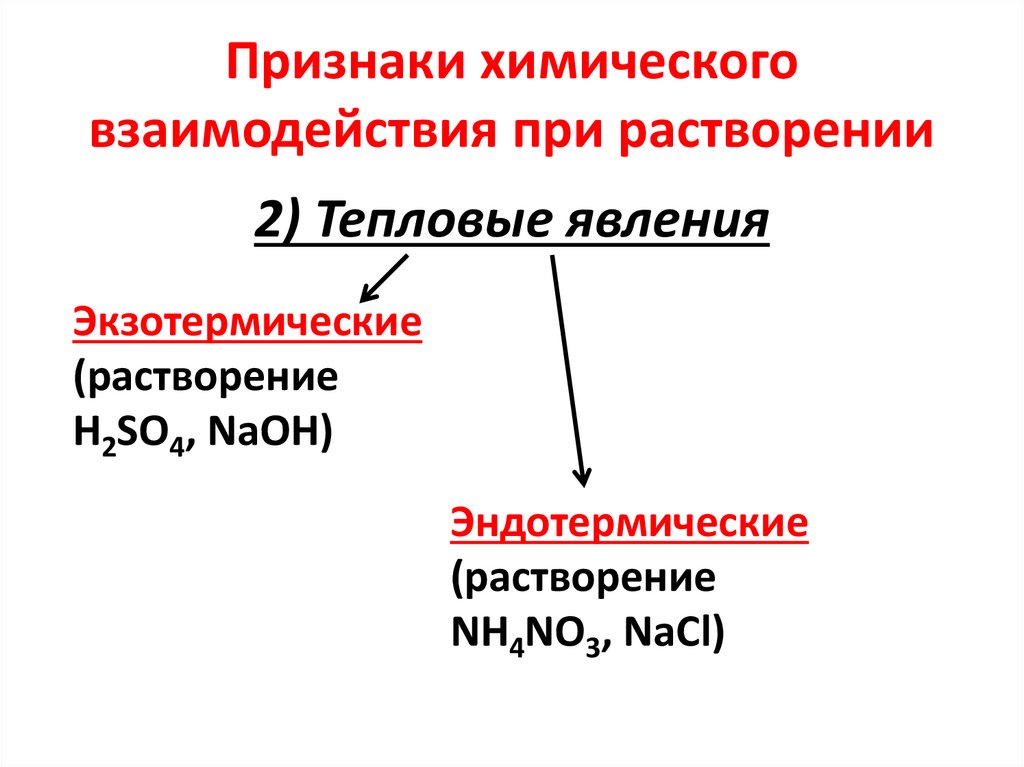
7. Признаки химического взаимодействия при растворении
2) Тепловые явленияЭкзотермические
(растворение
H2SO4, NaOH)
Эндотермические
(растворение
NH4NO3, NaCl)
8. Факторы, от которых зависит растворимость твёрдых веществ
1) От природы веществ (на 1 г H2O при 20 0С)-Хорошо растворимые ( более 1 г)
- Малорастворимые (менее 1 г)
-Практически нерастворимые (меньше 0,01г)
2) От температуры
9. Типы растворов по содержанию растворённого вещества
1) Ненасыщенные – вещество приданной температуре еще
растворяется
2) Насыщенные- больше не
растворяется
3) Перенасыщенные- содержат в
растворе больше вещества, чем
насыщенный раствор







 Химия
Химия








