Похожие презентации:
Растворение. Растворимость веществ в воде
1. Растворение. Растворимость веществ в воде.
2. Роль растворов
3. Что такое раствор и процесс растворения?
Теории растворовЯ. Х. Вант-Гофф,
С. Аррениус,
В. Оствальд.
Растворение-процесс
диффузии.
Растворы однородная
смесь.
Д.И. Менделеев,
И.А. Каблуков
Растворение-процесс
химическое
взаимодействие
растворённого вещества с
молекулами воды
4. Доказательство химического взаимодействия
Гидраты – непрочные соединениявеществ с водой, существующие в
растворе
Кристаллогидраты – соли и другие
твердые вещества, в состав которых
входит вода.
(и вода в данном случае называется
кристаллизационной)
5.
CuSO4 . 5H2O – медный купоросCuSO4
Раствор
CuSO4 в воде
Примеры
кристаллогидратов:
гипс CaSO4 · 2H2O,
сода Na2CO3 · 10Н2O.
6. Современная теория растворов – физико-химическая теория
Растворение-это физико-химическийпроцесс.
Раствор - однородная система, состоящая
из частиц растворённого вещества,
растворителя и продуктов их
взаимодействия.
7. Факторы, от которых зависит растворимость веществ
ТемператураС повышением температуры растворимость
твердых веществ увеличивается,
газообразных - уменьшается
8.
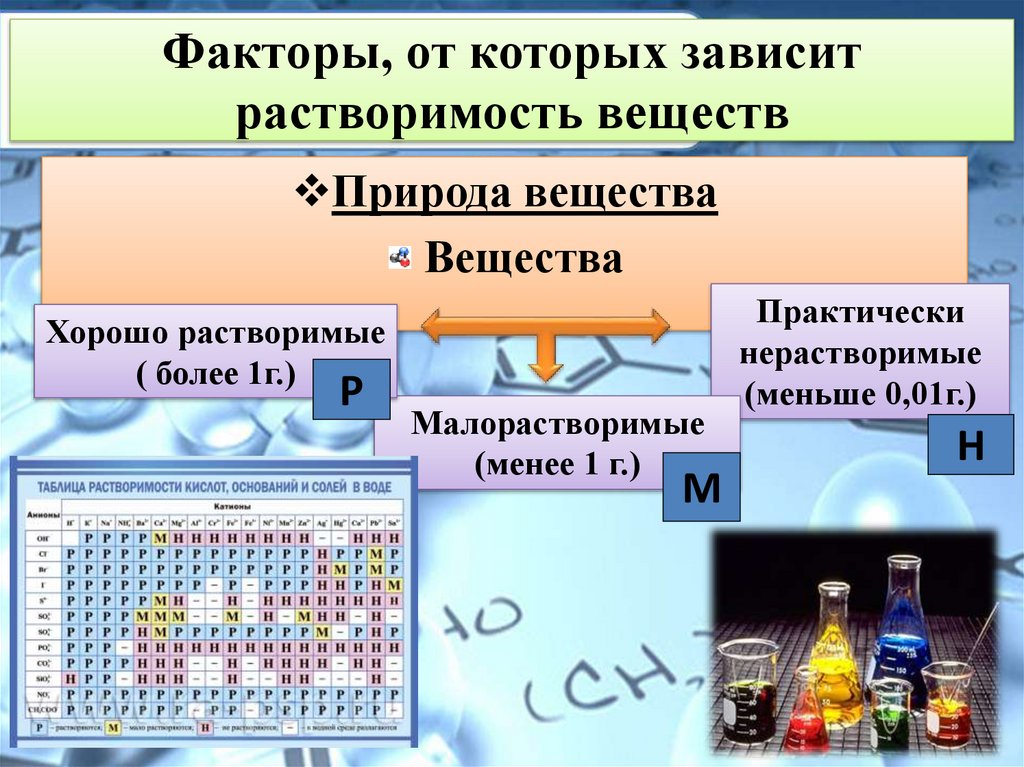
Факторы, от которых зависитрастворимость веществ
Природа вещества
Вещества
Хорошо растворимые
( более 1г.)
Р
Малорастворимые
(менее 1 г.)
М
Практически
нерастворимые
(меньше 0,01г.)
Н
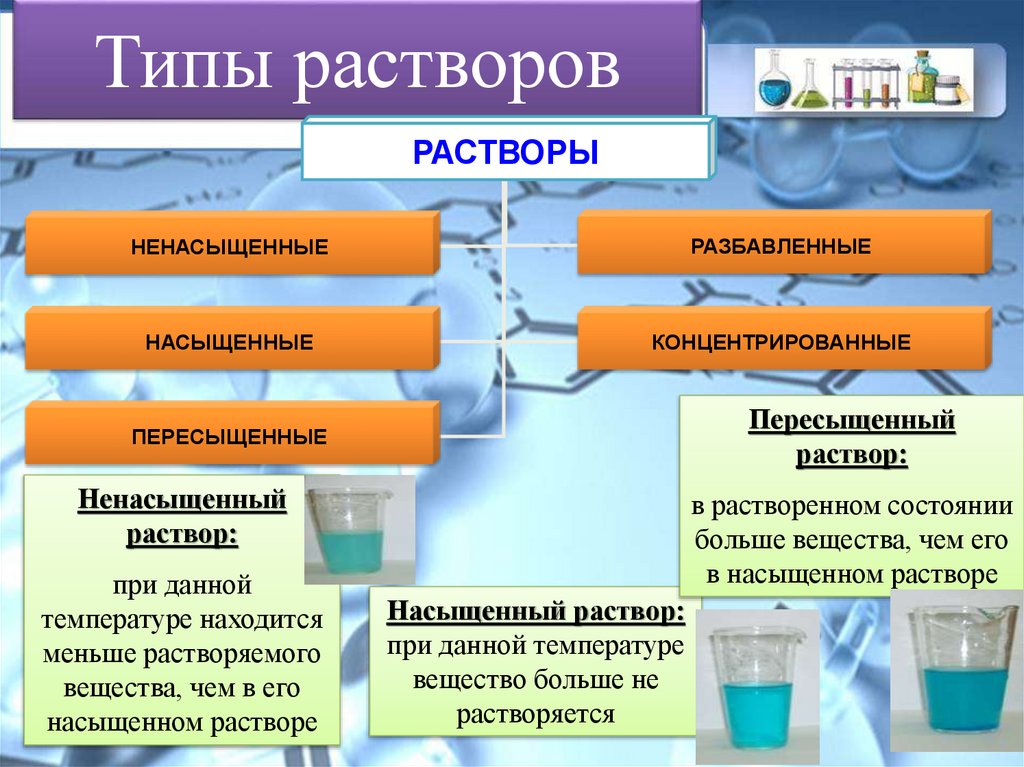
9. Типы растворов
РАСТВОРЫНЕНАСЫЩЕННЫЕ
РАЗБАВЛЕННЫЕ
НАСЫЩЕННЫЕ
КОНЦЕНТРИРОВАННЫЕ
Пересыщенный
раствор:
ПЕРЕСЫЩЕННЫЕ
Ненасыщенный
раствор:
при данной
температуре находится
меньше растворяемого
вещества, чем в его
насыщенном растворе
в растворенном состоянии
больше вещества, чем его
в насыщенном растворе
Насыщенный раствор:
при данной температуре
вещество больше не
растворяется
10. Как обозначают массовую долю вещества в растворе?
Задача. Для консервирования огурцовприготовили рассол: на 2 л воды взяли 200 г
соли, а для консервирования томатов –
рассол из 200 г соли и 3 л воды. Какой
рассол получится более
концентрированным?
11. Работа с учебником
Стр. 213, рис. 126 ответьте на вопросы:Какова растворимость хлорида калия при
30 0 С?
Какова растворимость сульфата калия при
80 0 С?











 Химия
Химия








