Похожие презентации:
Пятичленные гетероциклы с двумя гетероатомами - азолы
1. Химия биологически активных веществ
Лекция 7Пятичленные гетероциклы
с двумя гетероатомами - азолы
2.
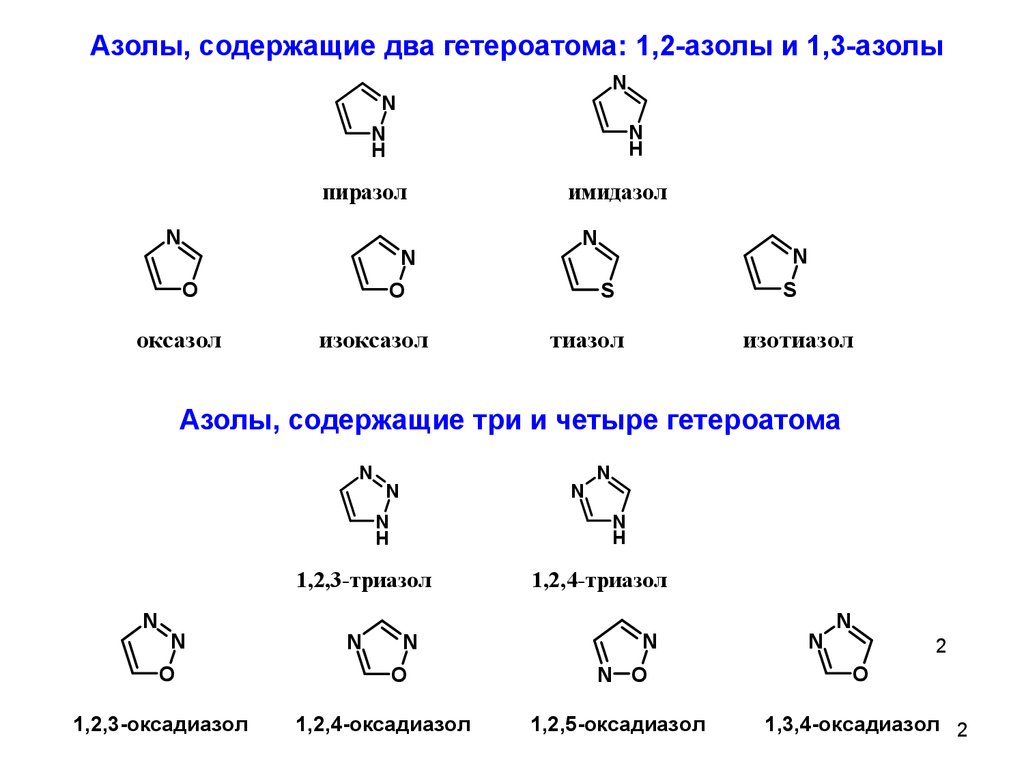
Азолы, содержащие два гетероатома: 1,2-азолы и 1,3-азолыN
N
N
H
N
H
пиразол
N
N
O
оксазол
имидазол
N
O
изоксазол
N
S
S
тиазол
изотиазол
Азолы, содержащие три и четыре гетероатома
N
N
N
N
H
N
H
1,2,3-триазол
N
N
O
1,2,3-оксадиазол
N
N
N
O
1,2,4-оксадиазол
1,2,4-триазол
N
N
N
2
3
N O
O
1,2,5-оксадиазол
1,3,4-оксадиазол 2
3.
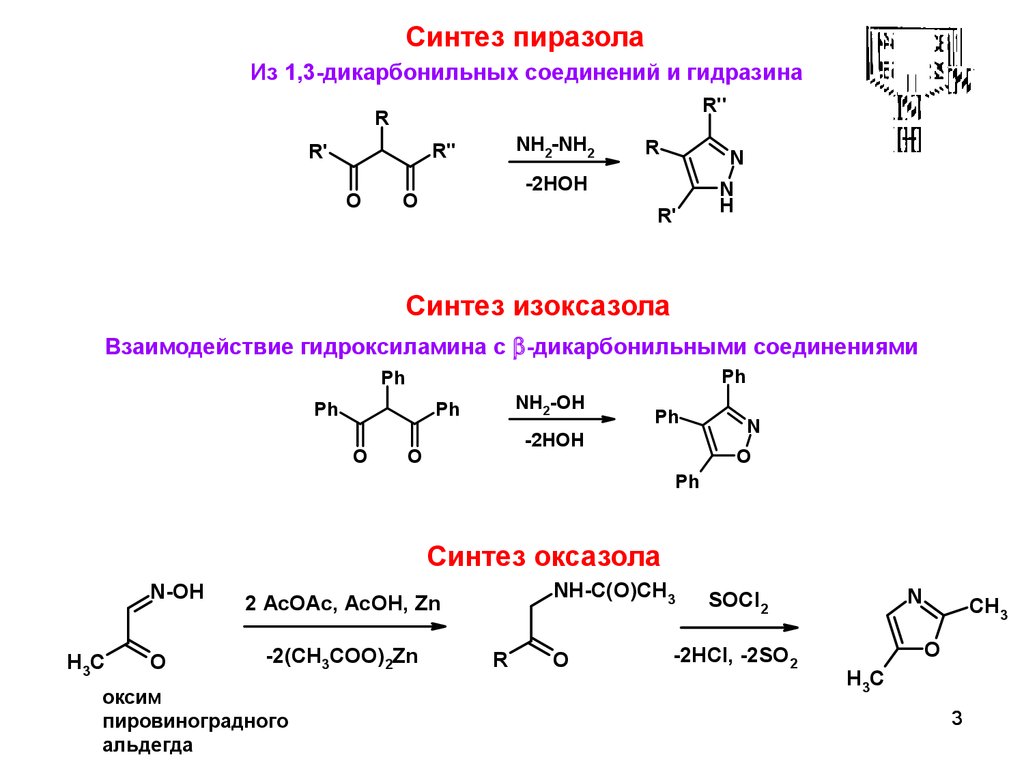
Синтез пиразолаИз 1,3-дикарбонильных соединений и гидразина
R''
R
NH2-NH2
R''
R'
O
R
N
-2HOH
O
R'
N
H
Синтез изоксазола
Взаимодействие гидроксиламина с -дикарбонильными соединениями
Ph
Ph
NH2-OH
Ph
Ph
O
Ph
-2HOH
O
N
O
Ph
Синтез оксазола
N-OH
H3C
O
NH-C(O)CH3
2 AcOAc, AcOH, Zn
-2(CH3COO)2Zn
оксим
пировиноградного
альдегда
R
O
N
SOCl2
-2HCl, -2SO2
CH3
O
H3C
36
4.
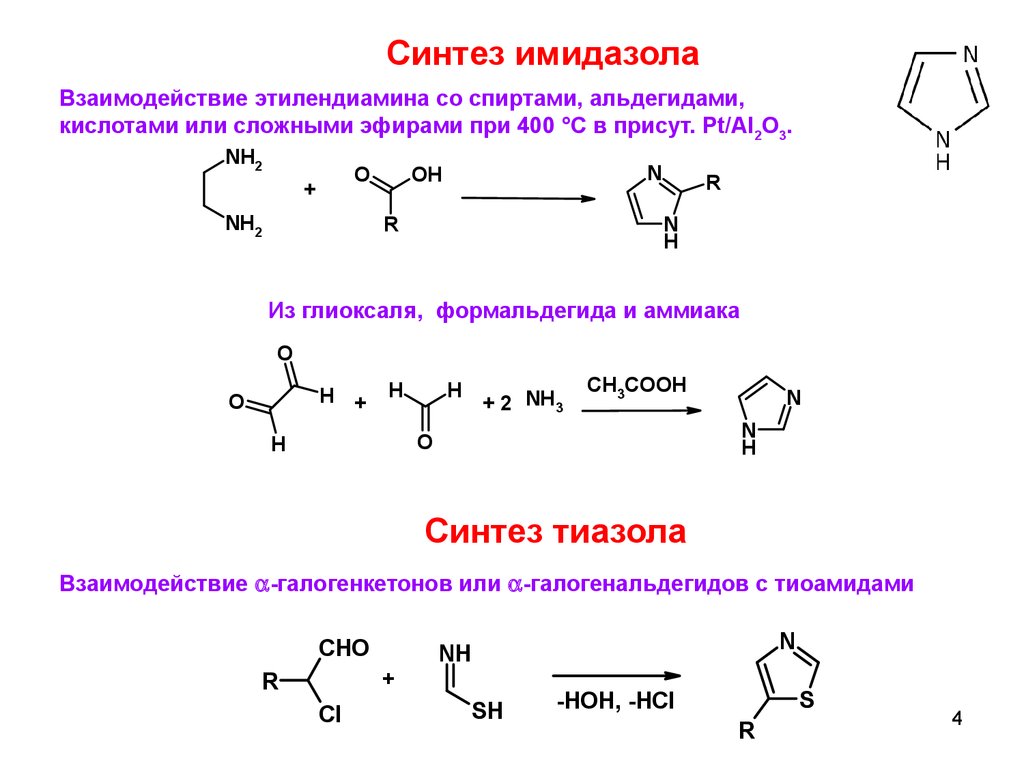
Синтез имидазолаВзаимодействие этилендиамина со спиртами, альдегидами,
кислотами или сложными эфирами при 400 °С в присут. Pt/Al2O3.
NH2
O
+
NH2
N
OH
R
R
N
H
Из глиоксаля, формальдегида и аммиака
O
H +
O
H
H
+ 2 NH3
CH3COOH
N
H
O
H
N
Синтез тиазола
Взаимодействие -галогенкетонов или -галогенальдегидов с тиоамидами
CHO
+
R
Cl
N
NH
SH
S
-HOH, -HCl
R
4
5.
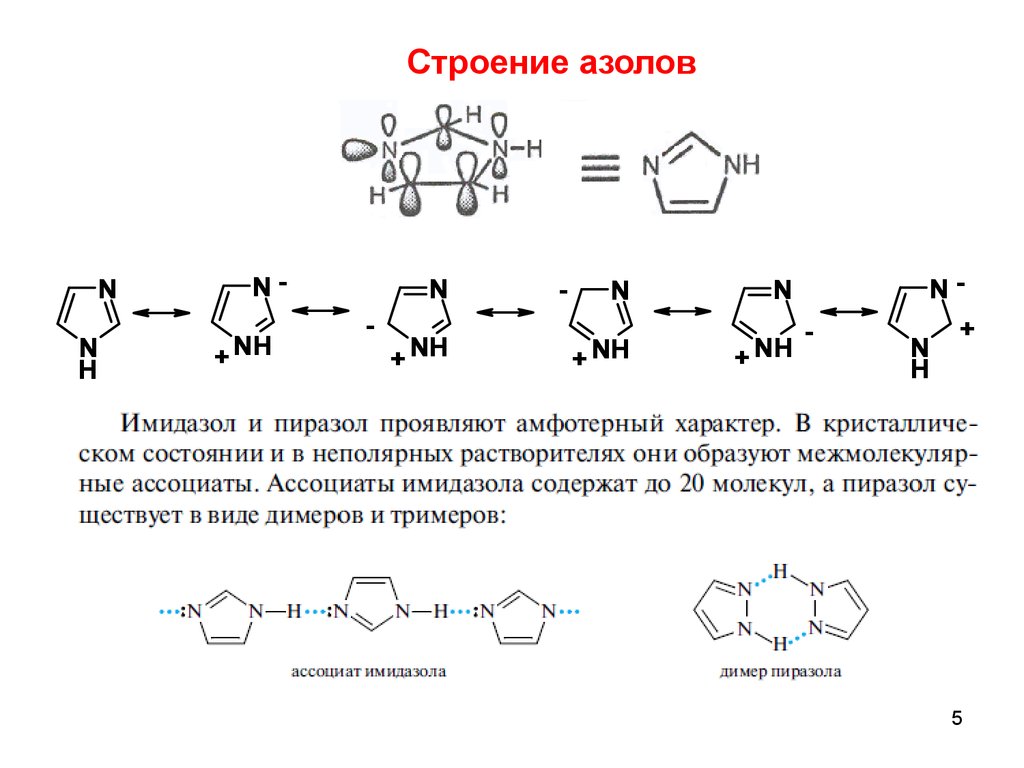
Строение азоловN
N
H
N+ NH
N
-
+ NH
-
N
N
+ NH
+ NH
-
N+
N
H
5
9
6.
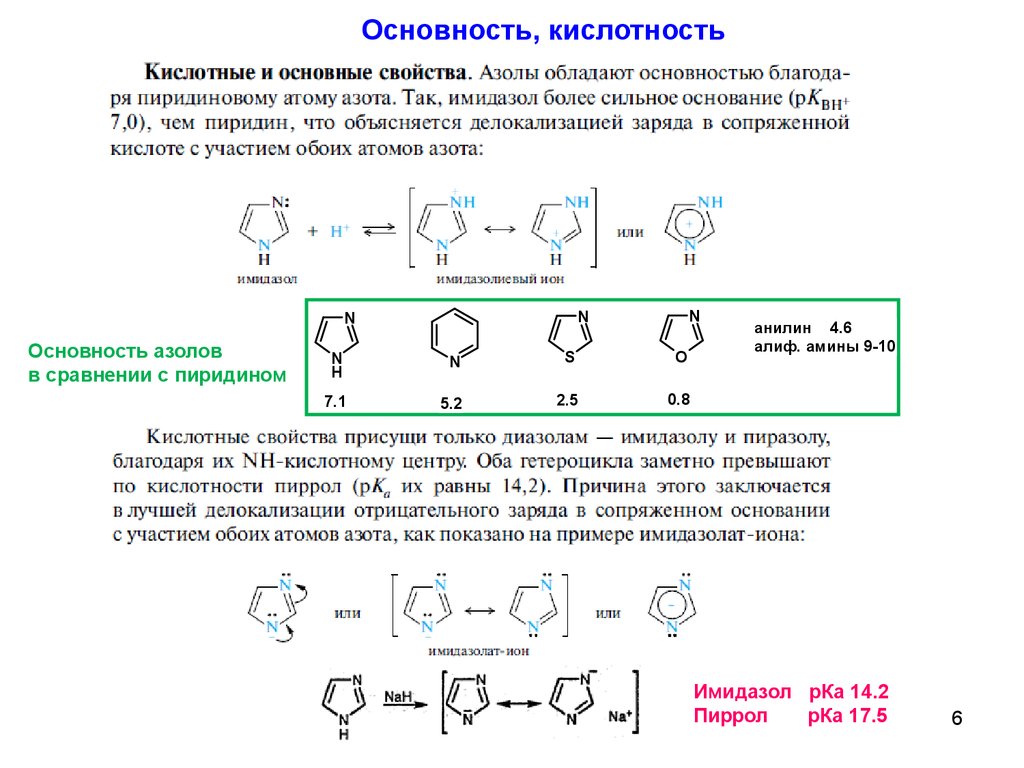
Основность, кислотностьОсновность азолов
в сравнении с пиридином
N
N
N
N
H
N
S
O
7.1
5.2
2.5
0.8
анилин 4.6
алиф. амины 9-10
Имидазол рКа 14.2
Пиррол
рКа 17.5
6
7.
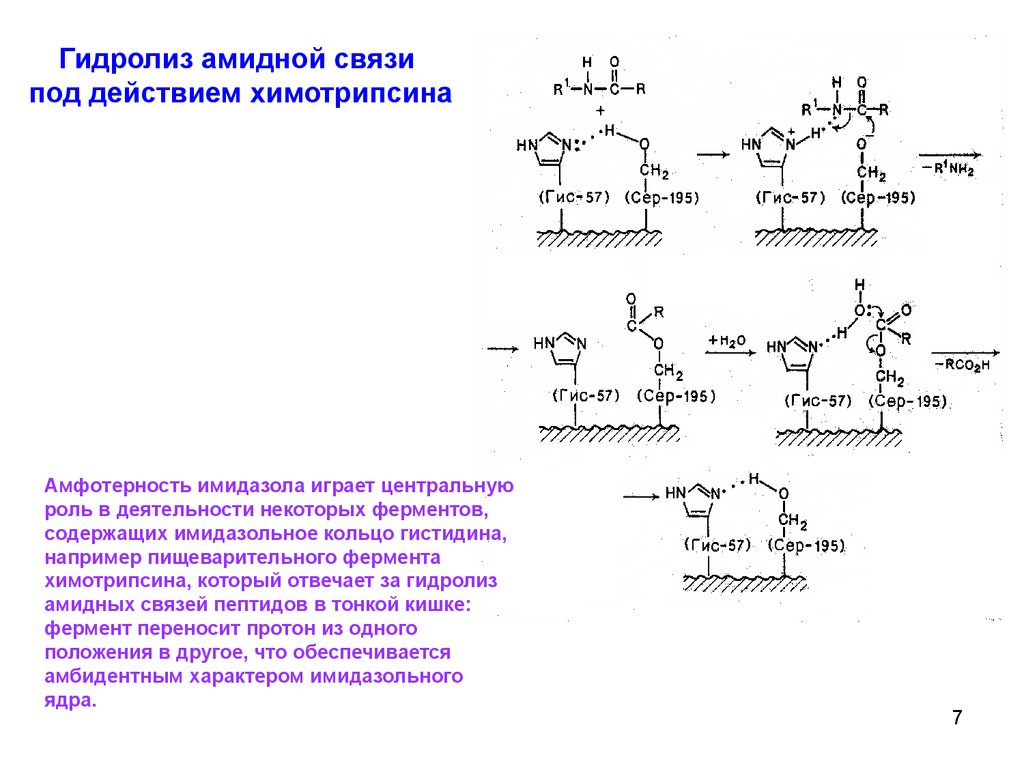
Гидролиз амидной связипод действием химотрипсина
Амфотерность имидазола играет центральную
роль в деятельности некоторых ферментов,
содержащих имидазольное кольцо гистидина,
например пищеварительного фермента
химотрипсина, который отвечает за гидролиз
амидных связей пептидов в тонкой кишке:
фермент переносит протон из одного
положения в другое, что обеспечивается
амбидентным характером имидазольного
ядра.
7
8.
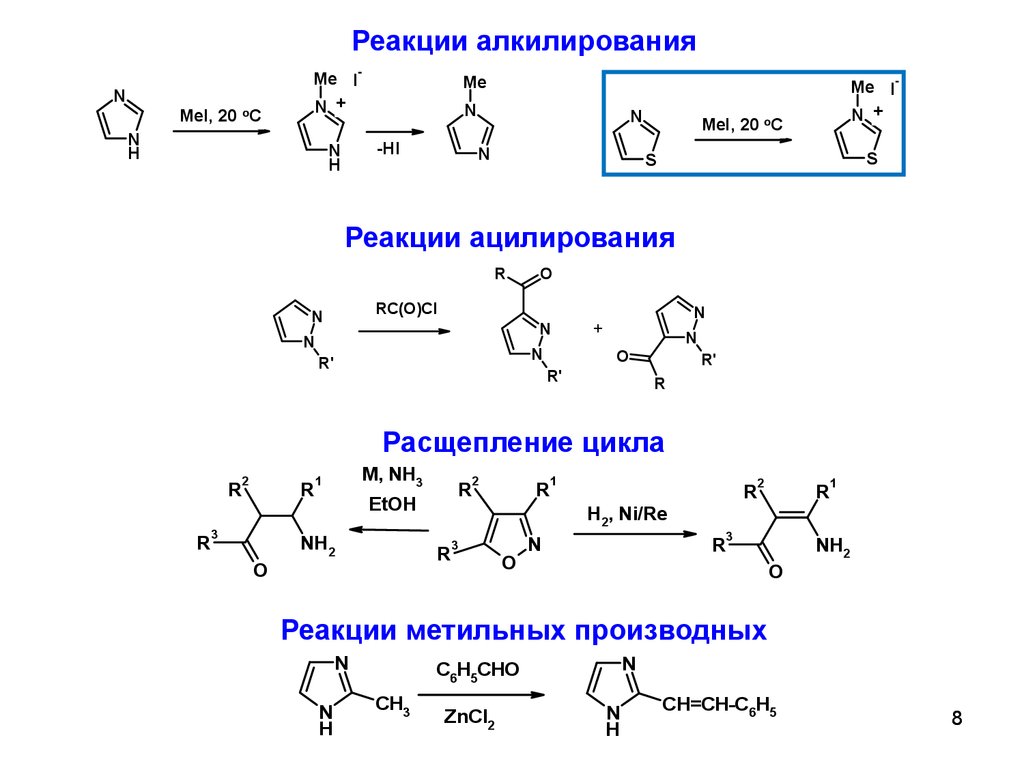
Реакции алкилированияN
MeI, 20 oC
Me IN +
N
H
Me
N
-HI
N
H
N
N
Me IN +
MeI, 20 oC
S
S
Реакции ацилирования
R
O
RC(O)Cl
N
N
N
N
R'
N
+
N
O
R'
R'
R
Расщепление цикла
R
R
2
R
3
M, NH3
1
R
EtOH
NH2
R
1
2
R
R
1
H2, Ni/Re
R
O
2
3
O
N
R
3
NH2
O
Реакции метильных производных
N
N
H
N
C6H5CHO
CH3
ZnCl2
N
H
CH=CH-C6H5
8
9.
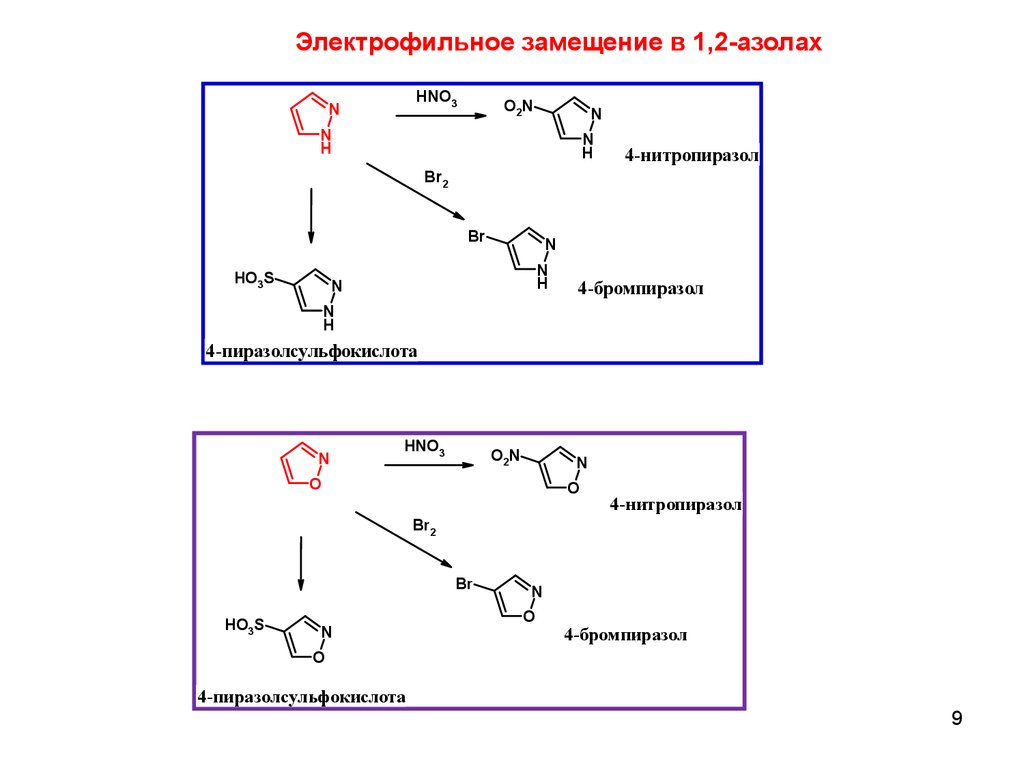
Электрофильное замещение в 1,2-азолахHNO3
N
O2N
N
N
H
N
H
4-нитропиразол
Br2
Br
HO3S
N
N
H
N
4-бромпиразол
N
H
4-пиразолсульфокислота
N
HNO3
O2N
N
O
O
4-нитропиразол
Br2
Br
HO3S
N
N
O
4-бромпиразол
O
4-пиразолсульфокислота
9
10.
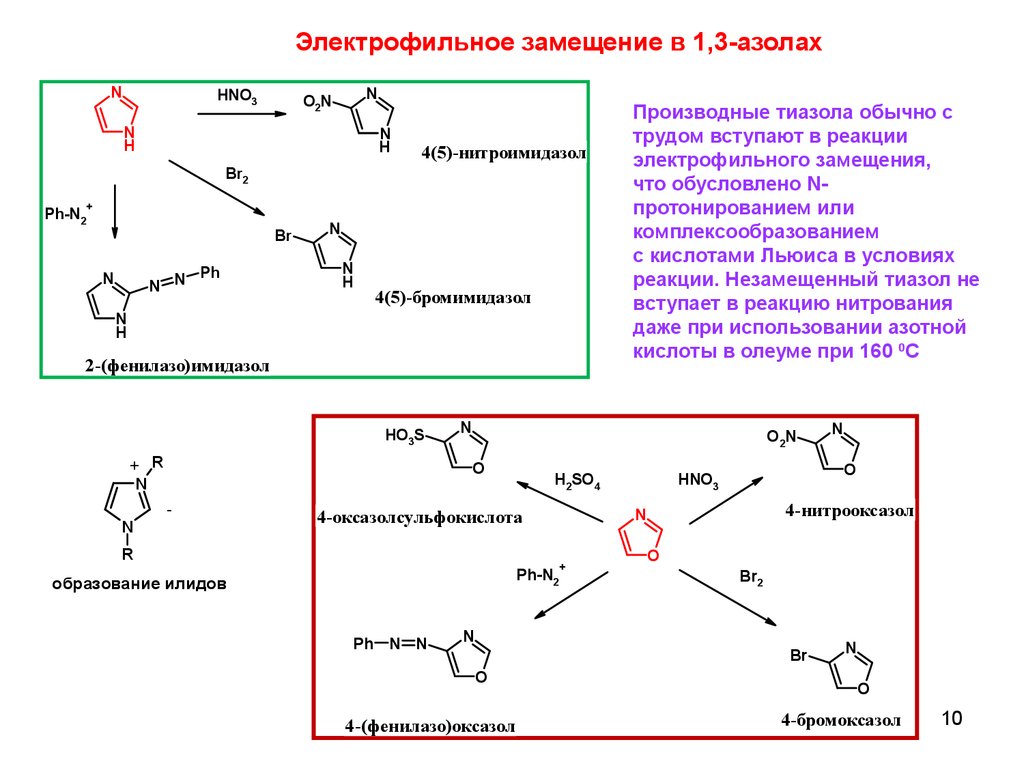
Электрофильное замещение в 1,3-азолахN
HNO3
N
O2N
N
H
N
H
4(5)-нитроимидазол
Br2
+
Ph-N2
Br
Ph
N N
N
N
N
H
4(5)-бромимидазол
N
H
2-(фенилазо)имидазол
HO3S
+ R
N
N
N
O2N
O
-
H2SO4
R
+
Ph-N2
образование илидов
4-нитрооксазол
O
Br2
N
Br
O
4-(фенилазо)оксазол
N
O
HNO3
N
4-оксазолсульфокислота
Ph N N
Производные тиазола обычно с
трудом вступают в реакции
электрофильного замещения,
что обусловлено Nпротонированием или
комплексообразованием
с кислотами Льюиса в условиях
реакции. Незамещенный тиазол не
вступает в реакцию нитрования
даже при использовании азотной
кислоты в олеуме при 160 0С
N
O
4-бромоксазол
10
11.
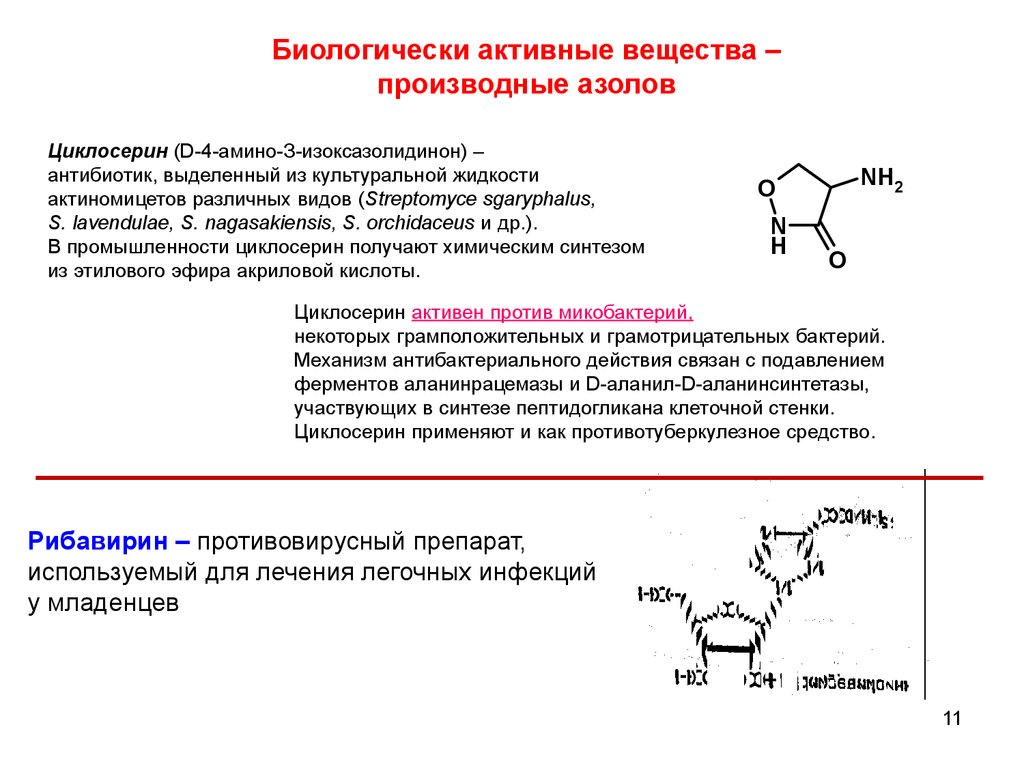
Биологически активные вещества –производные азолов
Циклосерин (D-4-амино-З-изоксазолидинон) –
антибиотик, выделенный из культуральной жидкости
актиномицетов различных видов (Streptomyce sgaryphalus,
S. lavendulae, S. nagasakiensis, S. orchidaceus и др.).
В промышленности циклосерин получают химическим синтезом
из этилового эфира акриловой кислоты.
NH2
O
N
H
O
Циклосерин активен против микобактерий,
некоторых грамположительных и грамотрицательных бактерий.
Механизм антибактериального действия связан с подавлением
ферментов аланинрацемазы и D-аланил-D-аланинсинтетазы,
участвующих в синтезе пептидогликана клеточной стенки.
Циклосерин применяют и как противотуберкулезное средство.
Рибавирин – противовирусный препарат,
используемый для лечения легочных инфекций
у младенцев
11
11
12.
ClN
H3 C
-
+
N
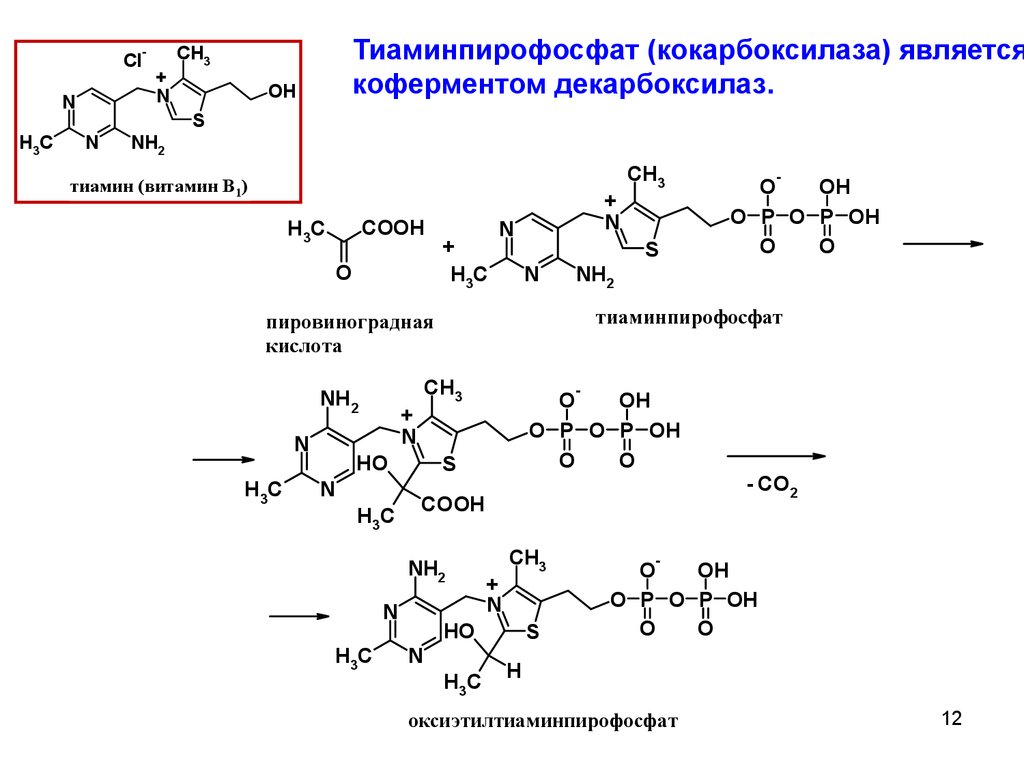
Тиаминпирофосфат (кокарбоксилаза) является
коферментом декарбоксилаз.
CH3
OH
S
N
NH2
тиамин (витамин В1)
COOH
H3C
O
+
H3C
+
N
N
S
N
тиаминпирофосфат
N
H3C
CH3
+
N
HO
N
H3C
COOH
NH2
H3 C
-
O
OH
O P O P OH
O
O
S
N
-
O
OH
O P O P OH
O
O
NH2
пировиноградная
кислота
NH2
CH3
+
N
CH3
HO
N
H3C
S
- CO2
-
O
OH
O P O P OH
O
O
H
оксиэтилтиаминпирофосфат
12
13.
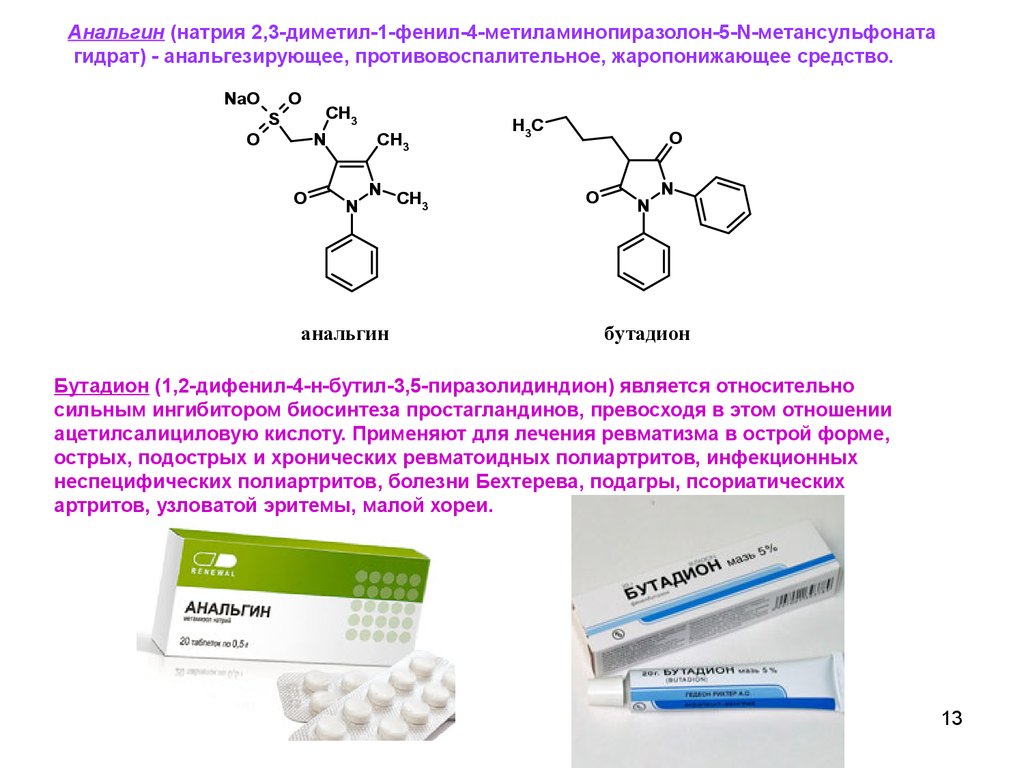
Анальгин (натрия 2,3-диметил-1-фенил-4-метиламинопиразолон-5-N-метансульфонатагидрат) - анальгезирующее, противовоспалительное, жаропонижающее средство.
NaO
O
S
CH3
N
O
O
CH3
N
N
анальгин
CH3
H3C
O
O
N
N
бутадион
Бутадион (1,2-дифенил-4-н-бутил-3,5-пиразолидиндион) является относительно
сильным ингибитором биосинтеза простагландинов, превосходя в этом отношении
ацетилсалициловую кислоту. Применяют для лечения ревматизма в острой форме,
острых, подострых и хронических ревматоидных полиартритов, инфекционных
неспецифических полиартритов, болезни Бехтерева, подагры, псориатических
артритов, узловатой эритемы, малой хореи.
13
14
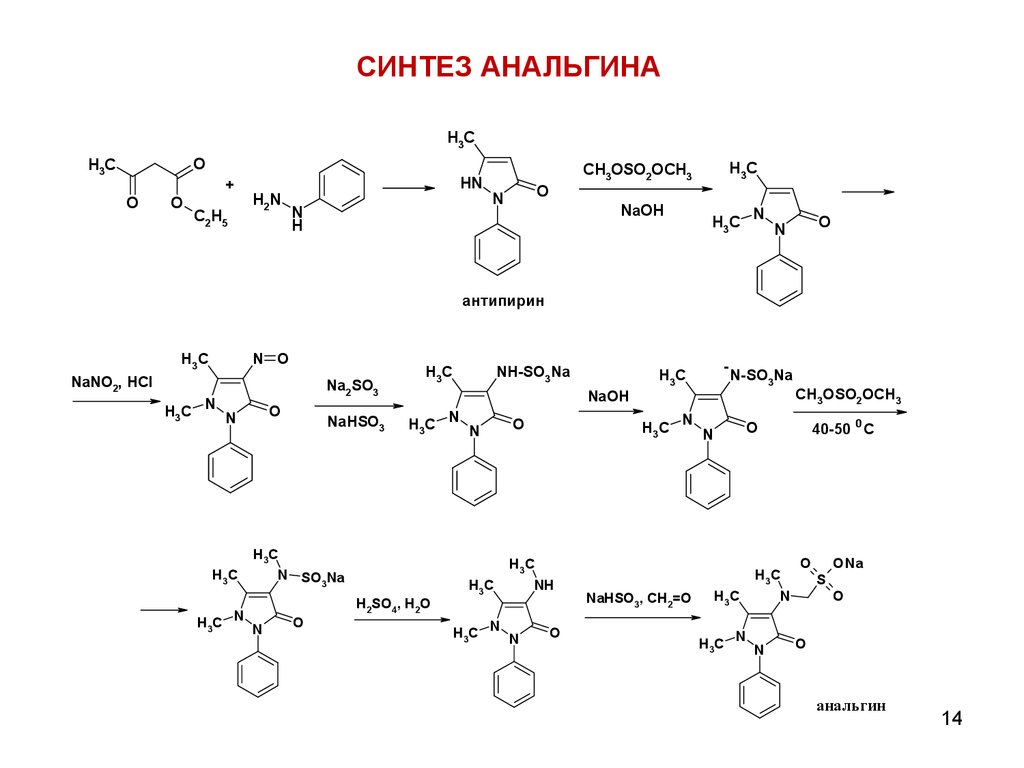
14.
СИНТЕЗ АНАЛЬГИНАH3C
O
H3C
+
O
O
C2H5
H2N
HN
N
H
O
N
H3C
CH3OSO2OCH3
NaOH
H3C
N
O
N
антипирин
H3C
N O
NaNO2, HCl
H3C
N
Na2SO3
O
N
NaHSO3
H3C
NH-SO3Na
NaOH
H3C
N
N
H3C
H3C
H3C
N
N SO Na
3
N
O
H2SO4, H2O
H3C
O
H3C
H3C
NH
H3C N N
O
-
H3C
N
NaHSO3, CH2=O
N-SO3Na
CH3OSO2OCH3
40-50 0 C
O
N
H3C
H3C
N
H3C
N
N
O Na
O
S
O
O
анальгин
14
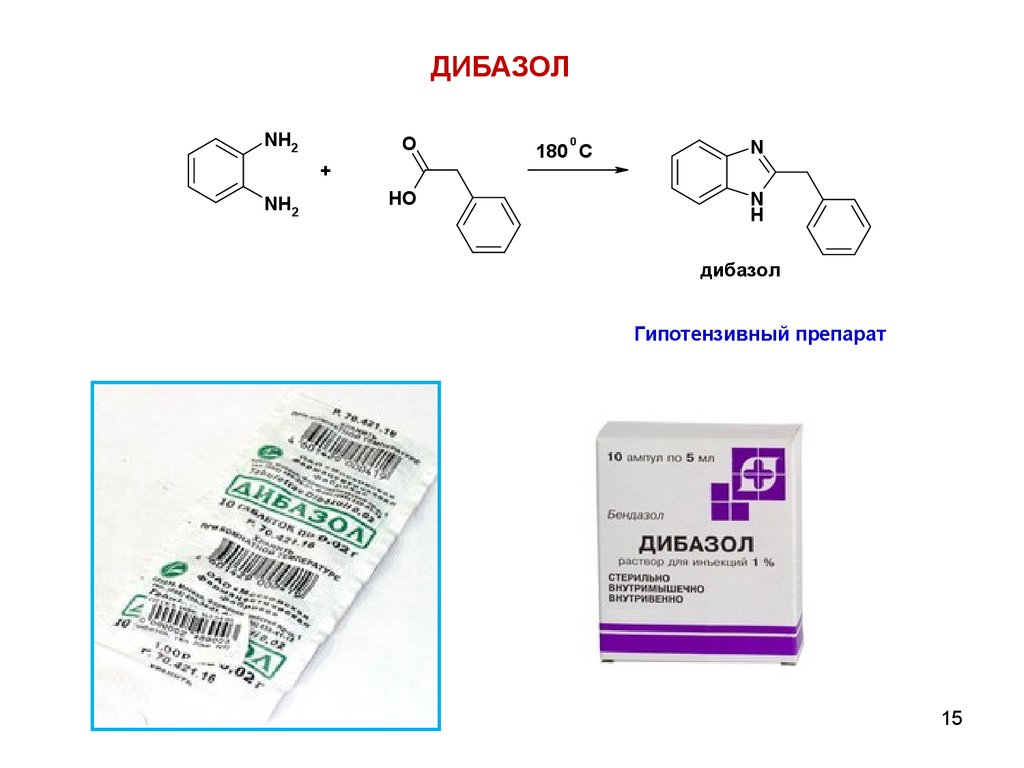
15.
ДИБАЗОЛNH2
O
+
NH2
HO
0
180 C
N
N
H
дибазол
Гипотензивный препарат
15
16.
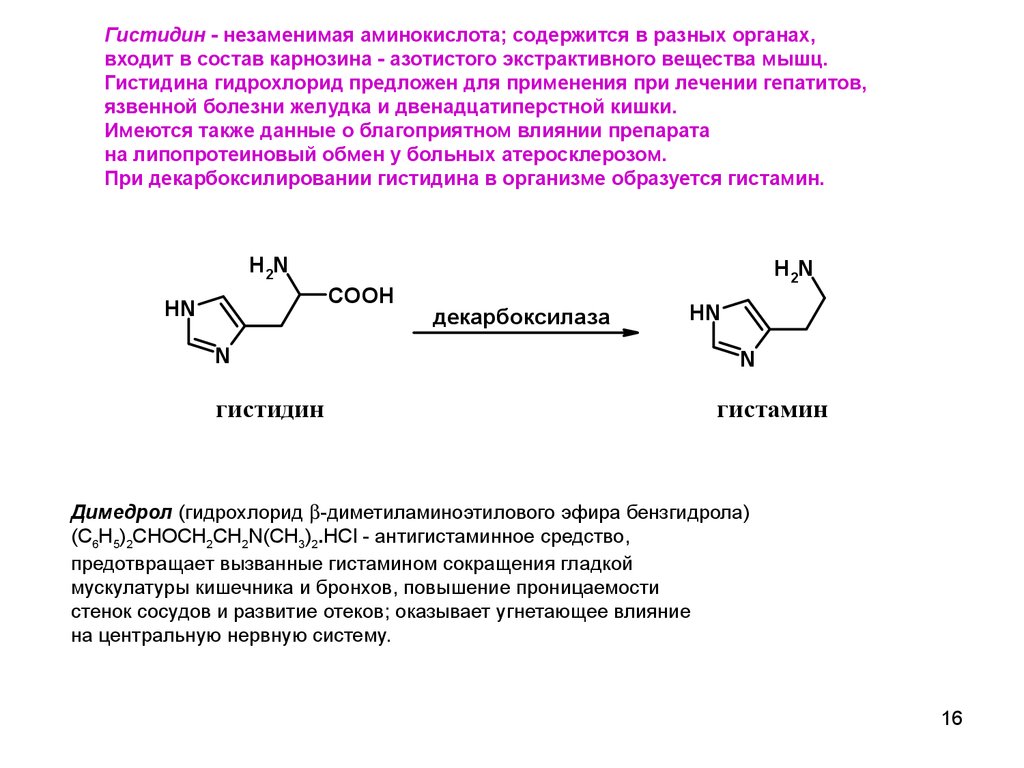
Гистидин - незаменимая аминокислота; содержится в разных органах,входит в состав карнозина - азотистого экстрактивного вещества мышц.
Гистидина гидрохлорид предложен для применения при лечении гепатитов,
язвенной болезни желудка и двенадцатиперстной кишки.
Имеются также данные о благоприятном влиянии препарата
на липопротеиновый обмен у больных атеросклерозом.
При декарбоксилировании гистидина в организме образуется гистамин.
H2N
COOH
HN
N
гистидин
H2N
декарбоксилаза
HN
N
гистамин
Димедрол (гидрохлорид -диметиламиноэтилового эфира бензгидрола)
(C6H5)2CHOCH2CH2N(CH3)2.HCl - антигистаминное средство,
предотвращает вызванные гистамином сокращения гладкой
мускулатуры кишечника и бронхов, повышение проницаемости
стенок сосудов и развитие отеков; оказывает угнетающее влияние
на центральную нервную систему.
16
15
17.
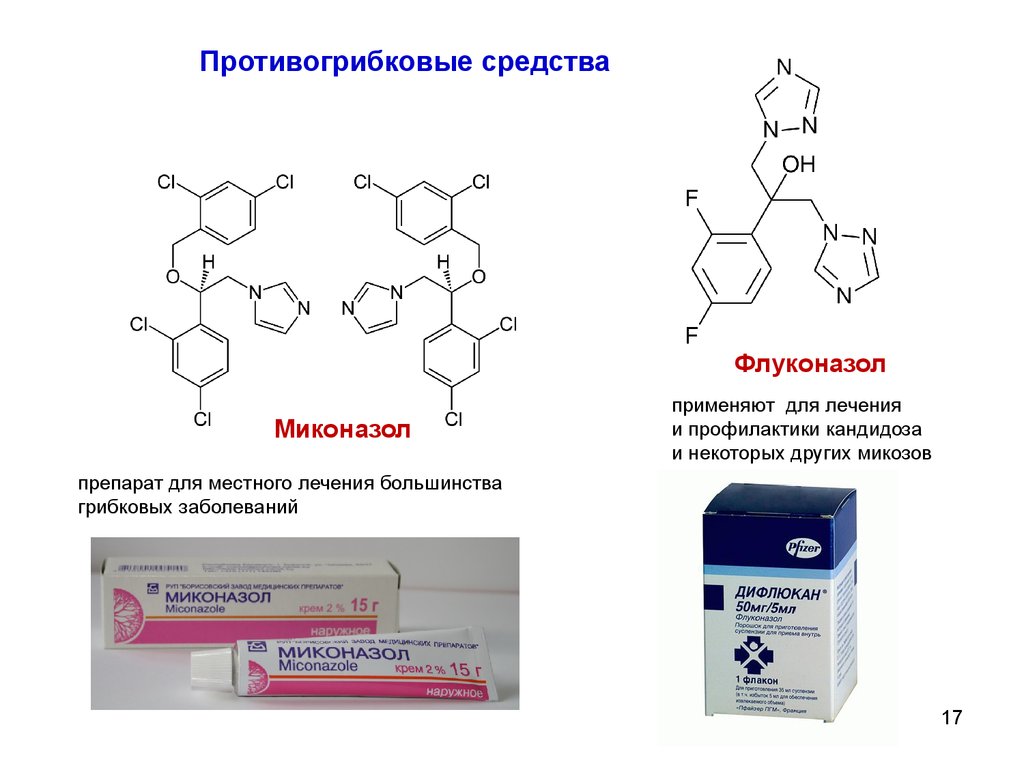
Противогрибковые средстваФлуконазол
Миконазол
применяют для лечения
и профилактики кандидоза
и некоторых других микозов
препарат для местного лечения большинства
грибковых заболеваний
17
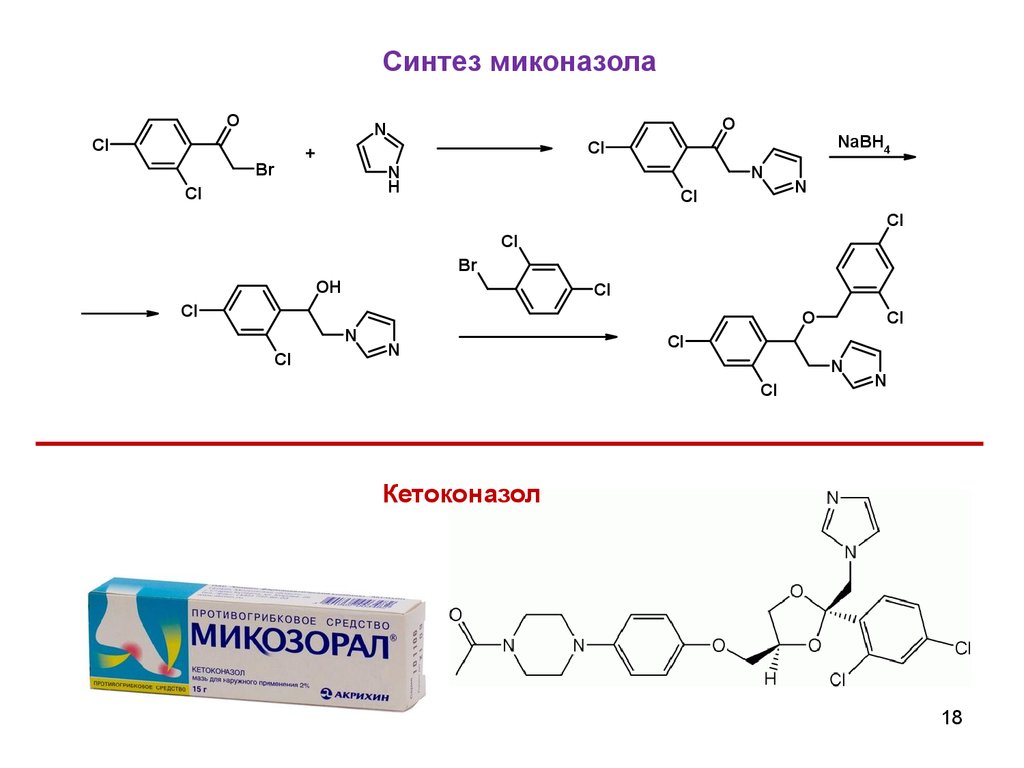
18.
Синтез миконазолаO
O
N
Cl
Br
+
N
N
H
Cl
NaBH4
Cl
Cl
N
Cl
Cl
Br
OH
Cl
Cl
N
Cl
O
N
Cl
Cl
N
Cl
N
Кетоконазол
18
19.
Курс лекций является частью учебно-методического комплекса«Химия биологически активных веществ»
автор:
Носова Эмилия Владимировна, д.х.н., доцент кафедры органической и
биомолекулярной химии ХТИ УрФУ
лектор
Учебно-методический комплекс подготовлен на кафедре органической химии
химико-технологического института УрФУ
Никакая часть презентации не может быть воспроизведена в
какой бы то ни было форме без письменного разрешения авторов
19 11


 Химия
Химия