Похожие презентации:
Тетраэдр или квадрат
1. Тетраэдр или квадрат? Или все же тетраэдр?
Бушмин Дмитрий Сергеевич2. Основоположники VSEPR
Н. СиджвикР. Гиллеспи
Р. Найхолм
3.
Основные модели VSEPR◉
Каждая электронная пара валентной оболочки центрального атома A в
молекуле AXn, содержащей одинарные связи A – X, является стереохимически
значимой, и отталкивание между ними определяет форму молекулы.
◉
Электрон-электронное отталкивание электронных пар уменьшается в
следующей последовательности: неподеленная-неподеленная > неподеленнаясвязывающая > связывающая-связывающая
◉
Если атом E образует кратные связи с атомом X, электрон-электронное
отталкивание связей уменьшается в следующем ряду: тройная-одинарная >
двойная-одинарная > одинарная-одинарная
4.
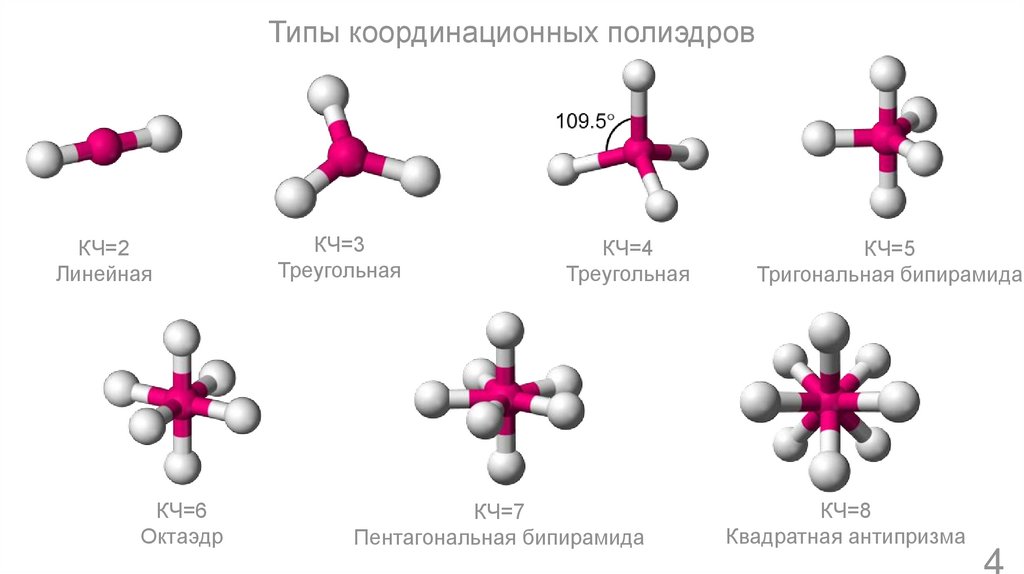
Типы координационных полиэдровКЧ=2
Линейная
КЧ=6
Октаэдр
КЧ=3
Треугольная
КЧ=4
Треугольная
КЧ=7
Пентагональная бипирамида
КЧ=5
Тригональная бипирамида
КЧ=8
Квадратная антипризма
4
5.
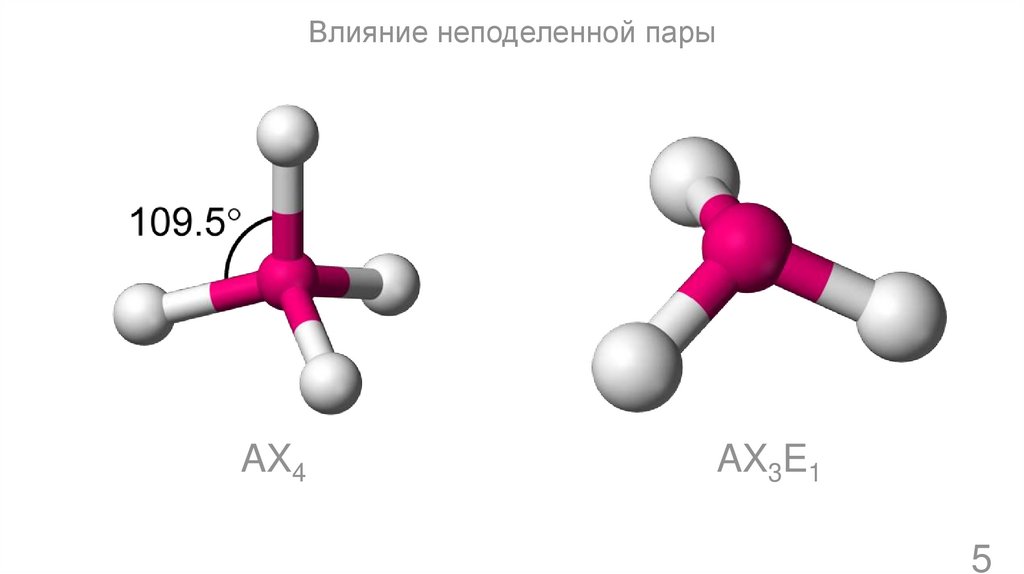
Влияние неподеленной парыAX4
AX3E1
5
6.
Порядок определения геометрии методом VSEPRОпределить число связей и неподеленных
электронных пар
◉
◉
◉
Определить «основную геометрию» для
данного количества электронных пар
Заполнить связи и неподеленны пары согласно
«основную геометрии» с учетом дополнения
Найхольма
7.
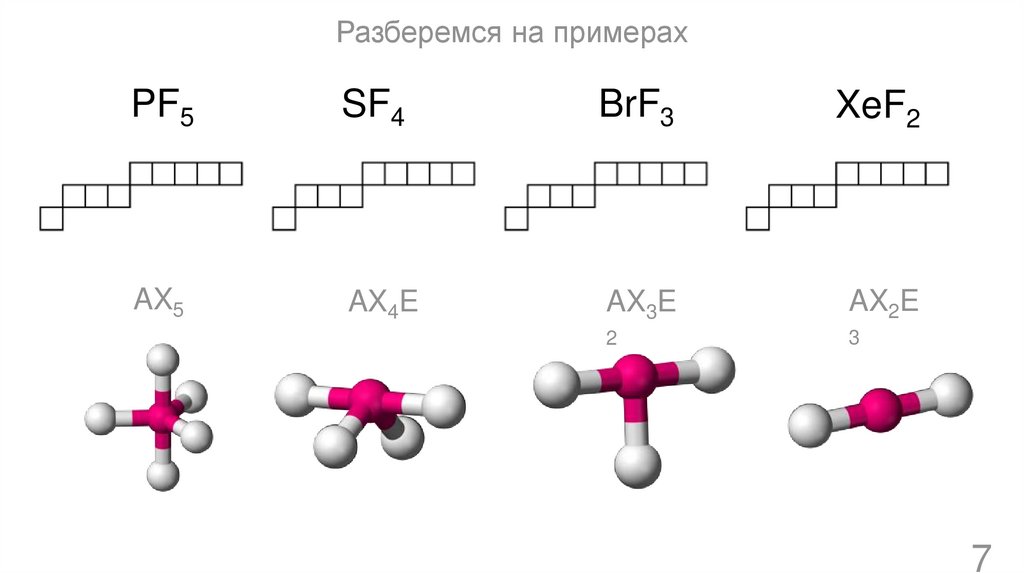
Разберемся на примерахPF5
SF4
BrF3
XeF2
AX5
AX4E
AX3E
AX2E
2
3
7
8.
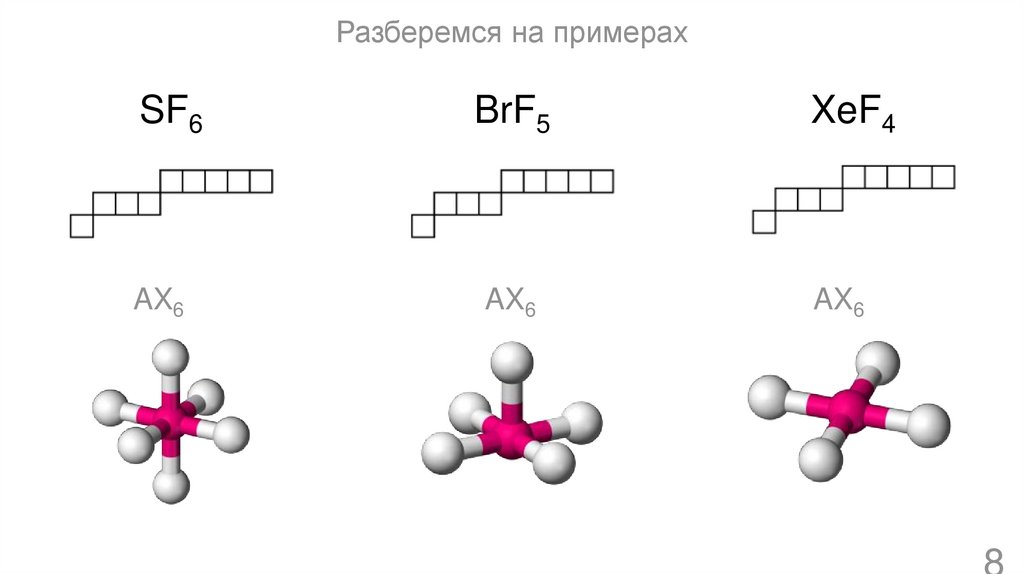
Разберемся на примерахSF6
AX6
BrF5
AX6
XeF4
AX6
8
9.
◉Задание для самостоятельного
изучения: изобразить
геометрию частиц IF7, XeOF5- ,
XeF5-
10.
Ограничения модели VSEPRНе учитывает стерического
фактора
Не учитывает стереохимически
неактивные пары (например в
XeF82◉ Не учитывает действие
неспаренных электронов
Не работает для комплексных
соединений d-элементов:
◉
◉
◉
[V(H2O)6]3+ (d2) , [Mn(H2O)6]2+ (d4), [Co(H2O)6]3+
(d6), [Ni(H2O)6]2+ (d8), [Zn(H2O)6]2+ (d10)
10
11.
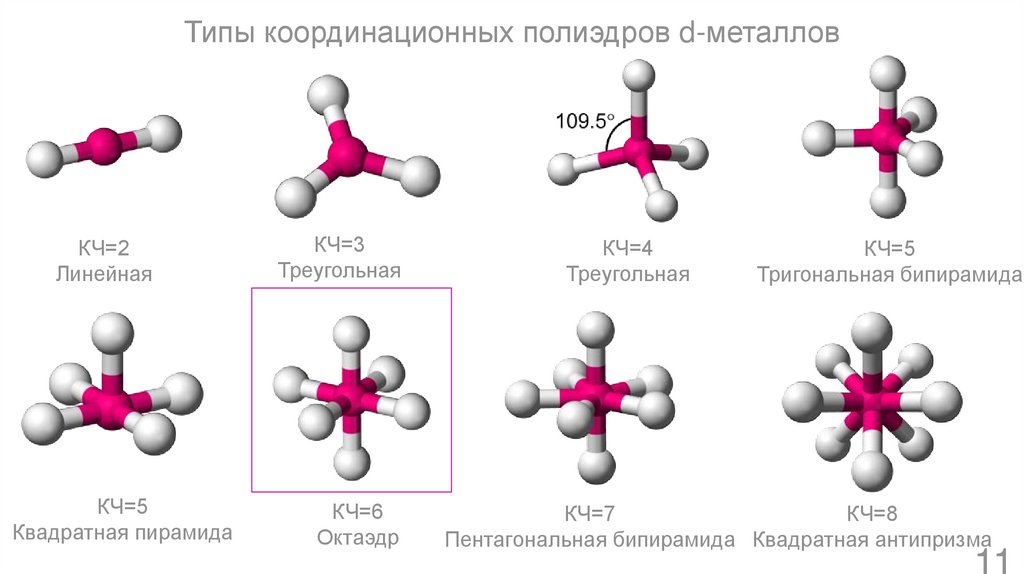
Типы координационных полиэдров d-металловКЧ=2
Линейная
КЧ=5
Квадратная пирамида
КЧ=3
Треугольная
КЧ=6
Октаэдр
КЧ=4
Треугольная
КЧ=5
Тригональная бипирамида
КЧ=7
КЧ=8
Пентагональная бипирамида Квадратная антипризма
11
12.
◉Спасибо за
внимание







 Химия
Химия








