Похожие презентации:
Строение атома углерода. Валентные состояния атома углерода
1.
Строение атомауглерода.
Валентные
состояния атома
углерода
2.
АтомЭлектронное
облако
Электроны
1s²
3.
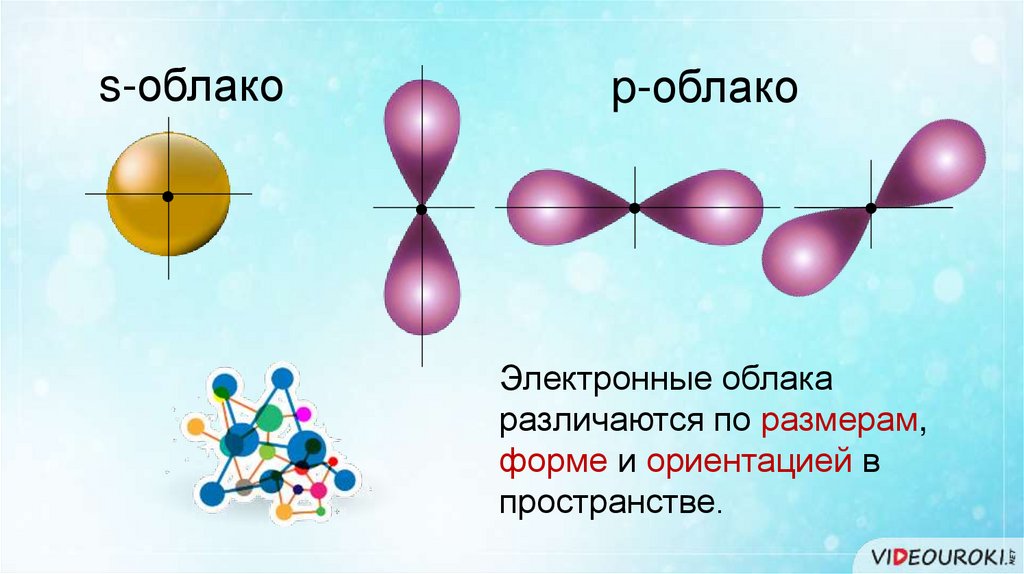
s-облакоp-облако
Электронные облака
различаются по размерам,
форме и ориентацией в
пространстве.
4.
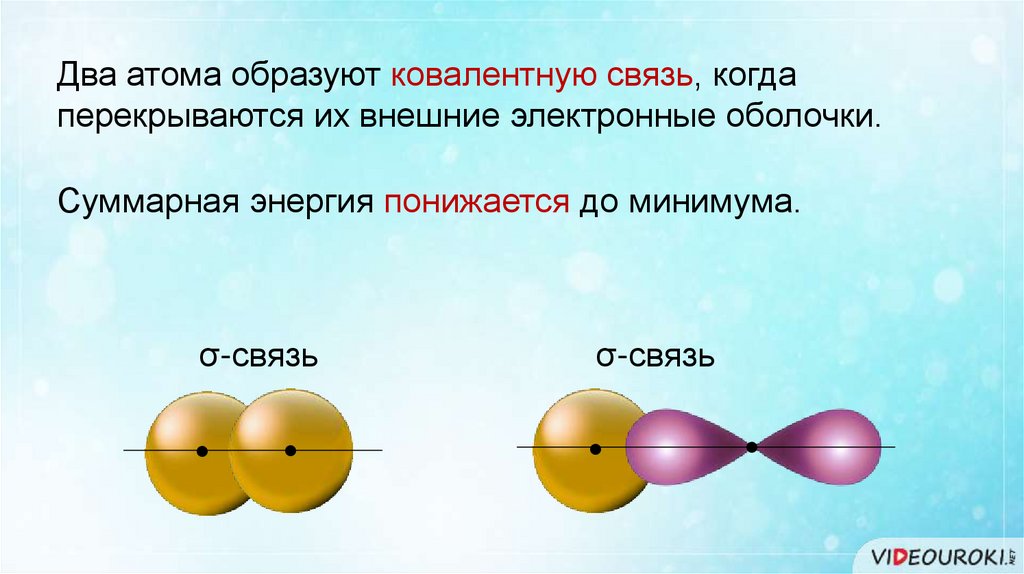
Два атома образуют ковалентную связь, когдаперекрываются их внешние электронные оболочки.
Суммарная энергия понижается до минимума.
σ-связь
σ-связь
5.
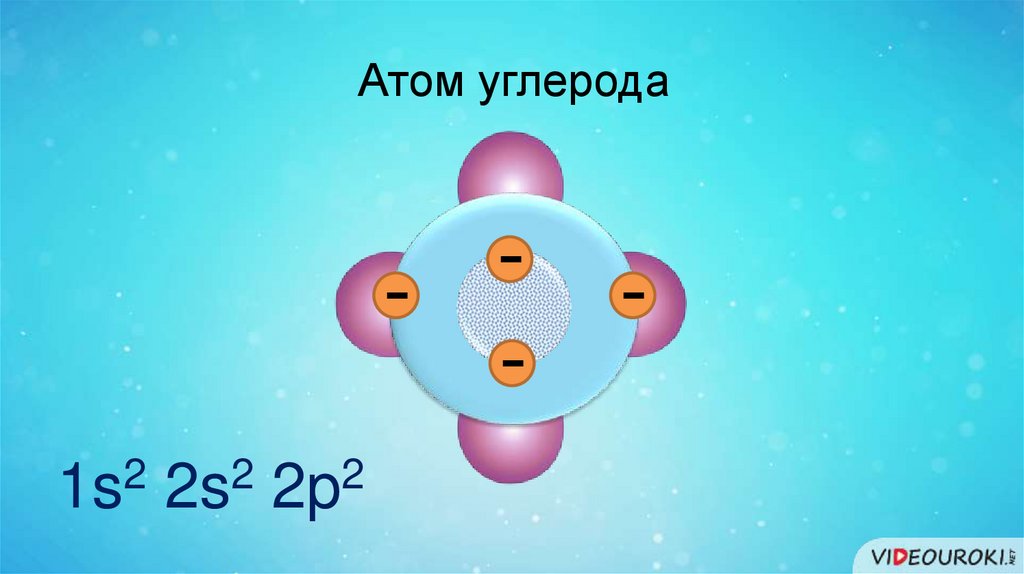
Атом углерода2
2
2
1s 2s 2p
-
6.
Углерод6
С
+6
2р2
2s²
1s²
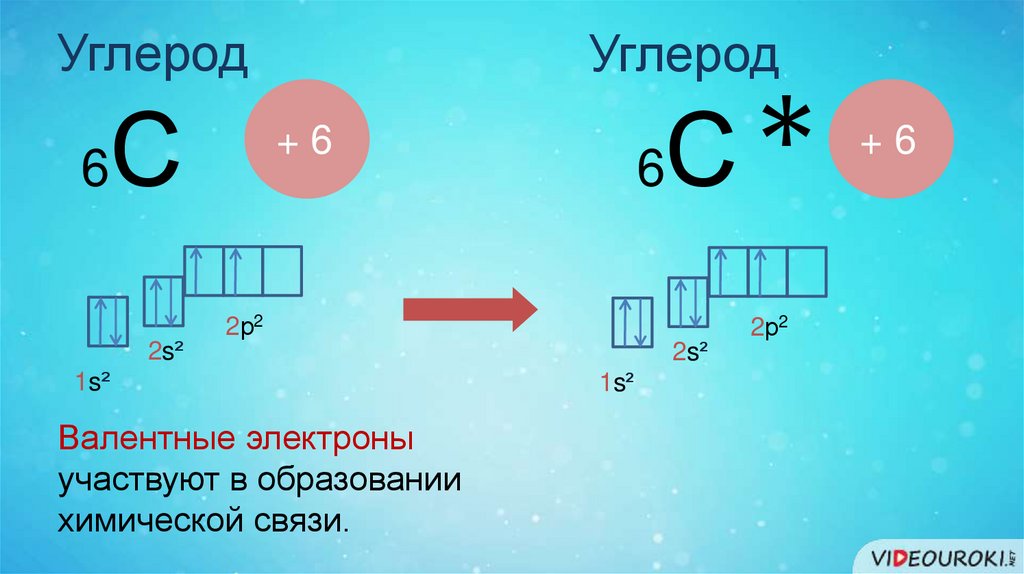
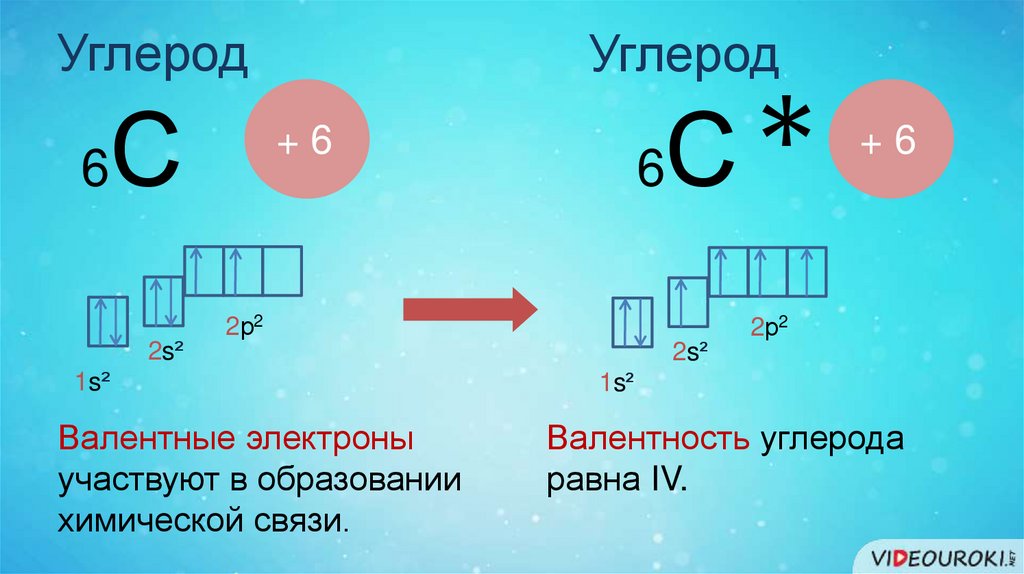
Валентные электроны
участвуют в образовании
химической связи.
7.
Углерод в соединенияхобразует четыре
равноценные связи.
8.
Углерод6
С
Углерод
+6
6
С*
2р2
2р2
2s²
1s²
Валентные электроны
участвуют в образовании
химической связи.
2s²
1s²
+6
9.
Углерод6
С
Углерод
+6
6
С*
2р2
2р2
2s²
1s²
Валентные электроны
участвуют в образовании
химической связи.
+6
2s²
1s²
Валентность углерода
равна IV.
10.
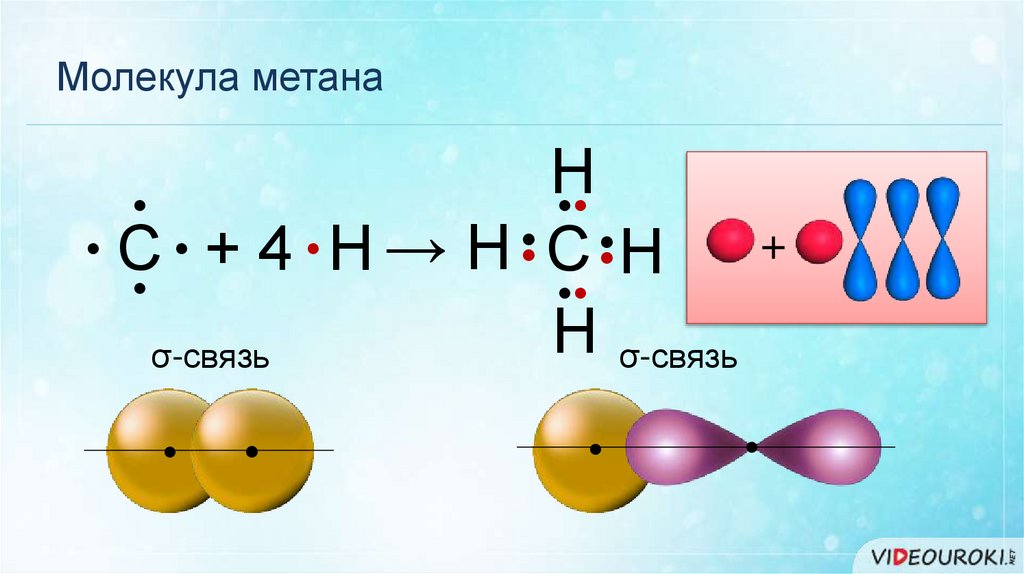
Молекула метанаН
●
+
С● ● + 4 ● Н → Н С
Н
●
Н σ-связь
σ-связь
●
●
11.
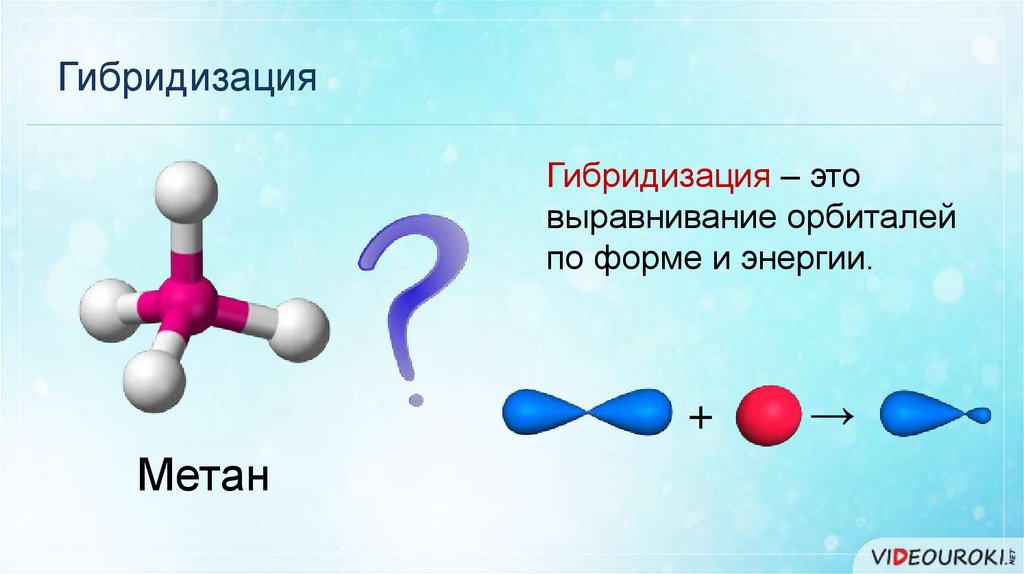
ГибридизацияГибридизация – это
выравнивание орбиталей
по форме и энергии.
+
Метан
→
12.
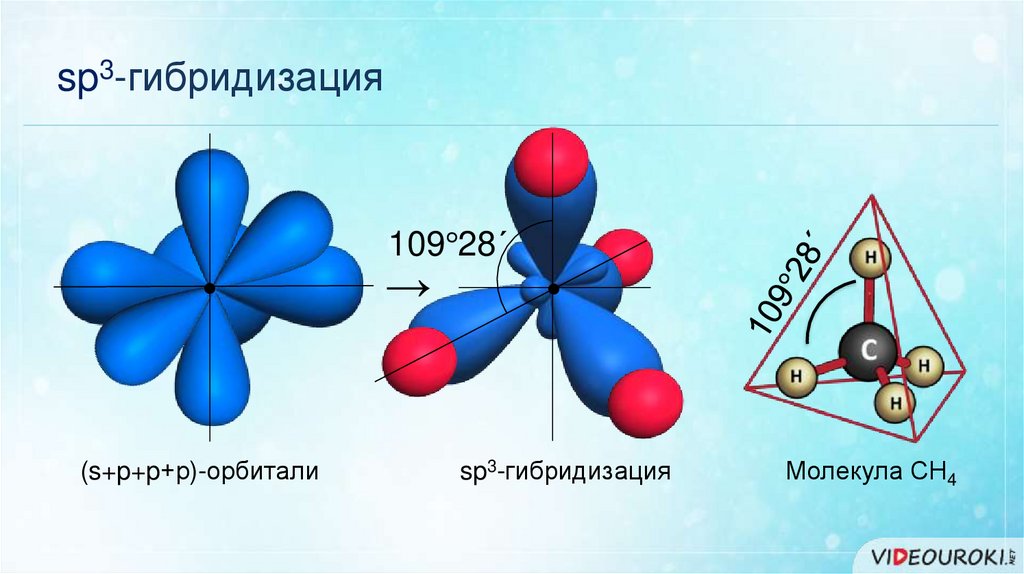
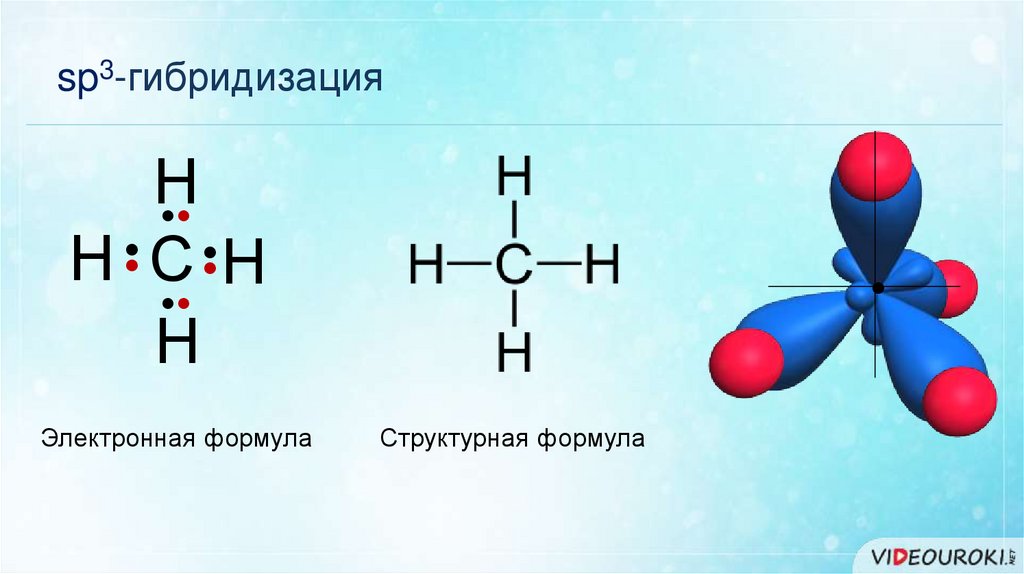
sp3-гибридизация109°28´
(s+p+p+р)-орбитали
→
sp3-гибридизация
Молекула СН4
13.
sp3-гибридизация●
●
Н
●
Н С
Н
●
Н
Электронная формула
Структурная формула
14.
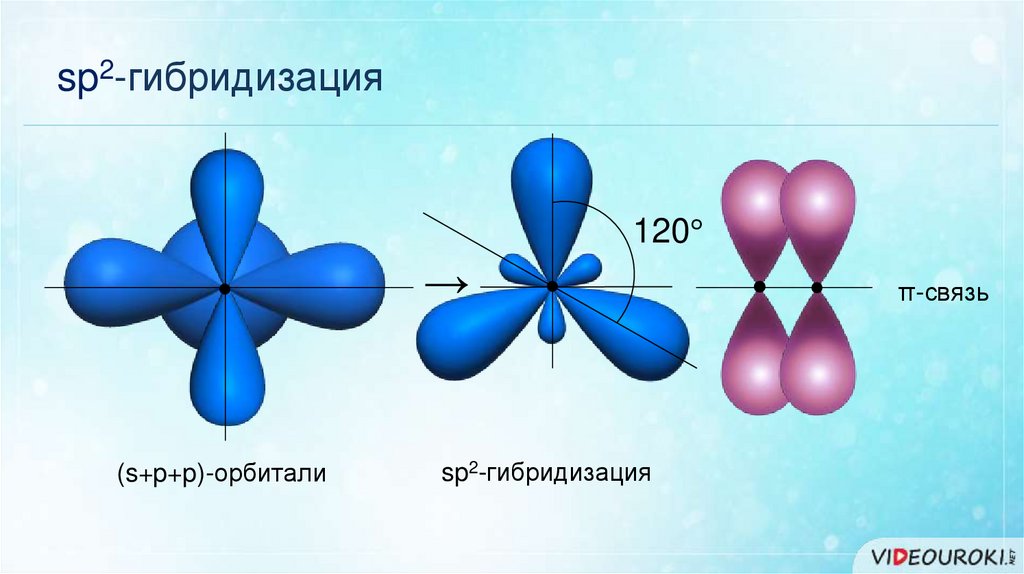
sp2-гибридизация120°
(s+p+p)-орбитали
→
sp2-гибридизация
π-связь
15.
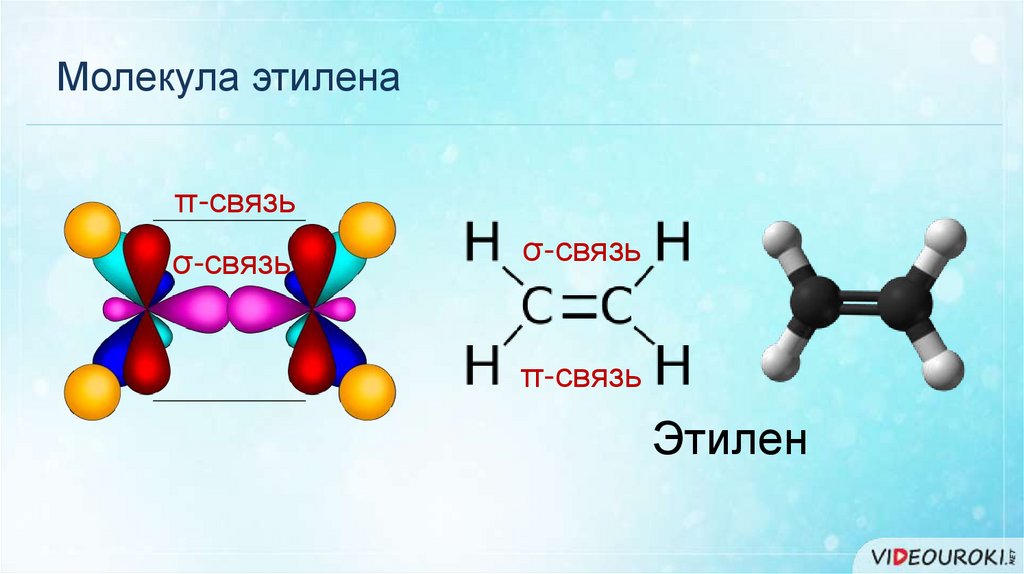
Молекула этиленаπ-связь
σ-связь
σ-связь
π-связь
Этилен
16.
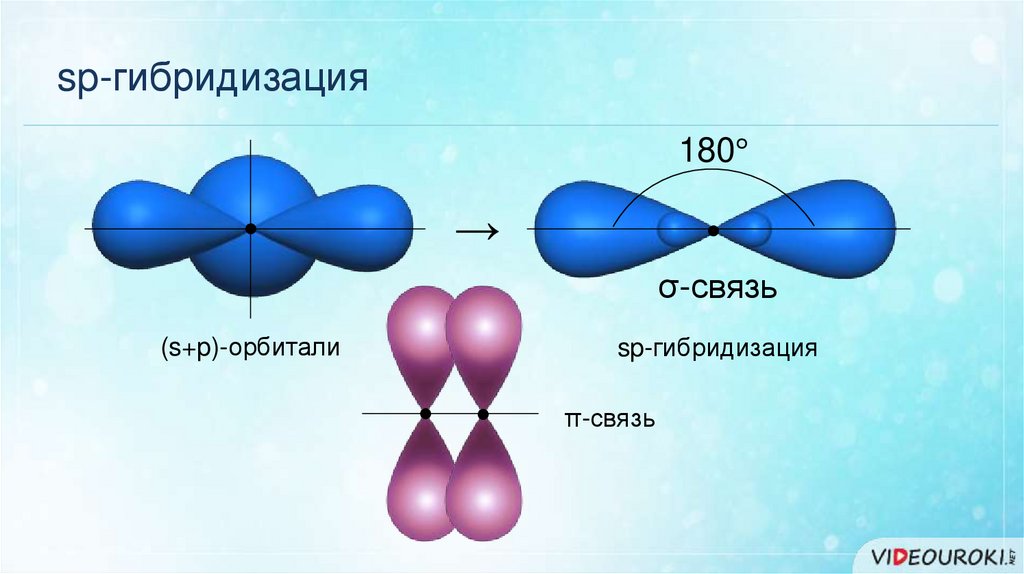
sp-гибридизация180°
→
σ-связь
(s+p)-орбитали
sp-гибридизация
π-связь
17.
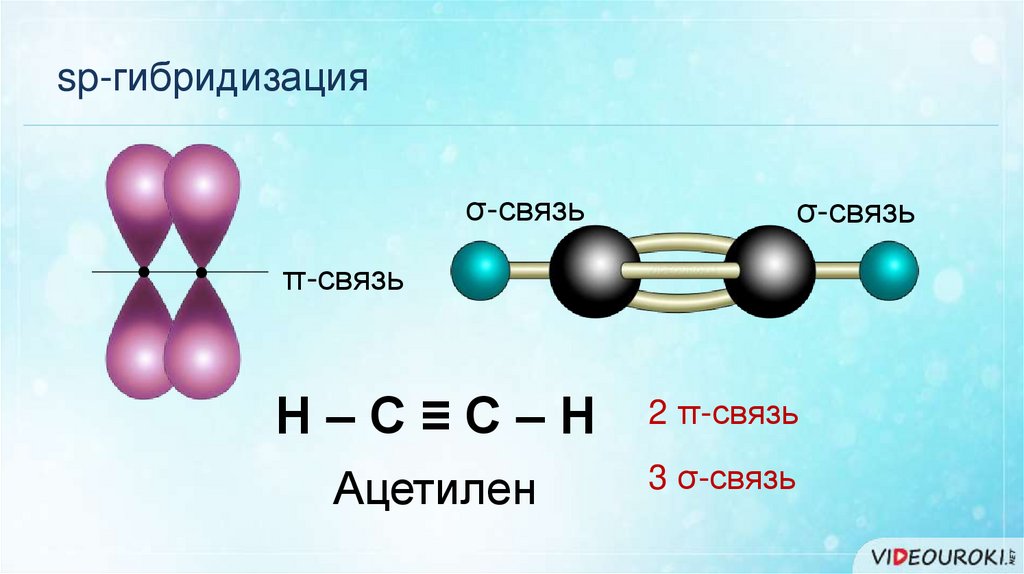
sp-гибридизацияσ-связь
σ-связь
π-связь
Н–С≡С–Н
2 π-связь
Ацетилен
3 σ-связь
18.
Типы гибридизацииsp3-гибридизация атома углерода в молекуле,
если он связан с четырьмя атомами;
sp2-гибридизация атома углерода в молекуле,
если он связан с тремя атомами, при этом есть
двойная связь;
sp-гибридизация атома углерода, если он
образует связь с двумя атомами, при этом есть
тройная связь.
19.
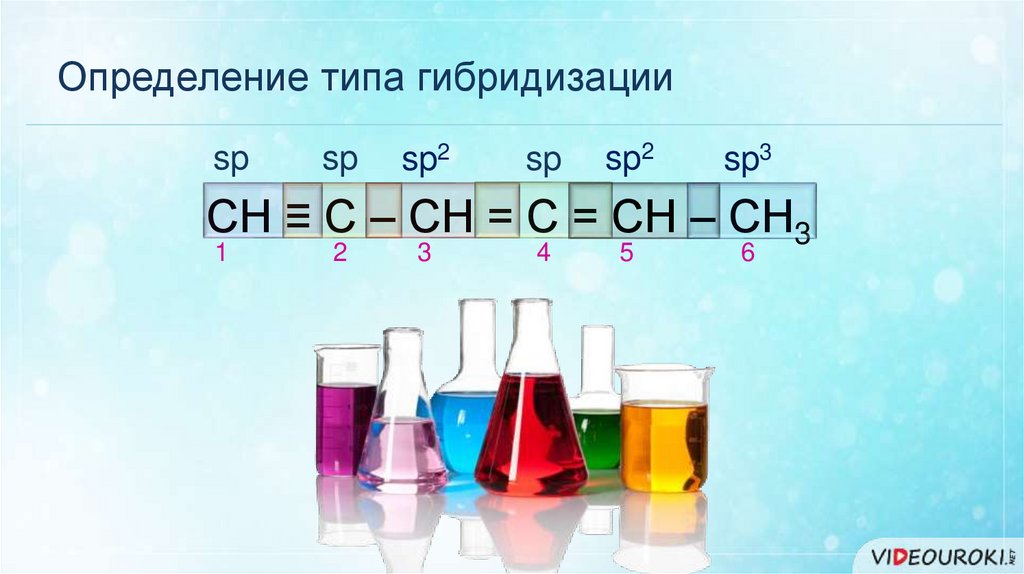
Определение типа гибридизацииsp
sp
sp2
sp
sp2
sp3
СН ≡ С – СН = С = СН – СН3
1
2
3
4
5
6
20.
В органическихсоединениях атом
углерода четырёхвалентен
за счёт перехода
электронов с 2s- на
2p-подуровень.
Атом углерода в
органических соединениях
может находиться в
состоянии sp3-, sp2- и spгибридизации.






 Химия
Химия








