Похожие презентации:
Кремний и его соединения
1.
Кремний и егосоединения
2.
I. Химический элемент1) №14, Si, 3 период, IV группа,
главная подгруппа
3.
2.Строение атомаВозможные степени окисления:
-4, 0, +2, +4
4.
3.Нахождение в природе• Второй по распространенности на
земном шаре после кислорода (по массе
его в земной коре - 27,6%)
• В свободном виде не встречается
5.
• В природе находится в связанном виде – в виде SiO2Горный
хрусталь
Кварц
Песок
Астбест
6.
Радуга кремнезёмаОпал
Яшма
Агат
Агат
Халцедон
Аметист
Сердолик
7.
широко распространены алюмосиликатыВ составе глин
Слюда
Полевой шпат
K2O*Al2O3*6SiO2*H2O
K2O*Al2O3*SiO2
Кварц
Кварц
8.
4.Биологическое значение- Животные, человек - микроэлемент (кости – гладкость и
прочность)
- Прочность частям растений (стебли, колючки, острые кря
листьев ..)
5. Русское название «кремний» введено в 1834 году
российским химиком Германом Ивановичем Гессом. В
переводе с древнегреческого κρημνός — «утес, гора»
II.ПРОСТОЕ ВЕЩЕСТВО
9.
1. Аллотропные модификацииАморфный кремний
- Бурый порошок
- Не имеет упорядоченной
структуры и определенной
температуры плавления
Кристаллический кремний
• Темно-серый с
металлическим блеском
• Тугоплавок
• Хрупок
• Слабо проводит
электрический ток
• Инертен при обычных
условиях
10.
2. Получение кремния1. В промышленности - восстановлением диоксида
кремния коксом в электрических печах:
SiO2+2C=Si+2CO
2. В лаборатории кремний получают прокаливанием с
магнием или алюминием белого песка:
SiO2 + 2Mg = 2MgO + Si
3SiO2 + 4Al = 2Al2О3 + 3Si
11.
3. Химические свойстваSi-4
Si
Si+4
Окислитель Восстановитель
1. С металлами (продукты – 1. С галогенами (с хлором при
силициды)
нагревании)
t
Si + 2Mg = Mg2Si
Si + 2F = SiF
2
4
2.С кислородом:
Si + O2 = SiO2
3.С другими неметаллами:
t
Si + C = SiC
4. Восстанавливает металлы из
оксидов
t
2FeO + Si = 2Fe + SiO2 + Q
5. Со щелочами
Si + 2NaOH + H2O = Na2SiO3 + 2H2
12.
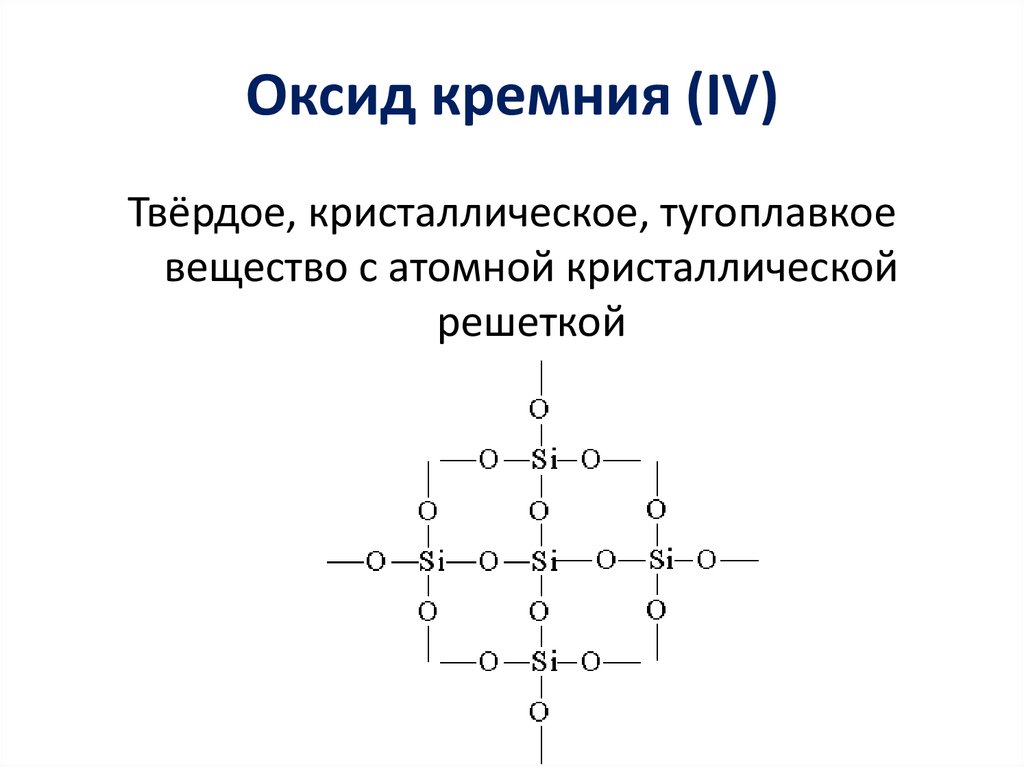
Оксид кремния (IV)Твёрдое, кристаллическое, тугоплавкое
вещество с атомной кристаллической
решеткой
13.
Химические свойства• Кислотный оксид
НО! Не реагирует с водой.
1. С основными оксидами:
t˚
SiO2 + CaO → CaSiO
CaSiO
33
2. Со щелочами:
t˚
SiO2 + 2NaOH → Na
Na2SiO
3 3++HH
2O
2SiO
2O
3. С солями:
t˚
SiO2 + K2CO3 → K2KSiO
CO
CO
2SiO
3+
3+
2 2
14.
Кремниевая кислотаФизические свойства: непрочная,
малорастворимая, не имеет кислого вкуса.
Получение:
Действие сильных кислот на силикаты
Na2SiO3 + 2HCl → 2NaCl + H2SiO3↓
Выделяется в виде силикагеля
Применяющегося для поглощения водяных
паров.
Химические свойства: Слабее угольной!
При нагревании разлагается:
t
H2SiO3 → H2O + SiO2
15.
Применение кремнияSi
16.
Применение кремнияSiО2















 Химия
Химия