Похожие презентации:
Химическая связь
1. ХИМИЧЕСКАЯ СВЯЗЬ
2. ХИМИЧЕСКАЯ СВЯЗЬ
совокупность сил,обуславливающих
взаимодействие
атомов в химических
соединениях
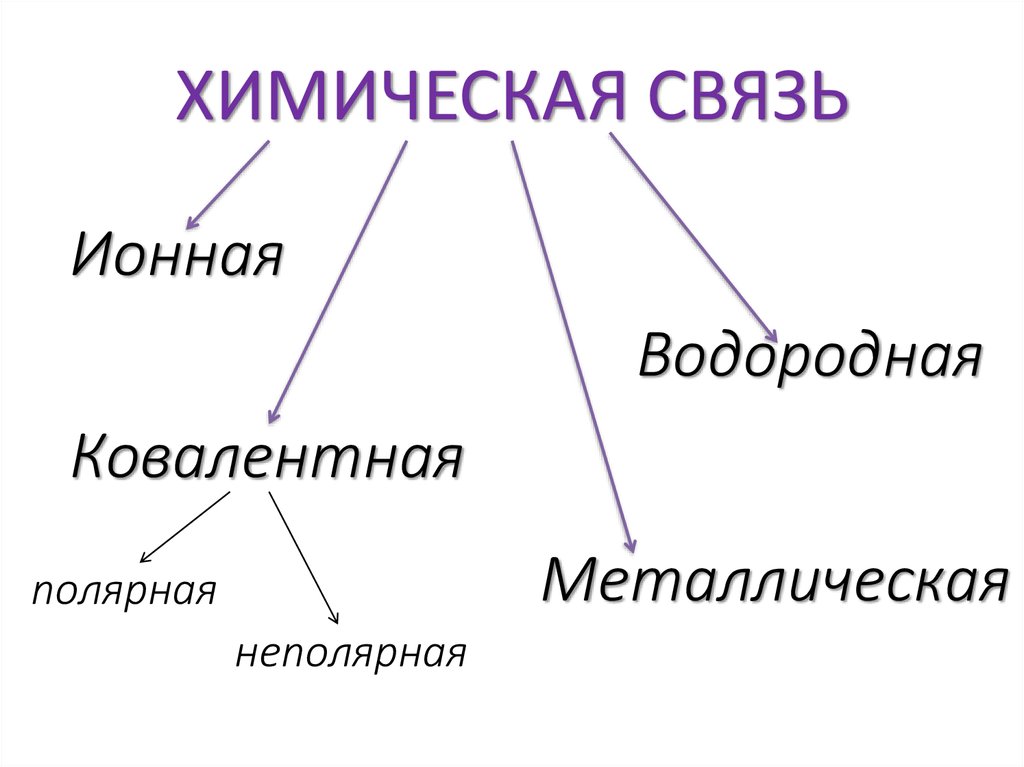
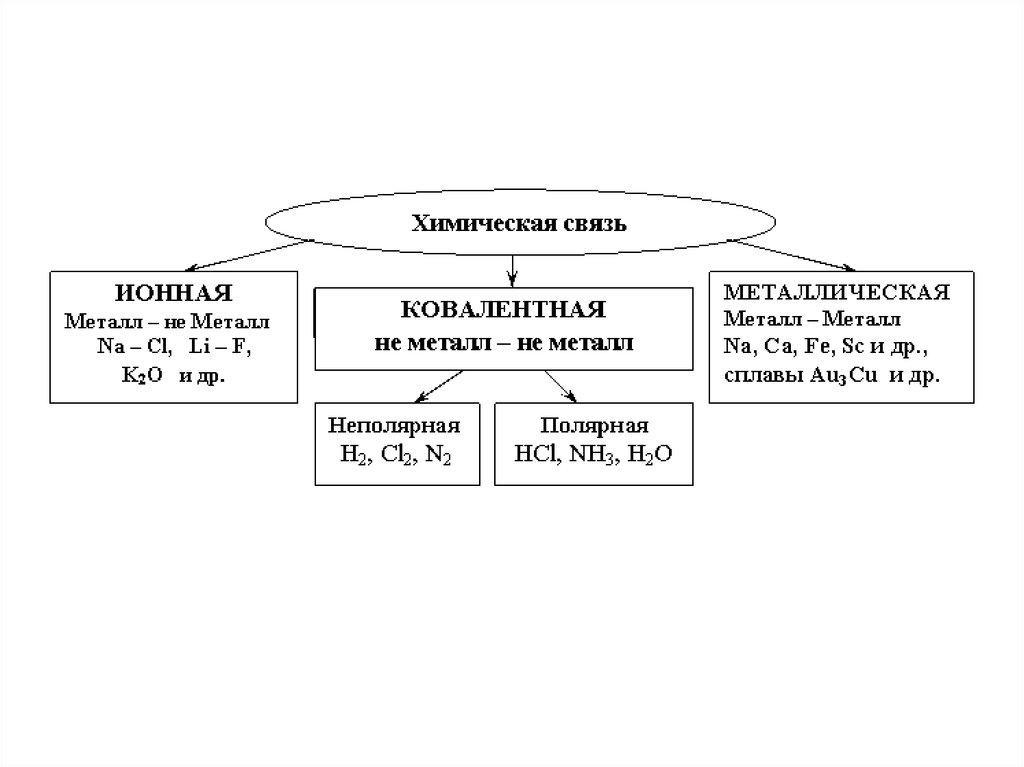
3. ХИМИЧЕСКАЯ СВЯЗЬ
ИоннаяВодородная
Ковалентная
Металлическая
полярная
неполярная
4.
5. Ионная связь
Связь, образовавшаясямежду катионами и
анионами за счет их
электростатического
притяжения
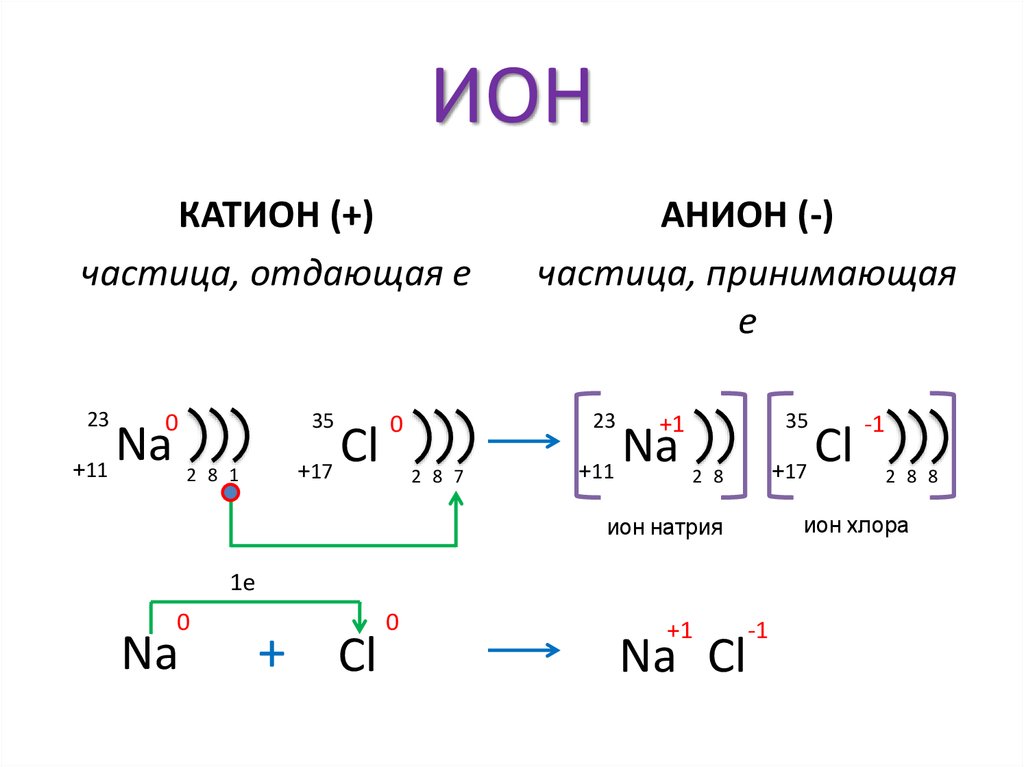
6. ИОН
КАТИОН (+)частица, отдающая е
23
+11
35
0
Na
2 8 1
+17
Cl
АНИОН (-)
частица, принимающая
е
23
0
2 8 7
+11
35
+1
Na
+17
2 8
1e
Na
+ Cl
0
+1
Na Cl
2 8 8
ион хлора
ион натрия
0
Cl
-1
-1
7.
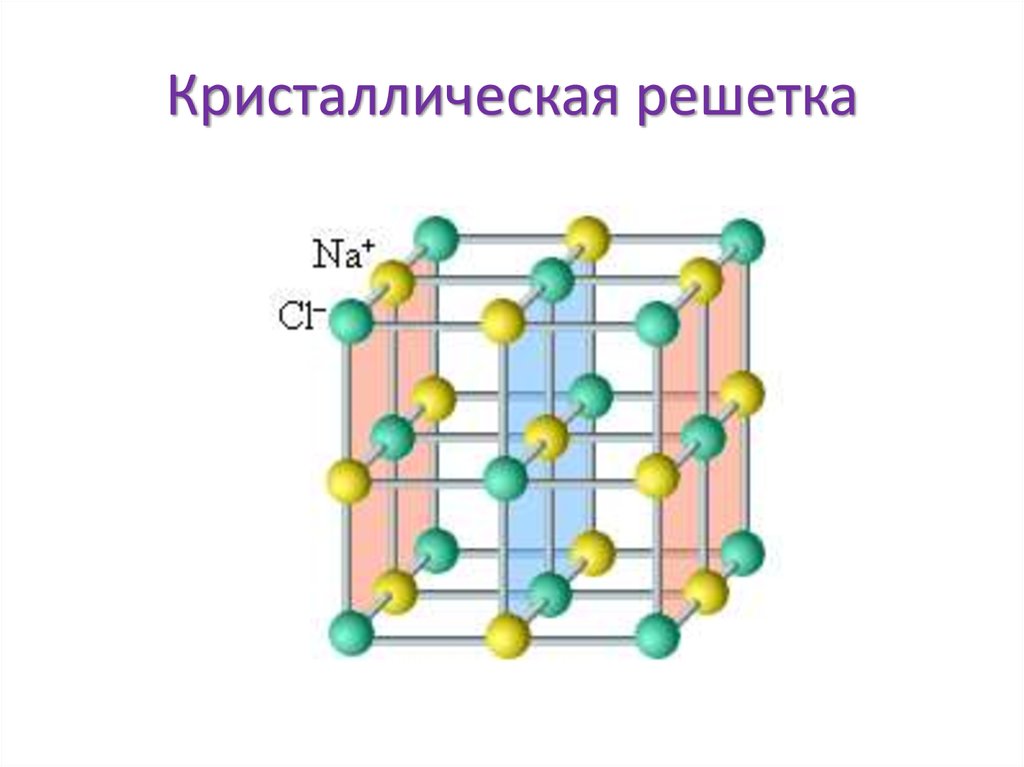
8. Кристаллическая решетка
9. Ионные соединения в природе
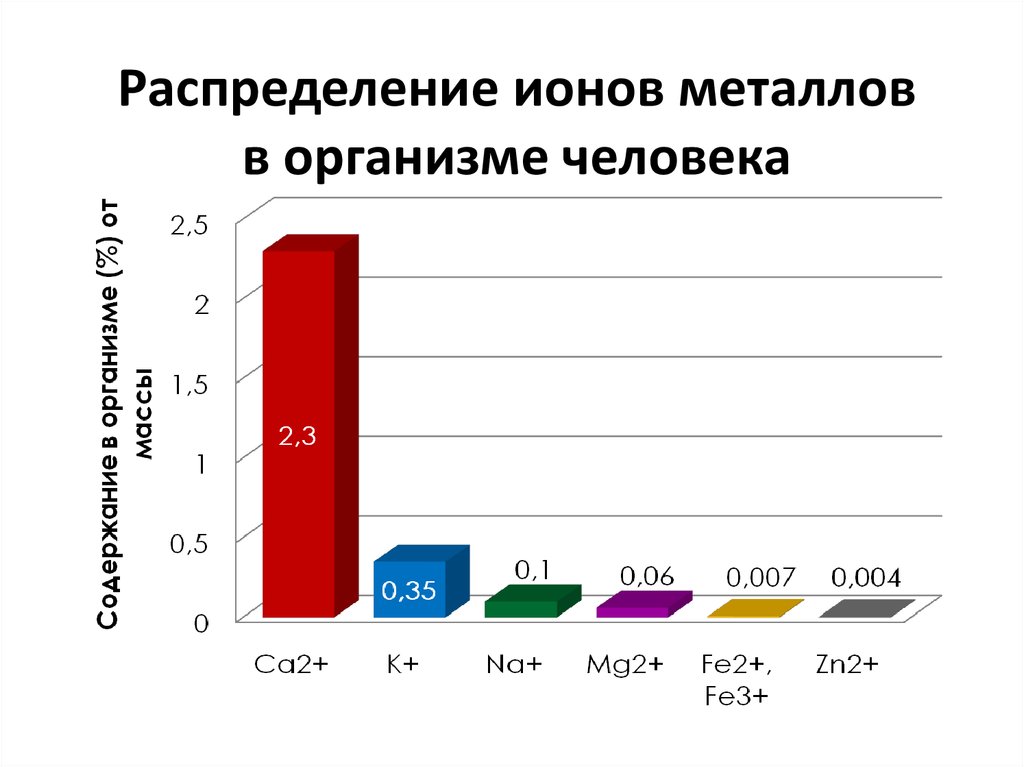
10. Распределение ионов металлов в организме человека
11. Ковалентная связь
Связь, возникающаямежду атомами за
счет образования
общих электронных
пар
12. Ковалентная связь
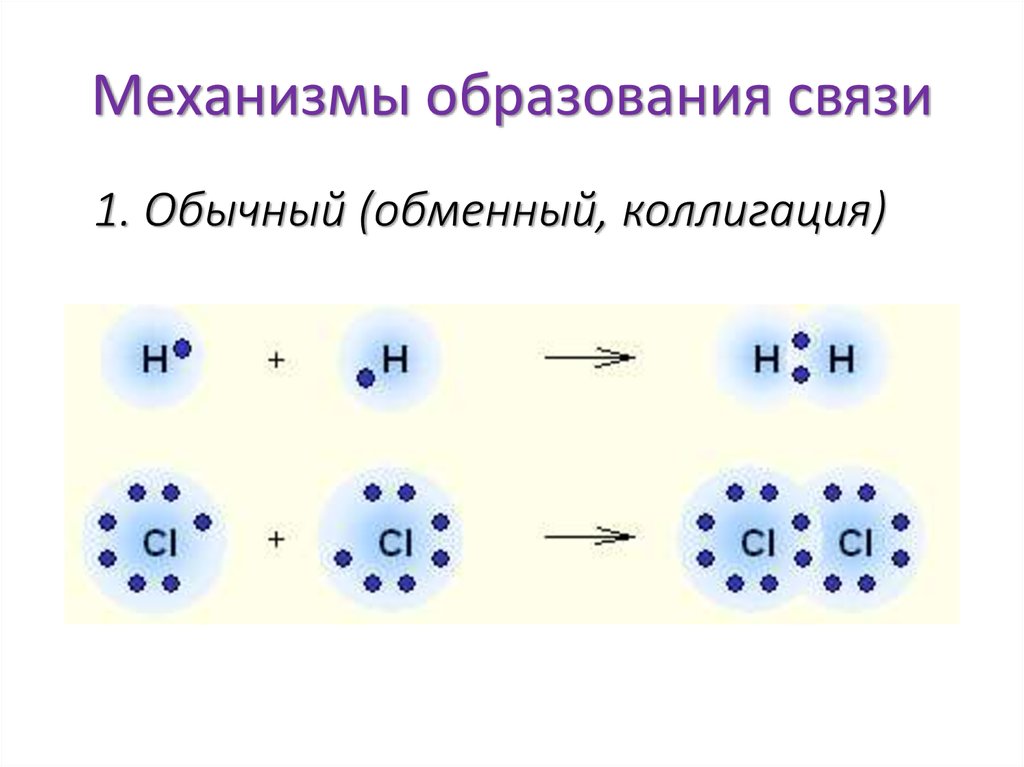
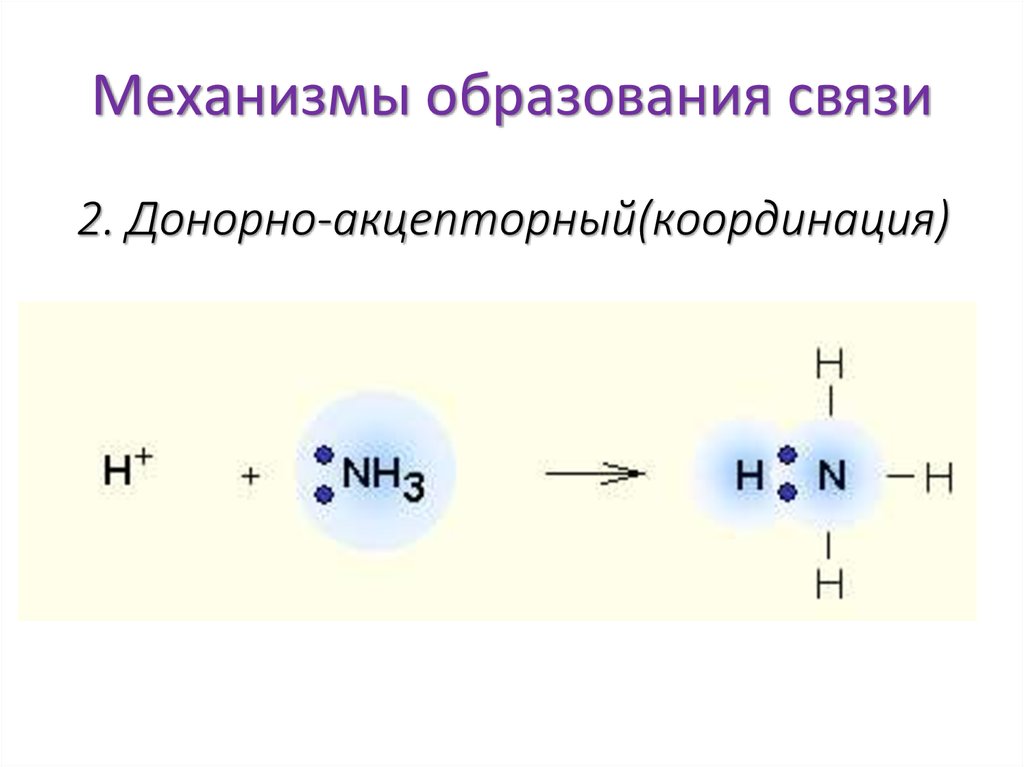
Атомная связь13. Механизмы образования связи
1. Обычный (обменный, коллигация)14. Механизмы образования связи
2. Донорно-акцепторный(координация)15. Электроотрицательность
Способность атомовхимических элементов
оттягивать к себе
общие электронные
пары
16. Электроотрицательность
• ЭО < 2 - металл• ЭО > 2 - неметалл
• В периоде ЭО возрастает
• В группе ЭО уменьшается
• Чем > металличность, тем < ЭО
• Чем > неметалличность, тем < ЭО
17. Сравнить ЭО
Na и K
СиN
Ba и Ca
O и S
H и Сl
F и Cl
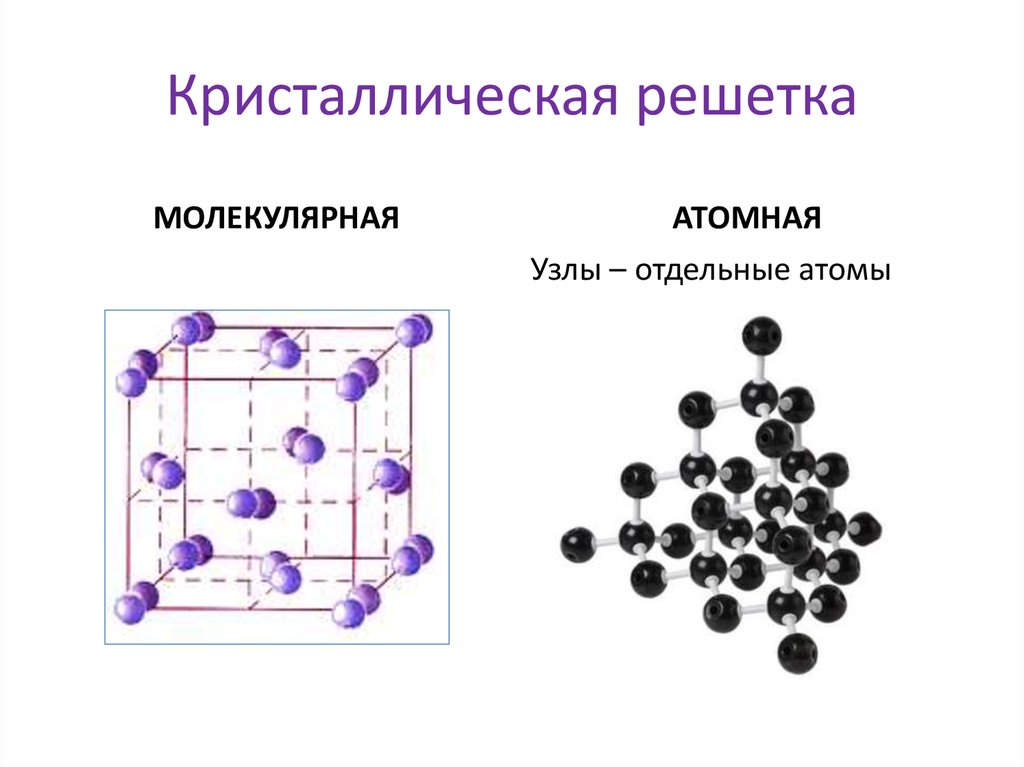
18. Кристаллическая решетка
МОЛЕКУЛЯРНАЯАТОМНАЯ
Узлы – отдельные атомы
19. Аллотропия
• Существование одного и того жехимического элемента в виде двух или
нескольких простых веществ;
• Может быть обусловлена образованием
молекул с различным числом атомов либо
образованием кристаллов различных
модификаций
20. Металлическая связь
Связь в металлах исплавах между атомионами металлов,
осуществляемая
совокупностью
валентных
электронов
21. Механизм металлической связи
Me0
- ne
n+
Me
22. Свойства металлов
Пластичность
Электропроводность
Теплопроводность
Металлический блеск
23. ПЛАСТИЧНОСТЬ
24. ЭЛЕКТРОПРОВОДНОСТЬ
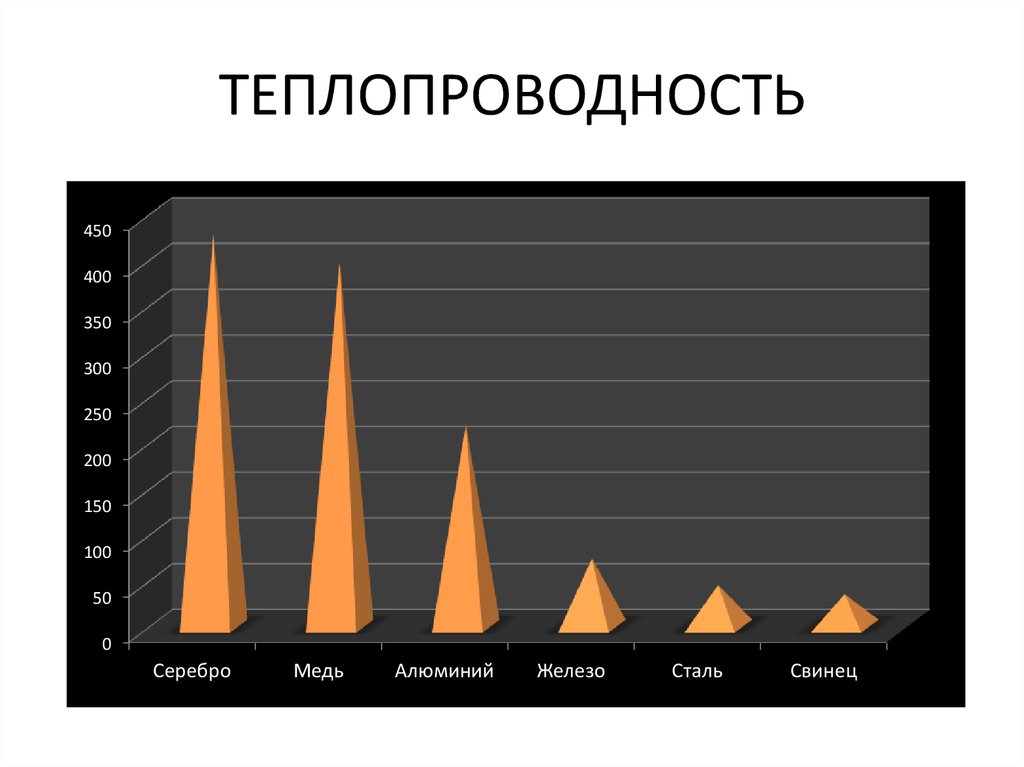
25. ТЕПЛОПРОВОДНОСТЬ
450400
350
300
250
200
150
100
50
0
Серебро
Медь
Алюминий
Железо
Сталь
Свинец
26. МЕТАЛЛИЧЕСКИЙ БЛЕСК
27.
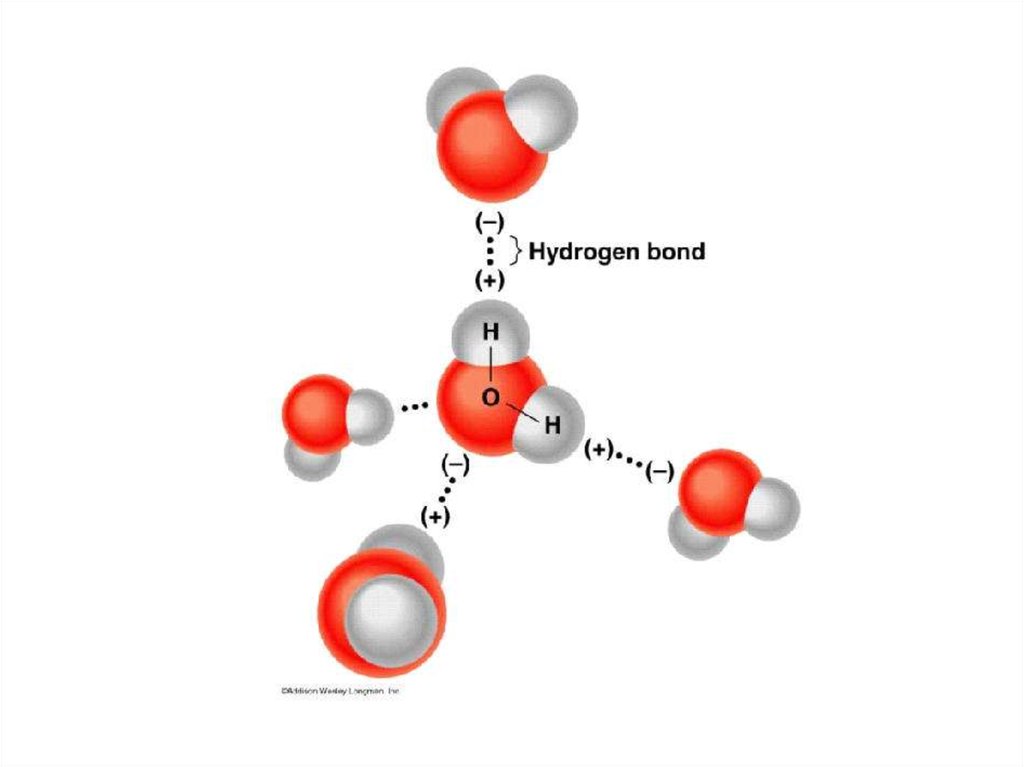
28. Водородная связь
Связь междуатомами водорода
одной молекулы и
атомами ЭО
элементов
(О; N ; Cl; F; S)
29.
30.
1. внутримолекулярная2. межмолекулярная
31. ВОДА
Н-О … Н-О… Н-О|
|
|
H
H
H
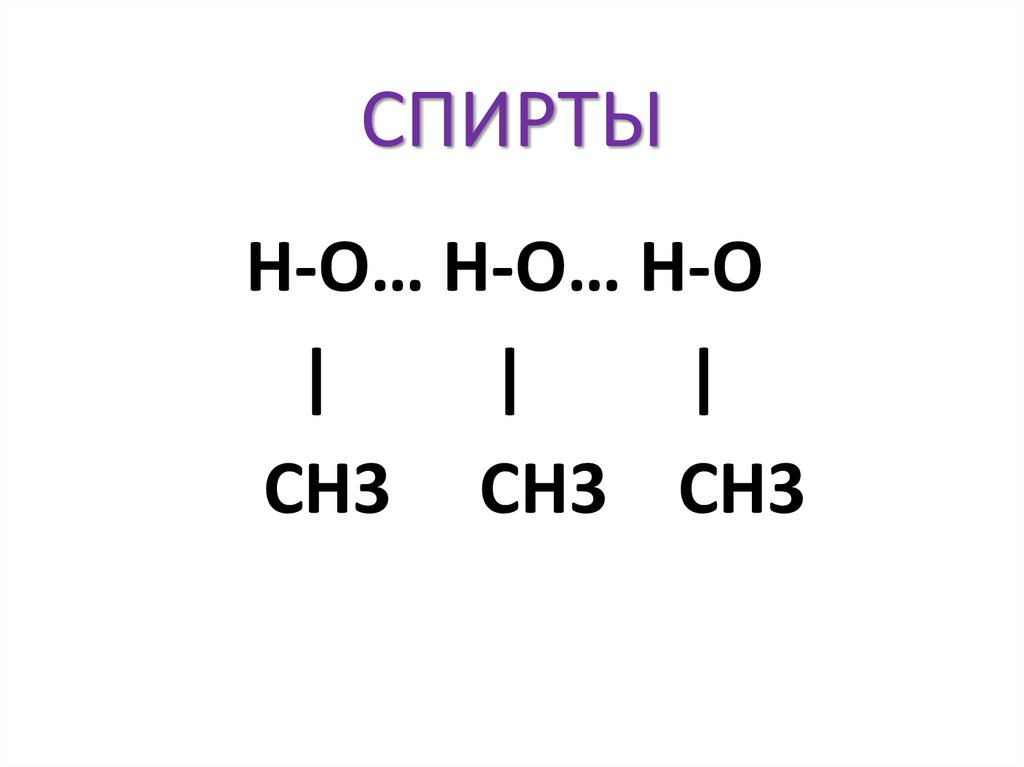
32. СПИРТЫ
H-O… Н-O… H-O|
|
|
СH3 СH3 СH3
33. Источники
• Естествознание 11 класс Габриелян (§3-5)• http://bourabai.kz/physics/img/3-6-1000.gif
• http://investments.academic.ru/pictures/investments/img778315_7_Min
eral_Realgar_klassa_sulfosoley.jpg
• http://www.syl.ru/misc/i/ai/210210/964442.jpg
• http://images.myshared.ru/5/379762/slide_7.jpg
• http://900igr.net/prezentatsii/khimija/khimicheskaja-svjaz.html
• http://www.myshared.ru/slide/63772/
• http://mining-info.ru/wp-content/uploads/2016/03/Highelectroconductivity-1.jpg
• http://pixdaus.com/files/items/pics/2/98/515298_4f2f124094f60cef82d3
4364c77fd7a1_large.jpg
• http://ipadwallpapers.ucoz.net/_ld/0/36308223.jpg
• http://moszerkala.ru/_mod_files/ce_images/source/silver-mirror.jpg
• http://www.nyf.hu/others/html/kornyezettud/KemiaI/Kornykemalapmenu/kemiko4.jpg




















 Химия
Химия








