Похожие презентации:
Электролитическая диссоциация. Химия. 8 класс
1.
Электролитическаядиссоциация
8 класс
13.07.2023
урок 50. 1
2.
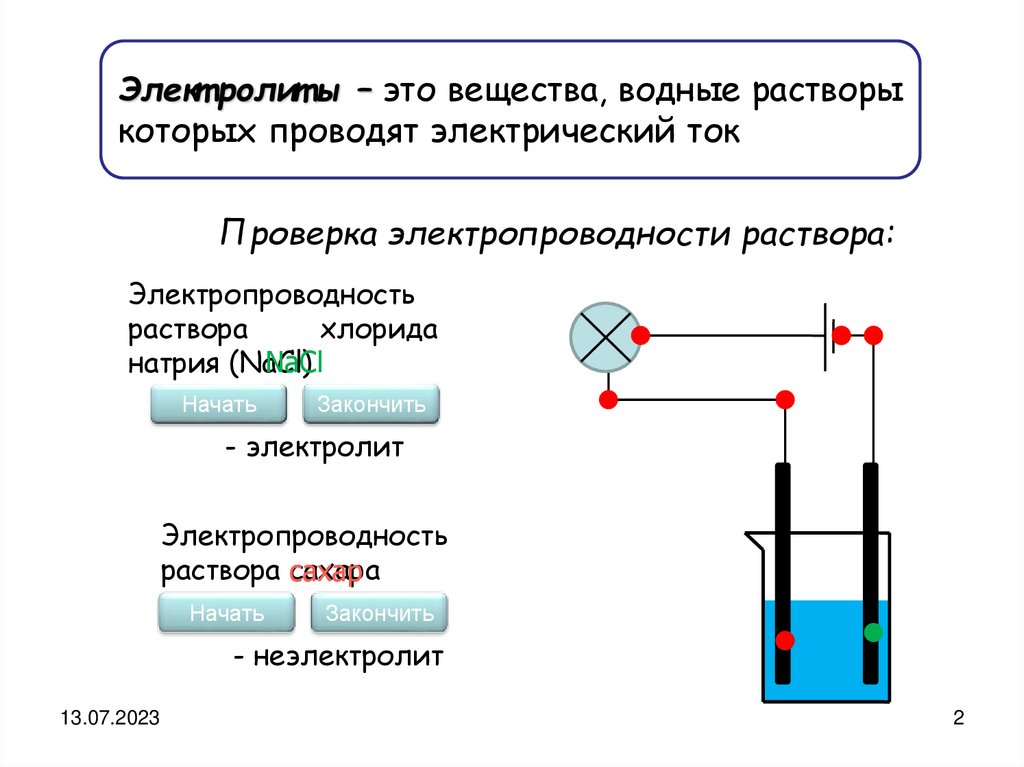
Элект ролит ы – это вещества, водные растворыкоторых проводят электрический ток
Проверка электропроводности раствора:
Электропроводность
раствора
хлорида
натрия (NaCl)
NaCl
Начать
Закончить
- электролит
Электропроводность
раствора сахара
сахар
Начать
Закончить
- неэлектролит
13.07.2023
2
3.
Электропроводность веществ13.07.2023
3
4.
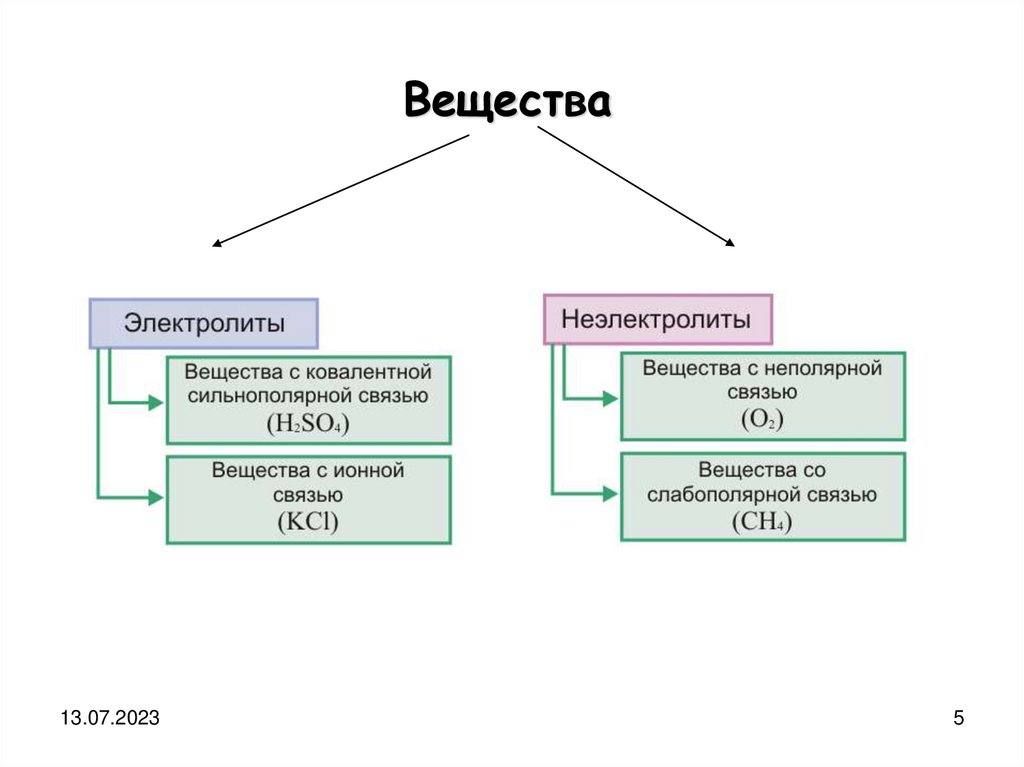
ВеществаЭлектролиты
(проводят
электрический ток)
• Кислоты (HCl;
H2SO4);
• Основания
(NaOH; Ba(OH)2);
• Соли (NaCl;
CuSO4).
13.07.2023
Неэлектролиты
(не проводят
электрический ток)
• Органические
вещества;
• Газы (O2; H2;
CO2);
• Оксиды (CuO;
Fe2O3).
4
5.
Вещества13.07.2023
5
6.
Электролитическая диссоциация процесс распада электролита на ионы прирастворении в воде или расплавлении.
Свант е Август
Аррениус
1859-1927гг.
Шведский физико-химик,
создатель теории
электролитической
диссоциации.
13.07.2023
6
7.
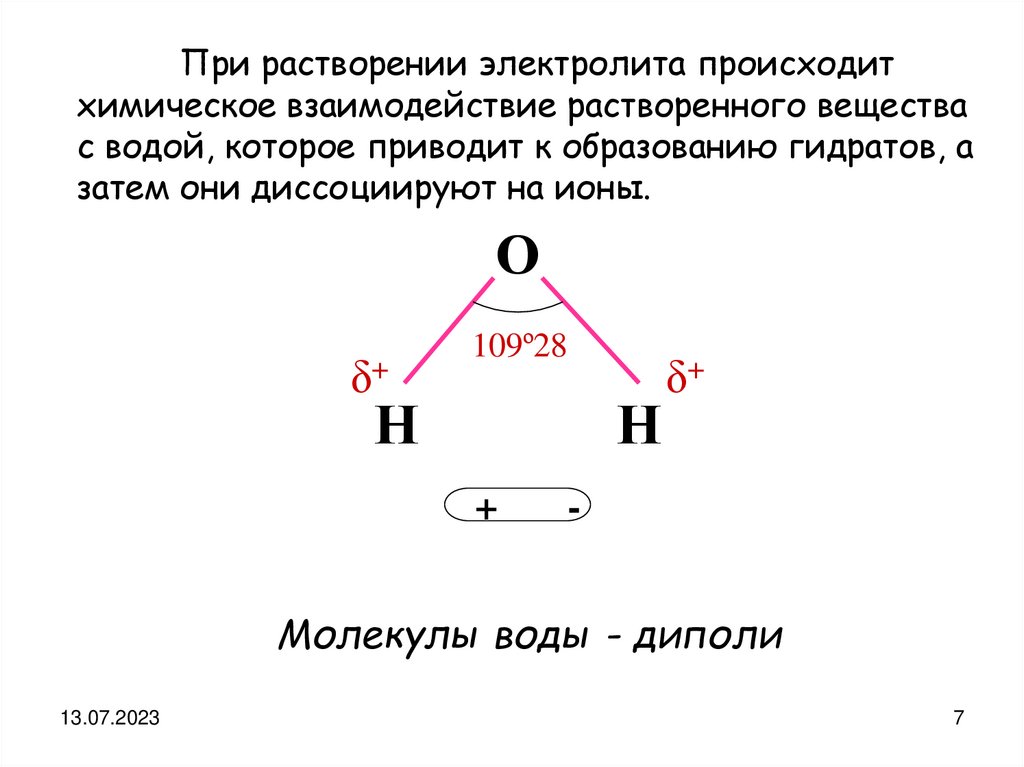
При растворении электролита происходитхимическое взаимодействие растворенного вещества
с водой, которое приводит к образованию гидратов, а
затем они диссоциируют на ионы.
О
δ+
109º28
Н
Н
+
δ+
-
Молекулы воды - диполи
13.07.2023
7
8.
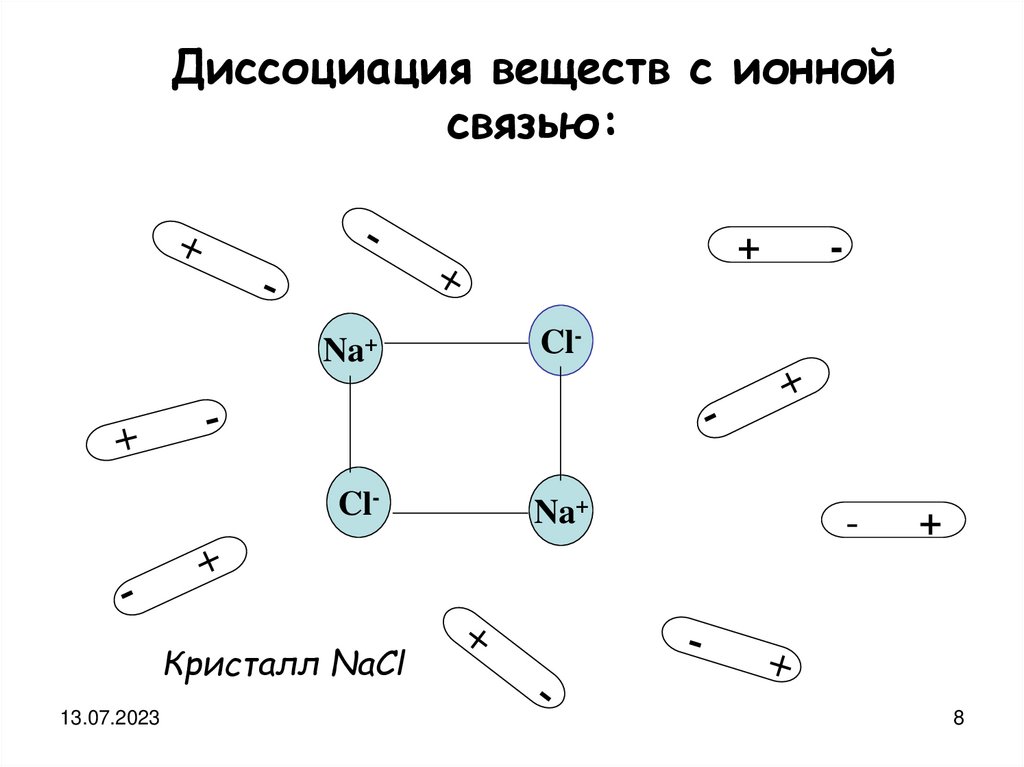
Диссоциация веществ с ионнойсвязью:
+
Na+
Cl-
Cl-
Na+
-
-
+
Кристалл NaCl
13.07.2023
8
9.
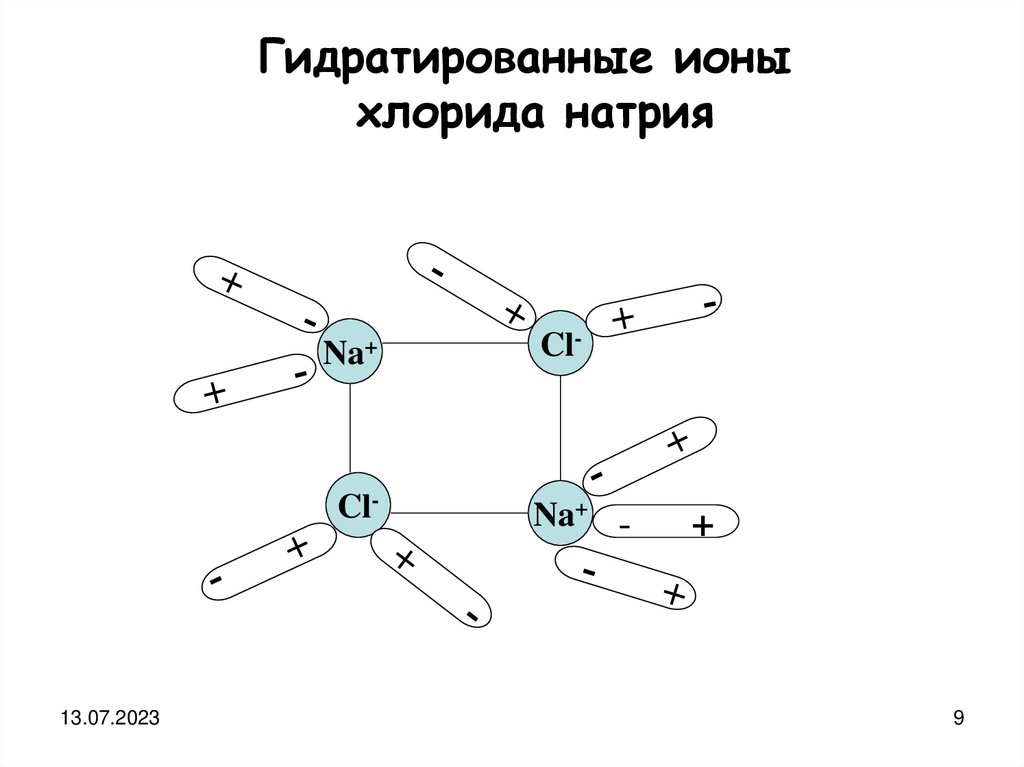
Гидратированные ионыхлорида натрия
Na+
Cl-
13.07.2023
Cl-
Na+ -
+
9
10.
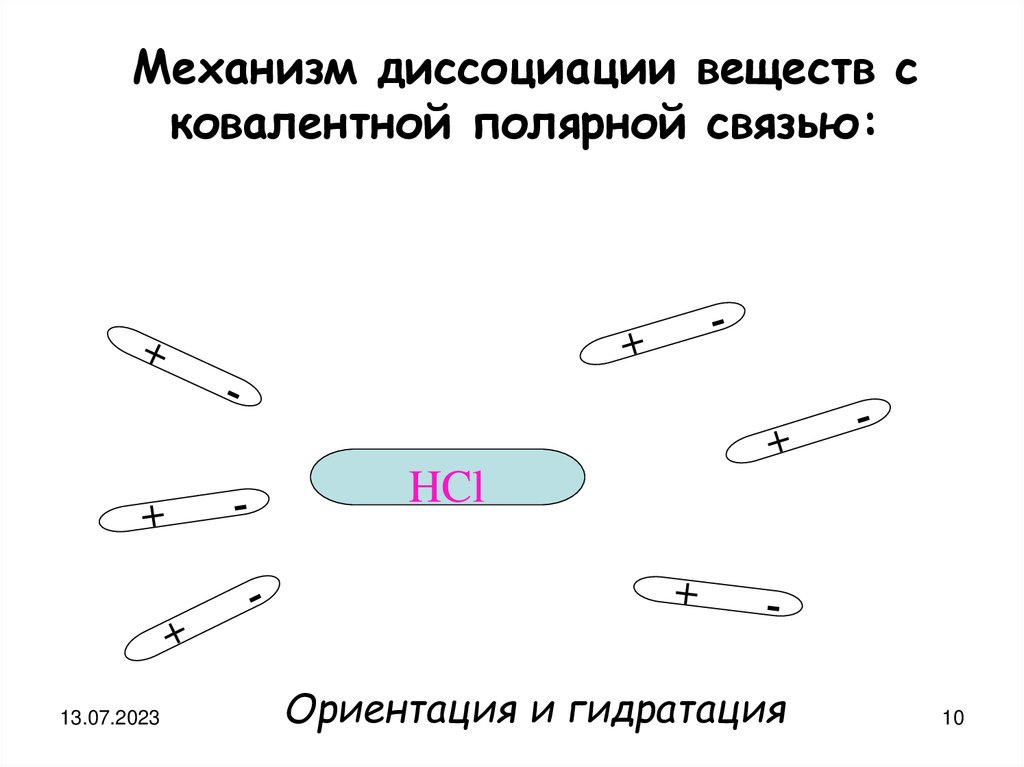
Механизм диссоциации веществ сковалентной полярной связью:
HCl
13.07.2023
Ориентация и гидратация
10
11.
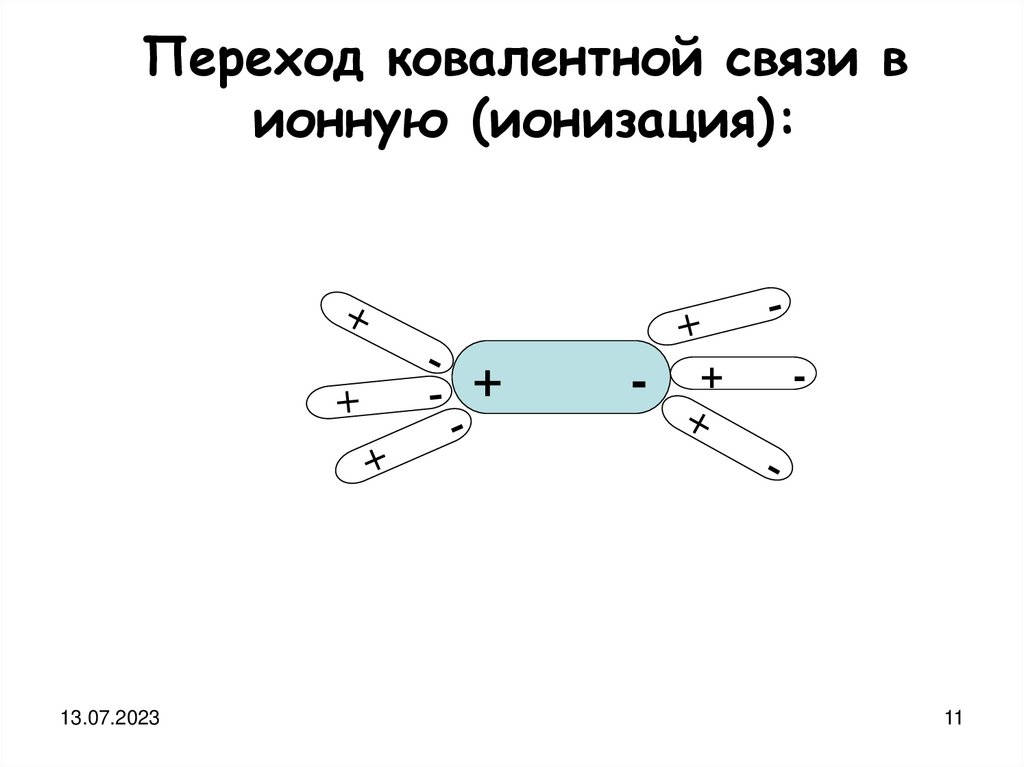
Переход ковалентной связи вионную (ионизация):
+
13.07.2023
-
+
-
11
12.
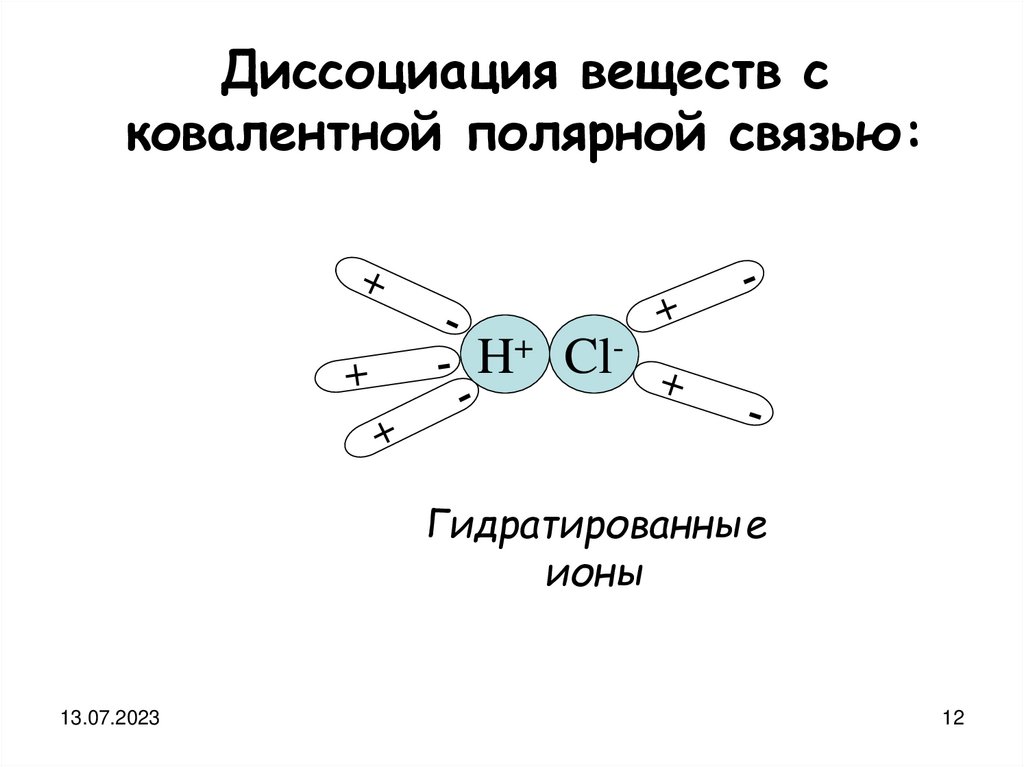
Диссоциация веществ сковалентной полярной связью:
H+ ClГидратированные
ионы
13.07.2023
12
13.
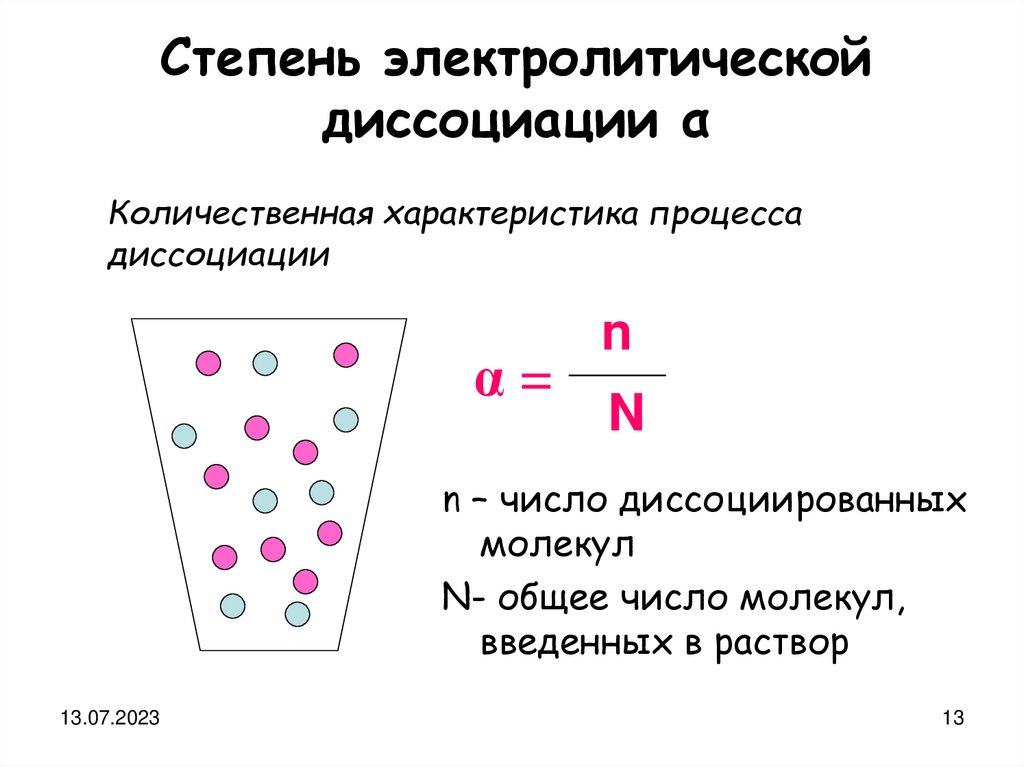
Степень электролитическойдиссоциации α
Количественная характеристика процесса
диссоциации
α=
n
N
n – число диссоциированных
молекул
N- общее число молекул,
введенных в раствор
13.07.2023
13
14.
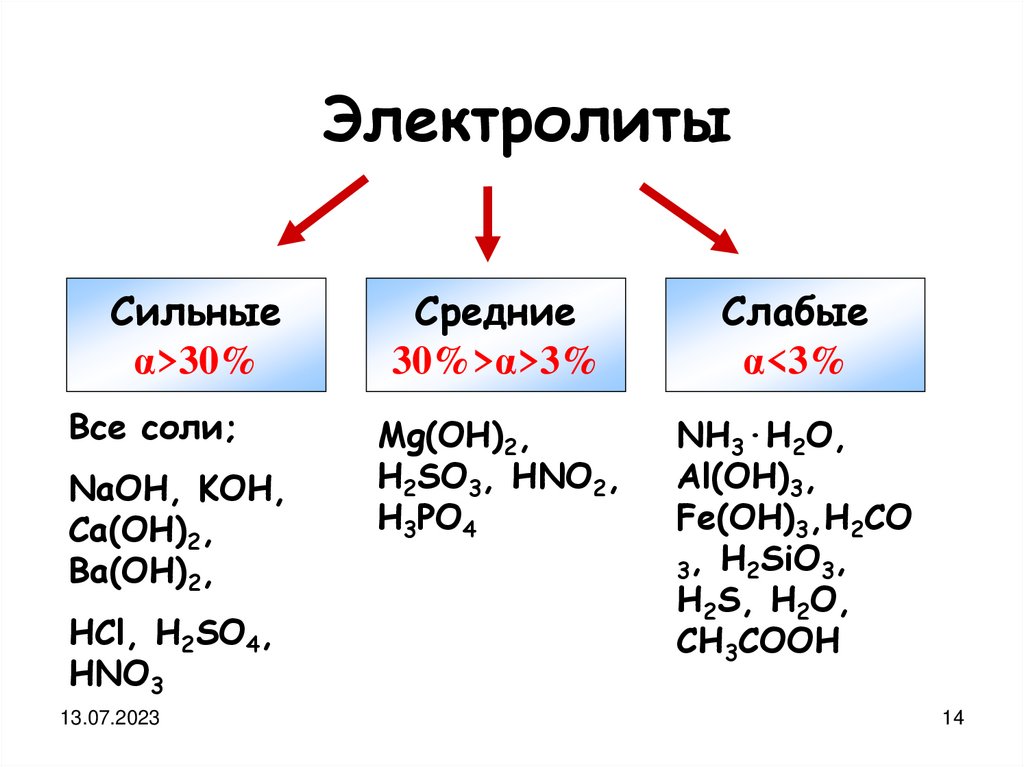
ЭлектролитыСильные
α>30%
Все соли;
NaOH, KOH,
Ca(OH)2,
Ba(OH)2,
HCl, H2SO4,
HNO3
13.07.2023
Средние
30%>α>3%
Слабые
α<3%
Mg(OH)2,
H2SO3, HNO2,
H3PO4
NH3·H2O,
Al(OH)3,
Fe(OH)3,H2CO
3, H2SiO3,
H2S, H2O,
CH3COOH
14
15.
13.07.202315
16.
Задание. Напиши уравнение диссоциациивеществ.
1. KNO3
2. HCl
3. NaOH
Для слабых электролитов диссоциация обратима!
13.07.2023
16
17.
• Что называют электролитическойдиссоциацией?
• Какие вещества называют электролитами?
Какие вещества к ним относятся? Какой тип
химической связи для них характерен?
• Какие вещества называют
неэлектролитами? Какие вещества к ним
относятся? Какой тип химической связи для
них характерен?
• Каков механизм ЭД при растворении в воде
веществ с ионной и ковалентной полярной
связями?
13.07.2023
17




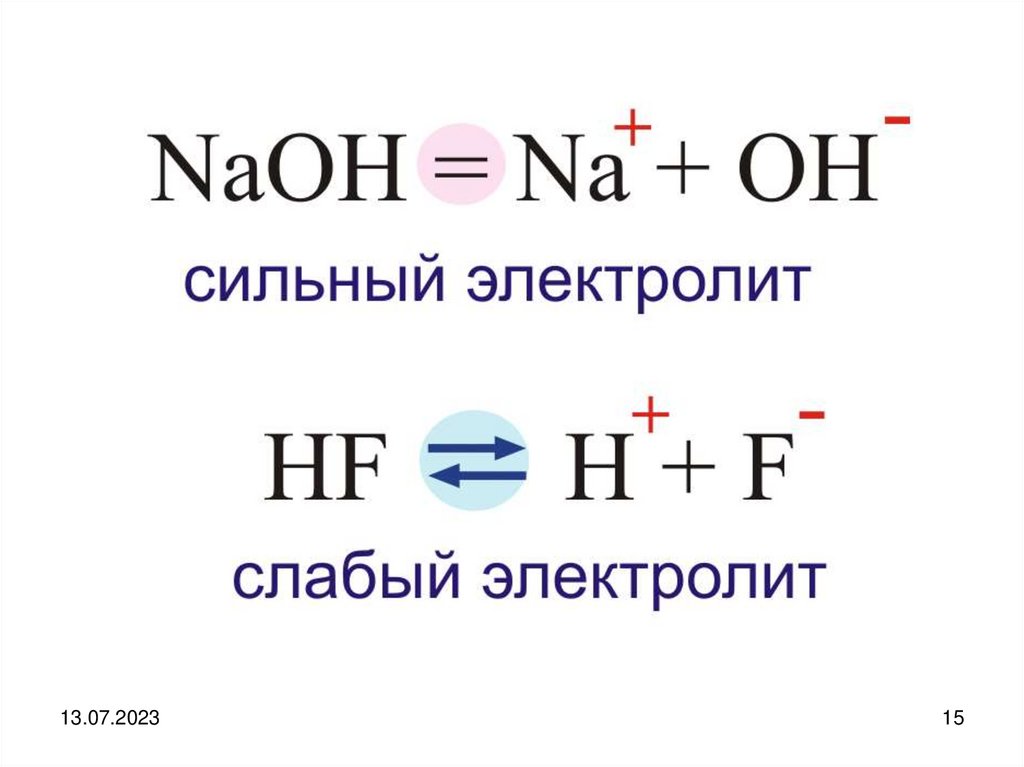


 Химия
Химия








