Похожие презентации:
Гомолитический и гетеролитический разрыв связи
1.
Гомолитический игетеролитический разрыв
связи
2.
Гомолитический разрыв связиГомолитический разрыв связи – разрыв химической связи, при котором
каждый атом получает при разрыве связи по одному электрону из общей
электронной пары.
Характерен для: слабополярных или неполярных связей
A:B → A∙ + ∙B
Дать определение свободным радикалам
3.
Условия протекания радикальныхреакций
Повышенная температура;
Неполярный растворитель или отсутствие растворителя
Реакция протекает под действием света или ультрафиолетового излучения
В системе присутствуют свободные радикалы или источники свободных
радикалов.
Пример: хлорирование метана
4.
Гетеролитический (ионный) разрывсвязи
Гетеролитический (ионный) разрыв связи – это разрыв химической связи,
при котором один из атомов получает при разрыве общую электронную пару.
Характерен для: полярных и легко поляризуемых связей
A:B → A:– + B+
Дать название атомам углерода на которых сосредоточен
положительный/отрицательный заряд
5.
Условия протекания ионных реакцийОтносительно невысокая температура;
Использование полярного растворителя;
Использование катализатора.
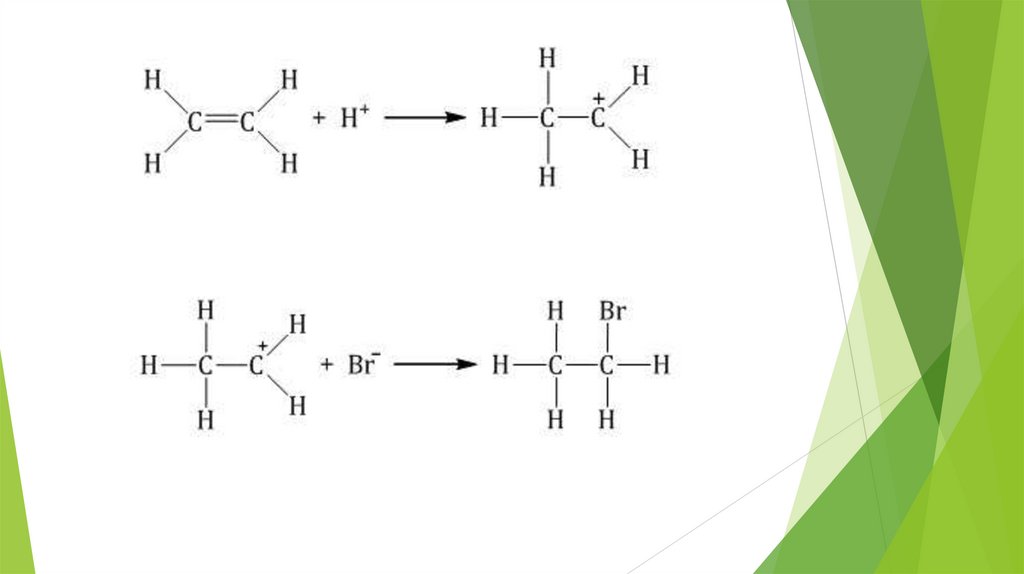
Пример: взаимодействие этилена с бромоводородом
6.
7.
Правило МарковниковаПравило Марковникова: при взаимодействии полярных молекул типа НХ с
несимметричными алкенами водород преимущественно присоединяется к
наиболее гидрогенизированному атому углерода при двойной связи.
Пример: взаимодействие хлороводорода с пропиленом
8.
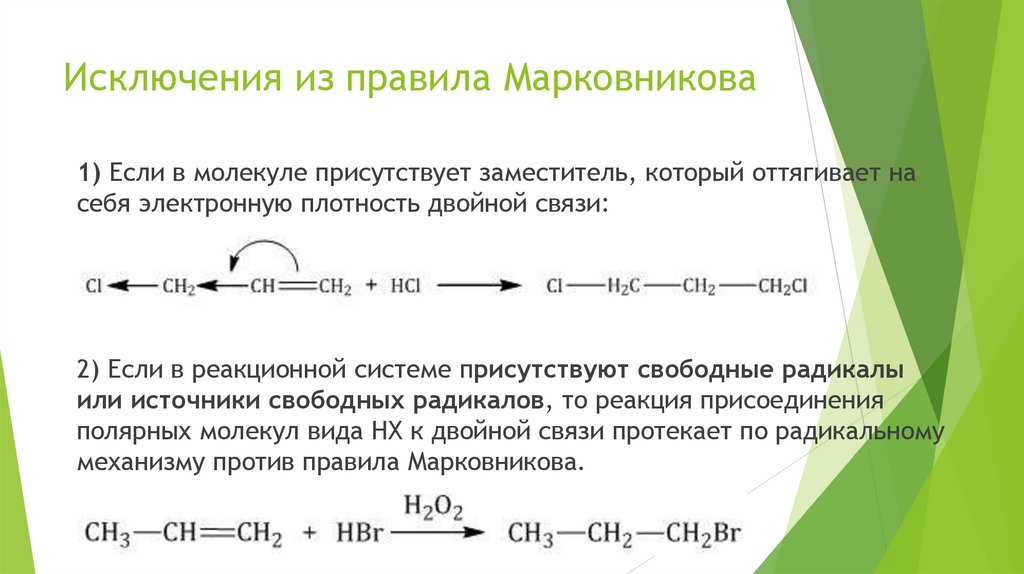
Исключения из правила Марковникова1) Если в молекуле присутствует заместитель, который оттягивает на
себя электронную плотность двойной связи:
2) Если в реакционной системе присутствуют свободные радикалы
или источники свободных радикалов, то реакция присоединения
полярных молекул вида НХ к двойной связи протекает по радикальному
механизму против правила Марковникова.
9.
Домашнее заданиеСтр.32, у.1,2







 Химия
Химия








