Похожие презентации:
Олефины. Химия
1.
2.
До недавнего времени подОлефинами подразумевались
вообще углеводороды общей
формулы С n Н 2n.
3.
Новые открытияПолучение триметилена и
других полиметиленовых
углеводородов показало, что
между ними возможны
вещества, обладающие
характером, который до
известной степени напоминает
характер углеводородов ряда
С n Н 2n+2 (Парафины), а
потому теперь определяют
Олефины, как замещенные
этилены
С 2 Н 4-mRm, где R = С n Н 2n+1, а
m = 1, 2, 3 и 4.
4.
Общая формула:СnH2n, где n≥2
ненасыщенные
ациклические
углеводороды,
содержащие в
молекуле одну
двойную связь
С=С.
5.
Первый член рядаолефин- этилен
СH2=СH2, поэтому
олефины называют
также этиленовыми
углеводородами.
6.
ФормулаC2H4
C3H6
C4H8
C5H10
C6H12
C7H14
C8H16
C9H19
Название
этилен (этен)
пропилен (пропен)
бутилен (бутен)
пентен
гексен
гептен
октен
нонен
По систематической
номенклатуре
суффикс
ан
заменяется на
суффикс
ен
!
7.
8.
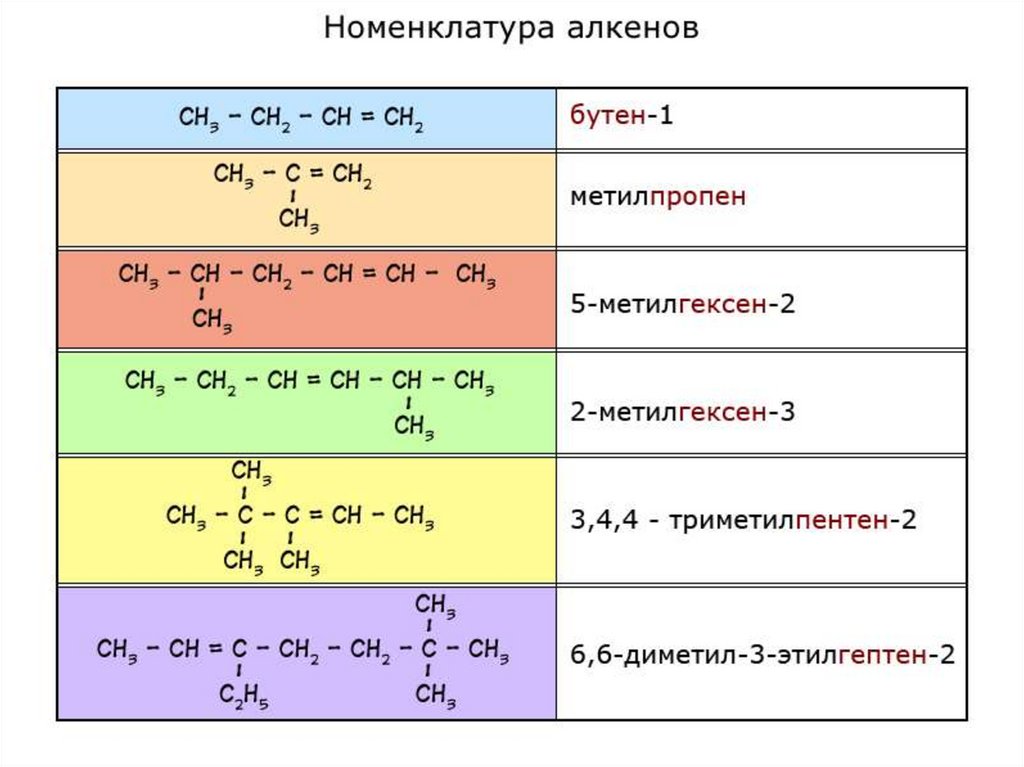
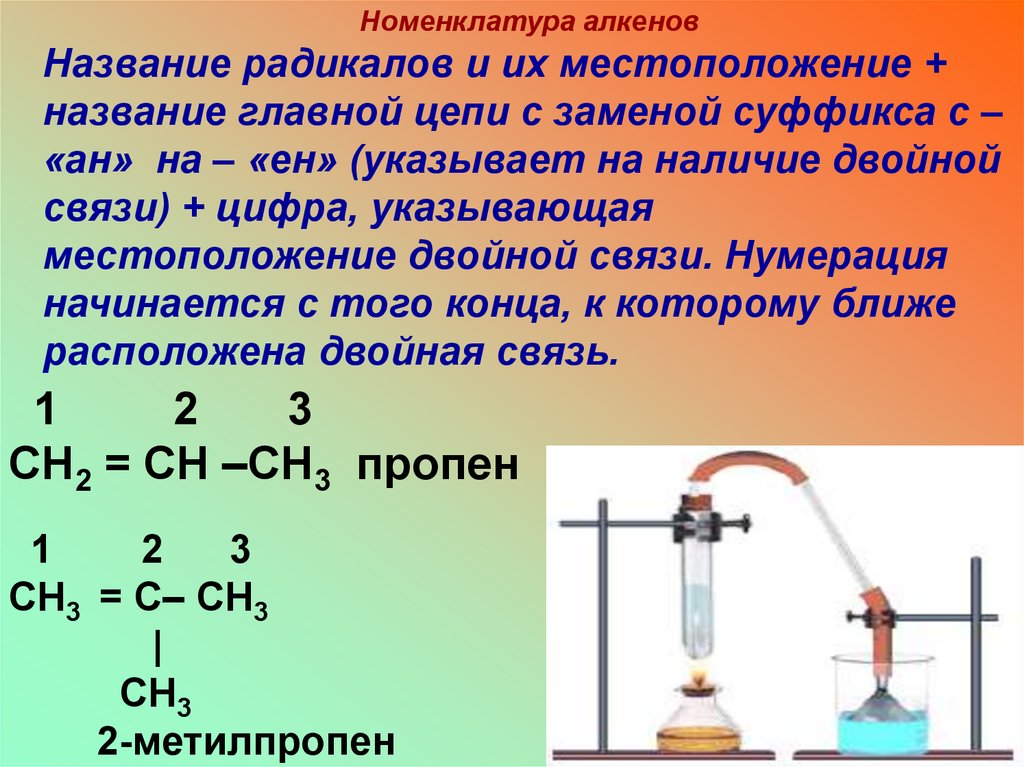
Номенклатура алкеновНазвание радикалов и их местоположение +
название главной цепи с заменой суффикса с –
«ан» на – «ен» (указывает на наличие двойной
связи) + цифра, указывающая
местоположение двойной связи. Нумерация
начинается с того конца, к которому ближе
расположена двойная связь.
1
2
3
СН2 = СН –СН3 пропен
1
2
3
СН3 = С– СН3
|
СН3
2-метилпропен
9.
В гомологическом рядунаблюдается следующие
закономерности:
Формула
C2H4-C4H8
Агрегатное
состояние
газы
C5H10 –C18H36
жидкости
с C19H38
твердые
10.
Этилен –бесцветный газ,
почти без запаха,
немного легче
воздуха плохо
растворим в
воде.
11.
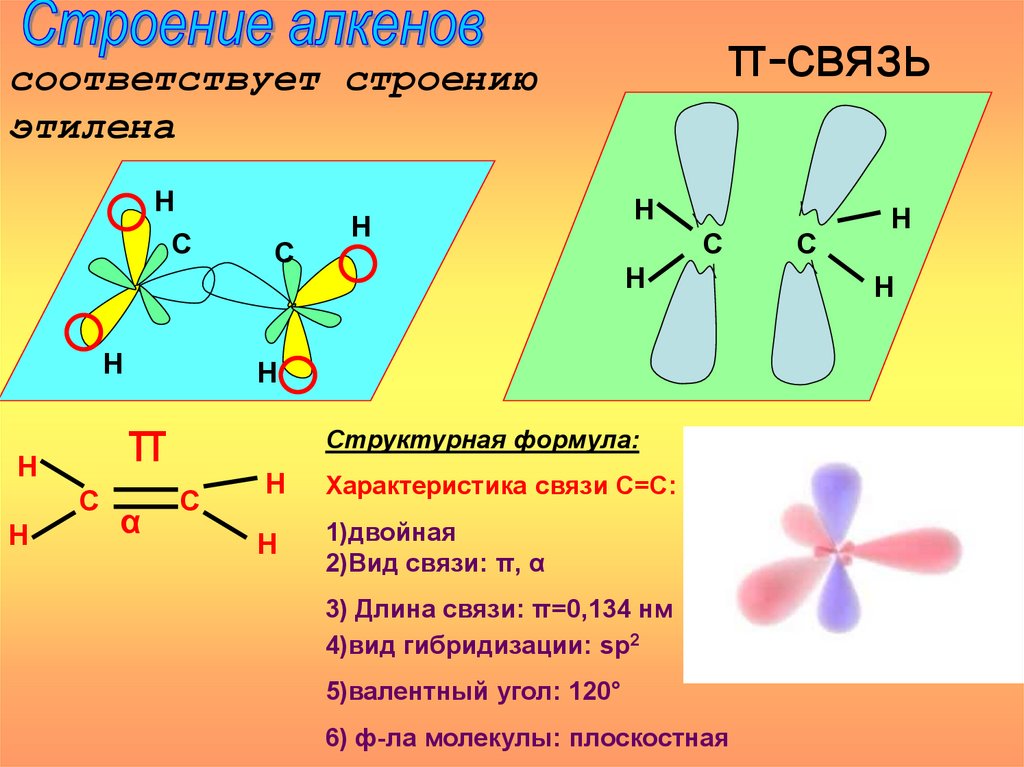
π-связьсоответствует строению
этилена
H
C
H
C
H
H
C
H
H
π
H
C
H
α
Структурная формула:
C
H
H
Характеристика связи С=С:
1)двойная
2)Вид связи: π, α
3) Длина связи: π=0,134 нм
4)вид гибридизации: sp2
5)валентный угол: 120°
6) ф-ла молекулы: плоскостная
C
H
H
12.
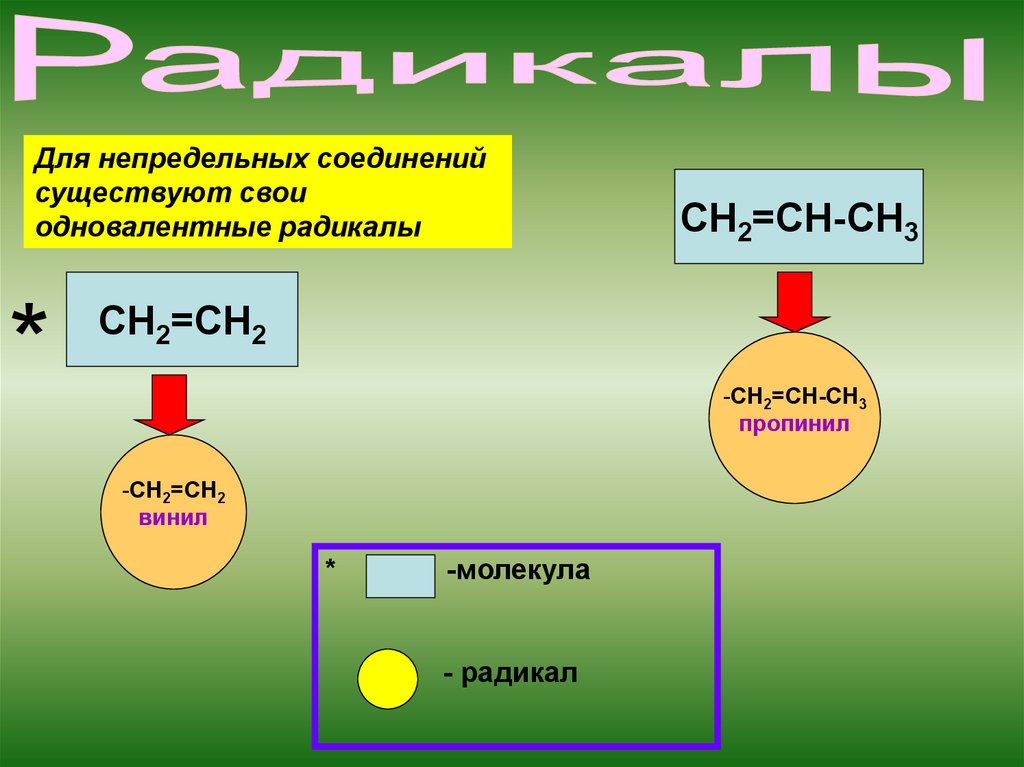
Для непредельных соединенийсуществуют свои
одновалентные радикалы
*
CH2=СH-CH3
CH2=CH2
-CH2=СН-CH3
пропинил
-CH2=CH2
винил
*
-молекула
- радикал
13.
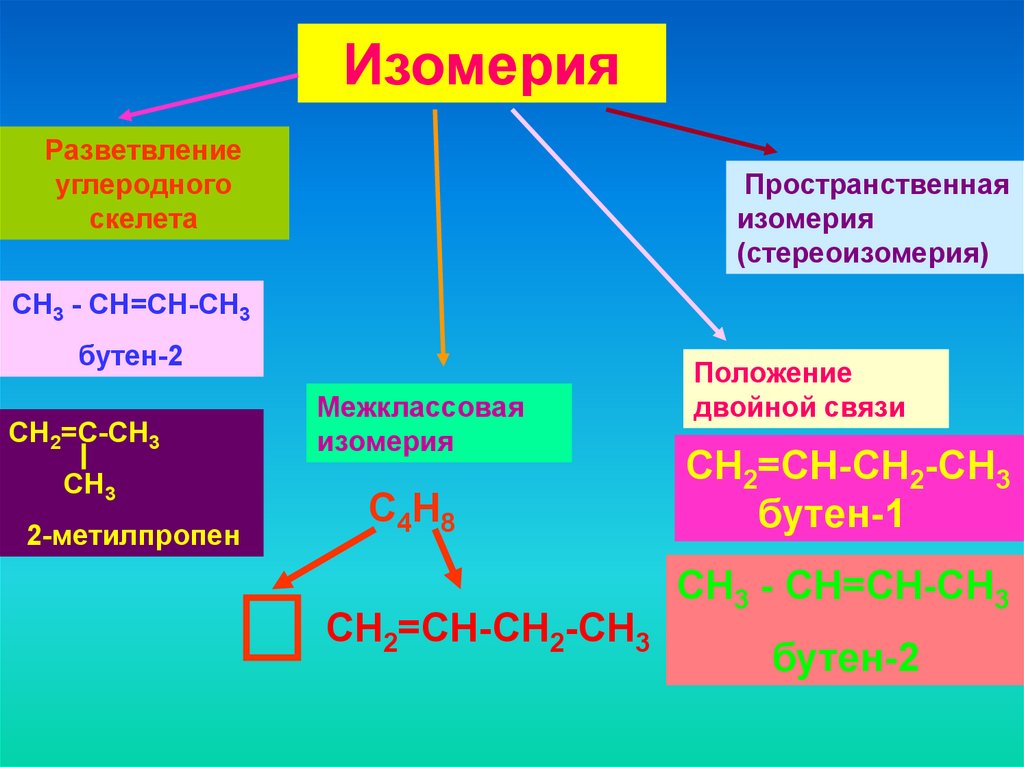
ИзомерияРазветвление
углеродного
скелета
Пространственная
изомерия
(стереоизомерия)
CH3 - CH=СH-СН3
бутен-2
CH2=С-СН3
CH3
2-метилпропен
Межклассовая
изомерия
С4Н8
CH2=СH-СН2-CH3
Положение
двойной связи
CH2=СH-СН2-CH3
бутен-1
CH3 - CH=СH-СН3
бутен-2
14.
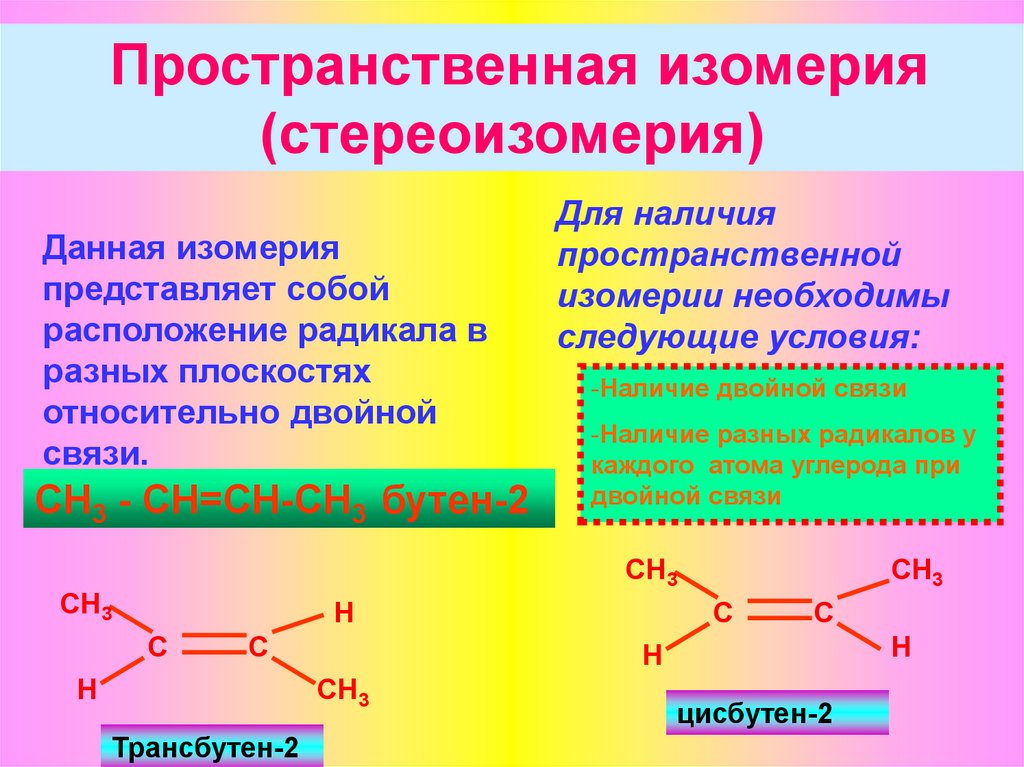
Пространственная изомерия(стереоизомерия)
Данная изомерия
представляет собой
расположение радикала в
разных плоскостях
относительно двойной
связи.
CH3 - CH=СH-СН3 бутен-2
Для наличия
пространственной
изомерии необходимы
следующие условия:
-Наличие двойной связи
-Наличие разных радикалов у
каждого атома углерода при
двойной связи
СH3
СH3
H
C
C
Трансбутен-2
C
C
H
H
СH3
H
СH3
цисбутен-2
15.
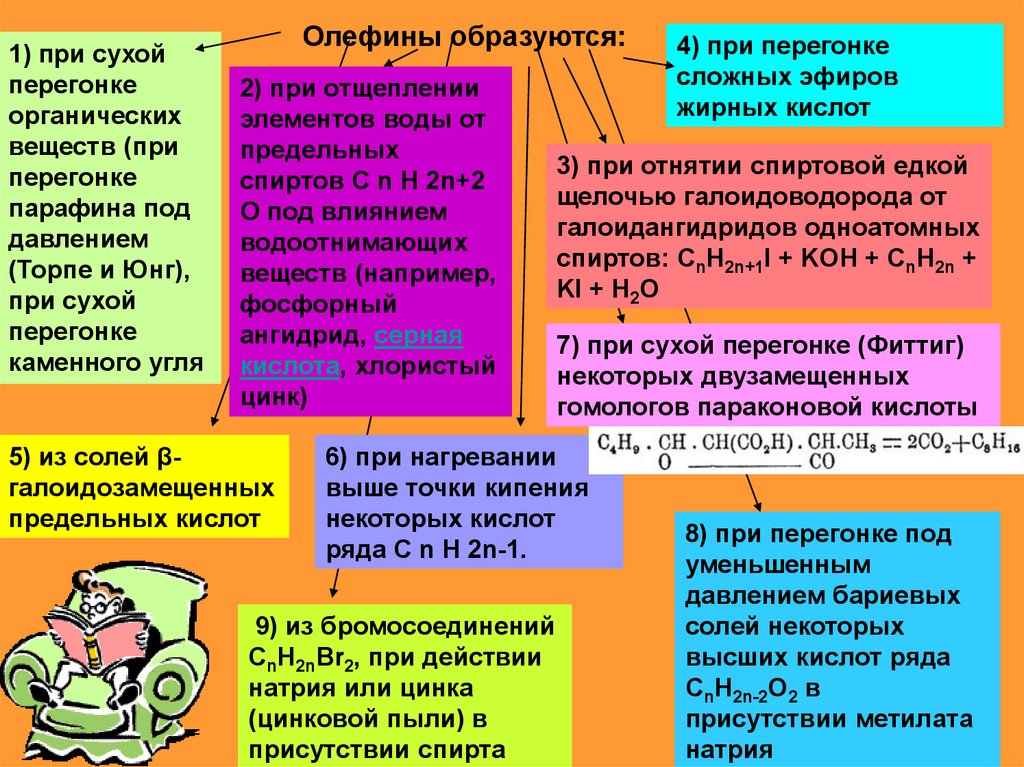
1) при сухойперегонке
органических
веществ (при
перегонке
парафина под
давлением
(Торпе и Юнг),
при сухой
перегонке
каменного угля
Олефины образуются:
2) при отщеплении
элементов воды от
предельных
спиртов С n Н 2n+2
O под влиянием
водоотнимающих
веществ (например,
фосфорный
ангидрид, серная
кислота, хлористый
цинк)
5) из солей βгалоидозамещенных
предельных кислот
3) при отнятии спиртовой едкой
щелочью галоидоводорода от
галоидангидридов одноатомных
спиртов: CnH2n+1I + KOH + СnН2n +
KI + Н2О
7) при сухой перегонке (Фиттиг)
некоторых двузамещенных
гомологов параконовой кислоты
6) при нагревании
выше точки кипения
некоторых кислот
ряда С n Н 2n-1.
9) из бромосоединений
СnН2nВr2, при действии
натрия или цинка
(цинковой пыли) в
присутствии спирта
4) при перегонке
сложных эфиров
жирных кислот
8) при перегонке под
уменьшенным
давлением бариевых
солей некоторых
высших кислот ряда
СnН2n-2О2 в
присутствии метилата
натрия
16.
CH2=СН2+Н2 => CH3-СН3этилен
этан
17.
2) Полное окисление алкенов сходство со всемиорганическими соединениями
t°
C2Н4+3О2 => 2CО2+3Н2О
18.
3)4) Присоединение галогенов- первая
качественная реакция
CH2=СН2+Br2 =>
бромная
вода
CH2-СН2
Br Br
дибромбутан
19.
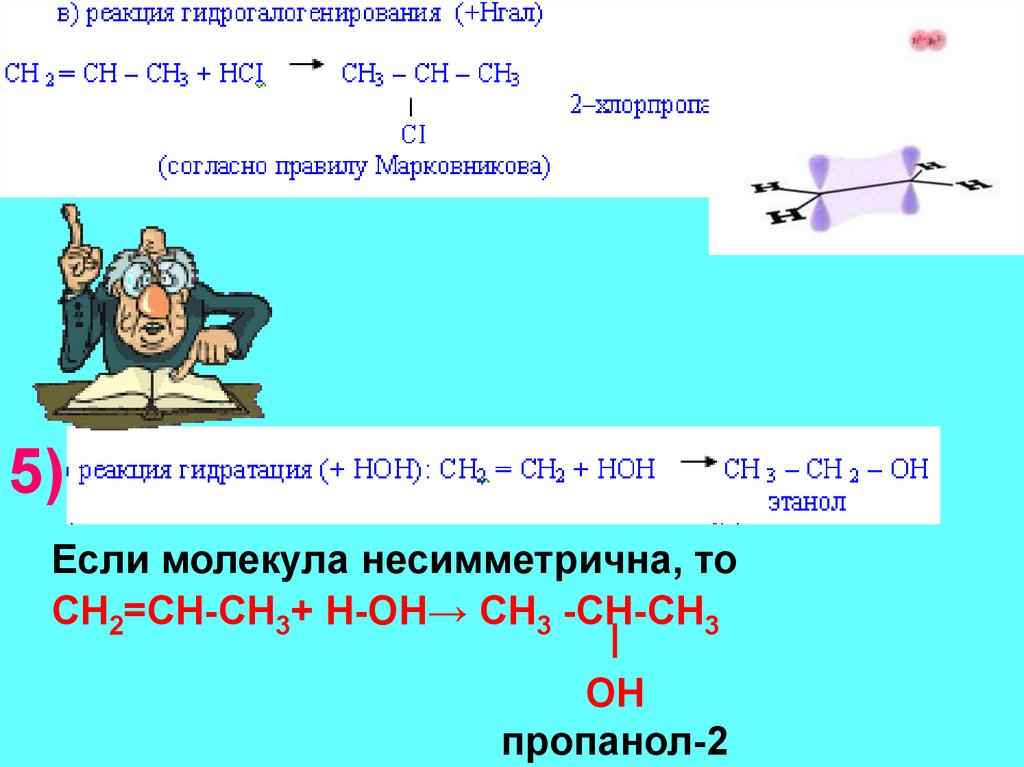
5)Если молекула несимметрична, то
CH2=СH-CH3+ Н-ОН→ CH3 -СH-CH3
ОН
пропанол-2
20.
Реакция неполного окисления- втораякачественная реакция на алкены
21.
22.
23.
1. получение пластмасс –изготовление посуды, труб,
пленки;
2. получение этанола –
растворитель, используется
в органическом синтезе
3. получение этиленгликоля –
антифриз – понижает
температуру замерзания
4. в продуктах переработки
нефти и природных газов.
5. для синтеза полимеров и
других ценных промышленных
продуктов.














 Химия
Химия








