Похожие презентации:
Кислоты. Организм человека
1.
КИСЛОТЫНовикова Екатерина Евгеньевна,
учитель химии
ГБОУ школы-интерната (I вида) №31
Невского района
2.
Организмчеловека
Кислоты
в нашей
жизни:
Растения
кислоты
Насекомые
Пища
Лекарства
Животные
3.
Кислотыв природе:
• Лимонная кислота
• Яблочная кислота
• Щавелевая кислота
• Муравьиная кислота
4.
Кислоты в продуктах питания:• Уксусная кислота
• Молочная кислота
• Лимонная кислота
5.
Кислоты в организмечеловека:
Аскорбиновая,
фолиевая,
оротовая,
пангамовая,
никотиновая
и другие кислоты
являются
витаминами.
6.
Кислоты в организме человека:Соляная кислота
находится в желудке.
Бактерии, попавшие в
желудок с пищей,
погибают под ее
действием.
7.
Кислоты в организме человека:Молочная кислота
образуется в мышцах
при физической
нагрузке.
8.
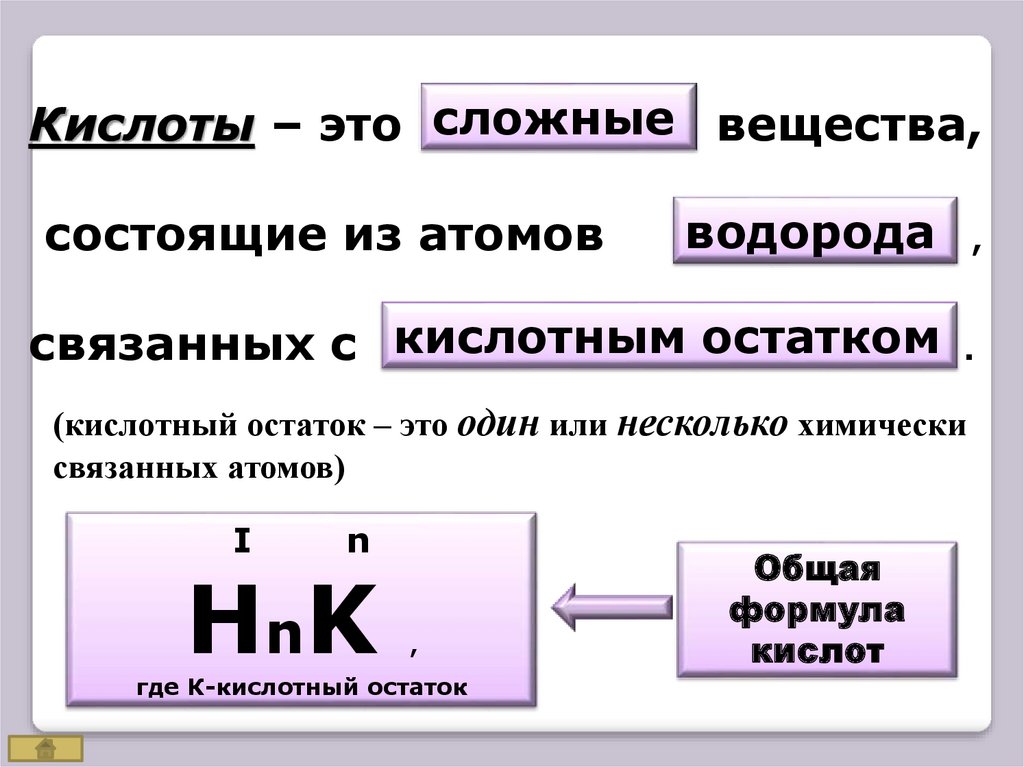
Кислоты – это сложныекакие?
вещества,
состоящие из атомов
водорода
какого элемента? ,
связанных с кислотным
чем? остатком
.
(кислотный остаток – это один или несколько химически
связанных атомов)
I
n
НnK
,
где К-кислотный остаток
Общая
формула
кислот
9.
Название кислотыФормула кислоты
Кислотный остаток,
его валентность
Азотная
HNO3
-NO3
Серная
H2SO4
=SO4
Угольная
H2CO3
=CO3
Кремниевая
H2SiO3
=SiO3
Метафосфорная
HPO3
-PO3
Ортофосфорная
H3PO4
PO4
Соляная
HCl
-Cl
10.
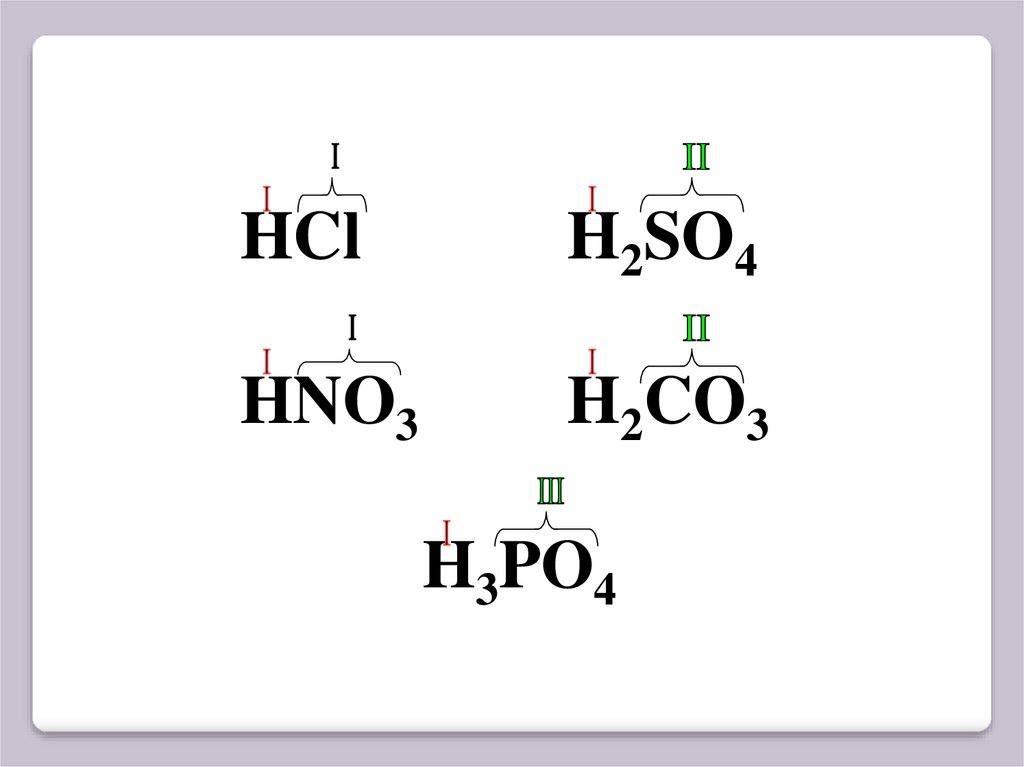
HClH2SO4
HNO3
H2CO3
H3PO4
11.
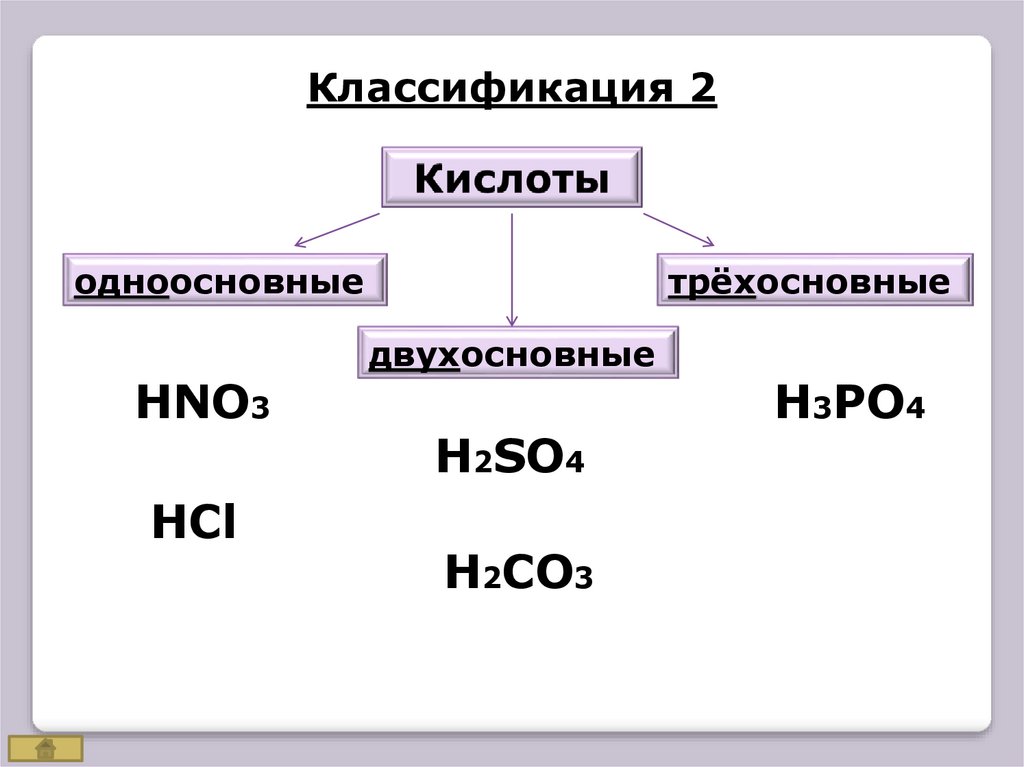
Классификация 1Кислоты
кислородные
бескислородные
HNO3
HCl
H2SO4
H 2S
H3PO4
HF
12.
Классификация 2одноосновные
HNO3
HCl
трёхосновные
двухосновные
H2SO4
H2CO3
H3PO4
13.
Это модель молекулы вещества.Скажите химическую формулу
вещества и назовите его.
НСl
Соляная
кислота
14.
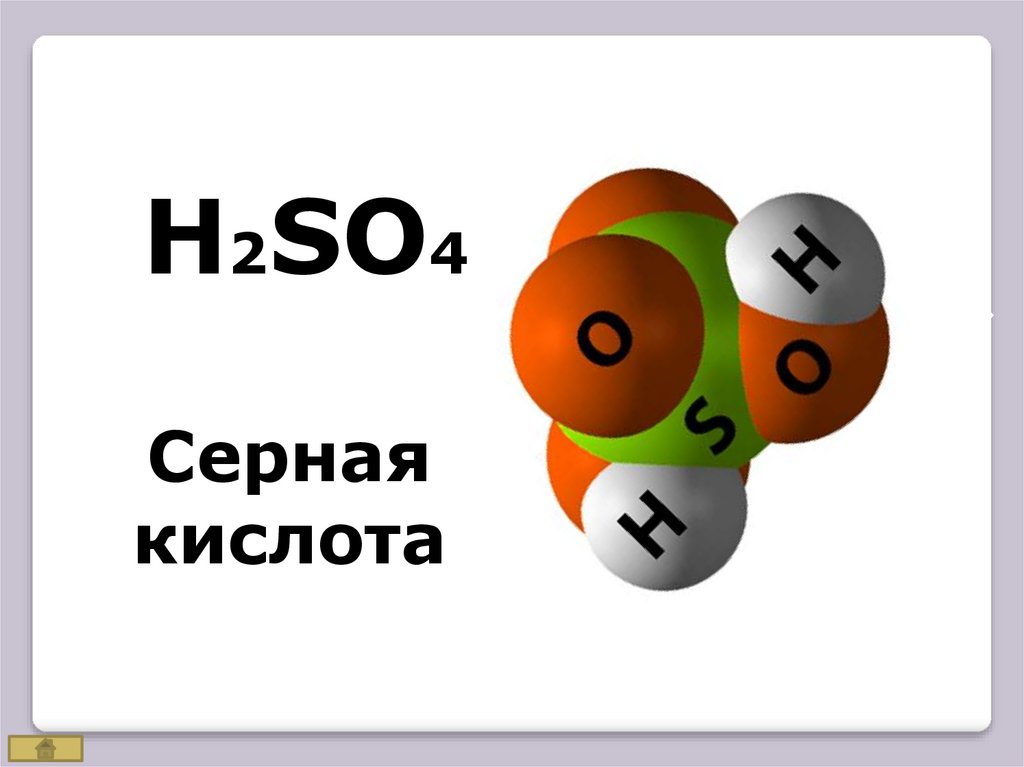
H2SO4Серная
кислота
15.
H2CO3С
С
Угольная
кислота
16.
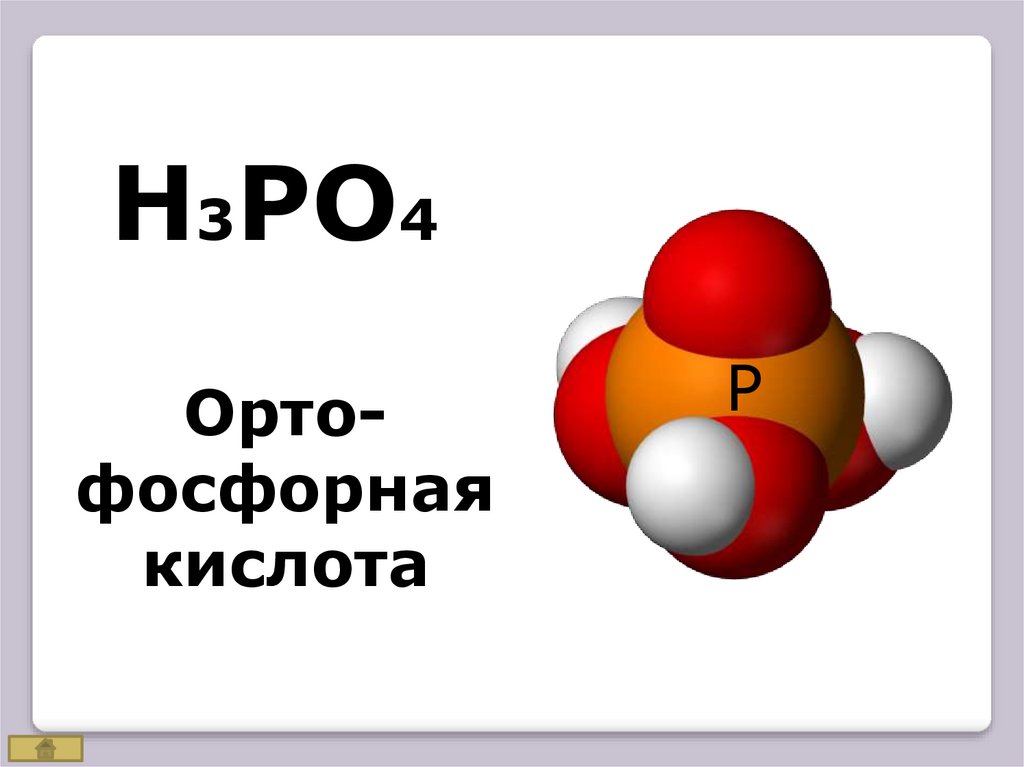
H3PO4Ортофосфорная
кислота
Р
17.
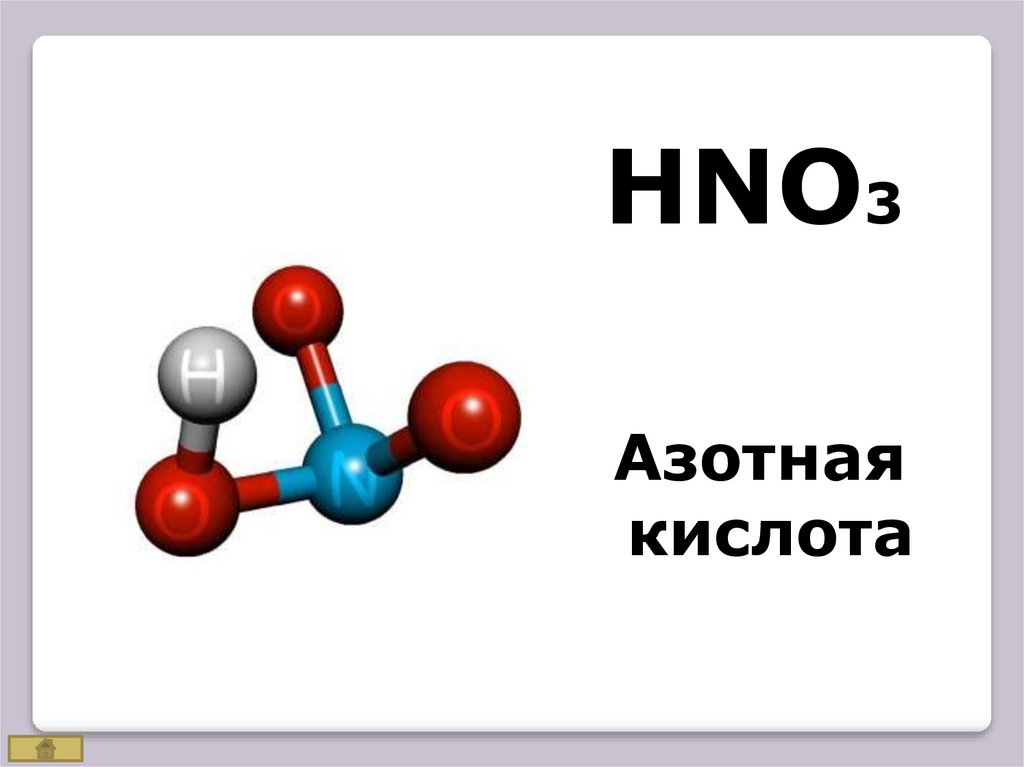
HNO3Азотная
кислота
18.
Физические свойства:Большинство
кислот – жидкие вещества.
Разъедают (разрушают):
• кожу,
• ткани,
• бумагу,
• древесину.
19.
Техникабезопасности
При попадании
кислоты на кожу,
необходимо
это место промыть
большим количеством
воды
и обработать
раствором соды
20.
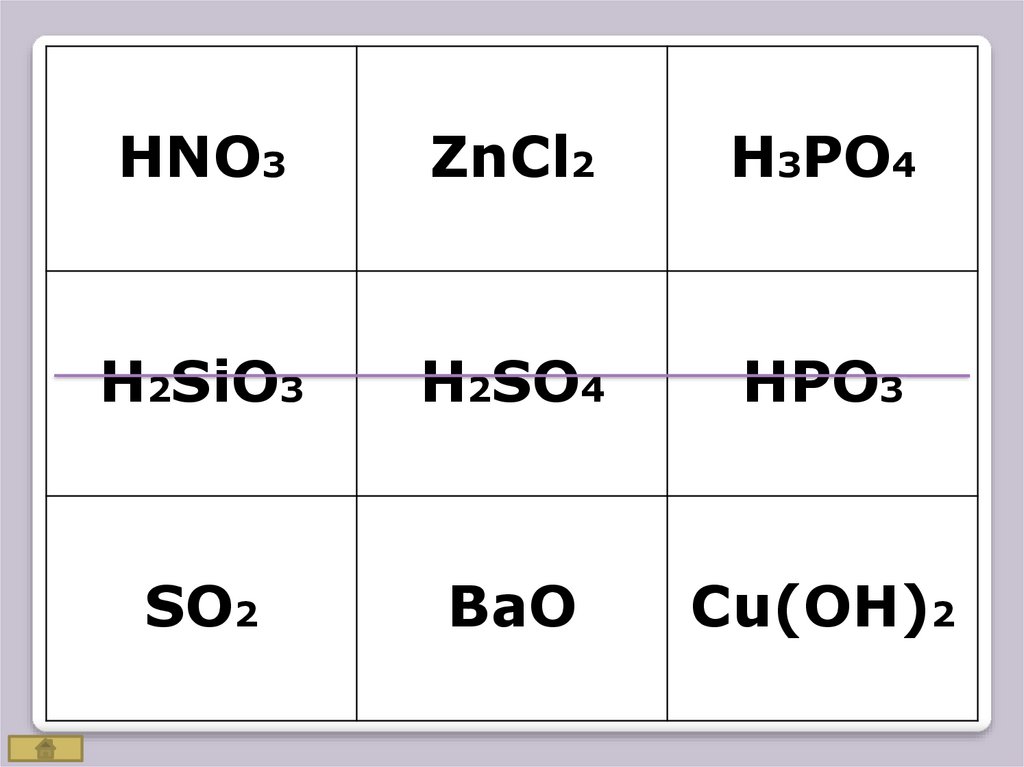
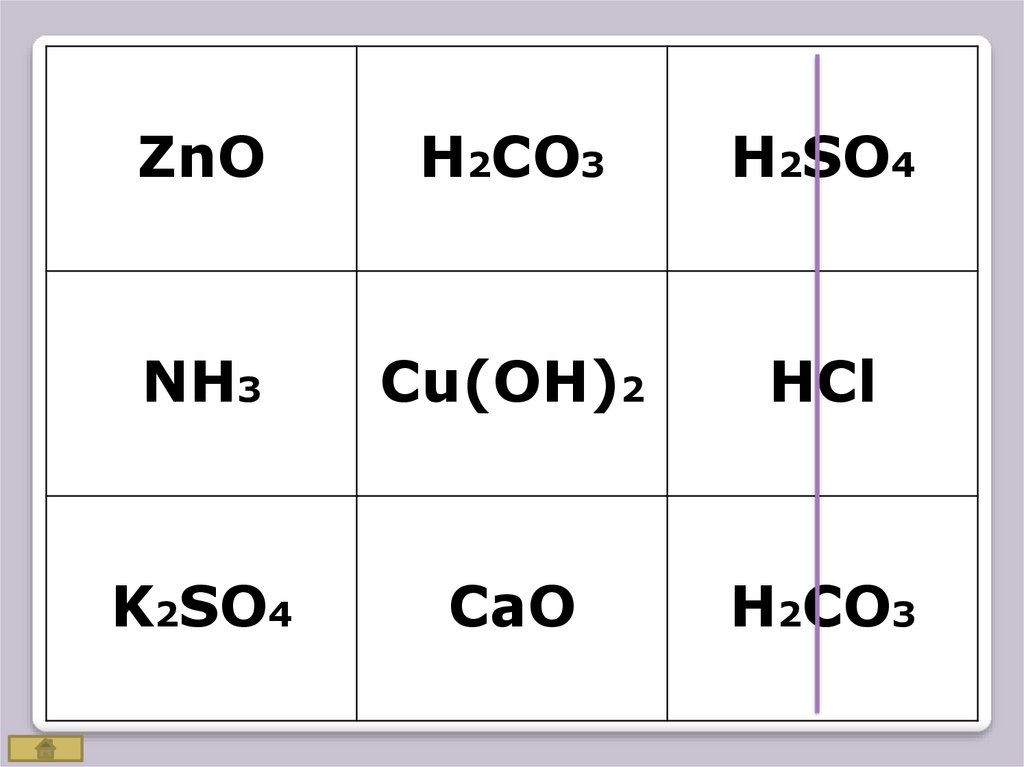
Игра«Крестики – нолики»
Покажите
выигрышный путь,
который составляют
формулы
КИСЛОТ
21.
HNO3ZnCl2
H3PO4
H2SiO3
H2SO4
HPO3
SO2
BaO
Cu(OH)2
22.
ZnOH2CO3
H2SO4
NH3
Cu(OH)2
HCl
K2SO4
CaO
H2CO3
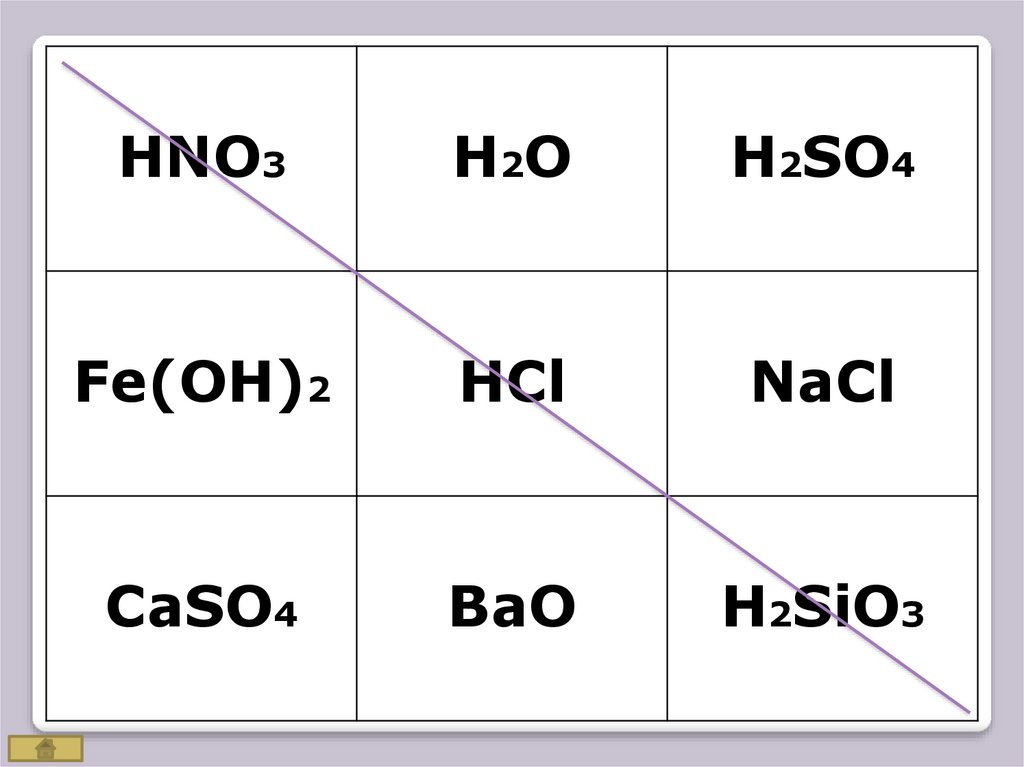
23.
HNO3H2O
H2SO4
Fe(OH)2
HCl
NaCl
CaSO4
BaO
H2SiO3
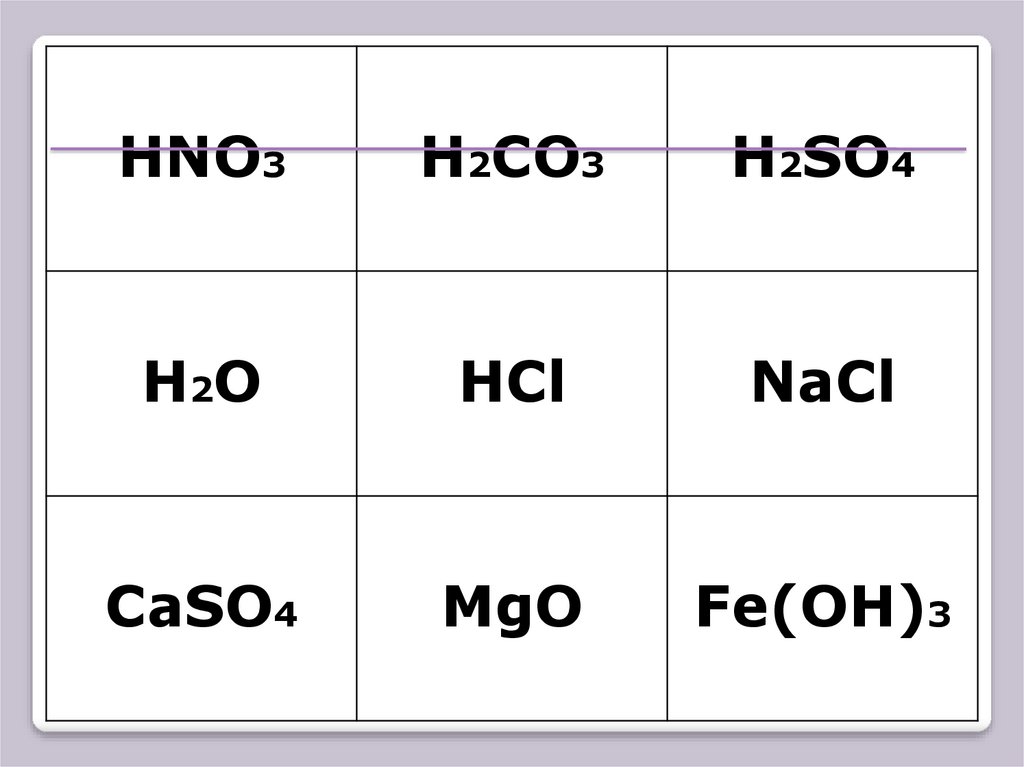
24.
HNO3H2CO3
H2SO4
H2O
HCl
NaCl
CaSO4
MgO
Fe(OH)3
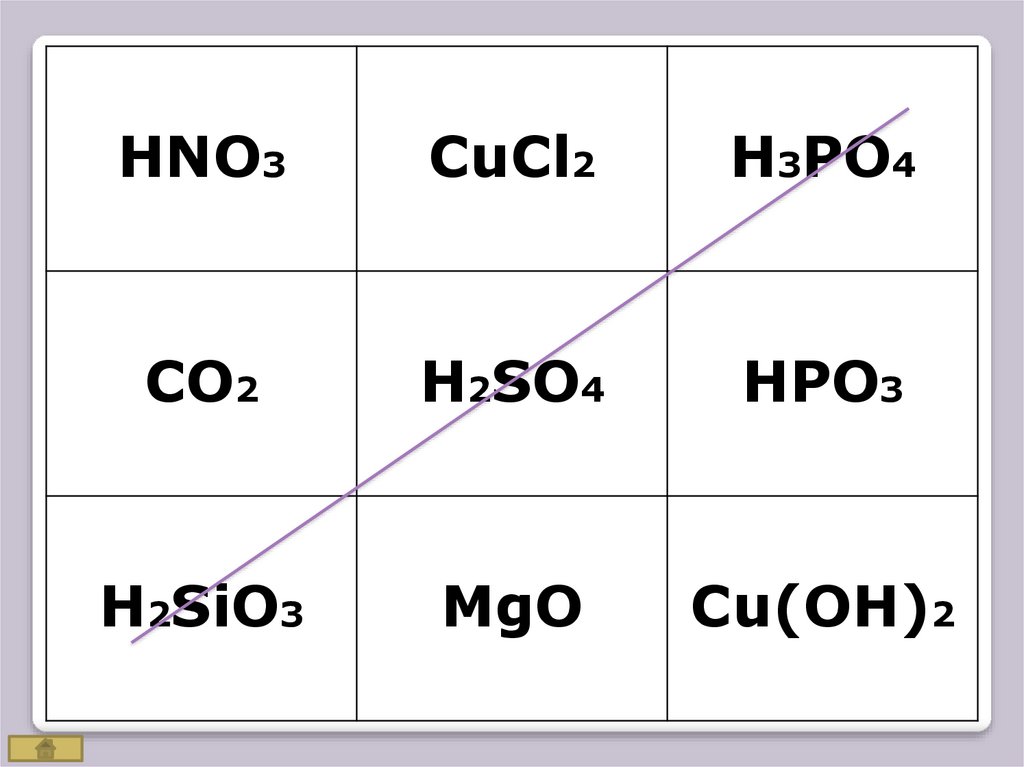
25.
HNO3CuCl2
H3PO4
СO2
H2SO4
HPO3
H2SiO3
MgO
Cu(OH)2
26.
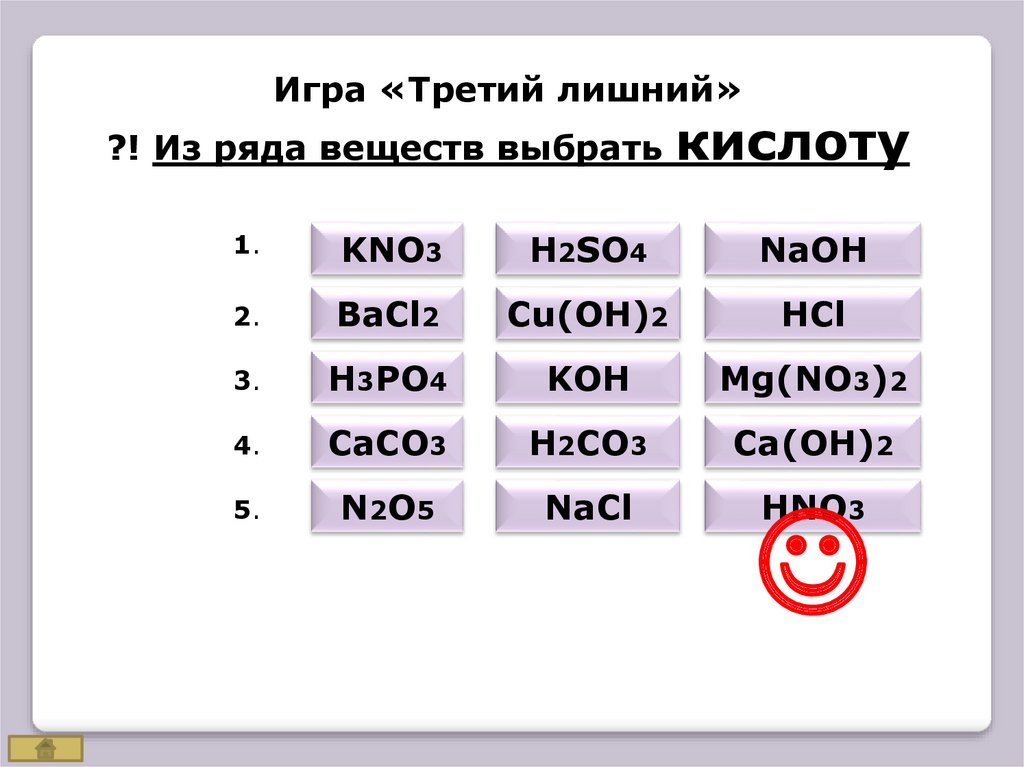
Игра «Третий лишний»?! Из ряда веществ выбрать
кислоту
1.
KNO3
H2SO4
NaOH
2.
BaCl2
Cu(OH)2
HCl
3.
H3PO4
KOH
Mg(NO3)2
4.
CaCO3
H2CO3
Ca(OH)2
5.
N2O5
NaCl
HNO3
27.
?! Выбрать соответствующуюформулу:
Соляная
HNO3
HCl
Азотная
H2CO3
H3PO4
Серная
HCl
H2SiO3
H2SO4
HNO3
H2SO4
28.
?! Выбрать название кислоты:H2SO4
соляная
серная
HCl
угольная
кремниевая
HNO3
азотистая
H2CO3
сернистая
H3PO4
азотная
азотная
угольная
соляная
сернистая
соляная
соляная
серная
ортофосфорная
29.
?! Определить число атомовводорода (индекс) в кислотах:
H SO4
1
2
3
H NO3
1
2
3
H PO4
1
2
H CO3
1
2
3
3
30.
Что делать, если забыл(а)формулу кислородсодержащей
кислоты:
1.Составить формулу
высшего оксида
2.Прибавить молекулу
воды
31.
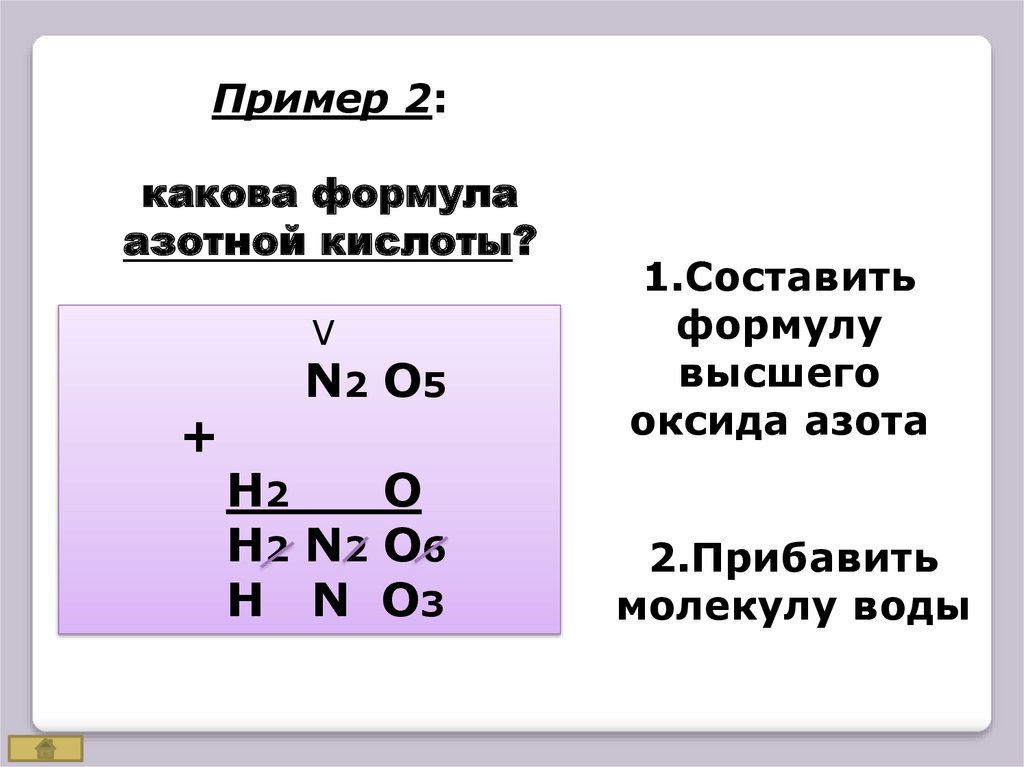
Пример 2:какова формула
азотной кислоты?
V
+
N2 O5
H2
O
H2 N2 O6
H N O3
1.Составить
формулу
высшего
оксида азота
2.Прибавить
молекулу воды
32.
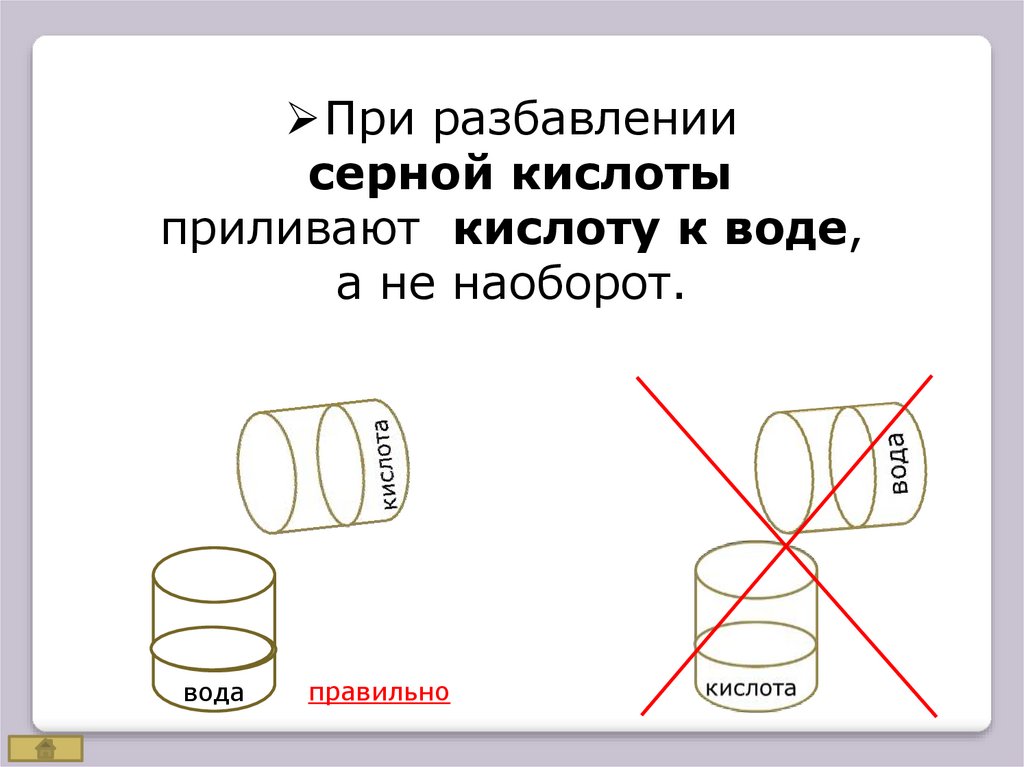
При разбавлениисерной кислоты
приливают кислоту к воде,
а не наоборот.
вода
правильно
33.
Нельзя приливатьводу к кислоте,
потому что
происходит сильное
разогревание
раствора и его
разбрызгивание.
Брызги кислоты могут
попасть на одежду,
лицо и руки.
Это очень опасно!
34.
Спасибоза внимание



















 Биология
Биология Химия
Химия








