Похожие презентации:
Жидкие лекарственные формы
1.
Жидкиелекарственные
формы
2.
Изготовление водных растворовмассо-объемным методом
Массо – объемный метод изготовления
жидких лекарственных форм с водной и
водно-спиртовой дисперсионной средой
принят действующей ГФ, как основной,
и подробно рассматривается в
3.
Приказе №308 от 16.10.97«Инструкция по изготовлению
жидких лекарственных форм в
аптеках»
Приказе №751н от 26.10.2015
«Об утверждении правил
изготовления и отпуска ЛП для мед.
применения аптечными
организациями …
4.
• При изготовлении ЖЛФ, если впрописи не указан растворитель,
изготавливают водный раствор.
• Под названием «вода» при отсутствии
особых указаний понимают воду
очищенную, полученную методом
дистилляции, обратным осмосом или
методом ионного обмена.
5.
Факторы, влияющие наобразование раствора
1. Добавление ВВ для
образования легко
растворимых
комплексных
соединений
2. Перемешивание способствует
переносу молекул твердого
вещества из близлежащих в
более отдаленные слои до
выравнивания концентрации
раствора
3. Нагревание раствора или
растворителя усиливает
колебательные движения самих
молекул вещества, обеспечивая
разрушение кристаллизационной
решетки; уменьшает вязкость
растворителя; растворимость и
скорость растворения веществ
возрастает
4. Измельчение
твердого вещества
увеличивает суммарную
его поверхность; при
этом больше контакт с
растворителем,
скорость растворения
растет
-
6.
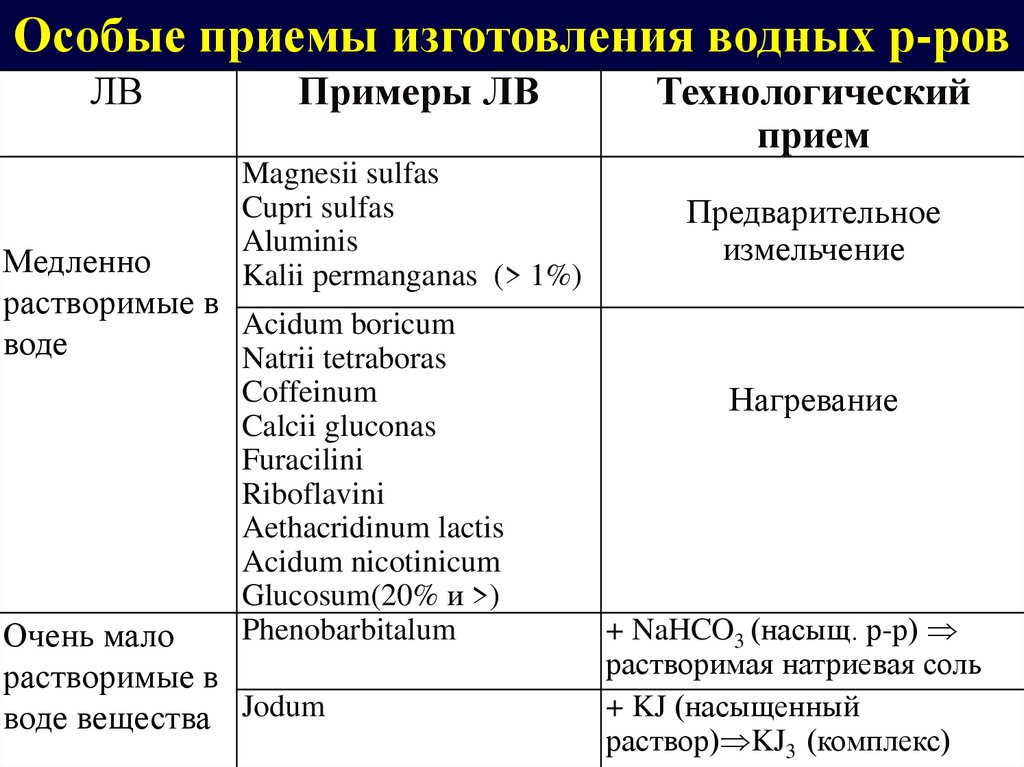
Особые приемы изготовления водных р-ровЛВ
Примеры ЛВ
Magnesii sulfas
Cupri sulfas
Aluminis
Kalii permanganas (> 1%)
Медленно
растворимые в
Acidum boricum
воде
Natrii tetraboras
Coffeinum
Calcii gluconas
Furacilini
Riboflavini
Aethacridinum lactis
Acidum nicotinicum
Glucosum(20% и >)
Phenobarbitalum
Очень мало
растворимые в
воде вещества Jodum
Технологический
прием
Предварительное
измельчение
Нагревание
+ NaHCO3 (насыщ. р-р)
растворимая натриевая соль
+ KJ (насыщенный
раствор) KJ3 (комплекс)
7.
Алгоритм изготовления ЖЛФФармацевтическая экспертиза рецепта
1. Проверка правильности выбора формы
рецептурного бланка (приказ №4 н от 26.03.19)
2. Проверка совместимости ингредиентов
3. Проверка доз ЛВ ядовитых и сильнодействующих
4. Расчет количества ингредиентов и оформление
оборотной стороны ППК
5. Выбор оптимального варианта технологии
Растворение
Фильтрование
Смешивание
Упаковка и укупорка
Оформление к отпуску
8.
Проверка дозИзготавливать можно :
Vобщ (общий объем раствора) = 1. РД и СД веществ
ядовитых и СД
сумме объемов всех жидких
не превышают ВРД
компонентов по рецепту
и ВСД;
N (общее число приемов) =
2. Доза завышена, но
V раствора(микстуры)
имеются
V объем разовой дозы
специальные
РД = M вещества по рецепту
пометки врача (доза
прописью и «!»);
N
СД = РД х число приемов в сутки 3. Доза завышена и
нет специальных
пометок, то готовят
Сравнение РД с ВРД и СД с ВСД
из расчета ½ ВРД на
1 прием
Расчеты:
9.
Нормы отпуска наркотических иприравненных к ним веществ
Количество наркотических
и приравненных к ним ЛВ:
• Не должно превышать
установленную норму
• Может превышать
установленную норму не
более чем в 2 раза для
онкологических больных ,
прикрепленных к данной
аптеке
Нормы отпуска
наркотических веществ
Этилморфина г/х – 0,2 г
Кодеин
– 0,2 г
Морфина г/х
– 0,1 г
Промедол
– 0,25 г
Приказ (№4н)
10.
Rp.: Solutionis Analgini (Metamizolinatrici) ex 4,0 – 200 ml
Da. Signa: по 1 ст. л. 3 раза в
день
V общ = 200 мл
N = 200 мл : 15 мл = 13 раз
РД = 4,0 : 13 = 0,3 ВРД = 1,0
СД = 0,3 * 3 = 0,9 ВСД = 3,0, т.е. ДНЗ
11.
РАСЧЕТ ОБЪЕМА ВОДЫ ОЧИЩЕННОЙN -норма допустимого отклонения,%
(приказ №751н)
Допустимое отклонение:
200 мл ±2% (±4 мл)
КУО (мл/г) показывает увеличение объема
(мл) при растворении 1,0 г вещества
(приказ №751н)
Анальгин – 0,68мл/г 4,0 = 2,72 мл < 4 мл
Прирост объема не учитываем.
12.
Последовательность добавленияингредиентов
При изготовлении ЖЛФ с водной дисперсной средой в первую
очередь отмеривают рассчитанный объем воды очищенной, в
которой последовательно растворяют твердые лекарственные и
вспомогательные вещества с учетом растворимости и возможного
их взаимодействия.
Первыми в отмеренном объеме воды растворяют ядовитые и
наркотические вещества, затем сильнодействующие), а далее
несильнодействующие с учетом их растворимости. Для
повышения растворимости веществ умеренно (1 30 – 100 мл.),
мало (1 100 – 1000 мл.) или медленно (время растворения более 10
мин.) растворимых их предварительно измельчают, а в процессе
изготовления их растворы нагревают с учетом физико –
химических свойств и перемешивают.
13.
Последовательность добавления ингредиентовППК №1
Вода очищенная
Анальгин
14.
Последовательность добавления ингредиентовПри изготовлении препарата по приведенной
прописи специалист выполняет следующие
действия по стадиям:
I. Растворение.
В подставку отмеривают 200 мл воды очищенной.
Отвешивают 4,0 анальгина и растворяют его.
Контроль полноты растворения.
II. Фильтрование.
Водный раствор анальгина фильтруют через
промытый тампон ваты в отпускной флакон.
15.
Последовательность добавления ингредиентовIII. Смешивание.
Если в состав лекарственной формы входят другие
жидкие лекарственные средства, их добавляют к водному
раствору в следующей последовательности:
• Водные нелетучие и непахучие жидкости;
• Иные нелетучие жидкости, смешивающиеся с
водой;
• Водные летучие жидкости;
• Жидкости, содержащие спирт в порядке
возрастания его концентрации (приложение 8);
• Летучие и пахучие жидкости.
После добавления спиртосодержащих лекарственных средств
(галеновые и новогаленовые препараты) фильтрование не
допускается.
16.
Последовательность добавления ингредиентовIV. Упаковка.
Флакон укупоривают пластмассовой пробкой и
навинчивающимся колпачком. Проверяют на
герметичность при переворачивании.
V. Оформление.
Основная этикетка «Внутреннее» . Номер препарата по
квитанционной книге. Предупредительные надписи:
«Сохранять в прохладном месте» «Сохранять в
защищенном от света месте» (при отсутствии флакона
темного стекла), «Хранить в недоступном от детей
месте»
17.
Последовательность добавления ингредиентовППК № 1
Aquae purificatae 200 ml
Analgini 4,0
_____________________________
Vобщ = 200 мл±2% (±4 мл)
Подписи
18.
Частные случаиизготовления
растворов
19.
Растворы медленно растворимых ЛВк-та борная
Na2B4O7
квасцы алюмокалиевые
амидопирин
кальция глюконат
1. Высокая прочность кристаллической
решетки, плохая смачиваемость
поверхности водой.
2. В горячей или кипящей воде очищенной,
с предварительным измельчением в ступке
Rp: Sol. Acidi borici 2% - 200 ml в присутствии части растворителя
D.S.: Для промывания
Дата
ППК №4
Aquae purificatae 200 ml
Acidi borici
4,0
V общий - 200 мл
В 200 мл горячей воды растворяют 4 г
кислоты борной, перемешивают.
После охлаждения объем раствора
измеряют и, если необходимо, доводят
водой до 200 мл, фильтруют во флакон.
Rp: Sol. Cupri sulfatis 2%- 200 ml
D.S.: Для промывания
Дата
ППК №5
Aqua purificata 200 ml
Cupri sulfas
4,0
V общий = 200 мл
Технология:
Технология:
4 г меди сульфата измельчают в
сухом виде в ступке, добавляют
порцию воды 30 - 40 мл и
продолжают растирание. Полученный
раствор осторожно сливают во флакон, а
с остатком препарата повторяют туже
операцию, добавляя воду порциями до
полного растворения ЛВ.
20.
Раствор ЛюголяДля внутреннего
применения
5%
Йода 5,0
Калия йодида 10,0
Воды очищенной
до 100мл
Для наружного
применения
1%
Йода 1,0
Калия йодида 2,0
Воды очищенной
до 100мл
Водные р-ры йода могут быть получены только в виде
растворимого комплекса, образующегося в насыщенном
водном растворе калия иодида (растворимость KJ в воде
1:0,75).
Калия иодида по отношению к йоду берут в двойном
количестве.
21.
Растворы окислителейAgNO3, KMnO4
Растворяют в свежеприготовленной и предварительно
профильтрованной воде очищенной не фильтруя, а в случае
необходимости фильтруют через стеклянный фильтр №1 или 2
или через ватный тампон промытый горячей водой очищенной
Раствор KMnO4 отпускают во флаконе темного стекла,
ЛВ растворяют в горячей воде (растворимость в горячей 1:3,5,
в холодной 1:18).
В концентрации выше 1 % готовят - предварительно растирая
в ступке с небольшими порциями свежеперегнанной
профильтрованной воды очищенной. Полученные порции
раствора сливают в отпускной флакон и растирают калия
перманганат с новой порцией воды до его растворения.
Раствор Ag NO3 Список А - этикетка «Обращаться осторожно!»,
флакон опечатывают и выписывают сигнатуру
22.
Изготовление микстур спомощью бюреточной
системы
• Изготовление ЖЛФ растворением твердых
лекарственных веществ процесс достаточно
трудоемкий (в зависимости от числа
отвешиваемых ингредиентов), поэтому для
ускорения процесса растворения
рекомендуется использовать бюреточную
систему
23.
Бюреточная система представляет собойопределенную систему организации труда с
соблюдением:
• правил технологии изготовления;
• применения соответствующих
измерительных приборов (бюреточной
установки);
• специально изготовленных
концентрированных растворов.
24.
Концентрированные растворы (концентраты) – заранееизготовленные растворы ЛВ более высокой концентрации,
чем концентрация, в которой эти вещества выписываются
в рецептах.
Концентраты предназначены для быстрого и качественного
изготовления жидких лекарственных форм.
Концентрированные р-ры изготавливают:
• В массо-объемной концентрации
• В асептических условиях
• Концентрированные растворы ЛВ наркотических,
психотропных, снотворных и ядовитых веществ не
изготавливают.
• При изготовлении концентрированных растворов
особые требования
воде очищенной.
В.О. предъявляются
- свежеполученная, стерильная,
проверенная накотсутствие
ионов хлора,
кальция, сульфат ионов, восстанавливающих веществ, солей аммония, углерода
диоксида, рН 5,0-7,0.
Вода очищенная стерилизуется термическим методом (насыщенным паром)
при (120 + 2) ºС. Время стерилизации зависит от объема раствора:
V до 100 мл
- 8 мин
V > 100 ml < = 500 ml
- 12 мин
V > 500 ml < = 1000 ml - 15 мин.
Стерилизация объемов более 1000 мл запрещена.
25.
Приготовление концентрированных растворовдля бюреточной системы (Приказ 308)
Solutio Coffeini-natrii benzoatis 10% - 1500 ml
• C использованием мерной посуды:
Coffeini-natrii benzoas 150,0
Aqua purificata
ad 1500ml
• При отсутствии мерной посуды:
А) С учетом плотности приготовляемого
раствора 1,034 г/мл
М раствора 1500 мл х 1,034 г/мл = 1551,0 г
M воды 1551,0-150,0 = 1401 г
Coffeini-natrii benzoas 150,0
Aqua purificata
1401ml
Б) С учетом КУО кофеина-бензоата натрия
КУО = 0,65 мл/г
Coffeini-natrii benzoas 150,0
150 х 0,65 = 97,5 мл
Aqua purificata
1402,5ml
1500 - 97,5 = 1402,2 мл
Изменение объема, возникающее при растворении ЛВ при
изготовлении концентрированных р-ров, не укладывается в норму
допустимого отклонения, изменение объема следует учитывать.
26.
Технология изготовления1. Растворение. В подставку отмеривают рассчитанный объем
воды, растворяют ЛВ.
2. Проводят полный химический анализ.
Отклонение в концентрации растворов допускается в пределах:
- до 20% концентрации раствора (включительно) - не более; ± 2 %
- более 20% концентрации раствора - не более ± 1 %
С помощью “Рефрактометрической таблице” находят соответствие
между полученной концентрацией раствора и показателем
преломления (n).
3. Фильтрование
Фильтруют через промытый комбинированный фильтр (складчатый
бумажный фильтр с подложенным тампоном длинноволокнистой
ваты), стеклянные или полимерные мембранные фильтры
4. Упаковка с укупоркой
Используют флаконы из нейтрального стекла с притертой пробкой.
4. Оформление (маркировка)
Solutio Glucosi 50% - 500 ml
Этикетка с указанием наименования
Дата изготовления…
раствора, его концентрации, № серии, Серия ..... N анализа ...
датой изготовления, № анализа.
Приготовил..
27.
Приготовление концентрированных растворовдля бюреточной системы (Приказ 308)
Solutio Coffeini-natrii benzoatis 10% - 1500 ml
• C использованием мерной посуды:
Coffeini-natrii benzoas 150,0
Aqua purificata
ad 1500ml
• При отсутствии мерной посуды:
А) С учетом плотности приготовляемого
раствора 1,034 г/мл
М раствора 1500 мл х 1,034 г/мл = 1551,0 г
M воды 1551,0-150,0 = 1401 г
Coffeini-natrii benzoas 150,0
Aqua purificata
1401ml
Б) С учетом КУО кофеина-бензоата натрия
КУО = 0,65 мл/г
Coffeini-natrii benzoas 150,0
150 х 0,65 = 97,5 мл
Aqua purificata
1402,5ml
1500 - 97,5 = 1402,2 мл
Изменение объема, возникающее при растворении ЛВ при
изготовлении концентрированных р-ров, не укладывается в норму
допустимого отклонения, изменение объема следует учитывать.
28.
Требования к микстурам:Rp: Codeini phosphatis 0,2
быстрое
Natrii bromidi
фармакологическое
Acidi ascorbinici aa 2,0
действие,
Glucosi 10,0
ЛВ должны быть в
Tincturae Convallariae
растворенном виде или в
виде
Tincturae Valerianae ana 5 ml
тонкодиспергируемых
Aquae purificatae ad 200 ml
легко ресуспендируемых
Misce. Da. Signa: по 1 ст.л. 3
взвесей
раза в день
не обладать
раздражающим
действием на слизистые
ЛФ - раствор для внутреннего
оболочки ротовой
применения (микстура)
полости и желудка,
Пропись многокомпонентная,
ЛФ представляет собой р-р НМВ по возможности должны
обладать приятным
и ультрамикрогетерогенную
вкусом
систему с водно-спиртовой
дисперсионной средой
29.
Проверка совместимости ингредиентов –компоненты прописи совместимы
Проверка доз:
Общий объем препарата указан в рецепте, в этом случае
имеется указание «ad» (до определенного объема).
V общ = 200 мл
V 1дозы = 15 мл (1 ст.л.)
200 мл : 15 мл = 13,33
Микстура на 13 доз
Кодеина фосфат - сильнодействующее ЛВ
ВРД 0,1
РД 0,2 г : 13 = 0,015 г
ВСД 0,3
СД 0,015 х 3 = 0,046
Дозы не завышены, Вещество на ПКУ
Норма отпуска кодеина фосфата 0,2 г (приказ №4н)
НЕО не завышена
30.
Физико-химические свойства ЛВ:Acidum ascorbinicum – белый кристал. порошок, легко растворим
в воде, окисляется на воздухе и при действии света.
Codeini phosphas - сильнодействующее ЛВ. белый кристал.
порошок, на воздухе выветривается, легко растворим в воде,
мало растворим в спирте.
Natrii bromidum – белый кристал. порошок, гигроскопичен, на
свету разлагается. Растворим в 1,5 ч воды и в 10 ч спирта.
Водный раствор нейтральной или слабощелочной реакции.
Tinctura Valerianae – прозрачная жидкость красновато-бурого
цвета, ароматного запаха и сладковато-горького пряного
вкуса. Состава: корневищ с корнями валерианы
измельченных 200 г, спирта 70% до получения 1 л настойки.
Tinctura Сonvallariae – прозрачная жидкость зелено-бурого цвета,
своеобразного запаха и горького вкуса, содержит 70%
этанол.
Glucosum– белый мелкокристалл. порошок без запаха, сладкого
вкуса, растворим в 1,5 ч воды, трудно растворим в 95 %
спирте, на воздухе теряет кристаллизационную воду.
31.
Расчеты для изготовления растворовпутем растворения ЛВ
Оборотная сторона ППК
Лицевая сторона ППК
Масса твердых веществ:
заполняется сразу после
M кодеина фосфат = 0,2
изготовления ЛП
М NaBr = 2,0 КУО 0,26 г/мл
ППК №1
М к-ты аскорбиновой = 2,0 КУО 0,61
М глюкозы = 10,0
Дата ……
рецепт № 1
В рецепте указана глюкоза б/в, а в
Aqua purificata 180,7 ml
аптеке имеется глюкоза с
Codeini phosphas 0,2
влажностью 10 %
Acidum ascorbinicum 2,0
М глюкозы водной = 11,11
Natrii bromidum 2,0
X = a X 100 = 10 х 100 = 11,11
100 - b
100 – 10
Glucosum hydricum (10%)
КУО 0,69 г/мл
11,11
V настойки ландыша = 5 мл
Tinctura Convallariae 5 ml
V настойки валерианы = 5 мл
Tinctura Valerianae 5 ml
V воды очищенной = 180,65 мл
200 – (2х0,26 + 2х0,61 + 11,11х0,69 )- Vраствора = 200 ml
Подписи:
(5 +5) = 180,65 мл
32.
Расчет из концентрированных растворовОборотня сторона ППК
M кодеина фосфата 0,2
V настойки ландыша 5 мл
V настойки валерианы 5 мл
Объем растворовконцентратов:
Р-р натрия бромида 20% (1:5)
Vр-ра NaBr = 2,0х5=10мл
Р-р кислоты аскорбиновой 5%
(1:20)
V р-ра к-ты аскорбиновой =
2,0х20=40 мл
Раствор глюкозы 50% (1:2 )
Vр-ра глюкозы = 10,0х2=20мл
V воды очищенной
200-(40+10+20) – (5+5)=120 мл
Лицевая сторона ППК
заполняется сразу после
изготовления ЛП
ППК №2
Дата ………….рецепт № 1
Aqua purificata 120 ml
Codeini phosphas 0,2
Solutio acidi ascorbinici 1:20 –
40 ml
Solutio natrii bromidi 1:5 – 10ml
Solutio glucosi 1:2 – 20 ml
Tinctura Convallariae 5 ml
Tinctura Valerianae 5 ml
V раствора = 200 ml
Подписи:
33.
Фильтрование – процесс освобождения раствора отвзвешенных частиц
Недостатки фильтровальных материалов:
1. набухаемость,
2. недостаточная прочность,
3. сорбция веществ и ионов за счет диссоциации в воде
с приобретением «-» заряда
Вата
длинноволокнистая
Марля
хлопчатобумажная
Бумага
фильтровальная
Фильтры стеклянные
Фильтры мембранные
Требования, предъявляемые к
фильтровальным материалам:
прочность
наличие структуры
задерживающей частицы при
высокой проницаемости
не должны выделять в раствор
волокна или частицы
химическая индифферентность
биологическая
индифферентность
34.
Упаковка и укупорка растворовФлаконы стеклянные 25, 30, 50, 100, 150, 200
мл, прозрачные и светозащитные
(оранжевого стекла) с навинчивающимися
крышками и уплотнительными элементами
из полиэтилена или картона
Пробки корковые с бумажным уплотнением,
резиновые, полиэтиленовые по размеру
горлышка флакона
35.
Оформление к отпускуОформление к отпуску:
Этикетка «МИКСТУРА» с указанием
№ аптеки, № рецепта, ФИО больного, способа
применения, даты изготовления, срока годности
и цены.
Дополнительно:
этикетка «Беречь от детей» и «Сохранять в
защищенном от света месте», отдельный
рецептурный номер
Сигнатура, т.к. кодеина фосфат приравнен к
наркотическим и находится в аптеке на ПКУ
36.
Контроль при отпуске:1. Анализ документации: № препарата, рецепта и ППК
соответствуют; дозы вещества списка Б не завышены;
расчеты сделаны верно, ППК и сигнатура выписаны верно;
2. Оформление: наклеена соответствующая этикетка, и
предупредительные надписи, препарат имеет красивый
товарный вид;
3. Упаковка: V флакона соответствует объему ЛФ, цвет
стекла соответствует физико-химическим свойствам
входящих состав микстуры ингредиентов, при
переворачивании флакона жидкость не подтекает под
пробку;
4. Органолептический контроль: микстура для внутреннего
применения прозрачна с легкой опалесценцией,
желтоватого цвета, видимые механические включения
отсутствуют, со специфическим запахом, сладкого вкуса,
объем 200 мл в соответствии с рецептом;
5. Отклонения в объеме соответствуют нормам допустимых
отклонений для жидких лекарственных форм:
200 мл 2 %; 196 – 204 мл


































 Медицина
Медицина








