Похожие презентации:
Фенолы - производные ароматических углеводородов, содержащие одну или несколько гидроксильных групп у атомов углерода
1.
Фенолы2.
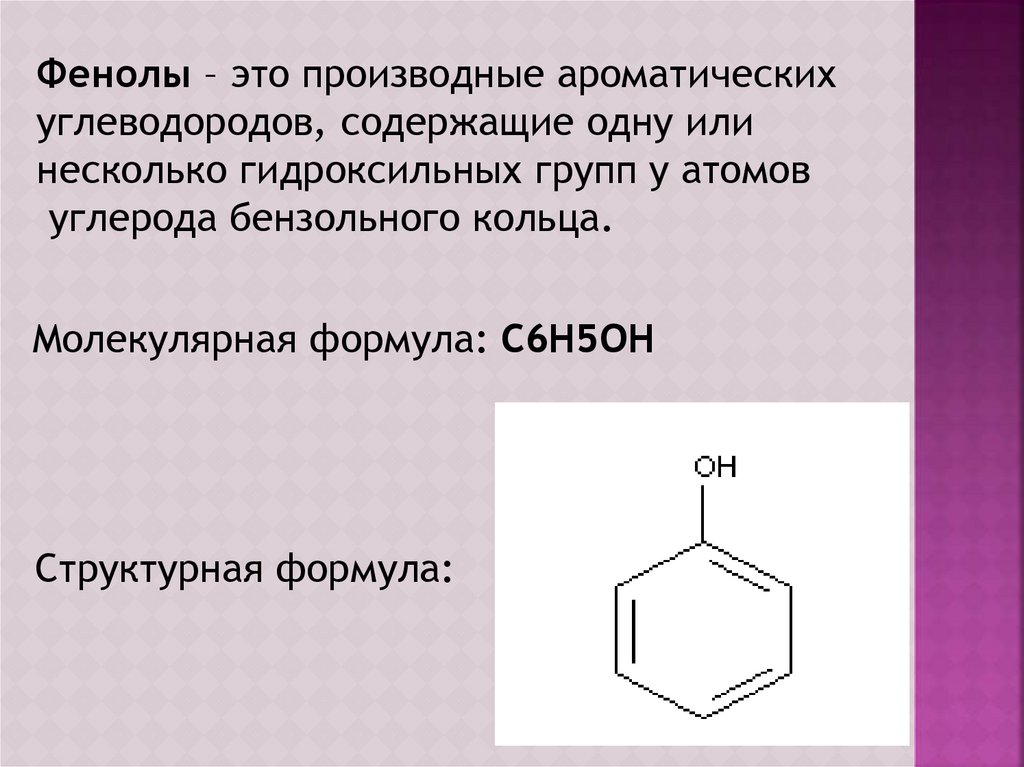
Фенолы – это производные ароматическихуглеводородов, содержащие одну или
несколько гидроксильных групп у атомов
углерода бензольного кольца.
Молекулярная формула: С6Н5ОН
Структурная формула:
3.
4.
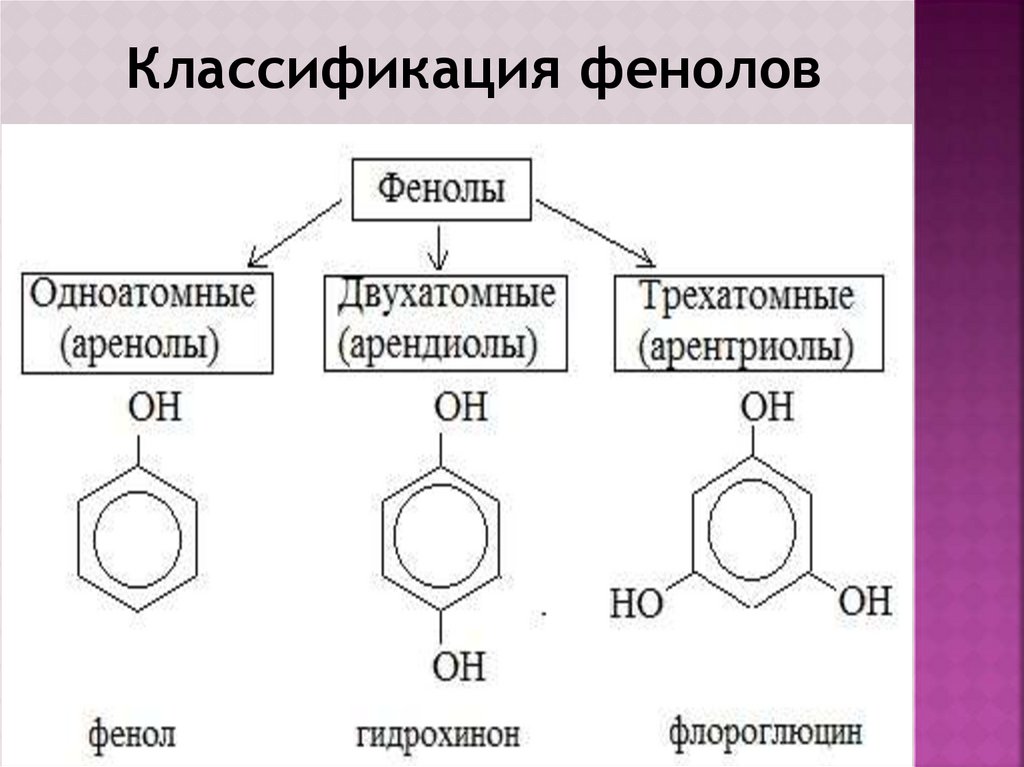
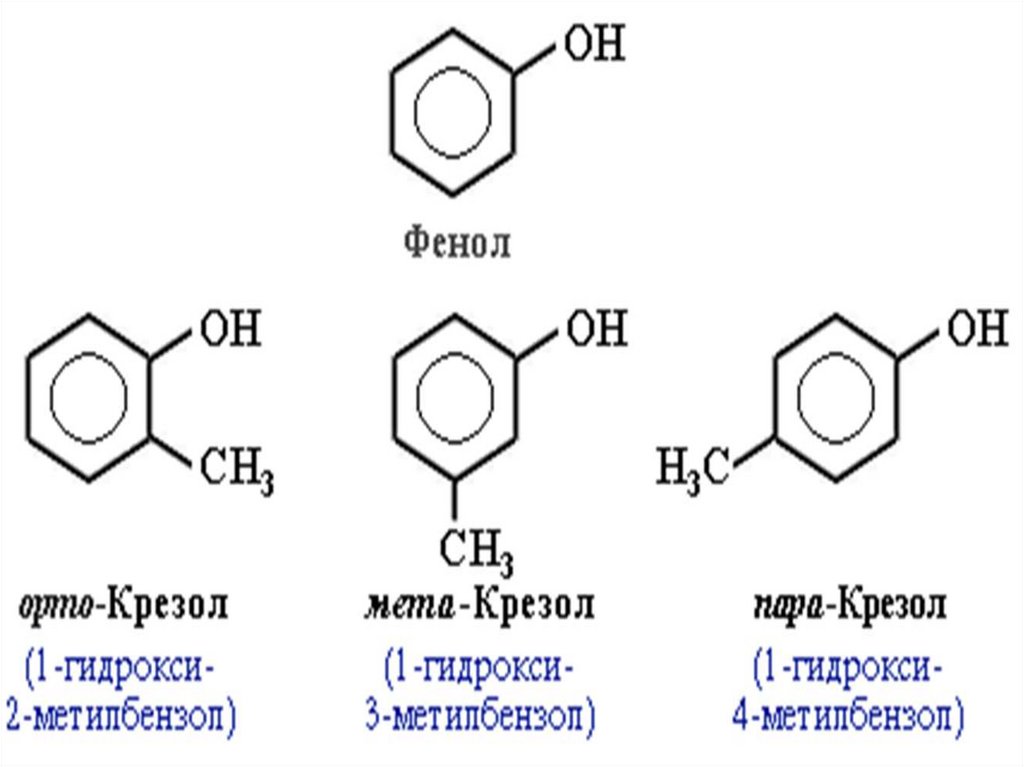
Классификация фенолов5.
6.
Типы изомерии:• Изомерия положения заместителей
в бензольном кольце;
• Изомерия боковой цепи.
7.
8.
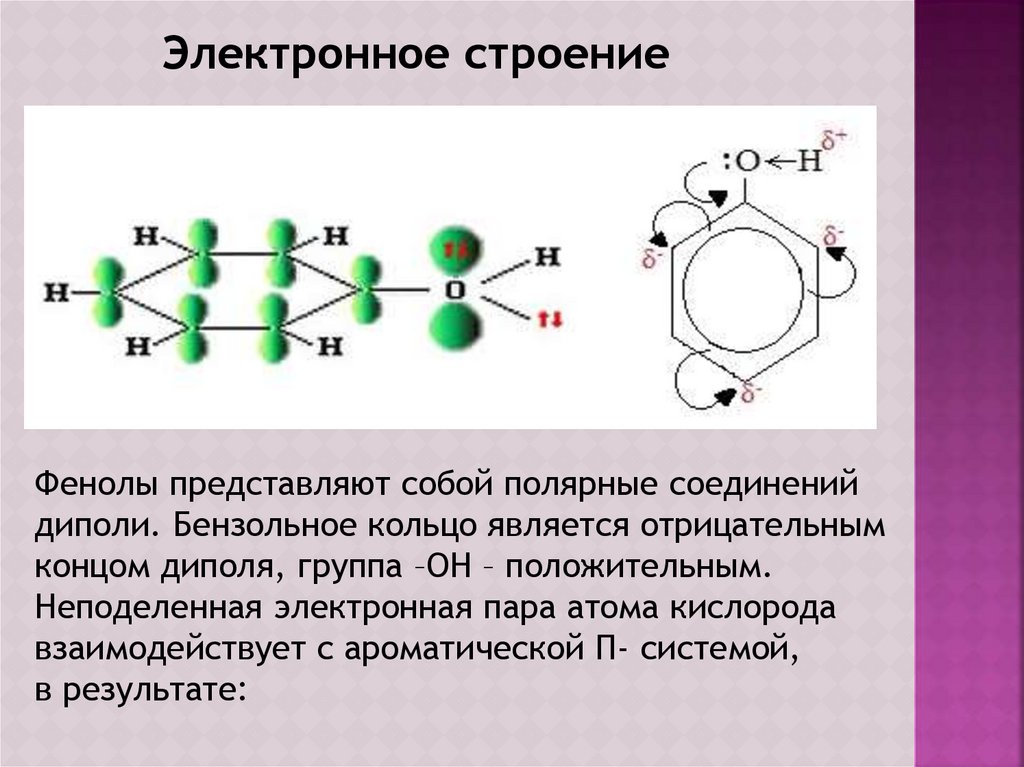
Электронное строениеФенолы представляют собой полярные соединений
диполи. Бензольное кольцо является отрицательным
концом диполя, группа –ОН – положительным.
Неподеленная электронная пара атома кислорода
взаимодействует с ароматической П- системой,
в результате:
9.
1. Увеличивается электронная плотность наароматической системе, происходит ее
перераспределение , и на атомах
2,4,6 появляется избыточный отрицательный
заряд;
2. Электронная пара связи О-Н смещается к
атому кислорода и связь становится менее
Прочная по сравнению со спиртами;
3. Увеличивается прочность связи атома
кислорода с атомом углерода, входящим в
ароматическое кольцо, и группа – ОН не способна
к реакциям замещения.
10.
Физические свойстваФенол С6Н5ОН (карболовая кислота) :
• Бесцветное кристаллическое вещество;
• На воздухе окисляется и становится розовым;
• При обычной температуре ограниченно
растворим в воде;
• Выше 66 градусов смешивается с водой в
любых соотношениях.
Фенол – токсичное вещество, вызывает
ожоги кожи!!!
11.
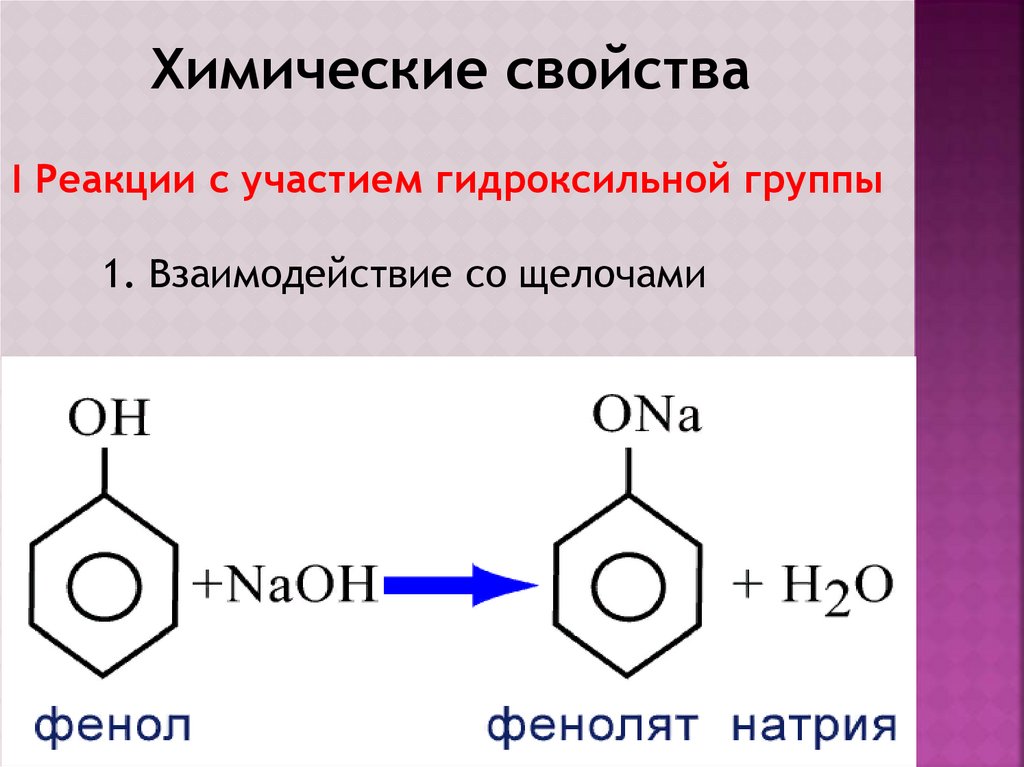
Химические свойстваI Реакции с участием гидроксильной группы
1. Взаимодействие со щелочами
12.
2. Взаимодействие с активными металламиФенолят натрия
13.
II Реакции с участием бензольного кольца( реакции замещения)
3. Галогенирование (бромирование)
2,4,6-трибромфенол – нерастворимое в воде вещество белого цвета,
Реакция используется как одна из качественных реакций для
определения фенола.
14.
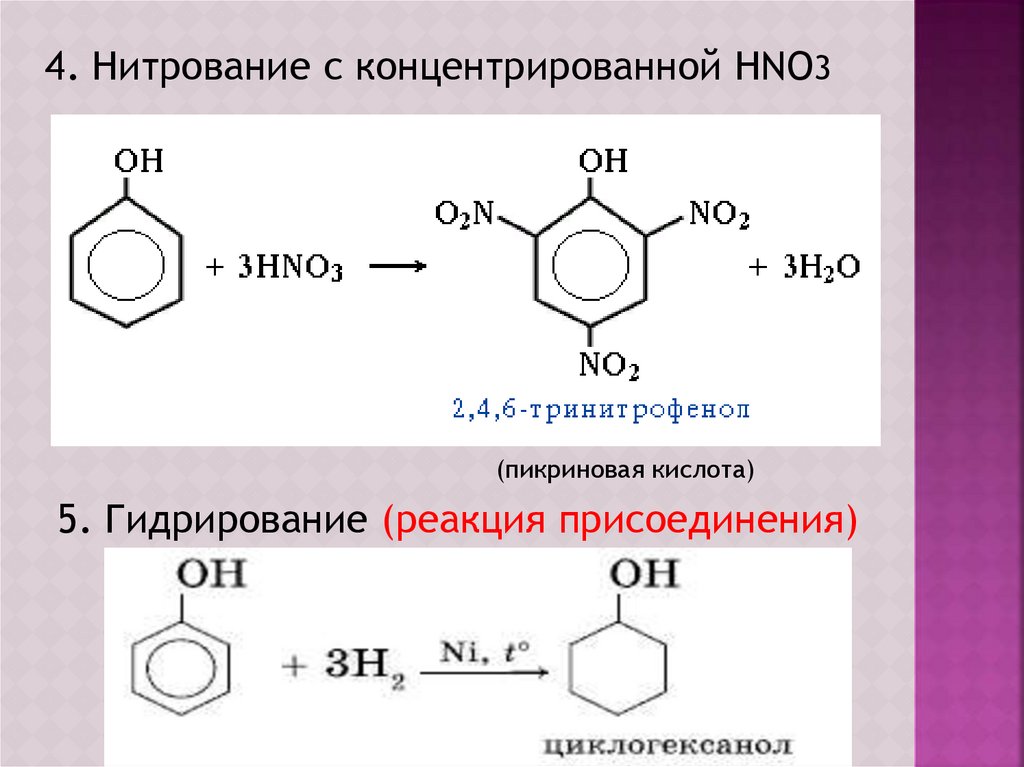
4. Нитрование с концентрированной HNO3(пикриновая кислота)
5. Гидрирование (реакция присоединения)
15.
III Качественные реакции на фенолыВ водных растворах одноатомные фенолы
взаимодействуют с хлоридом железа (III)
FeCl3 с образованием комплексных фенолятов,
которые имеют фиолетовую окраску;
окраска исчезает после прибавления
сильной кислоты.
16.
17.
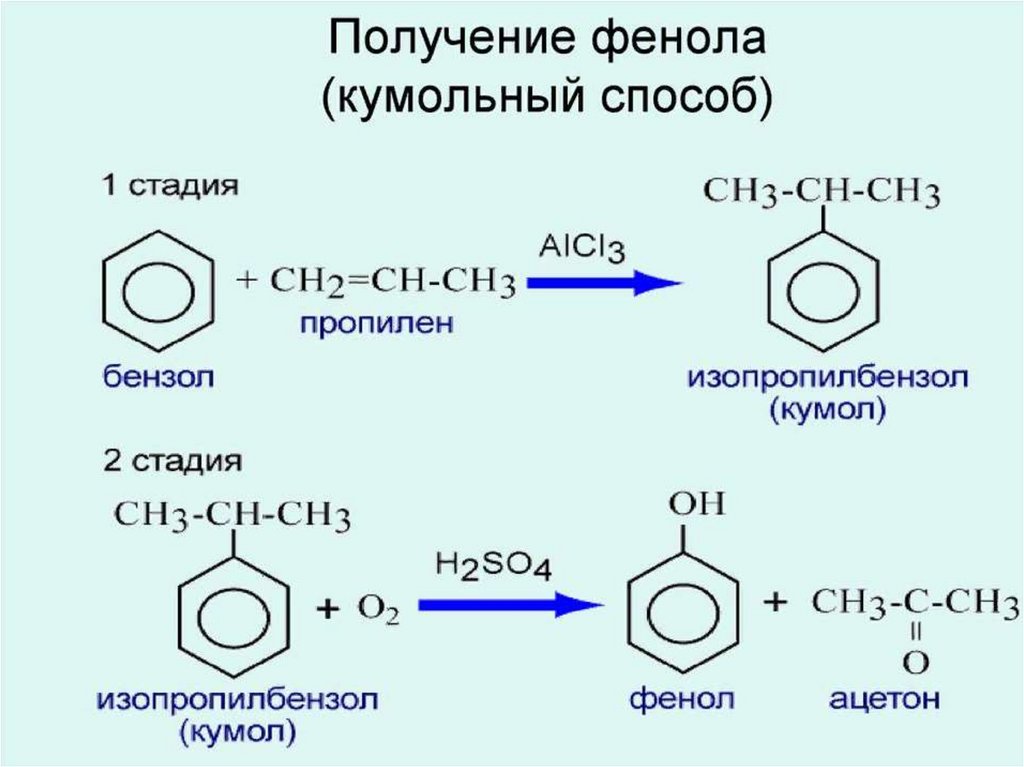
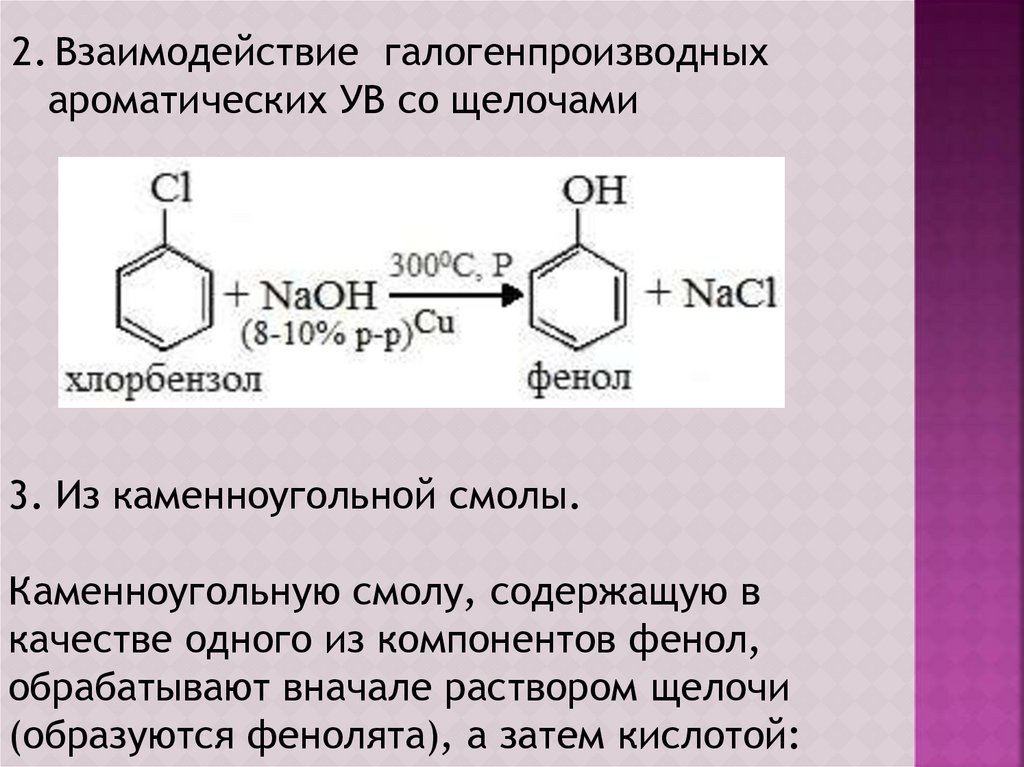
2. Взаимодействие галогенпроизводныхароматических УВ со щелочами
3. Из каменноугольной смолы.
Каменноугольную смолу, содержащую в
качестве одного из компонентов фенол,
обрабатывают вначале раствором щелочи
(образуются фенолята), а затем кислотой:
18.
C6H5OH + NaOH = C6H5ONa + H2O
Фенолят натрия
(промежуточный продукт)
• C6H5ONa + H2SO4 = C6H5OH + NaHSO3
фенол












 Химия
Химия