Похожие презентации:
Степень окисления
1.
Степень окисления2.
Степень окисления3.
Вспомним!Ионы – электрически заряженная частица,
образующаяся в результате потери или
присоединения электронов атомом или
группой атомов.
•Катион – положительно
заряженные ион (чаще
металл).
•Анион – отрицательно
заряженный ион.
4.
Правила определение степениокисления
1. Степень окисления водорода в соединении
с неметаллами «+1», а с металлами «-1».
H2+O-2
Na+H2. Степень окисления кислорода равна «-2»
(исключение – пероксиды H2+O2- ).
3. Степень окисления металлов главных
подгрупп равна “+ номер группы”.
Ca+2O-2
Na2+O-2
4. Степень окисления простых веществ
равна нулю.
Na0
H20
5.
5. Сумма всех степеней окисления равнанулю.
+ +6 -2
+ +4 -2
H2SO4
H2SO3
+2+X–8=0
X=6
+2+X–6=0
X=4
+2
+6 - 8
+2
+4 - 6
6.
++6 -2
К2CrO4
+2
+6
-8
+ 1*2 + X – 8 = 0
X=6
+2 +6
-2
СаCr2O7
+2
+12
- 14
+ 2 + (X:2) – 6 = 0
X=6
7.
ЗаданиеОпредели степень окисления всех
элементов в соединениях
Выбери свой вариант по первой букве твоей фамилии
А-Е
1. NO
2. NO2
3. HNO3
4. HNO2
5. Fe(NO3)3
6. Fe(NO2)2
7. NH3
8. NH4NO3
9. Na3N
10. N2O5
Ж-Н
1. SO2
2. SO3
3. H2SO3
4. H2SO4
5. FeSO4
6. Fe2(SO4)3
7. H2S
8. (NH4)2SO3
9. Al2S3
10. Cr2O3
O-Я
1. MnO2
2. Mn2O7
3. HMnO4
4. H2MnO4
5. NH4MnO4
6. MnO2
7. (NH4)2SO3
8. Al(MnO4)3
9. HNO3
10. Mn2O3
8.
ПодсказкаВне зависимости от класса соединения
(кислота или соль) степени окисления атомов
в кислотном остатке не изменяются! А
степень окисления катиона (тот, что на
первом месте) можно легко определить по
суммарному заряду кислотного остатка (см.
таблицу растворимости).
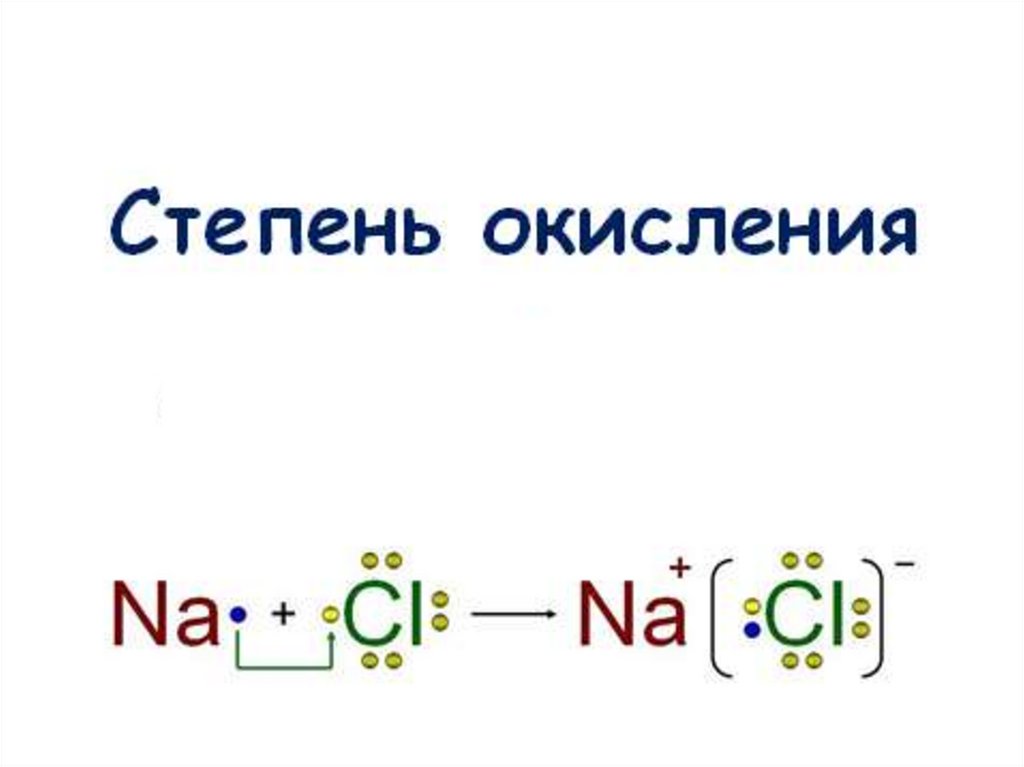




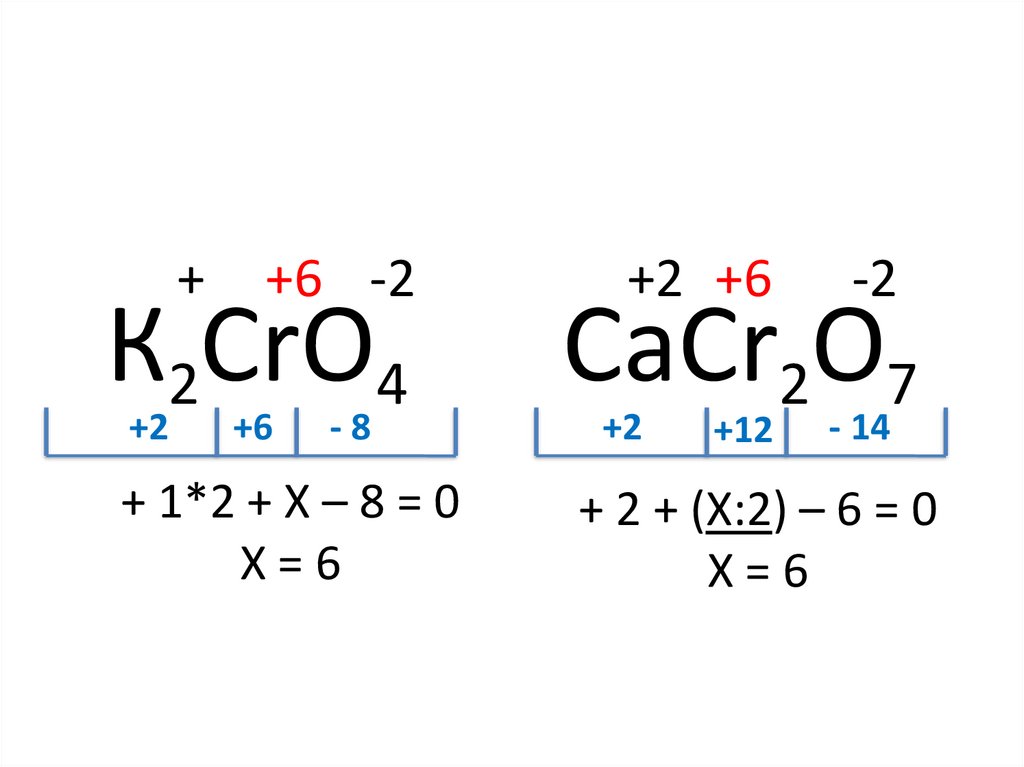


 Химия
Химия








