Похожие презентации:
Многоатомные спирты. Этиленгликоль
1.
1. За год до смерти Нобель сам, без помощи адвокатов,
составил завещание. Он считал, что унаследованное богатство
плодит бездельников, поэтому друзьям и
родственникам завещал немного. «Капитал мои
душеприказчики должны перевести в ценные бумаги, создав
фонд, проценты с которого будут выдаваться в виде премии
тем, кто в течение предшествующего года принёс большую
пользу человечеству..»
- За счёт какого изобретения у Альфреда Нобеля образовался
приличный капитал?
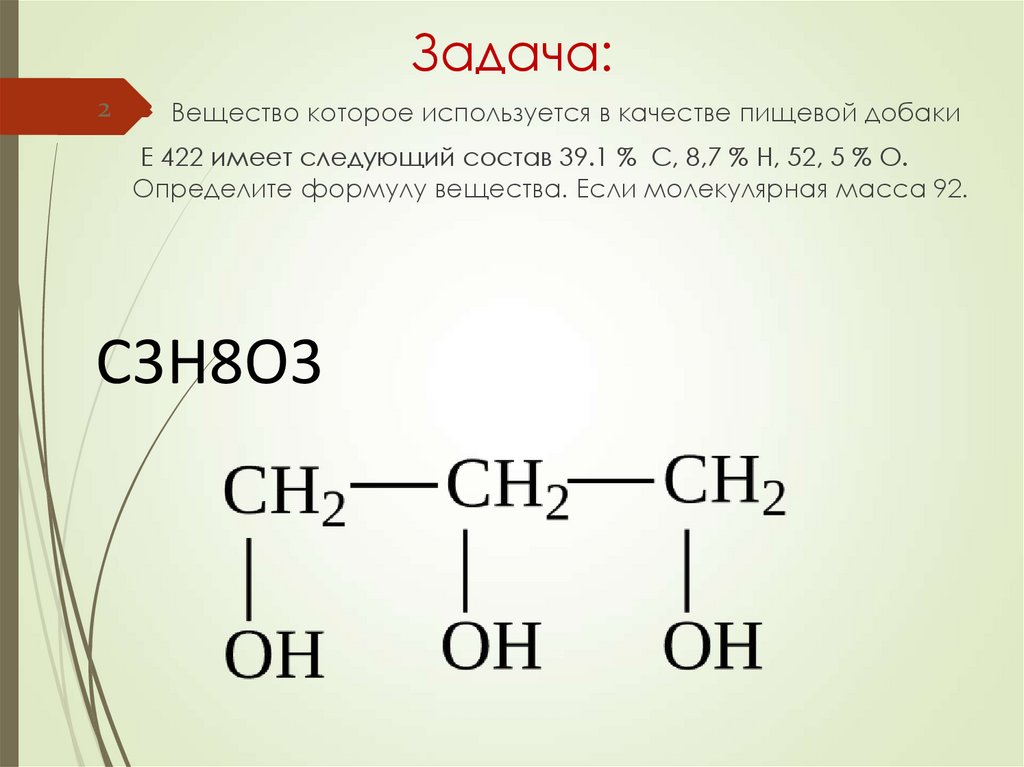
2. Задача:
2 Вещество которое используется в качестве пищевой добакиЕ 422 имеет следующий состав 39.1 % С, 8,7 % Н, 52, 5 % О.
Определите формулу вещества. Если молекулярная масса 92.
C3H8O3
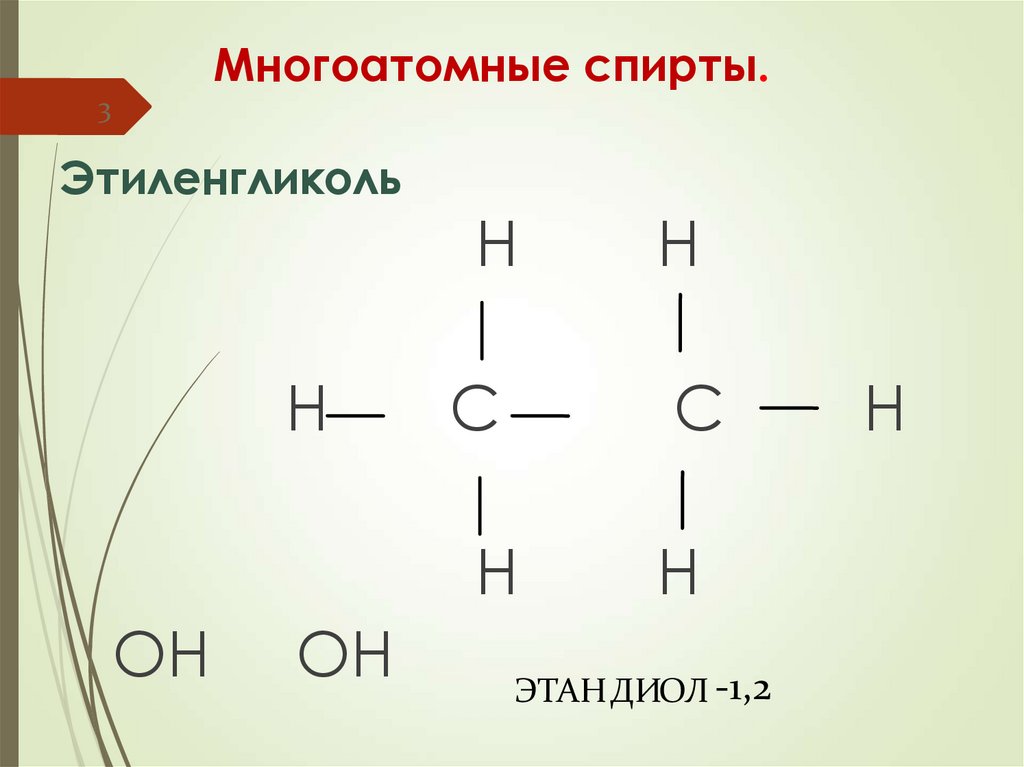
3. Многоатомные спирты. Этиленгликоль
Многоатомные спирты.3
Этиленгликоль
H
H
C
C
H
OH
OH
H
H
ЭТАН ДИОЛ -1,2
H
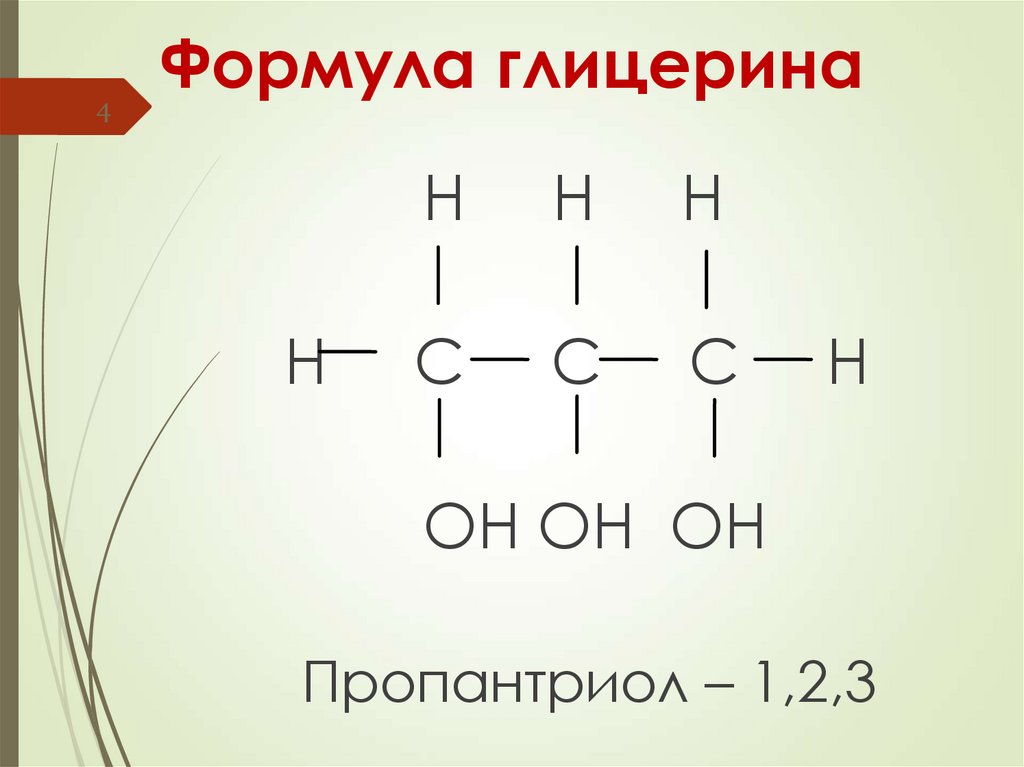
4. Формула глицерина
4Формула глицерина
H
H
H
H
C
C
C
H
OH OH OH
Пропантриол – 1,2,3
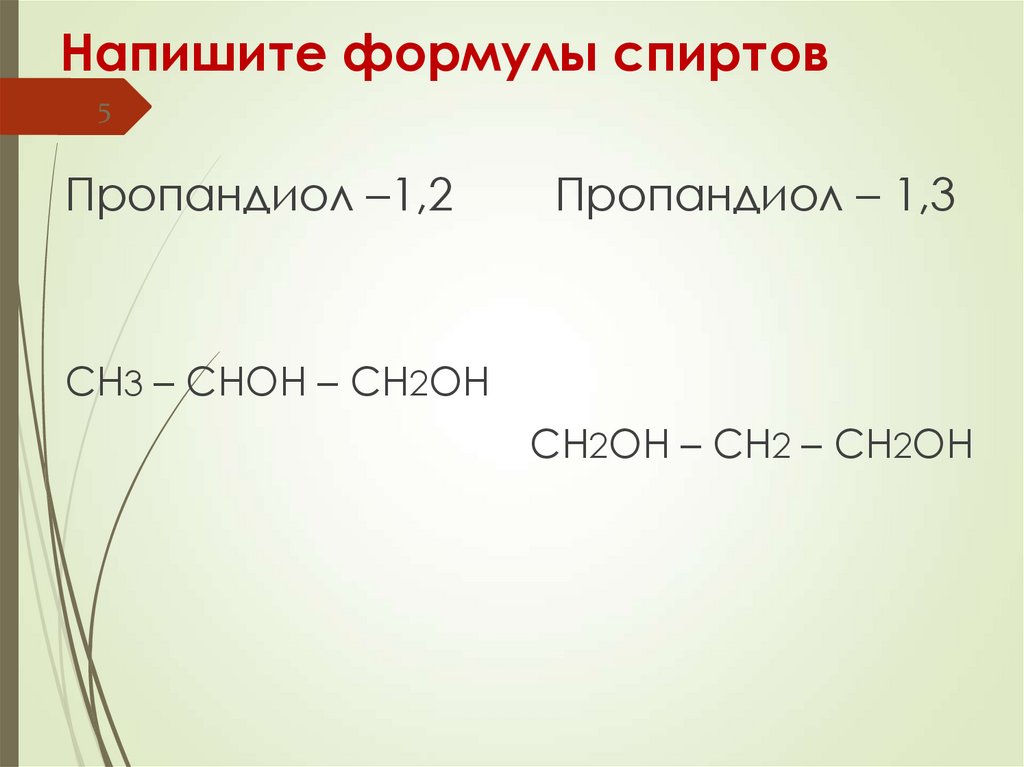
5. Напишите формулы спиртов
5Пропандиол –1,2
Пропандиол – 1,3
CH3 – CHOH – CH2OH
CH2OH – CH2 – CH2OH
6. Лабораторный опыт – изучение физических свойств глицерина
6Лабораторный опыт – изучение
физических свойств глицерина
Что делаю
Что наблюдаю
Выводы.
уравнения реакция
1. Растворимость
глицерина
2. Качественная
реакция
К одному мл воды в пробирке прилейте равный объем
глицерина и взболтайте смесь.
Затем добавьте еще столько же глицерина.
Что можно сказать о растворимости его в воде?
Опишите свойства, которые вы наблюдаете.
Глицерин – бесцветная, сиропообразная жидкость
сладковатого вкуса, хорошо растворимая в воде.
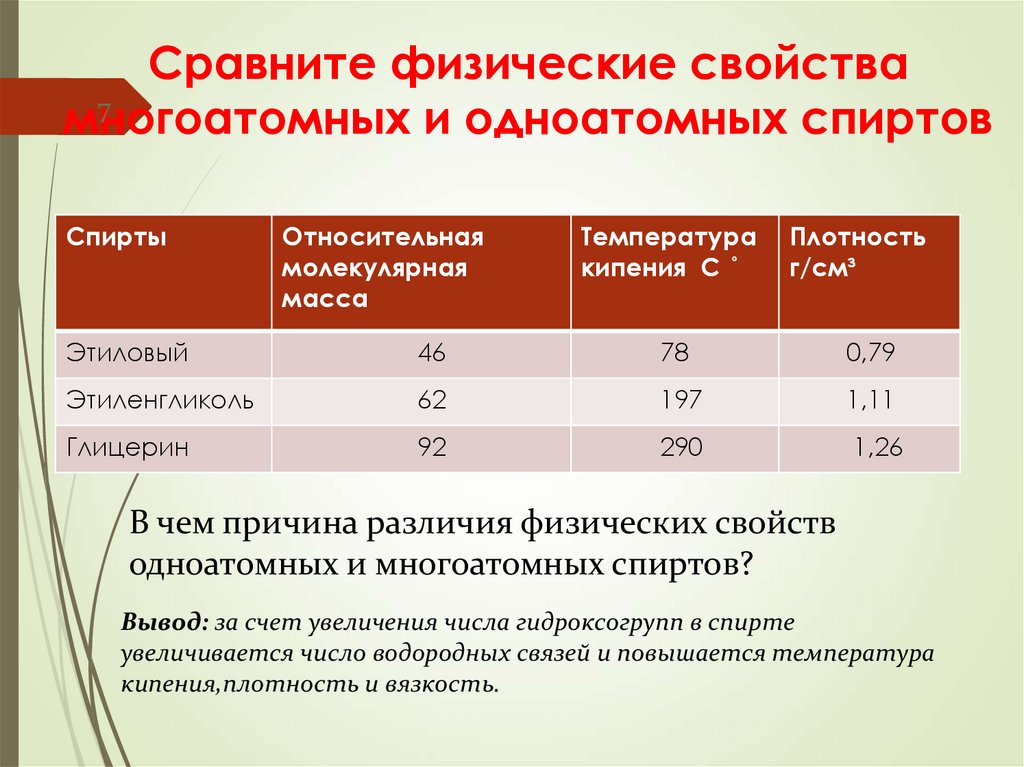
7. Сравните физические свойства многоатомных и одноатомных спиртов
Сравните физические свойства7
многоатомных
и одноатомных спиртов
Спирты
Относительная
молекулярная
масса
Температура
кипения С ̊
Плотность
г/см³
Этиловый
46
78
0,79
Этиленгликоль
62
197
1,11
Глицерин
92
290
1,26
В чем причина различия физических свойств
одноатомных и многоатомных спиртов?
Вывод: за счет увеличения числа гидроксогрупп в спирте
увеличивается число водородных связей и повышается температура
кипения,плотность и вязкость.
8. Химические свойства.
8Какие химические свойства характерны для одноатомных
спиртов?
Реакции горения, замещения гидроксильного водорода на
щелочной металл, реакция обмена гидроксогруппы на галоген,
дегидратация.
Будут ли эти свойства характерны
для многоатомных спиртов?
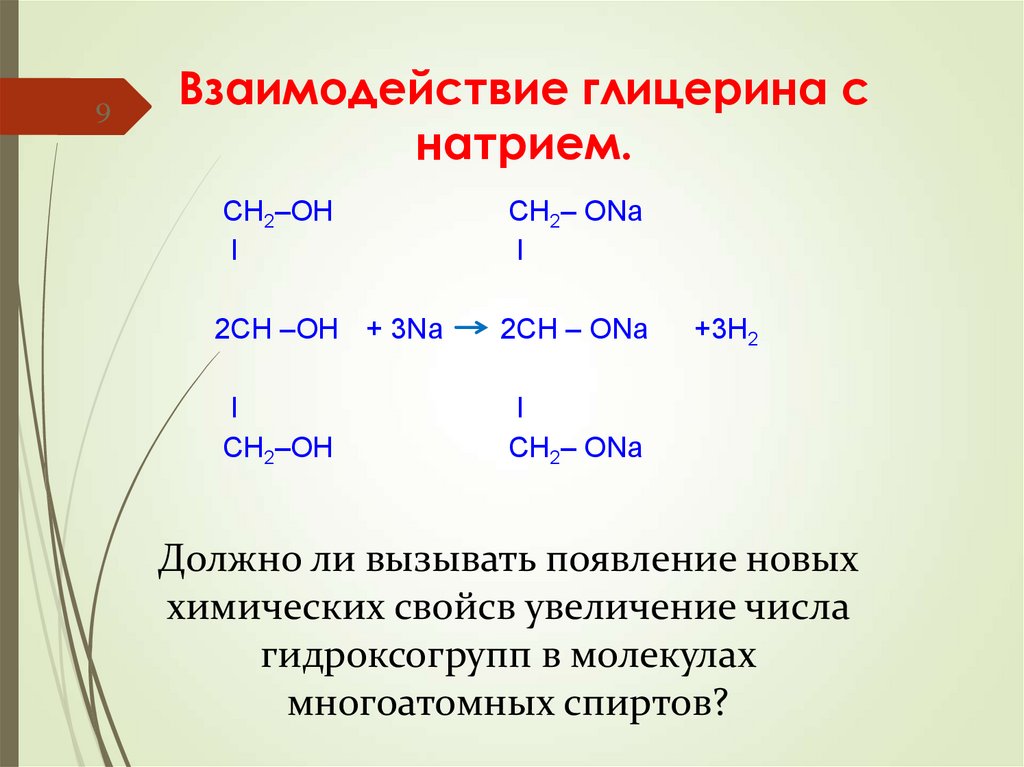
9. Взаимодействие глицерина с натрием.
9Взаимодействие глицерина с
натрием.
CH2–OH
I
CH2– ONa
I
2СH –OH + 3Na
2CH – ONa
I
CH2–OH
I
CH2– ONa
+3H2
Должно ли вызывать появление новых
химических свойсв увеличение числа
гидроксогрупп в молекулах
многоатомных спиртов?
10. Лабораторный опыт
10Лабораторный опыт
К 2 мл раствора щёлочи прибавьте несколько капель раствора
сульфата меди (II)
К образовавшемуся осадку гидроксида меди (II) прилейте
глицерин, смесь встряхните.
Что наблюдаете?
Запишите уравнение первой реакции
CuSO₄ + 2NaOH = Cu(OH)₂ + Na₂SO₄
11. Взаимодействие глицерина с гидроксидом меди (II)
11Взаимодействие глицерина с
гидроксидом меди (II)
Н
Увеличение числа
гидроксильных групп в
молекуле приводит к усилению
кислотных свойств
многоатомных спиртов по
сравнению с одноатомными.
12. Получение многоатомных спиртов
1. Подобно одноатомным спиртам, многоатомные12
спирты могут быть получены из соответствующих
углеводородов через их галогенопроизводные
(щелочной гидролиз):
СН2СI – СН2СI + 2Н2О
кон
СН2ОН – СН2ОН + 2НСI
этиленгликоль
2. При пропускании этилена через раствор
перманганата калия:
СН2 = СН2 + [ О ] + Н2О ––> СН2ОН – СН2ОН
Этиленгликоль
3. Глицерин получают :
- гидролизом жиров
- из пропилена
13. Получение нитроглицерина
13Глицерин легко нитруется, давая тринитроглицерин – сильное
взрывчатое вещество (основа динамита):
CH2–O--H
I
CH –O--H
CH2–O–NO2
HO--NO2
+
HO--NO2
I
H2SO4
––– CH–O–NO2
I
CH2–O--H
+ 3H2O
I
HO--NO2
CH2–O–NO2
При его взрыве выделяется большое количество газов и тепла
CH2–O–NO2
I
4CH–O–NO2
I
CH2–O–NO2
12CO2 + 6N2 + 10H2O + O2 + 5550 кДж
1% раствор нитроглицерина применяется для лечения стенокардии в качестве
сосудорасширяющего средства
14. Применение этиленгликоля
1415.
1516.
1617. Домашнее задание
17Домашнее задание
Выполнить тест.










 Химия
Химия








