Похожие презентации:
Фосфор и его соединения. Открытие фосфора
1.
и его соединения2. Открытие фосфора
Хеннинг Бранд(гамбургский алхимик) -
1669 год
«Фосфор» - от греческого
«светоносный»
3.
Фосфор как химический элементпериод
3
группа
VА
валентных электронов
5
степени окисления
-3, +3, +5
высший оксид
Р2О5
водородное соединение
РН3
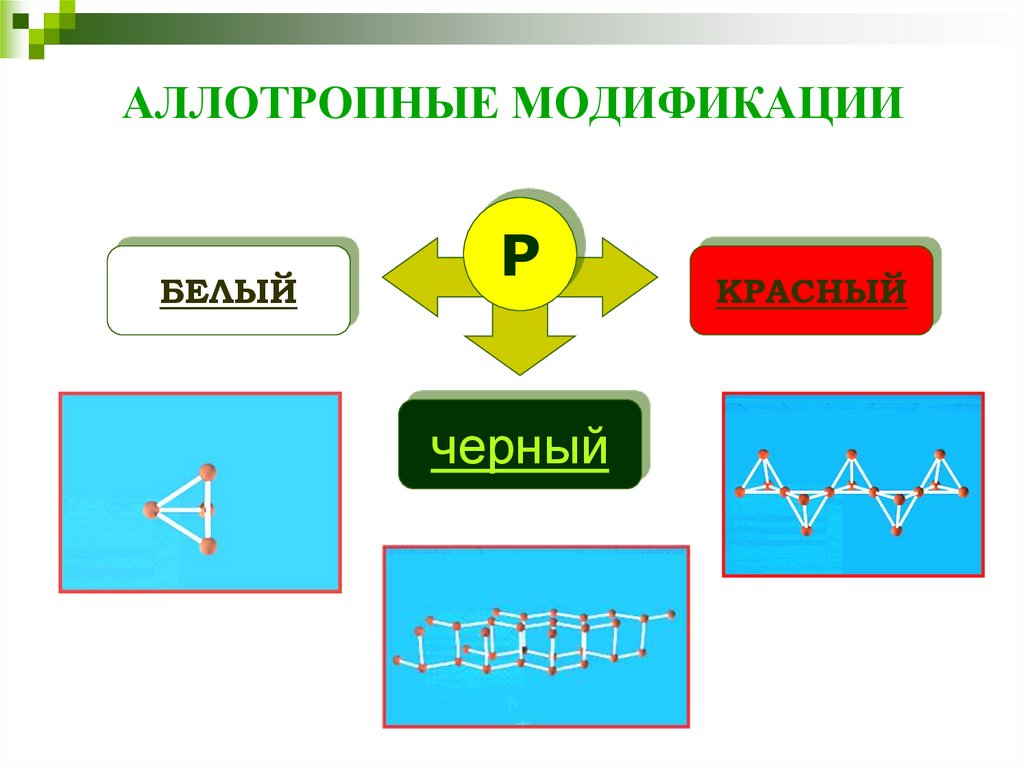
4. АЛЛОТРОПНЫЕ МОДИФИКАЦИИ
БЕЛЫЙР
черный
КРАСНЫЙ
5. БЕЛЫЙ ФОСФОР
Это мягкое, бесцветное воскообразное вещество.Хорошо растворяется в сероуглероде и ряде других
органических растворителей. Ядовит,
воспламеняется на воздухе (при температуре от 35
градусов), светится в темноте. Хранят его под
слоем воды.
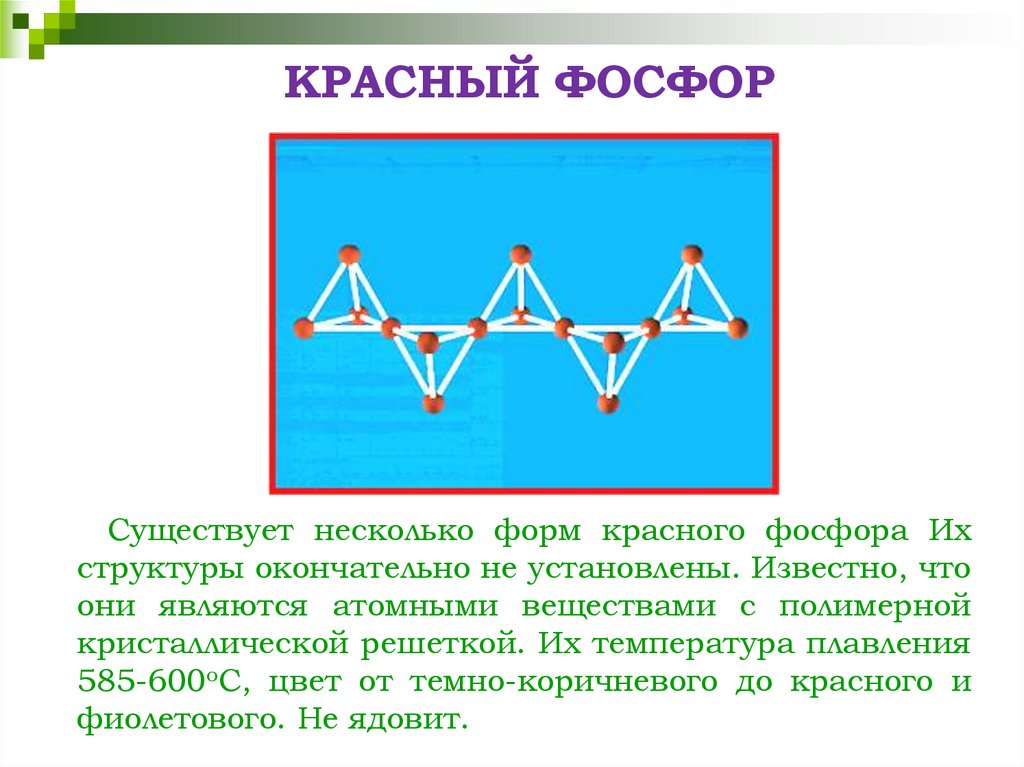
6. КРАСНЫЙ ФОСФОР
Существует несколько форм красного фосфора Ихструктуры окончательно не установлены. Известно, что
они являются атомными веществами с полимерной
кристаллической решеткой. Их температура плавления
585-600оС, цвет от темно-коричневого до красного и
фиолетового. Не ядовит.
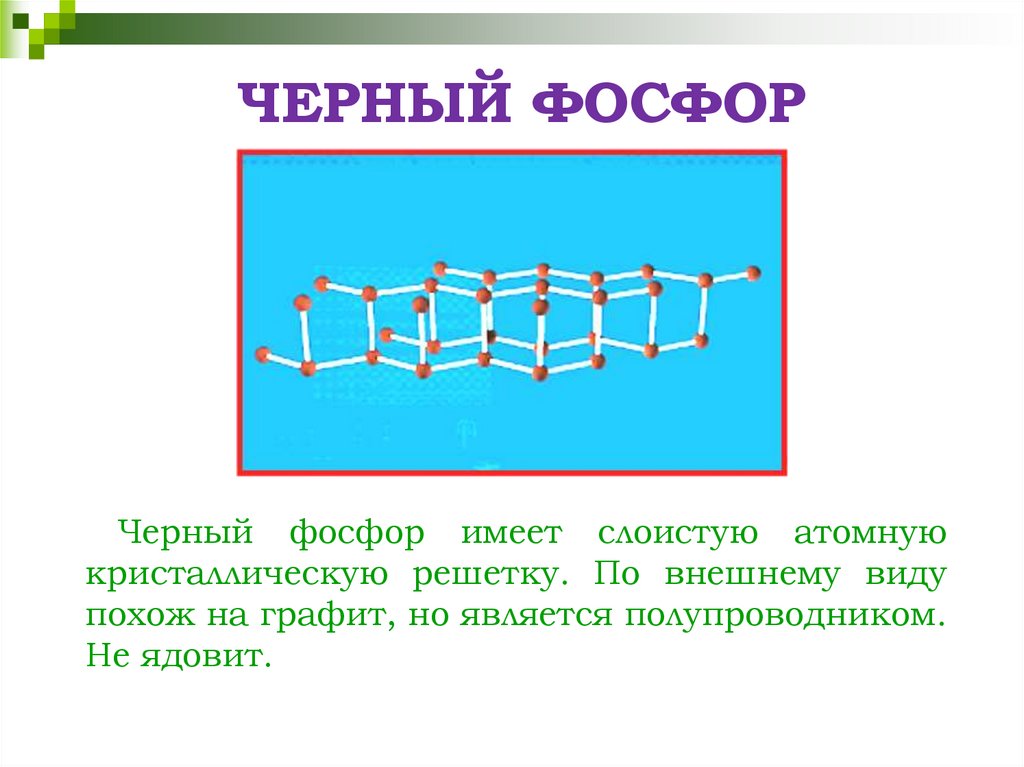
7. ЧЕРНЫЙ ФОСФОР
Черный фосфор имеет слоистую атомнуюкристаллическую решетку. По внешнему виду
похож на графит, но является полупроводником.
Не ядовит.
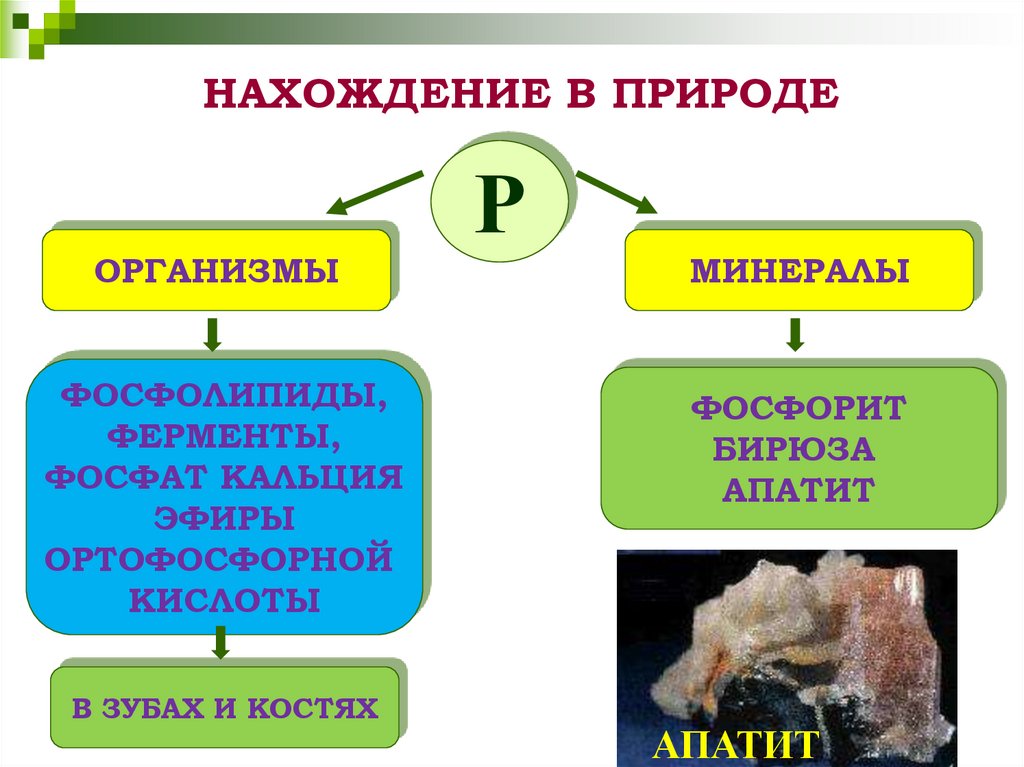
8. НАХОЖДЕНИЕ В ПРИРОДЕ
ОРГАНИЗМЫФОСФОЛИПИДЫ,
ФЕРМЕНТЫ,
ФОСФАТ КАЛЬЦИЯ
ЭФИРЫ
ОРТОФОСФОРНОЙ
КИСЛОТЫ
В ЗУБАХ И КОСТЯХ
Р
МИНЕРАЛЫ
ФОСФОРИТ
БИРЮЗА
АПАТИТ
АПАТИТ
9.
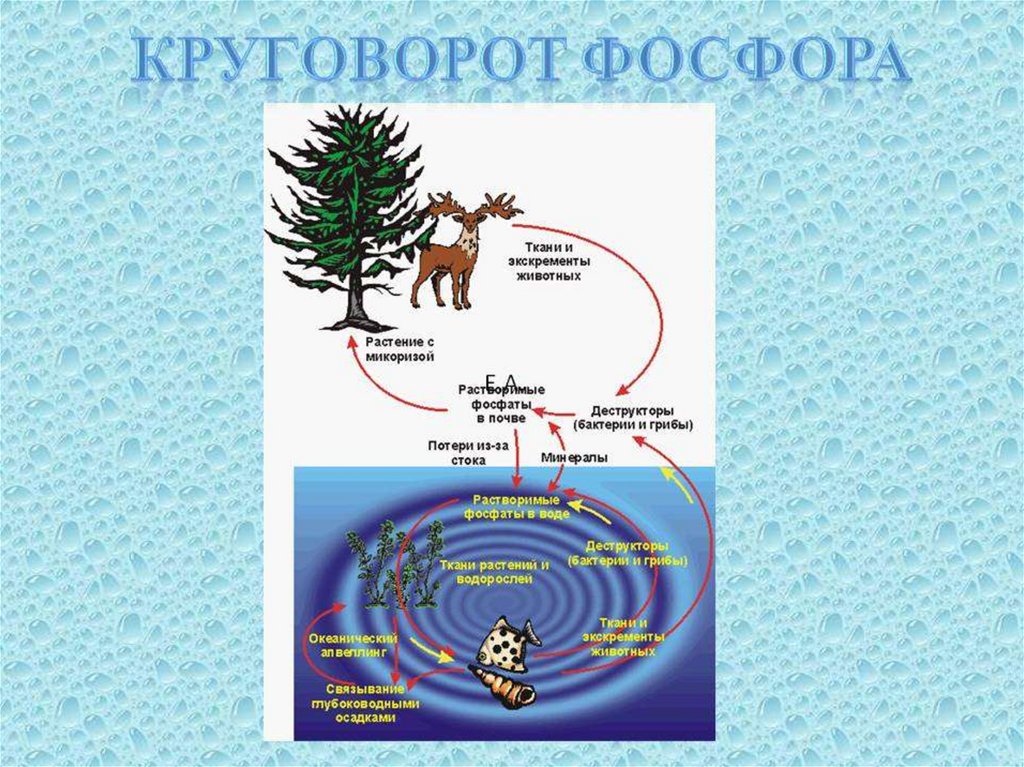
10. Антропогенное воздействие на круговорот фосфора состоит в следующем:
Добыча больших количеств фосфатных руд для минеральныхудобрений и моющих средств, приводит к уменьшению
количества фосфора в биотическом кругообороте;
Стоки с полей, ферм и коммунальные отходы приводят к
увеличению количества фосфат-ионов в водоемах, к резкому
росту водных растений и нарушению равновесия в водных
экосистемах.
11. Домашнее задание
§32 до стр.227 (до соединений);- Сделать характеристику красного
фосфора как простого вещества по
плану:
1) Молекулярная формула
2) Кристаллическая решетка
3) Физические свойства (агр состояние, цвет,
запах, растворимость и т.д.)
4) Химические свойства (как окислитель и как
восстановитель, ОВР)
5) Получение
6) Применение






 Химия
Химия








