Похожие презентации:
Фосфор и его соединения
1.
2. Открытие фосфора
Гамбургский алхимикХеннинг Бранд
1669 год
«Фосфор» от греческого
«светоносный»
3.
Фосфор как химический элементпериод
группа
валентных электронов
степени окисления
высший оксид
водородное соединение
4.
Фосфор как химический элементпериод
III
группа
VА
валентных электронов
степени окисления
5
-3, +3, +5
высший оксид
водородное соединение
Р2О5
РН3
5. АЛЛОТРОПНЫЕ МОДИФИКАЦИИ
Сравните физические свойстваАЛЛОТРОПНЫХ МОДИФИКАЦИЙ ФОСФОРА
БЕЛЫЙ
Р
ЧЕРНЫЙ
КРАСНЫЙ
6. БЕЛЫЙ ФОСФОР
Молекулы P4 имеют форму тетраэдра. Этолегкоплавкое t(пл)=44,1оС, t(кип)=275оС, мягкое,
бесцветное
воскообразное
вещество.
Хорошо
растворяется в сероуглероде и ряде других
органических
растворителей.
Ядовит,
воспламеняется на воздухе, светится в темноте.
Хранят его под слоем воды.
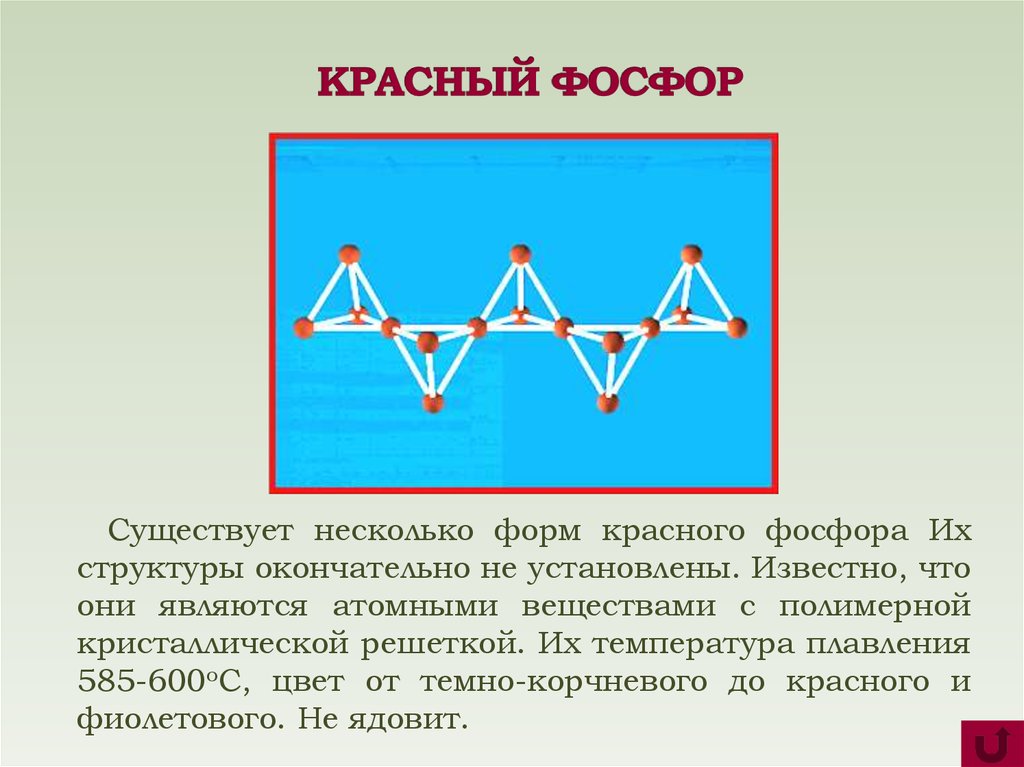
7. КРАСНЫЙ ФОСФОР
Существует несколько форм красного фосфора Ихструктуры окончательно не установлены. Известно, что
они являются атомными веществами с полимерной
кристаллической решеткой. Их температура плавления
585-600оС, цвет от темно-корчневого до красного и
фиолетового. Не ядовит.
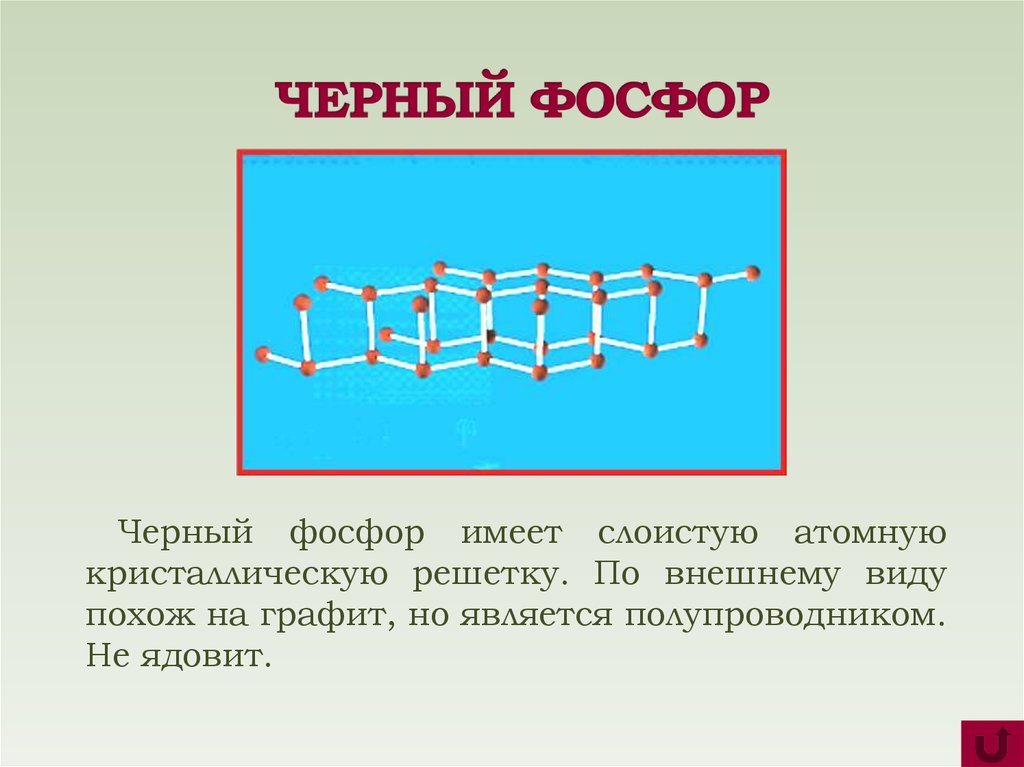
8. ЧЕРНЫЙ ФОСФОР
Черный фосфор имеет слоистую атомнуюкристаллическую решетку. По внешнему виду
похож на графит, но является полупроводником.
Не ядовит.
9. ХИМИЧЕСКИЕ СВОЙСТВА
С металлами:Ca + P =
C неметаллами:
P + O2 =
P+S=
10.
с бертолетовой солью приударе взрывается,
воспламеняется:
KClO3 + P = P2O5 + KCl
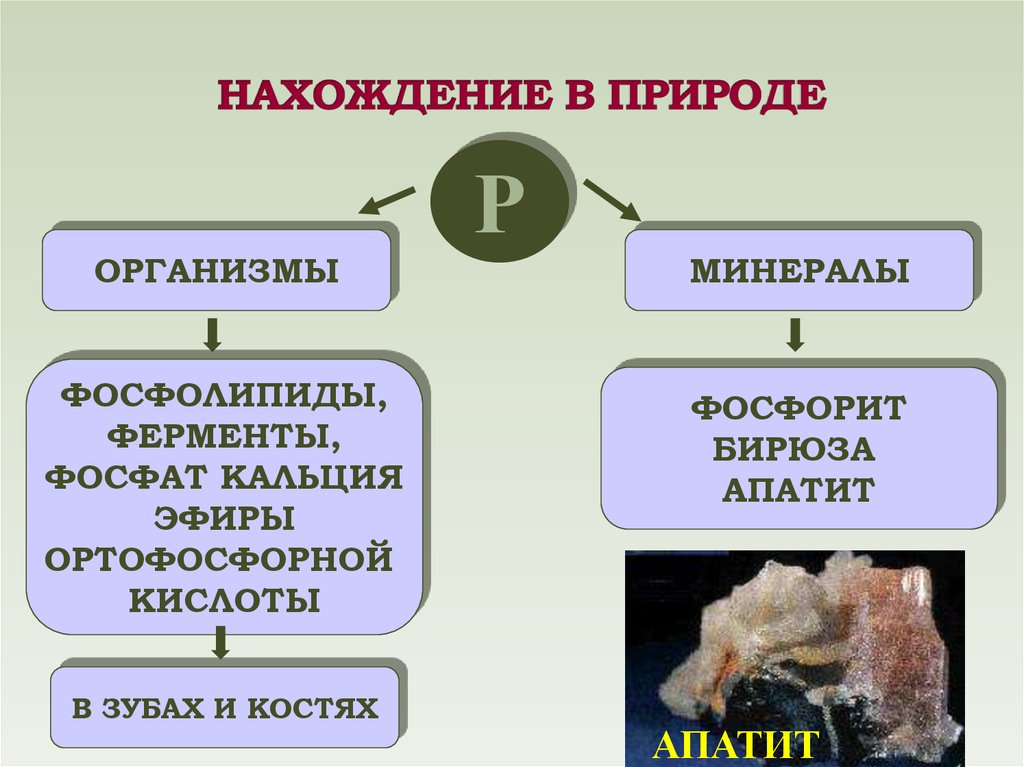
11. НАХОЖДЕНИЕ В ПРИРОДЕ
ОРГАНИЗМЫФОСФОЛИПИДЫ,
ФЕРМЕНТЫ,
ФОСФАТ КАЛЬЦИЯ
ЭФИРЫ
ОРТОФОСФОРНОЙ
КИСЛОТЫ
В ЗУБАХ И КОСТЯХ
Р
МИНЕРАЛЫ
ФОСФОРИТ
БИРЮЗА
АПАТИТ
АПАТИТ
12. Оксиды фосфора
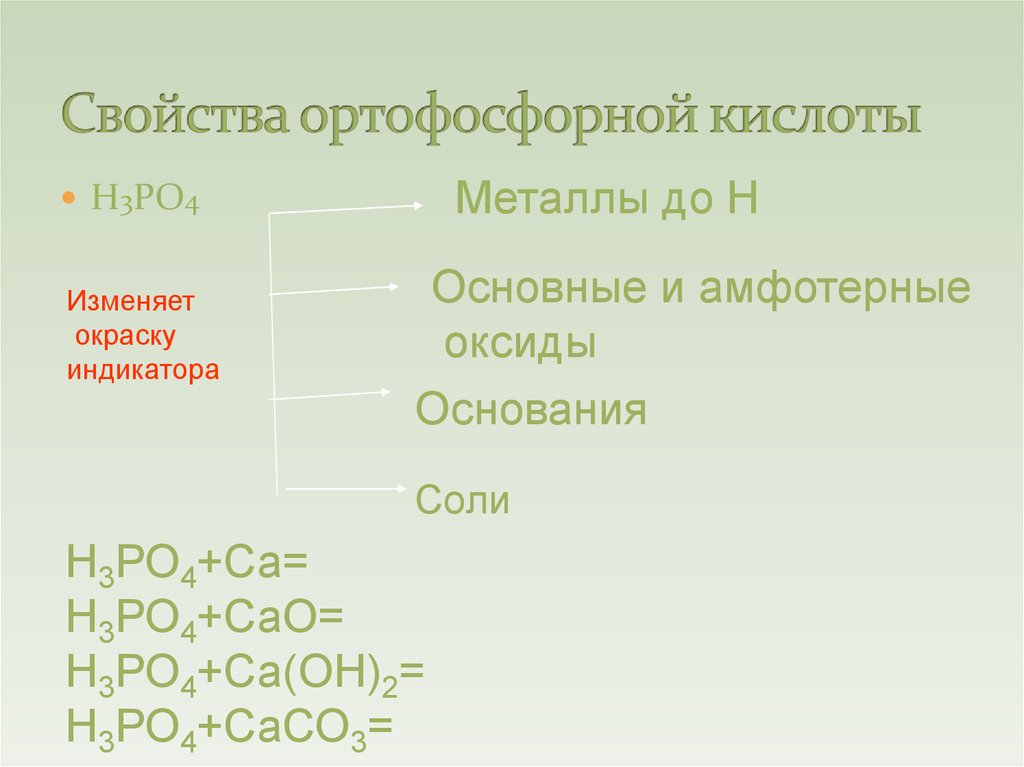
13. Свойства ортофосфорной кислоты
Металлы до НН3РО4
Изменяет
окраску
индикатора
Основные и амфотерные
оксиды
Основания
Соли
Н3РО4+Са=
Н3РО4+СаО=
Н3РО4+Са(ОН)2=
Н3РО4+СаСО3=
14. Фосфорная кислота и её свойства
15. Качественная реакция на фосфат ион- ионы серебра
K3PO4+3AgNO3=Ag3PO4↓+3KNO3при этом выпадает жёлтый осадок нитрата серебра
16. Физиологическое действие белого фосфора
Появление лягушек суродствами -результат
применения фосфорных
удобрений, которые
смываются в реки и пруды,
Фосфорный некроз
– поражение
челюстей
Результат применения
чрезмерного количества
фосфора
17. Получение фосфора
нагреванием смеси фосфорита, угля ипеска в электропечи:
Ca3(PO4)2 + C + SiO2 → P4 + CaSiO3 + CO
18. ПРИМЕНЕНИЕ ФОСФОРА
УдобренияМоющие средства
Ядохимикаты
Умягчение воды
Производство
спичек
Р
Создание
дымовых завес
Защита от
коррозии
Производство
красок
полупроводники
19.
Войска СШАиспользовали
фосфорные
Бомбы
в Ираке,
2004 г.
20. Самостоятельная работа
1.ЗАКОНЧИТЕ УРАВНЕНИЯ:Р + F2 =
Al + P =
Укажите окислитель и восстановитель
2. Задача:
Какова масса фосфора в вашем теле, если известно,
что фосфор составляет ≈1% от массы тела?
3.Осуществите превращения:
Р
РН3
Р2О5
Н3РО4
21. ДОМАШНЕЕ ЗАДАНИЕ
Индивидуальные задания.Подготовить сообщения:
1)об истории спичек;
2) о биологической роли
фосфора и его соединений.
















 Химия
Химия








