Похожие презентации:
Соли: свойства, получение, применение
1.
Соли:свойства, получение,
применение
2.
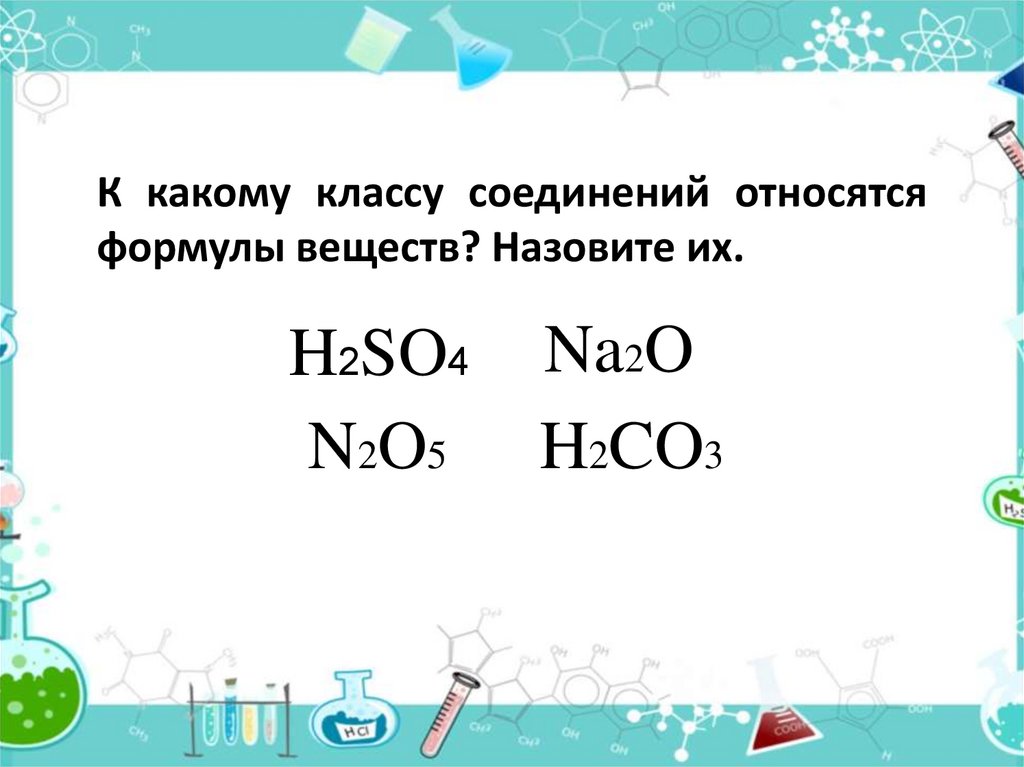
К какому классу соединений относятсяформулы веществ? Назовите их.
H2SO4
N2 O5
Na2O
H2CO3
3.
K3 PO4Na Cl
Ион
металла
Кислотный
остаток
Ион
металла
Кислотный
остаток
Соли – это сложные вещества, состоящие
из ионов металла и кислотного остатка.
Соли – сложные вещества, которые являются продуктами
замещения атомов водорода в кислоте на металл.
4.
Найдите среди формул веществформулы солей:CO2
BaSO4
HCl
H2 SO4
K2SO4
MgCO3
CaO
Fe(OH)3
H2O
5.
НоменклатураНазвание
металла в
родительном
падеже
Название
кислотного
остатка
МgСl2
хлорид
магния
6.
Составить формулы солей:нитрата магния,
фосфата кальция.
7.
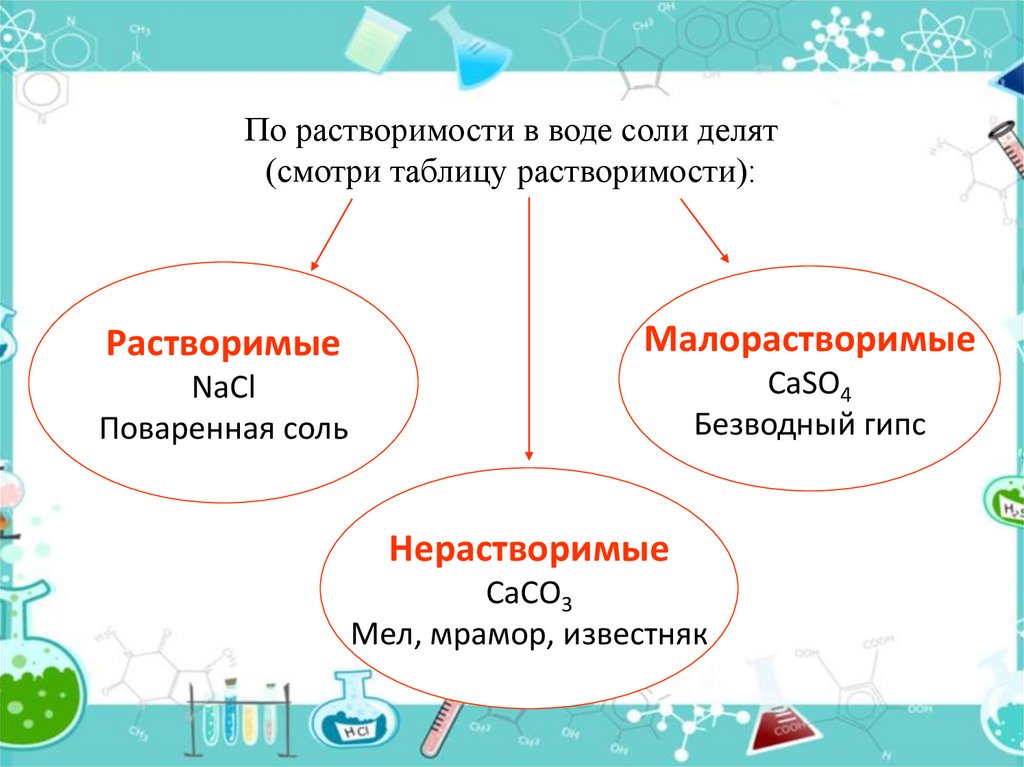
По растворимости в воде соли делят(смотри таблицу растворимости):
Растворимые
Малорастворимые
NaCl
Поваренная соль
CaSO4
Безводный гипс
Нерастворимые
CaCO3
Мел, мрамор, известняк
8.
Химические свойства1. Взаимодействие с металлами. Каждый
левее стоящий металл в ряду напряжений
вытесняет последующий из раствора его
соли.
Fe + CuCI2 = Cu + FeCI2
9.
Химические свойства2. Взаимодействие со щелочами:
В результате обязательно должно образоваться
нерастворимое основание.
2NaОН + CuSO4 → Cu(OH)2 + Na2SO4
3. Взаимодействие солей между собой:
КСl + AgNO3 → AgCl + KNO3
10.
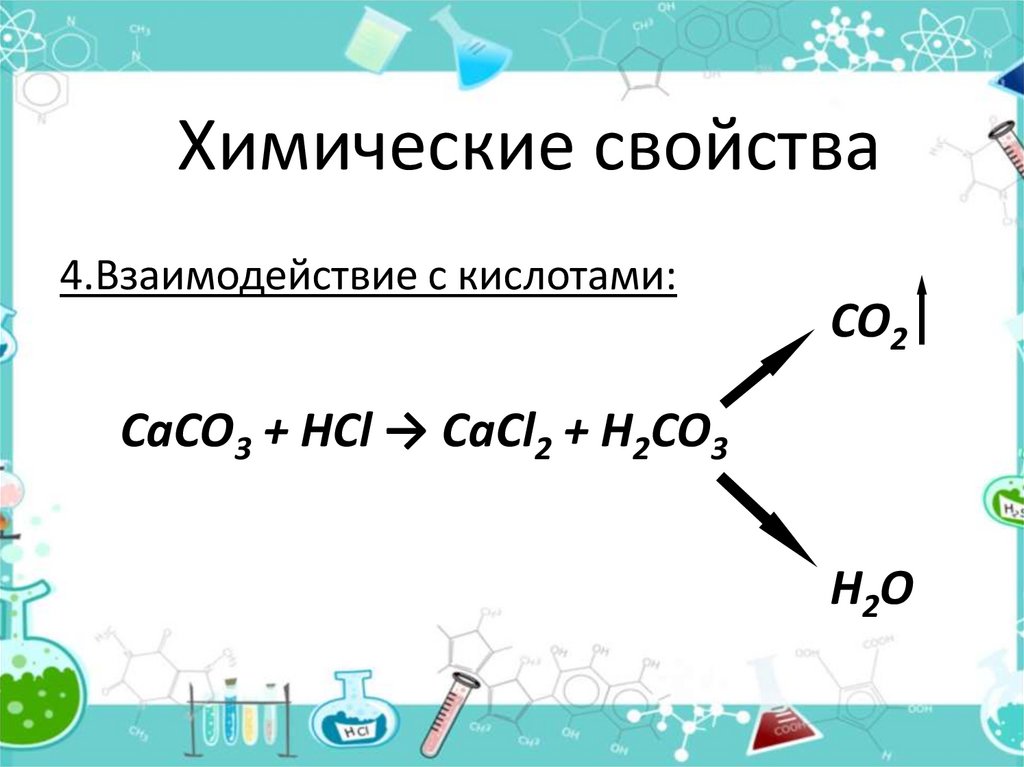
Химические свойства4.Взаимодействие с кислотами:
CO2
CaCO3 + HCl → CaCl2 + H2CO3
H2O
11.
Химические свойства5. Разложение при нагревании:
СаСО3= СО2 + СаО








 Химия
Химия








