Похожие презентации:
Гидролиз. Реакции обменного взаимодействия веществ с водой
1.
Гидролиз2.
• Реакции обменного взаимодействия веществ сводой, приводящее к их разложению
• Гидролиз
Обратимый
Необратимый
3.
Необратимый гидролиз• Необратимый гидролиз происходит, если
при гидролизе выделяется газ, осадок или
вода, т.е. вещества, которые при данных
условиях не могут взаимодействовать между
собой. Необратимый гидролиз является
химической реакцией, т.к. реагирующие
вещества взаимодействуют практически
полностью.
4.
Необратимый гидролизнеорганических веществ. Гидролиз
солей
• При сливании водных растворов карбоната натрия и
хлорида алюминия выпадает осадок и выделяется газ.
• В таблице растворимости стоит прочерк. Вещество
разлагается водой –гидролиз необратим
• 2AlCl3 + 3Na2CO3 + 3H2O = 6NaCl + 2Al(OH)3 + 3CO2↑
• 2Al3+ + 6Cl- + 6Na+ + 3CO32- + 3H2O = 6Na+ + 6Cl- +
2Al(OH)3 + 3CO2↑
• 2Al3+ + 3CO32- + 3H2O = 2Al(OH)3 + 3CO2↑
5.
Необратимый гидролизнеорганических веществ. Бинарные
соединения
• Гидролиз бинарных соединений металл-неметалл
• подвергаются соли бескислородных кислот:
взаимодействие с водой сульфидов алюминия ,
хрома (III) , железа,
• Аналогично карбиды, гидриды, нитриды,
фосфиды активных металлов
6.
7.
Необратимый гидролизнеорганических веществ. Бинарные
соединения
8.
Необратимый гидролиз органическихсоединений
• При разрыве связи более
электроотрицательный атом связывается с
водородом, менее электроотрицательный с
гидроксильной группой:
9.
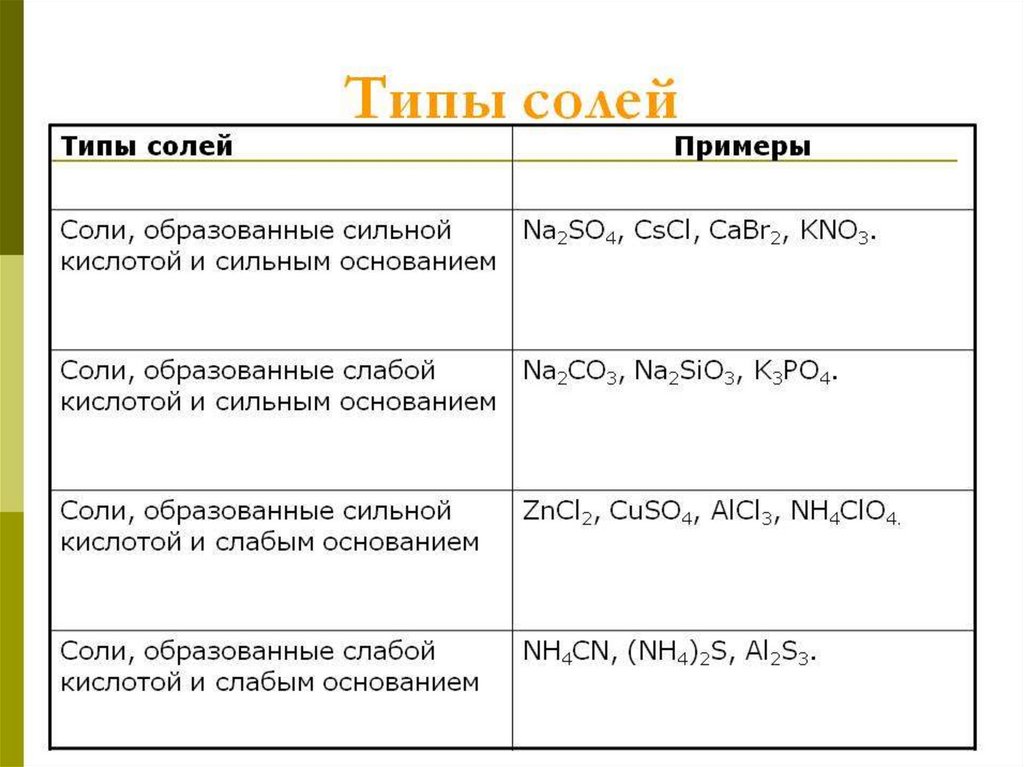
Обратимый гидролиз неорганическихсоединений
• Сущность обратимого гидролиза
неорганических солей сводится к обменному
химическому взаимодействию катионов
металла (аммония) или аниона кислотного
остатка с молекулами воды.
• любая соль это продукт взаимодействия
основания с кислотой
10.
11.
12.
13.
14.
15.
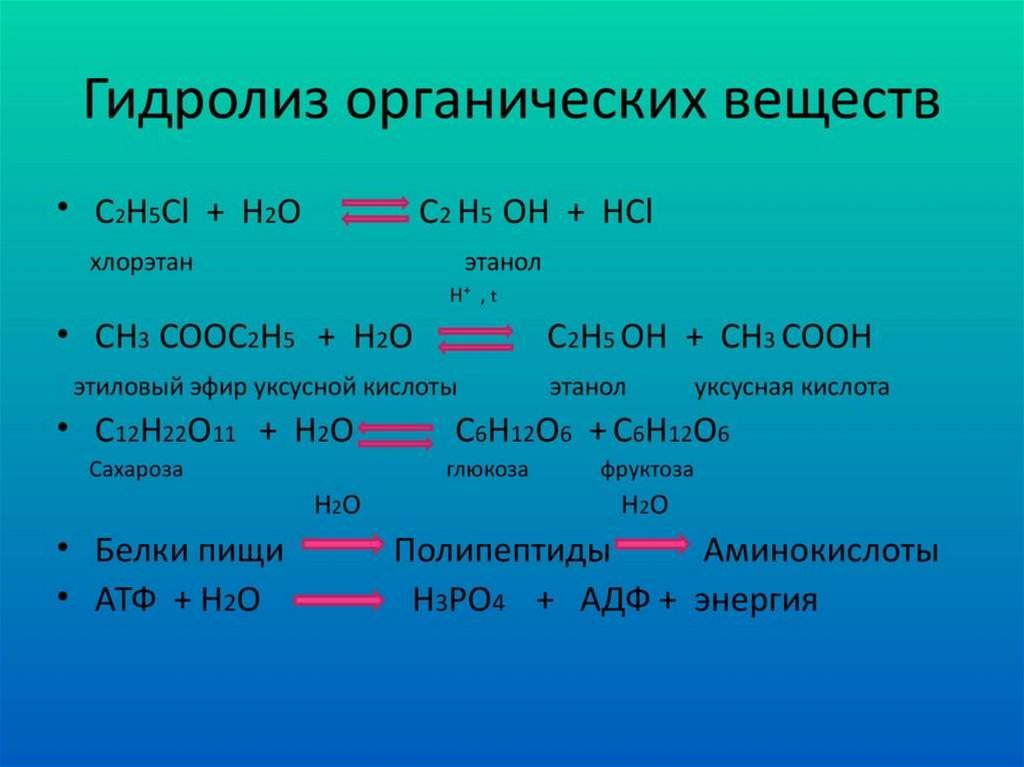
Обратимый гидролиз органическихвеществ
• Реакции обратимого обменного
взаимодействия органических веществ с
водой характерны не только для солей
карбоновых кислот
• Гидролизу подвергаются
галогенопроизводные предельных
углеводородов, сложные эфиры карбоновых
кислот, жиры –как частный случай,углеводы
16.
Обратимый гидролиз органическихвеществ


















 Химия
Химия








