Похожие презентации:
Основные положения теории электролитической диссоциации
1. Основные положения теории электролитической диссоциации
2. 1 положение.
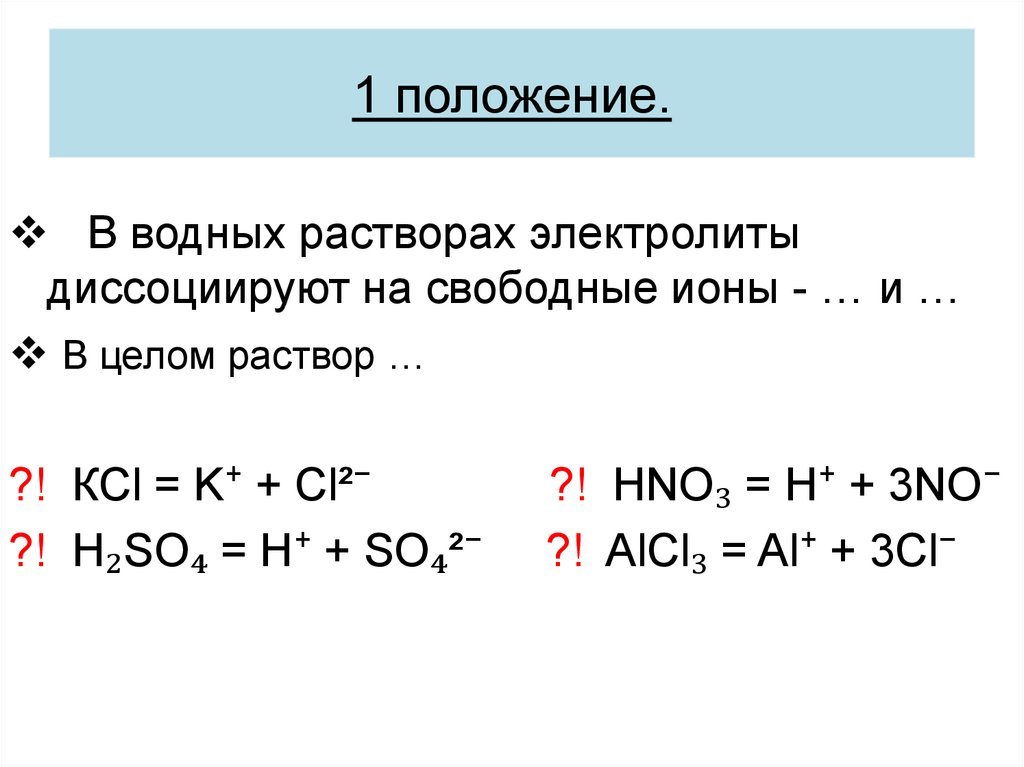
В водных растворах электролитыдиссоциируют на свободные ионы - … и …
В целом раствор …
?! КCl = K⁺ + Cl²⁻
?! H₂SO₄ = H⁺ + SO₄²⁻
?! HNO₃ = H⁺ + 3NO⁻
?! AlCl₃ = Al⁺ + 3Cl⁻
3. 2 положение.
Ионы отличаются от атомов как по …,так и по свойствам.
Атомы:
?! ₂₀Ca 2ē 8ē 2ē
?! ₁₃Al 3ē 8ē 2ē
Ионы:
?! ₁₆S²⁻ 2ē 8ē 6ē
?! ₈O⁻ 2ē 8ē
4. 3 положение.
Ионы в растворе хаотичноперемещаются.
Но при пропускании электрического тока, к
катоду направляются … , а к аноду - ….
?! Выпишите формулы ионов, которые при пропускании
через раствор электрического тока движутся к:
аноду
катоду
Mg²⁺, OH⁻, SO₄²⁻, H⁺, Na⁺, NO₃⁻, CO₃²⁻.
5. 4 положение.
Процесс электролитическойдиссоциации является …
6. Подберите формулы ионов для заполнения круговых схем.
Простыеионы
Анионы
7. Подберите формулы ионов для заполнения круговых схем.
Сложныеионы
Анионы
8. Подберите формулы ионов для заполнения круговых схем.
Сложныеионы
Катионы
9. На какие три равные группы можно разделить схемы электролитической диссоциации?
1)2)
3)
4)
5)
6)
Ca(OH)₂ →Ca²⁺ + OH⁻
Ca(NO₃)₂ → Ca²⁺ + NO₃⁻
HNO₃→ H⁺ + NO₃⁻
HCl → H⁺ + Cl⁻
KOH → K⁺ + OH⁻
Al₂(SO₄)₃ → Al³⁺ + SO₄²⁻
10. На какие две равные группы можно разделить схемы электролитической диссоциации?
1)2)
3)
4)
5)
6)
NaOH → Na⁺ + OH⁻
Ba(NO₃)₂ → Ba²⁺ + NO₃⁻
Ba(OH)₂ → Ba²⁺ + OH⁻
NaCl → Na⁺ + Cl⁻
BaCl₂ → Ba²⁺ + Cl⁻
Na₂CO₃ → Na⁺ + CO₃²⁻









 Химия
Химия








