Похожие презентации:
Степень окисления. Степень окисления неорганических веществ
1.
Степень окисления2.
Степень окисления –-
это условный заряд атомов химических
элементов в соединении, вычисленный на
основе предположения, что все
соединения состоят из ионов
3.
Возможные С.О.• Положительная «+» равна числу отданных
электронов. Максимальная с.о. равна номеру
группы
• Отрицательная «-» равна числу принятых
электронов. Минимальная с.о. равна 8 – номер
группы
• Нулевое значение с.о. имеют атомы в молекулах
с неполярной связью и металлической.
4.
ПРАВИЛА определения С.О.• С.О. атомов в простых веществах = 0
• С.О. фтора = -1
• С.О. кислорода = -2 (кроме Н2О2-1,O+2F2)
• С.О. водорода = +1 (кроме МеН-1)
• С.О. Ме I, II, III групп = номеру группы
• С.О неМе «+» = номеру группы
• С.О. неМе «-» = 8 – номер группы
5.
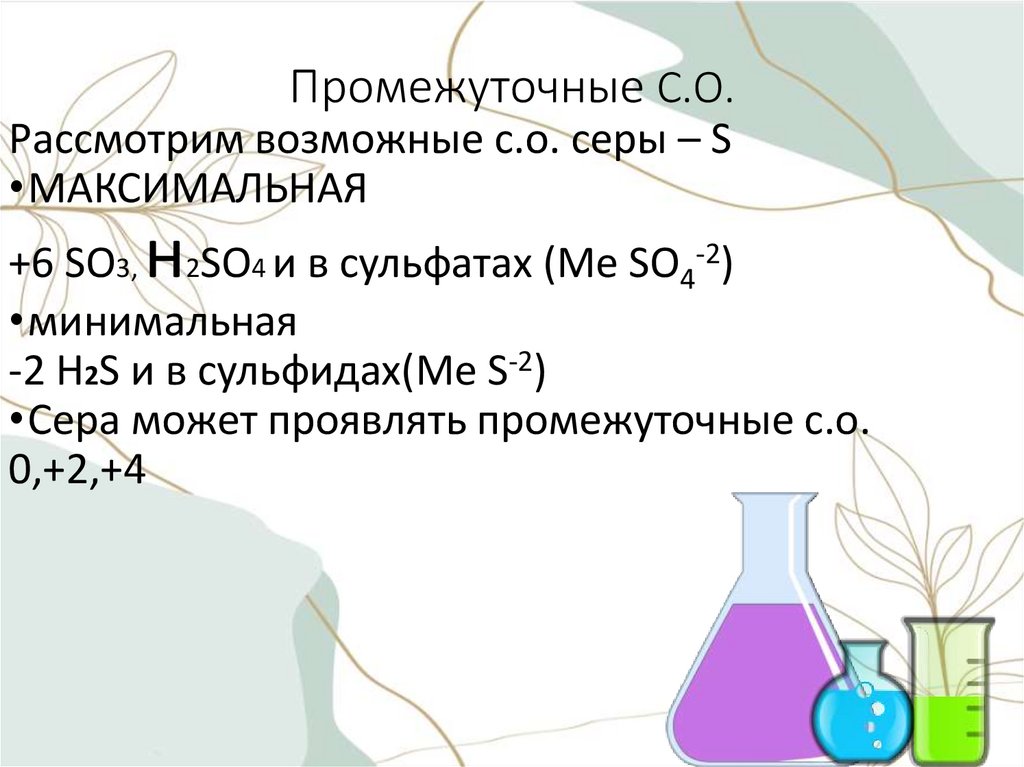
Промежуточные С.О.Рассмотрим возможные с.о. серы – S
•МАКСИМАЛЬНАЯ
н
+6 SO3, 2SO4 и в сульфатах (Ме SO4-2)
•минимальная
-2 H2S и в сульфидах(Ме S-2)
•Сера может проявлять промежуточные с.о.
0,+2,+4
6.
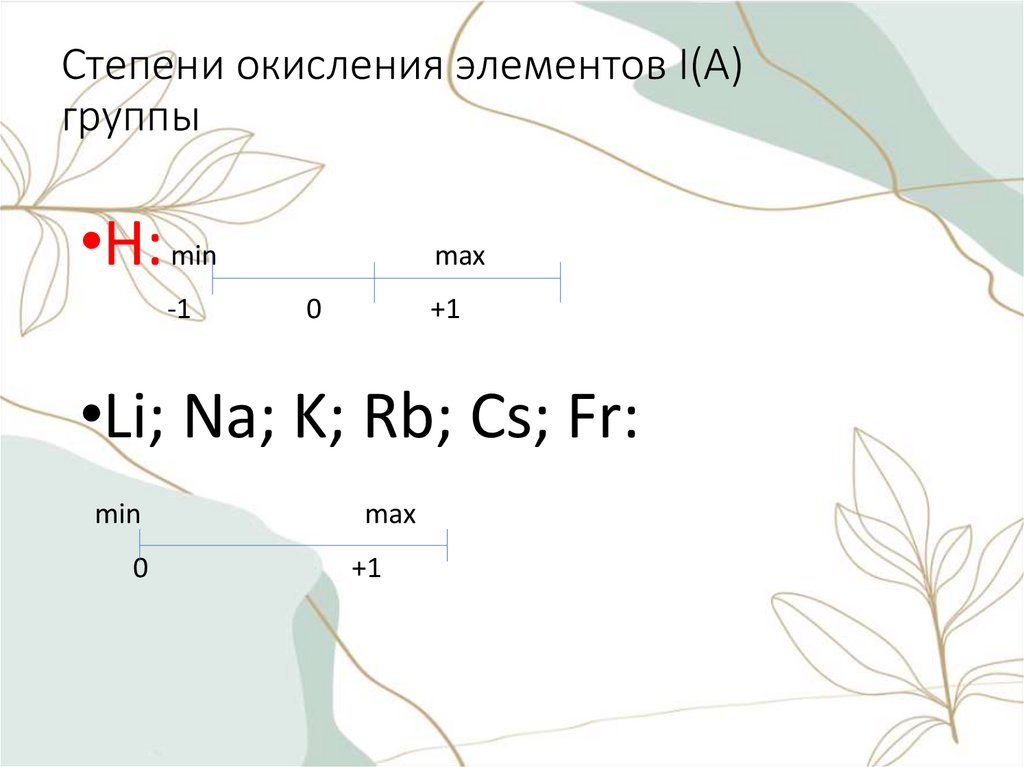
Степени окисления элементов I(A)группы
•Н: min
-1
max
0
+1
•Li; Na; K; Rb; Cs; Fr:
min
0
max
+1
7.
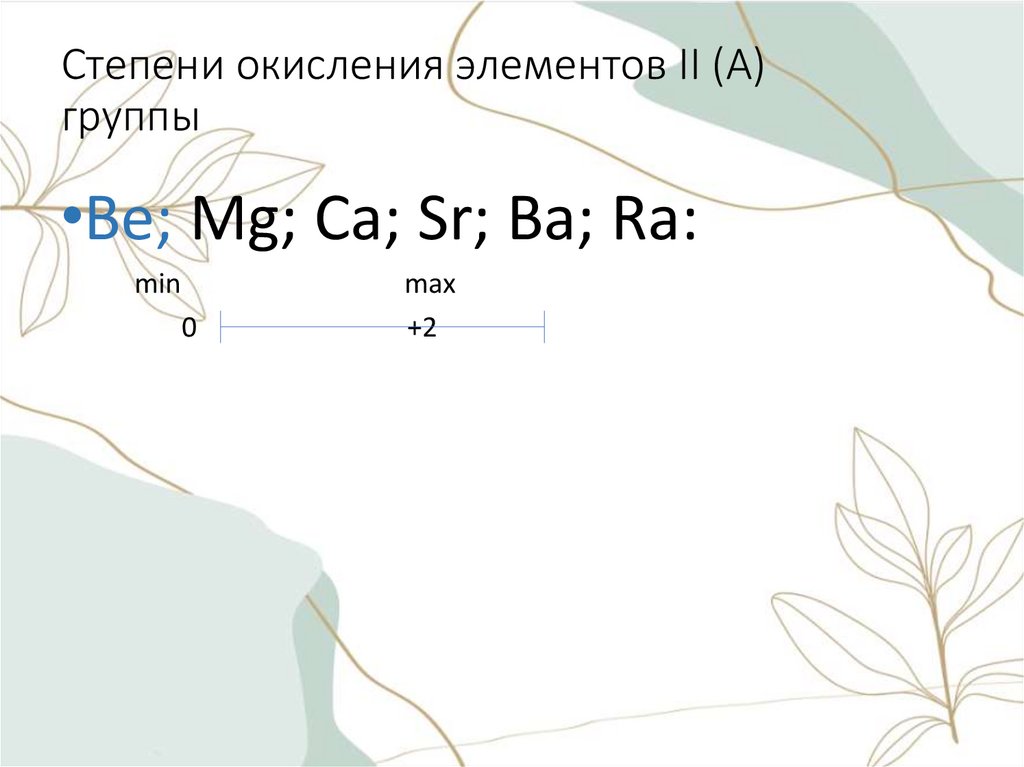
Степени окисления элементов II (A)группы
•Be; Mg; Ca; Sr; Ba; Ra:
min
0
max
+2
8.
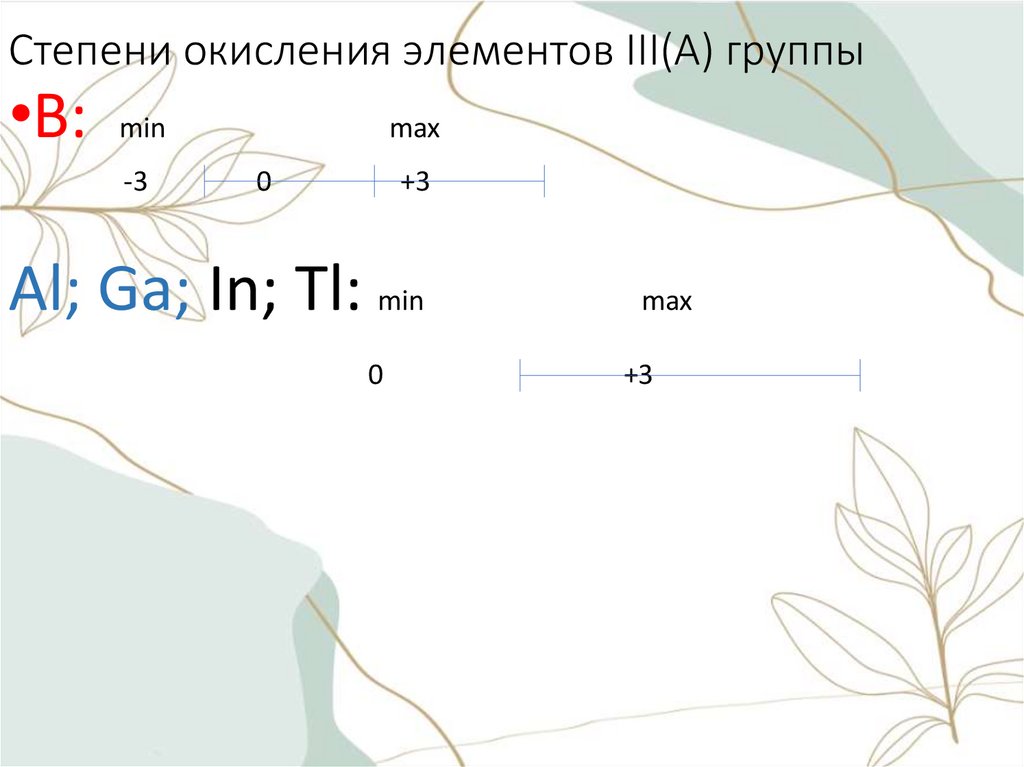
Степени окисления элементов III(A) группы•B:
min
-3
max
0
+3
Al; Ga; In; Tl: min
0
max
+3
9.
Степени окисления элементов IV(A) группы•C; Si: min
-4
max
0
+2
+4
Ge; Sn; Pb: min
0
max
+2
+4
10.
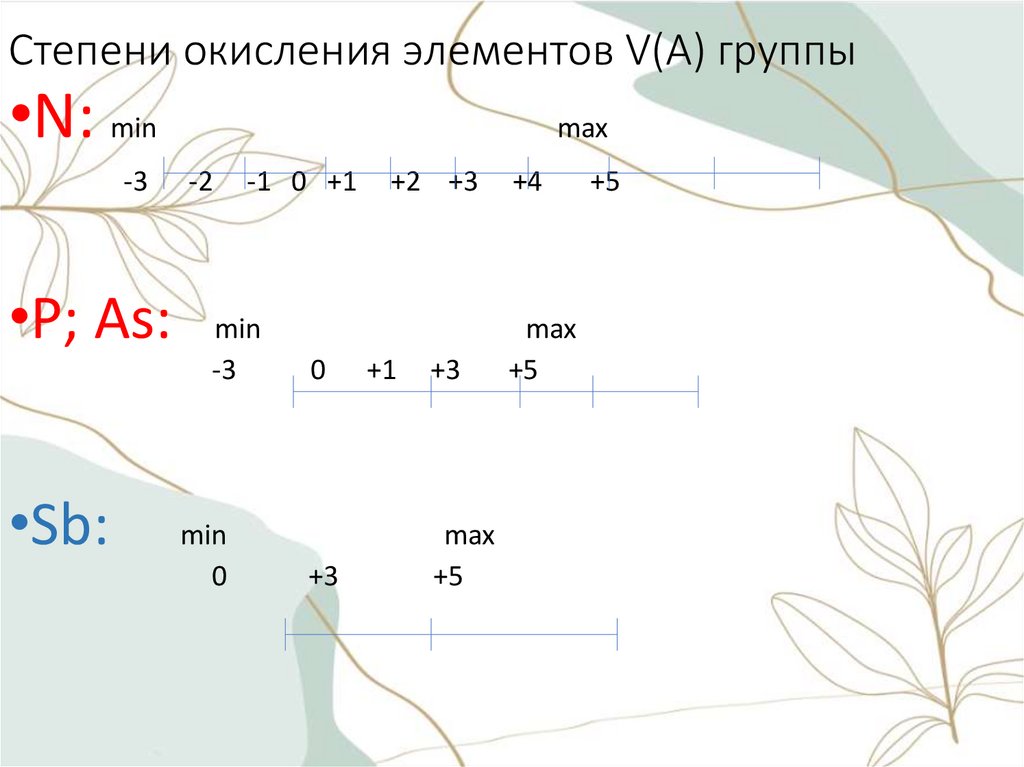
Степени окисления элементов V(A) группы•N: min
-3
•P; As:
•Sb:
max
-2
-1 0 +1
min
-3
min
0
0
+3
+2 +3
+1
+3
max
+5
+4
max
+5
+5
11.
Степени окисления элементов VI(A) группы•O: min
-2
max
-1 0 +1
+2
•S; Se; Te; Po: min
-2
0
+2
+4
max
+6
12.
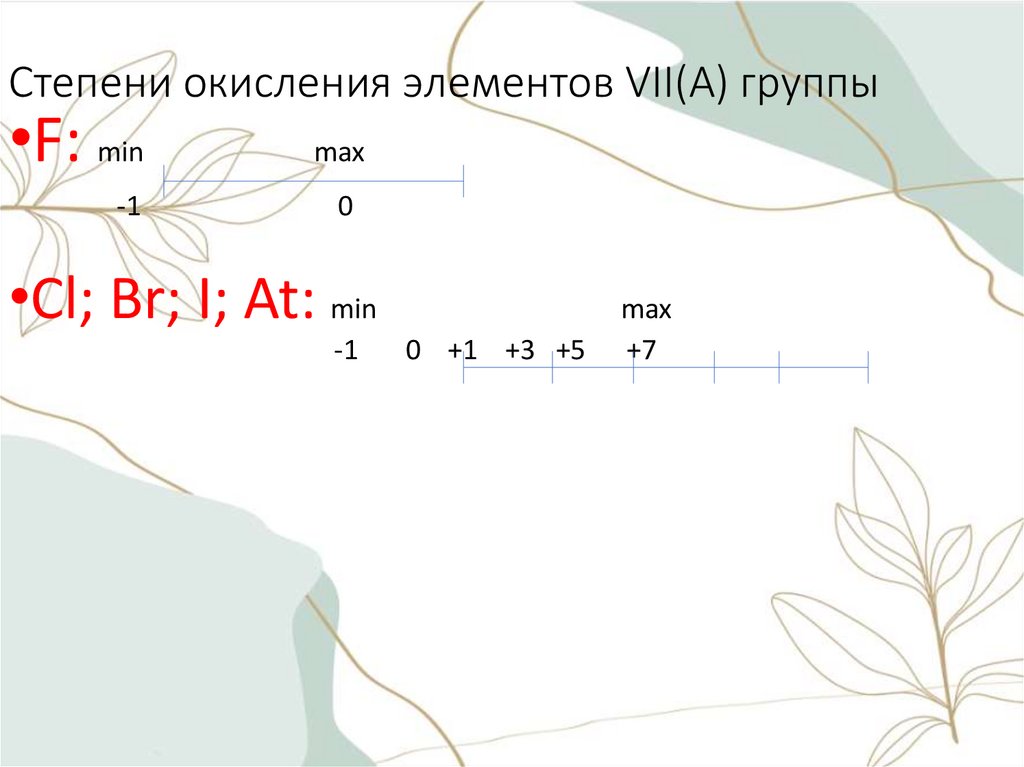
Степени окисления элементов VII(A) группы•F: min
-1
max
0
•Cl; Br; I; At: min
-1
0 +1 +3 +5
max
+7
13.
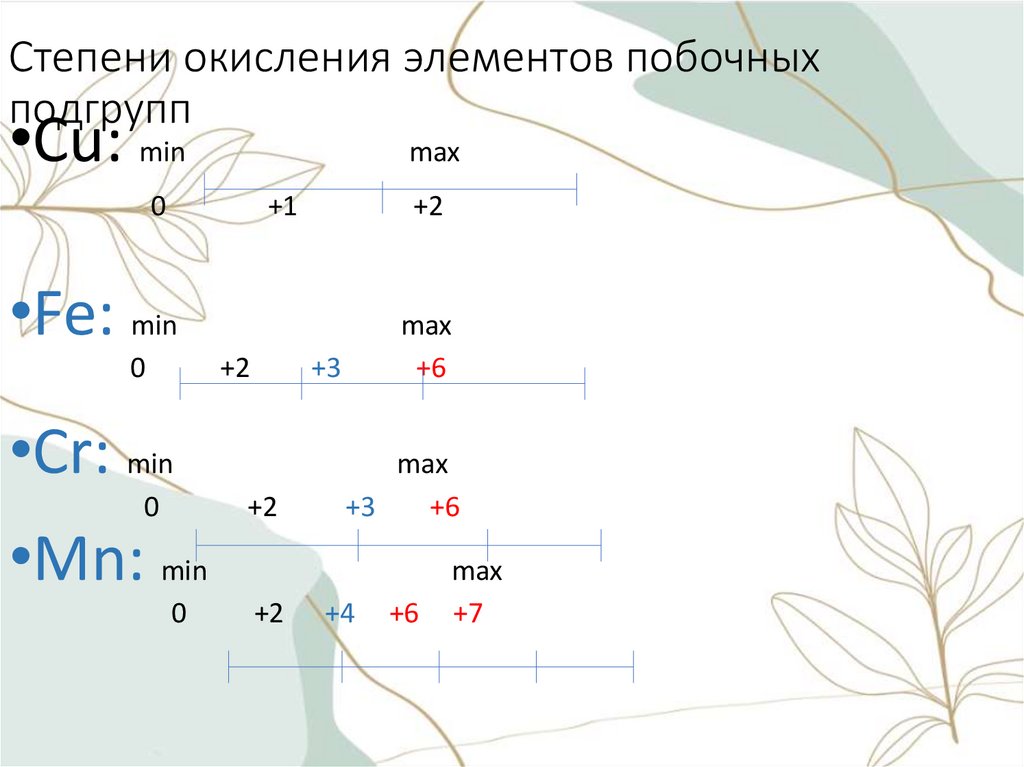
Степени окисления элементов побочныхподгрупп
•Cu: min
max
0
+1
+2
•Fe: min
0
+2
+3
•Cr: min
0
•Mn: min
0
max
+6
+2
+2
max
+3
+6
+4
+6
max
+7
14.
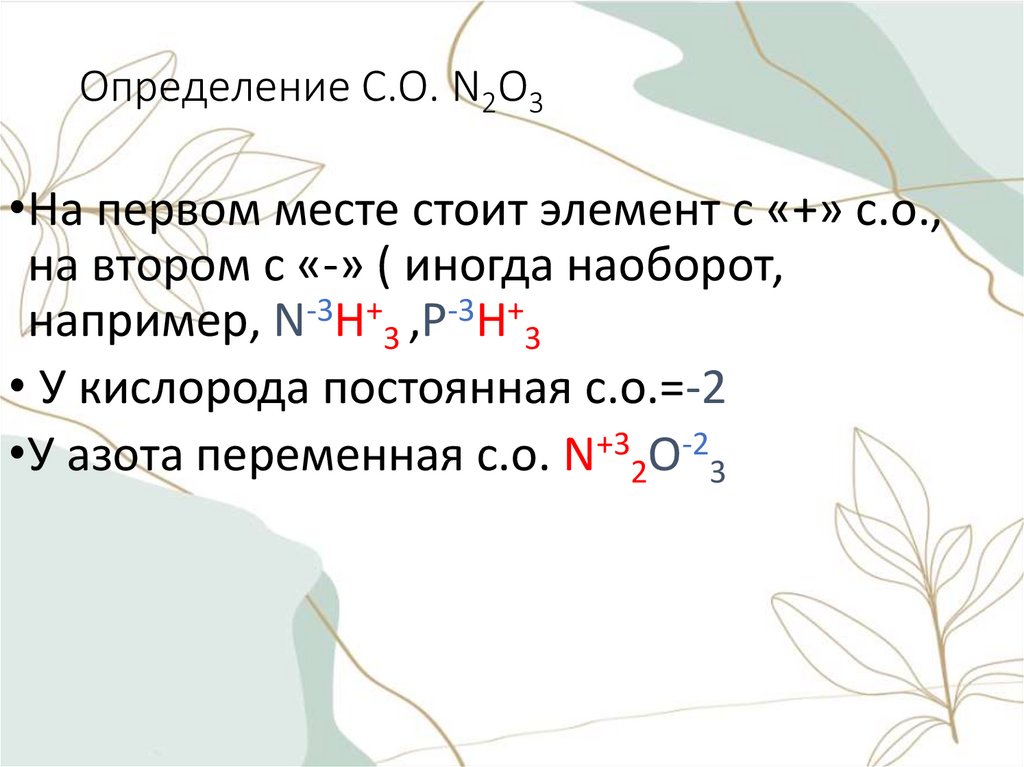
Определение С.О. N2O3•На первом месте стоит элемент с «+» с.о.,
на втором с «-» ( иногда наоборот,
например, N-3Н+3 ,Р-3Н+3
• У кислорода постоянная с.о.=-2
•У азота переменная с.о. N+32O-23
15.
Задание 1: Определите С.О. по формулам1. Cl2O7, NaH, Na2S, MgO, H3N.
2. N2, Al2S3, Cu2O, Na; K2O.
3. Fe; CaCO3; AlCl3; Li3N; BaSO4.
4. Zn; H2CO3; O3; OF2; CuSO4; NaOH.
5. O2; SO3; KH; KOH; BaH2; H2O; NH3.
16.
Задание 2. Составьте формулы бинарныхсоединений.
17.
Закрепление пройденного:Расставьте с.о.
1 группа:N2O, NH3, N2O5, Fe2O3, Al2S3
2группа: Na2S, Na3N, SO2, SO3, H2S
3 группа: MgS, Mg3N2, P2O5, PH3, P2O3
4 группа: Ca3N2, CaCl2, Cl2O3, HCl, Cl2O7








 Химия
Химия








