Похожие презентации:
Лавка возможностей
1. Лавка возможностей
2. Что объединяет эти понятия?
• Характер• Оксид
• Химическое соединение
• Кислота
• Соль
• Свойства
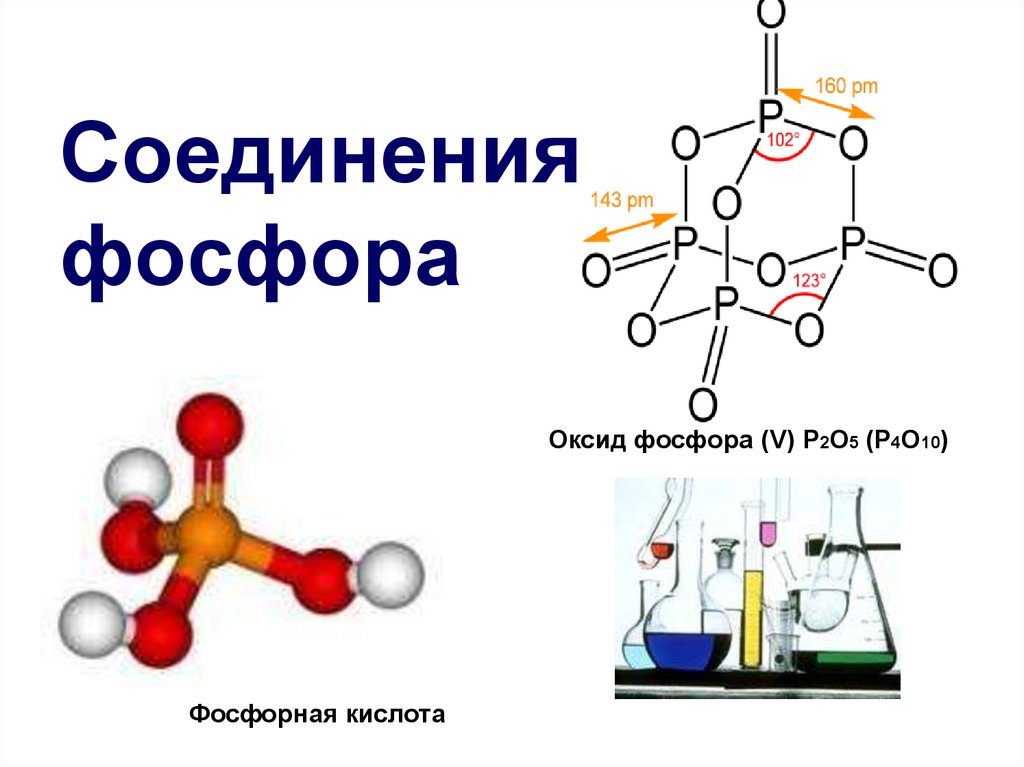
3. Соединения фосфора
Оксид фосфора (V) P2О5 (Р4О10)Фосфорная кислота
4. Что хочу узнать?
Выбор за тобой«Это невозможно!» - сказала Причина
«Это безрассудство!» - заметил Опыт
«Это бесполезно!» - отрезала
Гордость
«Попробуй…» - шепнула Мечта.
5. Выберите из списка и распределите (три колонки) оксиды, кислоты, соли, основания
SO2 H2SO4 CO2 P2O5NO2 HNO3 NaNO3
NaCl NaOH H3PO4
K3PO4
Подчеркните соединения фосфора
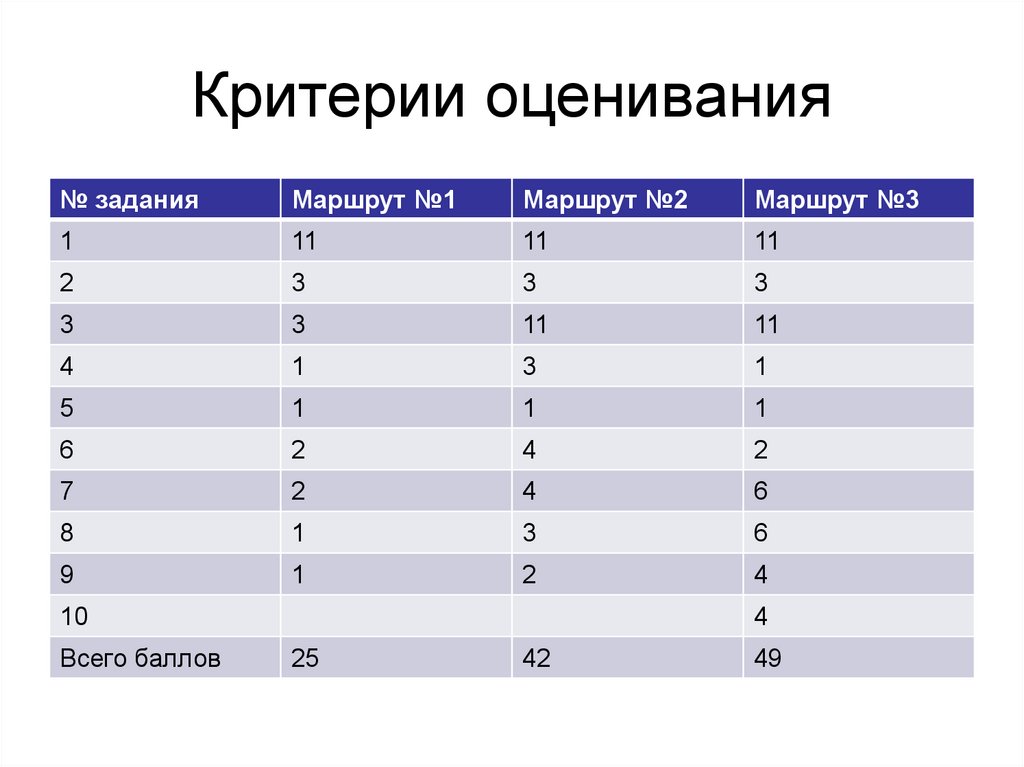
6. Критерии оценивания
№ заданияМаршрут №1
Маршрут №2
Маршрут №3
1
11
11
11
2
3
3
3
3
3
11
11
4
1
3
1
5
1
1
1
6
2
4
2
7
2
4
6
8
1
3
6
9
1
2
4
10
Всего баллов
4
25
42
49
7. Правила по технике безопасности.
1. Где б ты не работал,Запомни: везде
Рабочее место держи в чистоте.
2. С заданием справиться трудно бывает
Тому, кто небрежность в делах проявляет:
То что-то разлил, то рассыпал случайно.
Что может случиться? Коварная тайна!
Рассыпал? Бывает. Смотри не молчи,
Учителя живо на помощь зови!
Конечно, тебя поругает, быть может,
Но в этой беде только он и поможет.
8.
3. Склянка с кислотой упала –Капля на руку попала.
Тут на месте не сиди!
Живо к крану ты беги,
Смой водою кислоту,
Этим отведёшь беду.
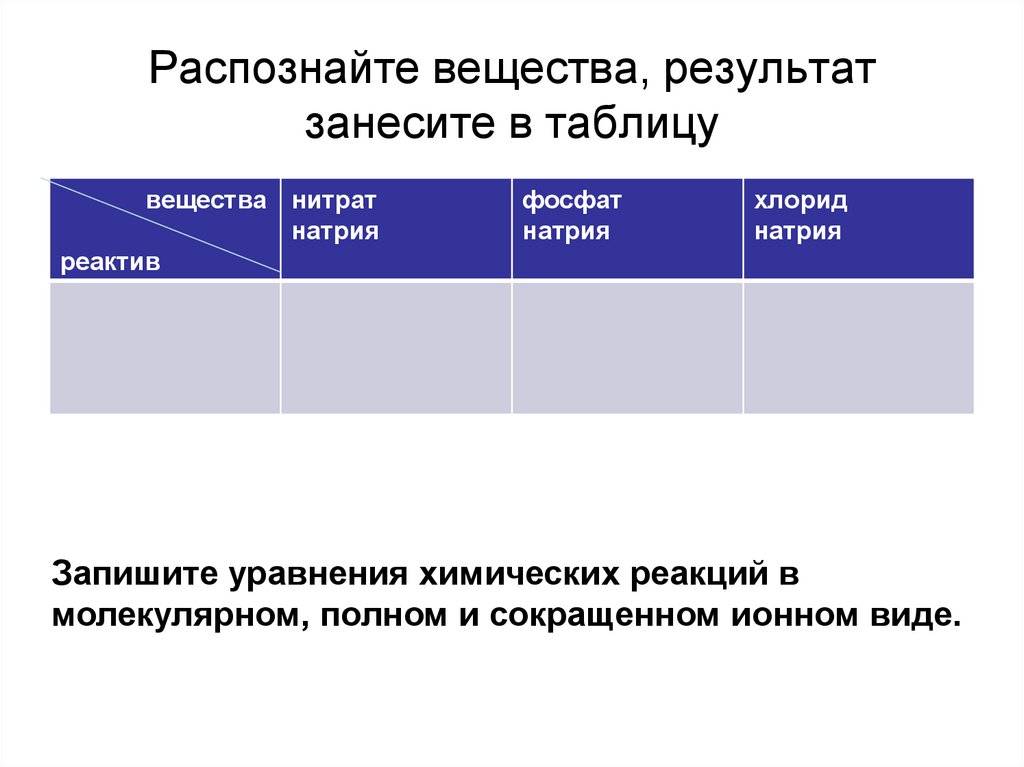
9. Распознайте вещества, результат занесите в таблицу
вещества нитратнатрия
реактив
фосфат
натрия
хлорид
натрия
Запишите уравнения химических реакций в
молекулярном, полном и сокращенном ионном виде.
10. Критерии оценки практического задания
• 1 балл – составление планаэксперимента
• 3 балла – распознавание веществ
• 6 баллов – запись уравнений реакций
11. Не забудьте!
Химик «правило обмена» не забудетникогда: если выделится газ – это
раз;
А получится вода – это два;
А еще - нерастворимый осаждаемый
продукт …
«Есть осадок»- говорим мы - это
третий важный пункт…
12. Сопоставьте свойства и области применения фосфорной кислоты
1. Фосфаты - необходимыйэлемент питания для
растений.
2. Фосфаты умягчают
жёсткую воду.
3. Обладает антиоксидантным
свойством.
4. Фосфаты являются
компонентом зубной ткани.
5. Фосфаты не горючи.
6. Раствор фосфорной
кислоты приятный на вкус.
1. Как добавка в мармелады,
лимонады и сиропы.
2. Как консервант для
продуктов питания.
3. Производство
синтетических моющих
средств.
4. Применяется для
получения зубных
цементов
5. Производство фосфорных
удобрений
6. Придание огнестойкости
древесине (пропитка).
Огнезащитные краски.
13.
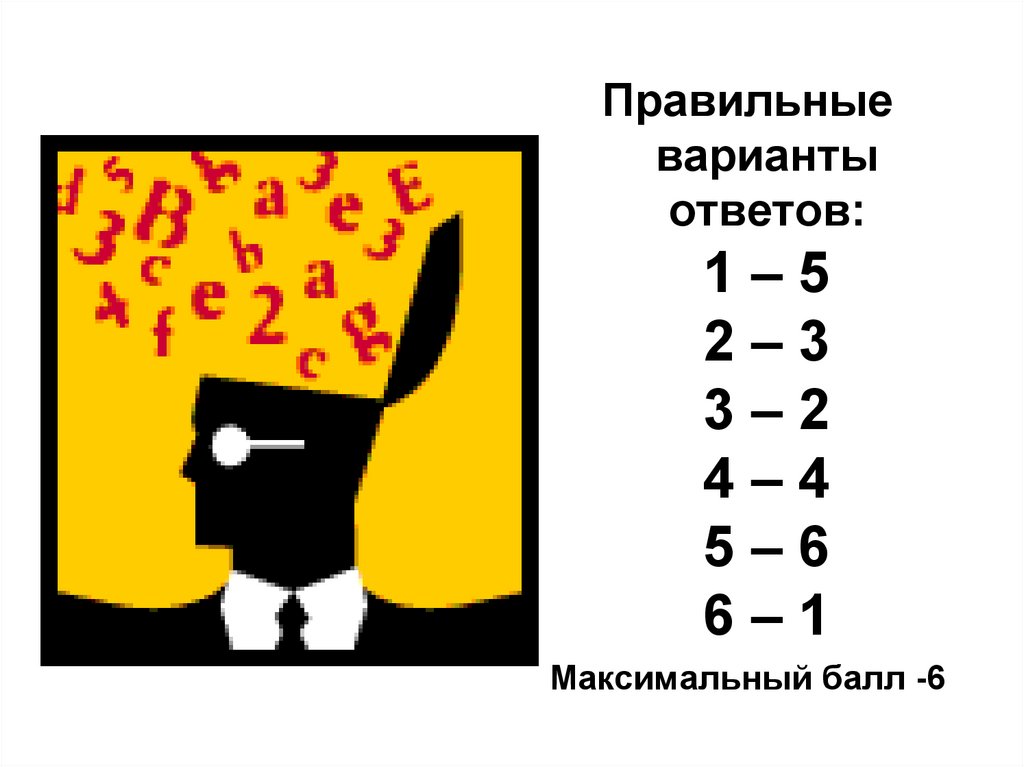
Правильныеварианты
ответов:
1–5
2–3
3–2
4–4
5–6
6–1
Максимальный балл -6
14. Примените знания на практике
Одним из особенных свойствфосфорной кислоты является
следующее: фосфорная кислота,
убирая с поверхности металла его
оксид, с самим железом
реагирует очень медленно.
Как практически можно использовать
это знание?
15. А вот так:
• Кислота фосфорнаяможет транспортироваться в стальных или
гуммированных цистернах.
• Фосфорную кислоту используют для
очистки железа от ржавчины (оксидов
железа). Фосфорная кислота, убирая с
поверхности металла его оксид, с самим
железом реагирует очень медленно. Оксид
железа превращается в растворимую соль
FePO4, которую смывают водой вместе с
остатками кислоты.
16. Домашнее задание
1.Изучить §22,выполнить упр. 2, 4-стр.702.Изучить §22,выполнить упр. 5,6 -стр.70.
3. Изучить §22,выполнить упр. 5,6,
задача 1-стр.70
- Творческое задание: найдите в литературных
произведениях информацию о свойствах и
применении соединений фосфора.
17. Подведение итогов
РейтингОценка
25 – 40 баллов
«3»
(удовлетворительно)
41 – 57 баллов
«4» (хорошо)
58 – 65 баллов
«5» (отлично)














 Химия
Химия








